1. 领域背景与文献引入
文献英文标题:Replication and transcription machinery for ranaviruses: components, correlation, and functional architecture;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:水生动物病毒学(蛙病毒科)
蛙病毒科(Ranavirus)属于核质大DNA病毒(NCLDVs),是一类能跨物种感染两栖类、鱼类、爬行类等变温动物的病原体,对野生水生生物多样性和经济水产养殖构成严重威胁。目前,蛙病毒科的研究主要集中在病毒分离鉴定、基因组测序及部分单个蛋白的功能分析,但其复制与转录的分子机制仍不明确。核质大DNA病毒的复制转录通常依赖自身编码的核心蛋白,并招募宿主蛋白参与,但蛙病毒科作为该类群中的重要分支,其复制转录机器的组成、各组分间的相互作用及调控网络尚未得到系统解析,尤其是宿主蛋白在其中的具体作用及病毒核心蛋白的调控机制,是领域内未解决的核心问题。
针对这一研究空白,本研究以两种蛙病毒(中国大鲵蛙病毒ADRV和虎纹蛙病毒RGV)为研究对象,结合iPOND(新生DNA结合蛋白分离)、重组病毒亲和纯化、NanoLuc互补实验等多种技术手段,系统鉴定了蛙病毒复制与转录机器的组成,解析了各组分间的相互作用及功能架构,为深入理解蛙病毒的复制转录机制及开发抗病毒策略提供了重要基础。
2. 文献综述解析
本文综述部分围绕蛙病毒科的研究现状与核质大DNA病毒的复制转录通用机制展开,明确了领域内现有研究的局限性,为自身研究的创新点奠定了基础。
作者首先介绍了蛙病毒科的分类地位、宿主范围及基因组特征,指出该类病毒具有跨物种感染能力,但复制转录机制研究滞后。随后回顾了核质大DNA病毒的复制转录通用机制,包括复制体的核心组分(如DNA聚合酶、增殖细胞核抗原(PCNA)、单链DNA结合蛋白等)及转录机器的组成,同时指出不同类群的核质大DNA病毒在利用宿主蛋白方面存在差异。现有研究主要通过生物信息学预测蛙病毒科编码的复制转录相关蛋白,部分蛋白(如dUTPase、胸苷激酶)的功能得到初步验证,但整体上仍缺乏对复制转录机器的系统鉴定,尤其是宿主蛋白的参与情况、病毒蛋白间的相互作用网络及复制与转录的偶联机制,均未得到明确解析,且现有研究多集中在单个蛋白,缺乏对整体功能架构的认识。
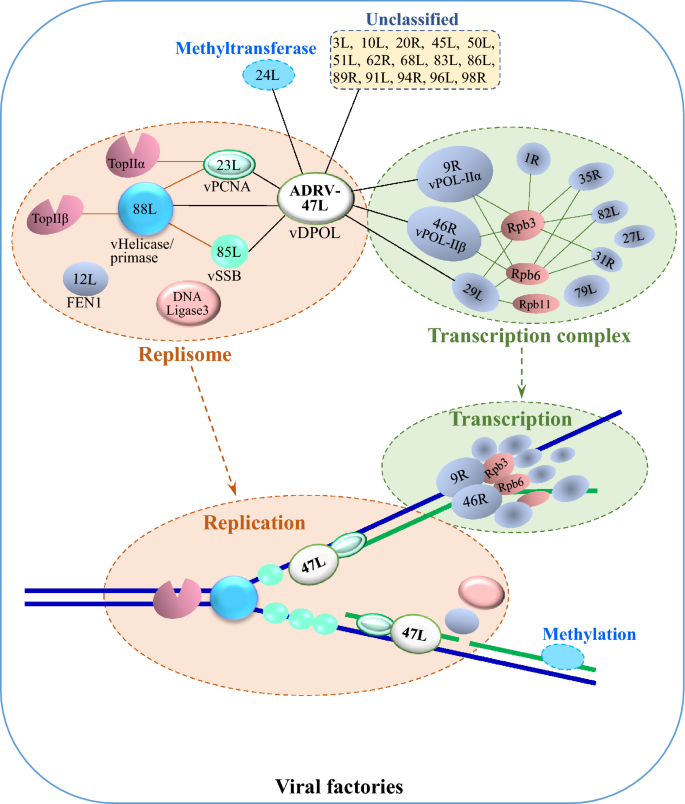
与现有研究相比,本研究的创新点在于首次将iPOND技术应用于水生动物病毒研究,系统鉴定了结合新生DNA的病毒和宿主蛋白,明确了蛙病毒复制体和转录复合物的完整组成;首次发现宿主RNA聚合酶II(RNAPII)的亚基Rpb3、Rpb6、Rpb11参与核质大DNA病毒的转录复合物,拓展了对核质大DNA病毒转录机制的认识;还发现病毒DNA聚合酶(vDPOL)作为核心调控因子,与多种病毒和宿主蛋白相互作用,连接复制与转录过程,揭示了蛙病毒复制转录的调控核心。这些成果填补了蛙病毒科复制转录机制研究的空白,为核质大DNA病毒的研究提供了新的视角。
3. 研究思路总结与详细解析
本研究的整体目标是系统鉴定蛙病毒科ADRV和RGV的复制与转录机器组成,解析各组分间的相互作用及功能架构,揭示病毒复制转录的调控机制。核心科学问题包括蛙病毒如何利用自身和宿主蛋白构建复制转录机器、核心蛋白如何调控复制与转录过程、宿主蛋白在其中的具体作用机制。研究采用“方法建立-组分筛选-功能验证-网络解析-架构构建”的闭环技术路线,通过多种实验手段的结合,全面解析了蛙病毒的复制转录机制。
3.1 iPOND方法的建立与优化
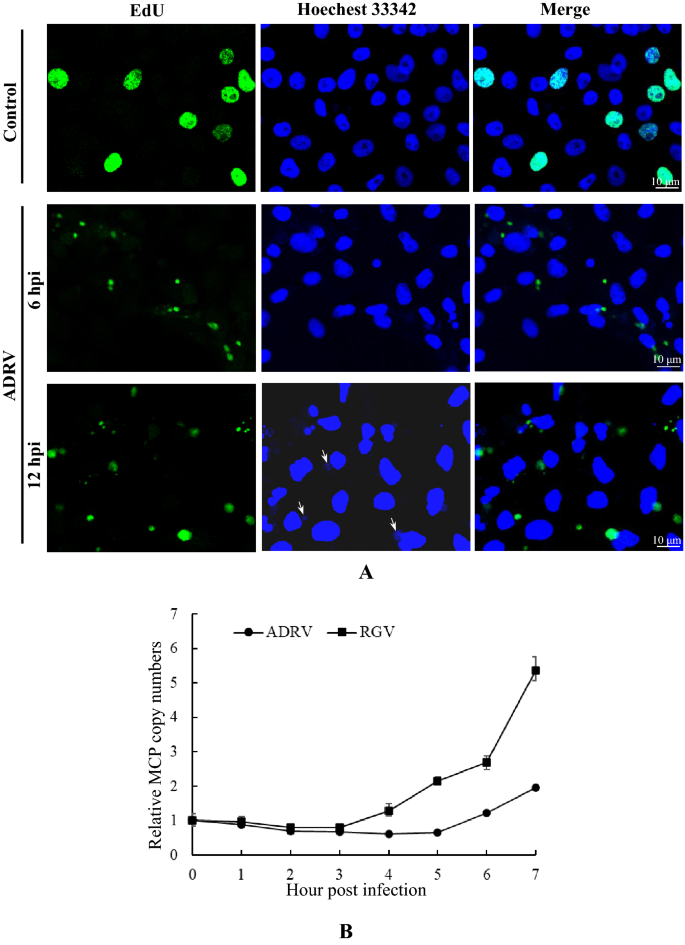
实验目的:验证EdU标记技术在水生动物细胞中标记蛙病毒新生DNA的可行性,确定iPOND实验的最佳条件,为后续筛选新生DNA结合蛋白奠定基础。方法细节:以中国大鲵胸腺细胞(GSTC)为模型,分别感染ADRV和RGV,在感染后6小时(hpi)和12hpi加入10μM EdU标记1小时,通过Click-iT反应结合免疫荧光观察EdU信号的定位;同时通过实时荧光定量PCR(qPCR)检测病毒基因组的复制动力学,确定EdU的最佳标记时间(10min、20min、30min)和标记时间点。结果解读:免疫荧光结果显示,未感染细胞的EdU信号主要定位在细胞核,而感染细胞的EdU信号在6hpi后主要聚集在细胞质的病毒工厂,且随感染时间延长,信号的强度和面积逐渐增加;qPCR结果显示,ADRV的基因组在5hpi后明显增加,RGV在3hpi后明显增加,结合EdU标记观察,最终选择7hpi作为标记时间点,30min作为标记时长,证明iPOND方法可有效应用于水生动物病毒的新生DNA结合蛋白筛选。实验所用关键产品:EdU(Invitrogen)、Click-iT Plus EdU Cell Proliferation Kit(Thermo Scientific)、TakaRa MiniBEST Universal Genomic DNA Extraction Kit。
3.2 新生DNA结合蛋白的筛选与鉴定
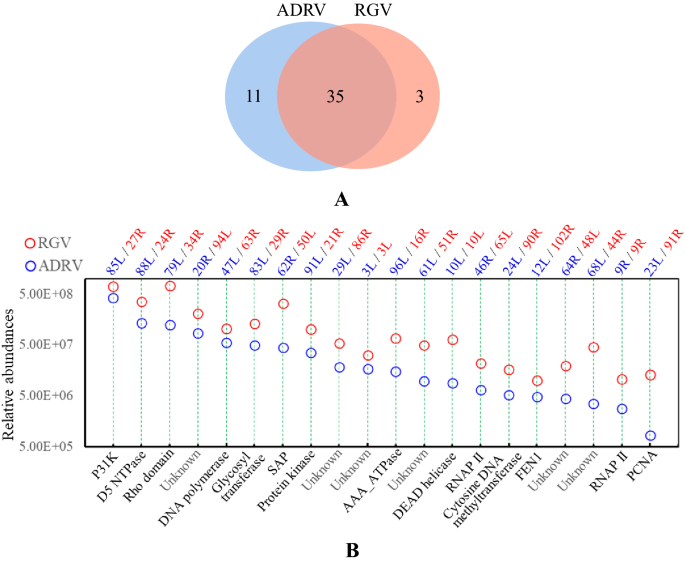
实验目的:筛选并鉴定结合ADRV和RGV新生DNA的病毒和宿主蛋白,明确复制转录机器的潜在组分。方法细节:对ADRV和RGV感染的GSTC细胞进行三次独立的iPOND-质谱(MS)实验,设置click(加入生物素叠氮化物)和nonclick(加入DMSO)对照,通过链霉亲和素琼脂糖珠捕获结合新生DNA的蛋白复合物,经质谱分析鉴定蛋白种类,并对鉴定到的蛋白进行功能分类。结果解读:质谱分析共鉴定到46种ADRV蛋白和38种RGV蛋白,其中35种为两种病毒共有的蛋白,这些蛋白可分为核苷酸前体代谢、DNA复制、基因组修饰、转录、核酸加工等类别,另有部分蛋白功能未知;同时鉴定到多种宿主蛋白,其中DNA拓扑异构酶IIα/β、RNAPII亚基等与复制转录功能直接相关,为后续功能验证提供了候选靶点。实验所用关键产品:链霉亲和素琼脂糖珠(Novagen)、Thermo LTQ Orbitrap Elite质谱分析系统。
3.3 病毒单链DNA结合蛋白(vSSB)的功能鉴定
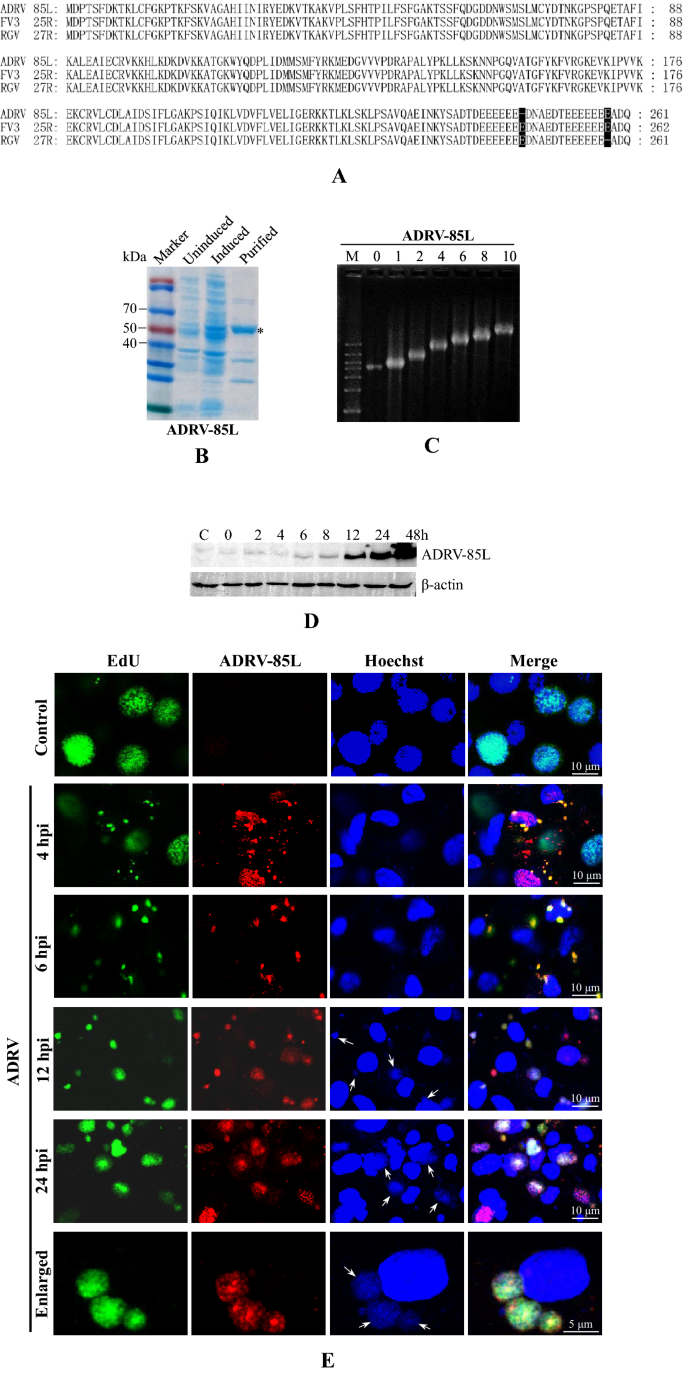
实验目的:验证ADRV-85L及其同源蛋白RGV-27R作为单链DNA结合蛋白的功能,明确其在病毒复制中的作用。方法细节:克隆ADRV-85L和RGV-27R基因,构建原核表达载体,在大肠杆菌中表达并纯化重组蛋白;通过电泳迁移率变动分析(EMSA)检测重组蛋白与ΦX174单链DNA的结合能力;通过蛋白质免疫印迹(Western blot)检测蛋白在感染细胞中的表达时序,通过免疫荧光检测其亚细胞定位。结果解读:电泳迁移率变动分析结果显示,重组ADRV-85L和RGV-27R均能以剂量依赖方式结合单链DNA,使DNA迁移速率减慢,证明其为病毒单链DNA结合蛋白(vSSB);Western blot显示ADRV-85L在6hpi后表达显著增强;免疫荧光显示vSSB定位在细胞质病毒工厂,与新生DNA共定位,随感染时间延长,定位信号逐渐增强,表明vSSB是病毒复制体的核心组分。实验所用关键产品:pET32a原核表达载体、NEB ΦX174 ssDNA、自制抗vSSB多克隆抗体。
3.4 复制体核心蛋白的相互作用分析
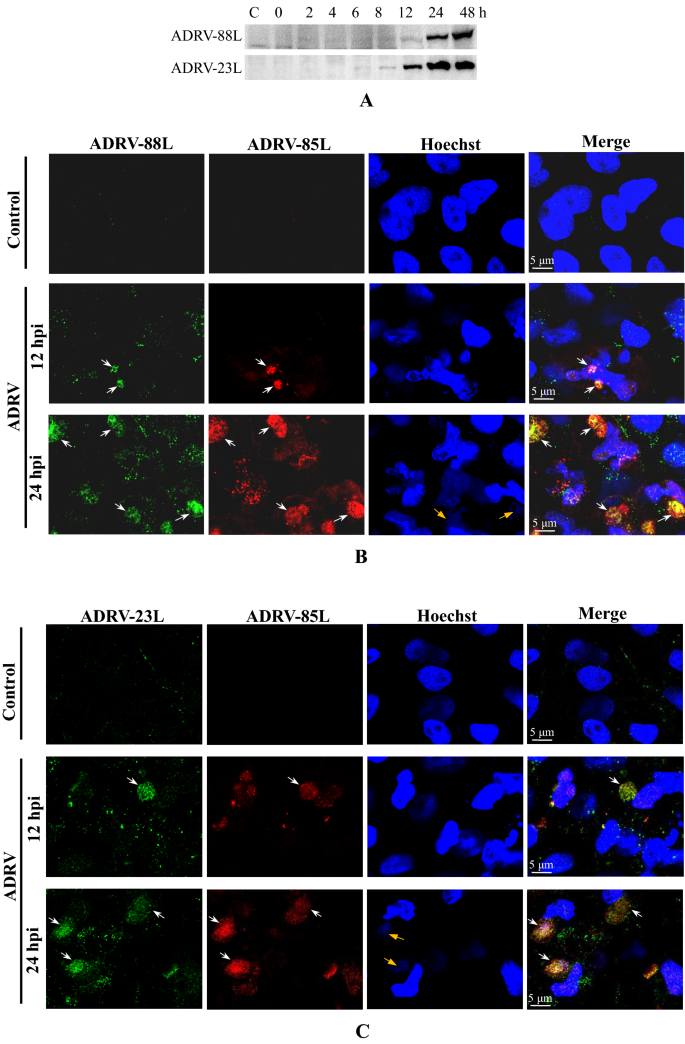
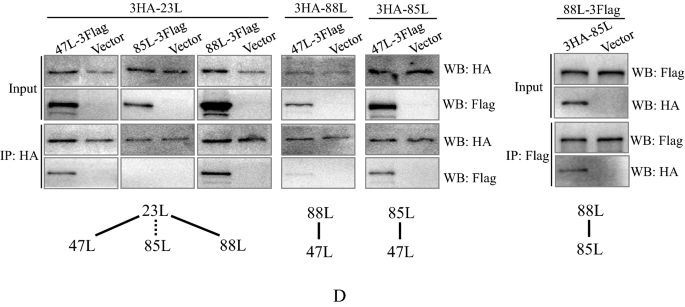
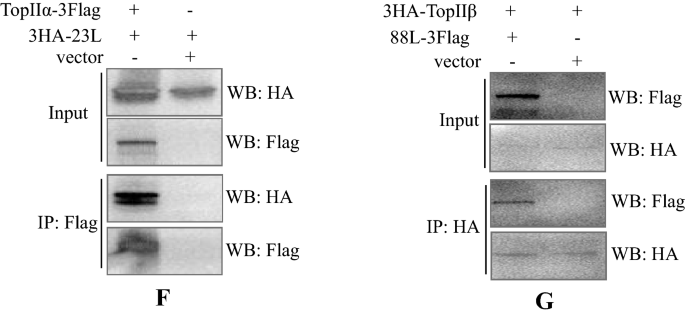
实验目的:解析复制体核心蛋白(vDPOL、vPCNA、vSSB、v解旋酶/引物酶)之间的相互作用,明确复制体的组装机制。方法细节:制备抗v解旋酶/引物酶(ADRV-88L)和vPCNA(ADRV-23L)的多克隆抗体,通过Western blot检测其在感染细胞中的表达时序,通过免疫荧光检测亚细胞定位;通过共免疫沉淀(co-IP)实验检测四种核心蛋白之间的相互作用。结果解读:Western blot显示ADRV-23L在8hpi检测到表达,ADRV-88L在12hpi检测到表达;免疫荧光显示两者均定位在细胞质病毒工厂,与vSSB共定位;co-IP结果显示,vDPOL与vPCNA、vSSB、v解旋酶/引物酶均存在相互作用,v解旋酶/引物酶与vPCNA、vSSB存在相互作用,仅vPCNA与vSSB未检测到相互作用,证明复制体核心蛋白形成复杂的相互作用网络,共同参与病毒DNA复制。实验所用关键产品:pMAL-c5x原核表达载体、anti-HA亲和凝胶、anti-FLAG M2亲和凝胶(Sigma)、Merck horseradish peroxidase标记二抗。
3.5 病毒DNA聚合酶(vDPOL)的相互作用组分析
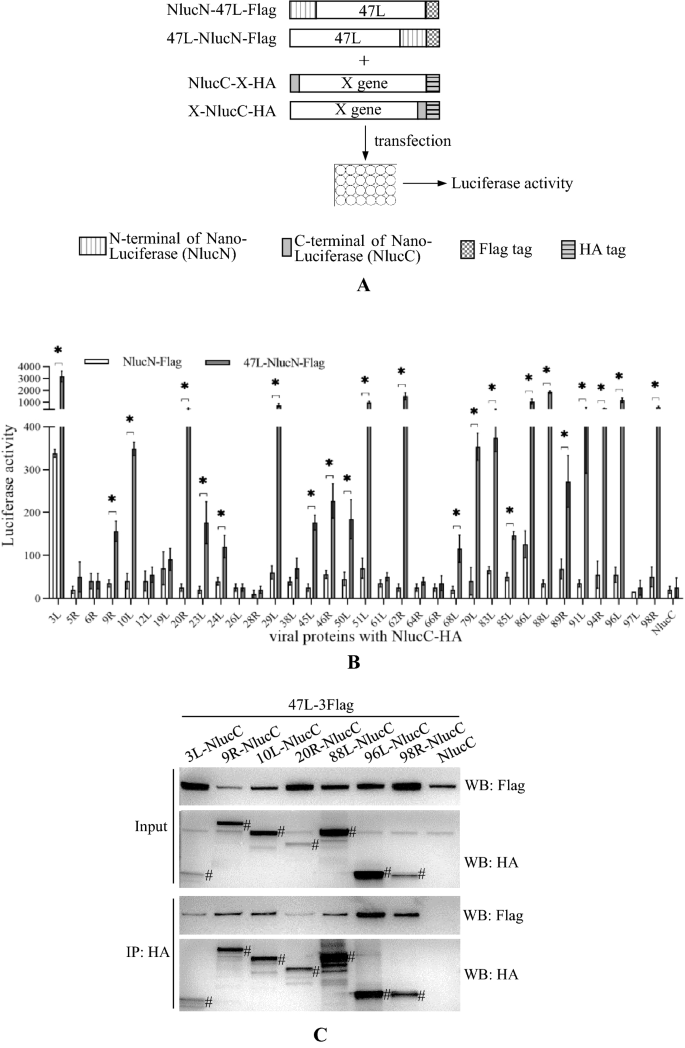
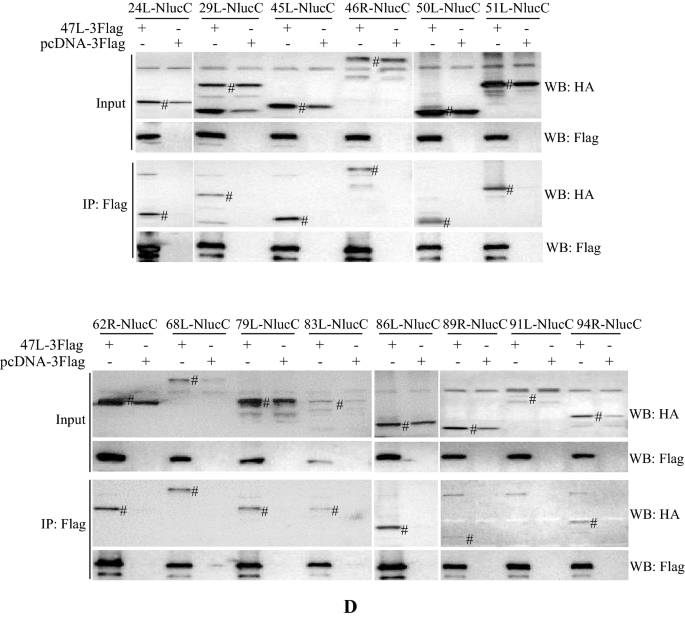
实验目的:系统鉴定与vDPOL相互作用的病毒蛋白,解析其在病毒复制转录中的调控作用。方法细节:采用NanoLuciferase(Nluc)互补实验,将vDPOL与Nluc的N端融合,其他病毒蛋白与Nluc的C端融合,在鲤鱼上皮瘤细胞(EPC)和GSTC细胞中检测荧光素酶活性,筛选相互作用蛋白;随后通过co-IP实验验证筛选到的相互作用。结果解读:Nluc互补实验显示,vDPOL与23种病毒蛋白存在相互作用,包括复制、转录、DNA修饰相关蛋白;co-IP实验进一步验证了其中20种蛋白的相互作用,表明vDPOL不仅是DNA复制的核心酶,还作为调控中心,连接复制、转录及DNA修饰等多个过程,在病毒生命周期中发挥关键作用。实验所用关键产品:Nano-Glo Luciferase Assay Reagent(Promega)、Lipofectamine 3000(Thermo Scientific)、pcDNA3.1载体。
3.6 宿主拓扑异构酶II的功能验证
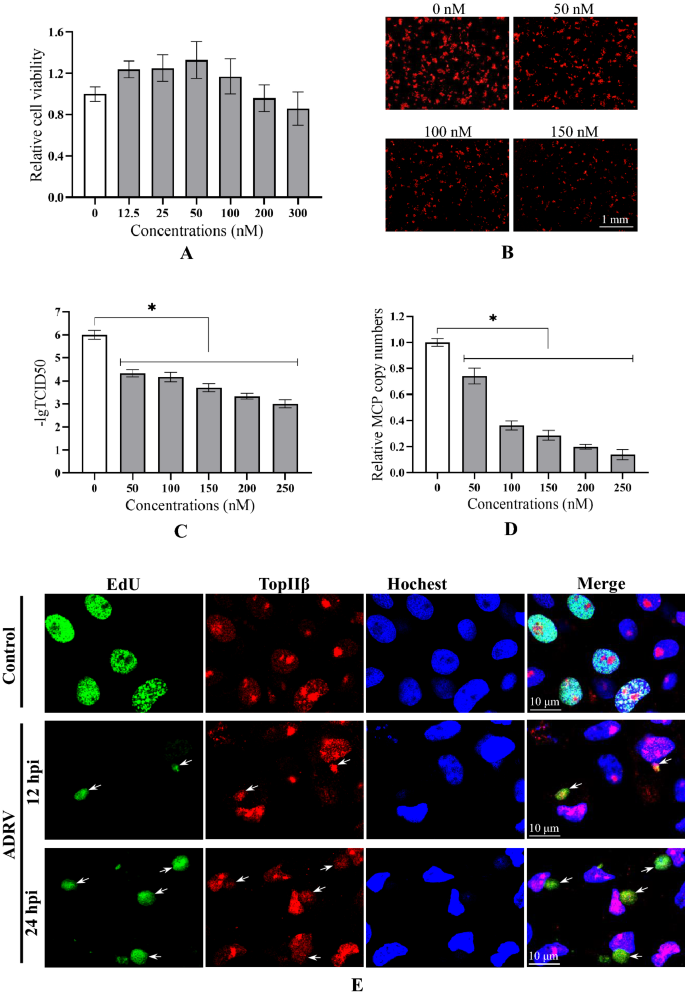
实验目的:验证宿主拓扑异构酶IIα/β在蛙病毒复制中的作用,明确其与病毒蛋白的相互作用。方法细节:用拓扑异构酶II抑制剂阿霉素处理感染ADRV的GSTC细胞,通过半数组织培养感染剂量(TCID50)检测病毒滴度,通过qPCR检测病毒基因组复制水平;通过免疫荧光检测TopIIβ在感染细胞中的亚细胞定位;克隆GSTC细胞的TopIIα/β基因,通过co-IP检测其与病毒蛋白的相互作用。结果解读:阿霉素在非细胞毒性浓度下,显著降低病毒感染率和基因组复制水平,病毒滴度随药物浓度增加而降低(n=3,P<0.05);免疫荧光显示,未感染细胞中TopIIβ定位在细胞核,感染后转移到细胞质病毒工厂,与新生DNA共定位;co-IP显示TopIIα与vPCNA相互作用,TopIIβ与v解旋酶/引物酶相互作用,证明宿主拓扑异构酶II是病毒复制体的核心组分,参与病毒DNA复制过程。实验所用关键产品:阿霉素(MedChemExpress)、anti-topoisomerase II抗体(Abcam,ab109524)、pcDNA3.1-3×Flag载体。
3.7 转录复合物的鉴定与宿主RNAPII亚基的功能验证
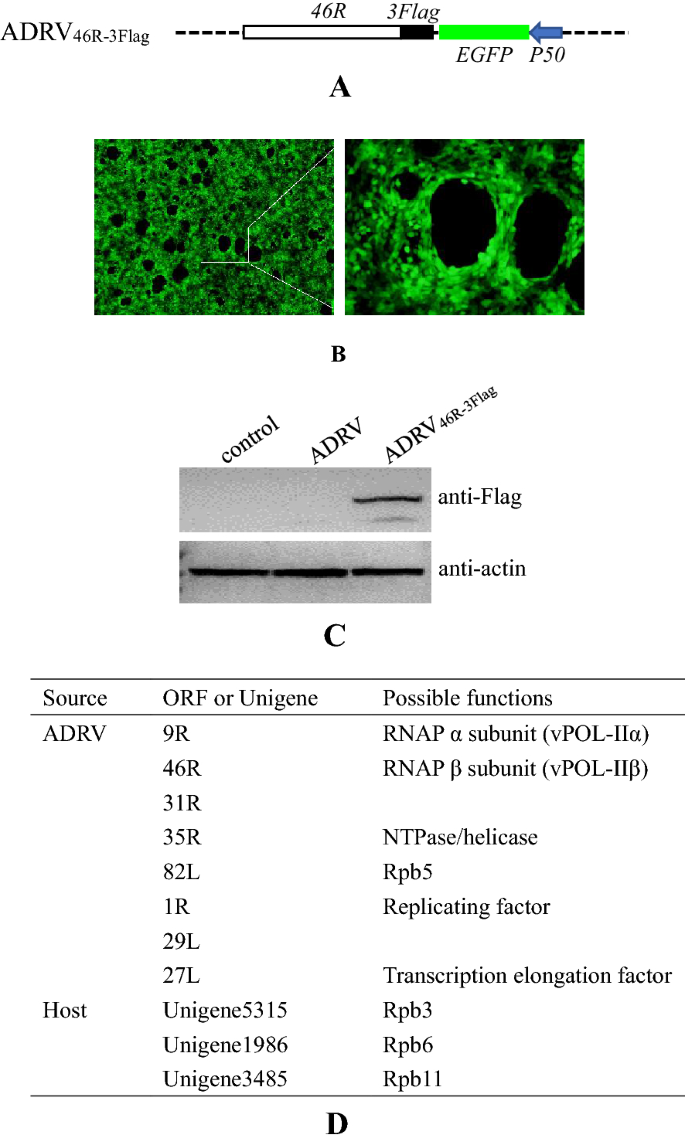
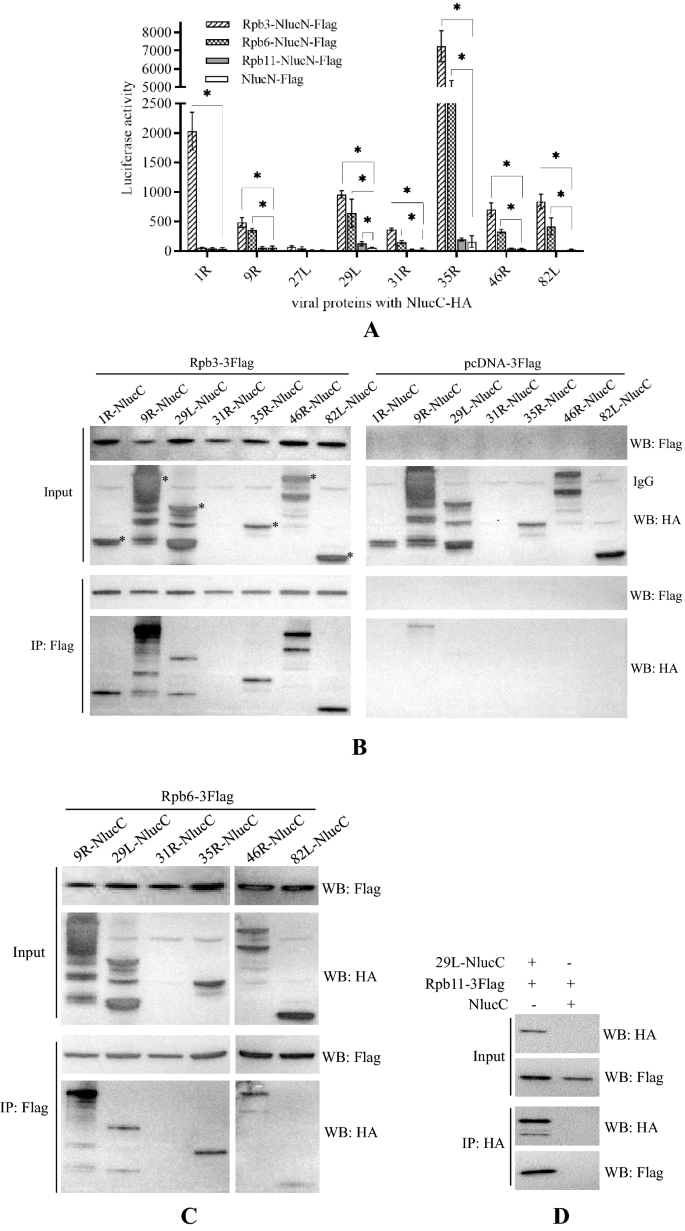
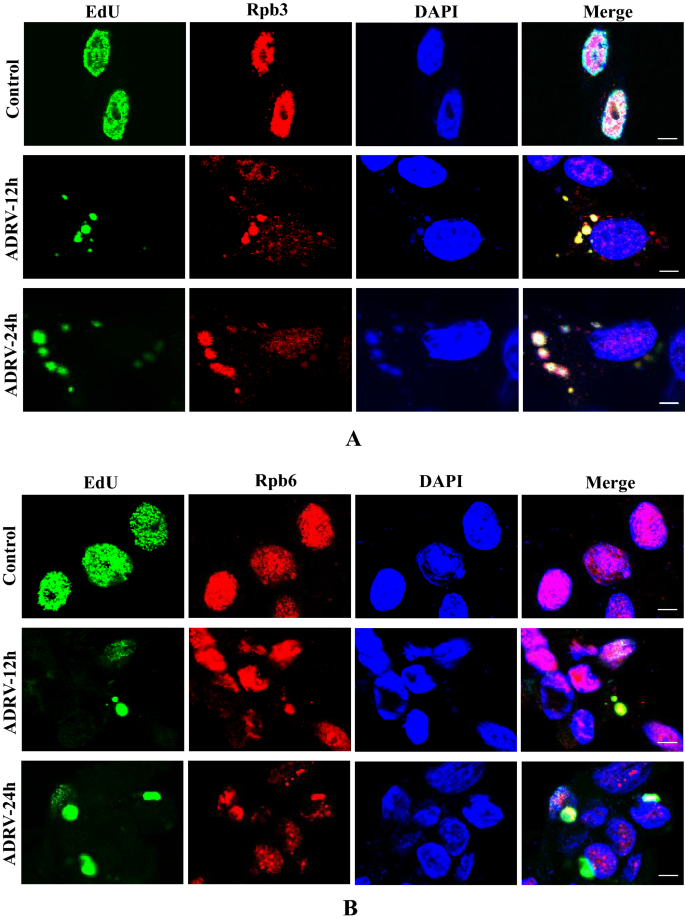
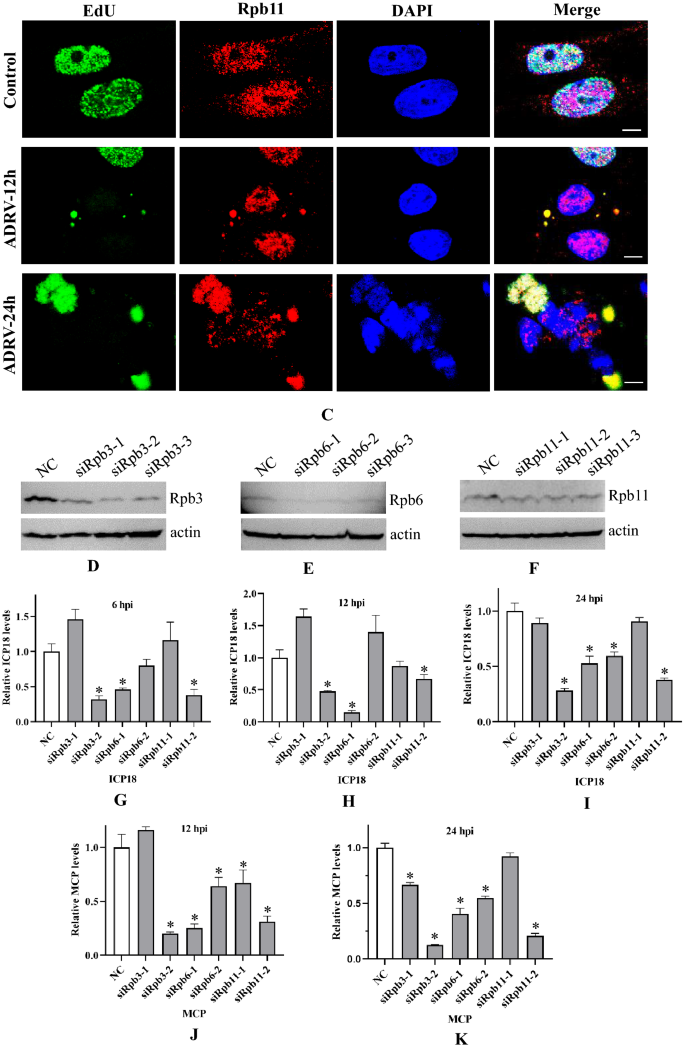
实验目的:鉴定蛙病毒转录复合物的组成,验证宿主RNAPII亚基在病毒转录中的作用。方法细节:构建表达Flag标记的vPOL-IIβ(ADRV-46R)的重组病毒ADRV46R-3Flag,通过亲和纯化结合质谱鉴定转录相关蛋白;克隆宿主Rpb3、Rpb6、Rpb11基因,通过Nluc互补实验和co-IP检测其与病毒蛋白的相互作用;在仓鼠肾成纤维细胞(BHK-21)中通过RNA干扰(RNAi)沉默Rpb3、Rpb6、Rpb11,通过反转录qPCR(RT-qPCR)检测病毒早期基因ICP18和晚期基因MCP的表达水平。结果解读:亲和纯化结合质谱鉴定到8种病毒蛋白和3种宿主RNAPII亚基(Rpb3、Rpb6、Rpb11);Nluc互补实验显示Rpb3与7种病毒蛋白相互作用,Rpb6与6种相互作用,Rpb11与1种相互作用,co-IP实验进一步验证了这些相互作用;RNAi结果显示,沉默Rpb3、Rpb6、Rpb11均显著降低病毒基因的表达水平(n=3,P<0.05),免疫荧光显示这些宿主蛋白在感染后转移到细胞质病毒工厂,与新生DNA共定位,证明宿主RNAPII亚基参与构建病毒转录复合物,是病毒转录的必需组分。实验所用关键产品:重组病毒构建载体pMD18-T、Lipofectamine RNAiMAX(Thermo Fisher)、anti-Rpb3抗体(ABclonal,A1785)、anti-Rpb6/11抗体(Proteintech)。
4. Biomarker研究及发现成果解析
本研究鉴定的蛙病毒复制转录机器核心组分,包括病毒蛋白vDPOL、vPCNA、vSSB、v解旋酶/引物酶及宿主蛋白TopIIα/β、Rpb3/6/11,可作为蛙病毒感染诊断及抗病毒药物研发的潜在功能型Biomarker,为相关研究提供了关键靶点。
Biomarker定位与筛选逻辑
这些Biomarker中,病毒蛋白为蛙病毒特异性表达的核心功能蛋白,宿主蛋白为病毒感染过程中被招募的关键调控蛋白。筛选逻辑为:通过iPOND技术筛选结合新生DNA的蛋白,获得候选Biomarker;随后通过功能实验(如抑制剂处理、RNAi、co-IP)验证其在病毒复制转录中的必需性,明确其功能关联;最终确定核心Biomarker的组成及相互作用网络,构建蛙病毒复制转录的功能架构。
研究过程详述
病毒Biomarker(vDPOL、vPCNA、vSSB、v解旋酶/引物酶)来源于病毒基因组编码,通过原核表达纯化后,经电泳迁移率变动分析、co-IP等实验验证其功能,其中vDPOL作为核心调控因子,与23种病毒蛋白相互作用,连接复制与转录过程;宿主Biomarker(TopIIα/β、Rpb3/6/11)来源于宿主细胞,通过抑制剂实验验证TopIIα/β对病毒复制的必需性,阿霉素处理后病毒滴度降低约50%(n=3,P<0.05);通过RNAi验证Rpb3/6/11对病毒转录的必需性,沉默后病毒晚期基因MCP的表达水平降低约60%(n=3,P<0.05)。这些Biomarker的特异性表现为:病毒蛋白仅在感染细胞中表达,宿主蛋白在感染后发生亚细胞定位变化,从细胞核转移到细胞质病毒工厂,与新生DNA共定位。
核心成果提炼
这些Biomarker的核心功能是构成蛙病毒的复制转录机器,其中vDPOL是关键调控中心,协调复制、转录及DNA修饰等过程;创新性在于首次发现宿主RNAPII亚基参与核质大DNA病毒的转录复合物,拓展了对核质大DNA病毒转录机制的认识;统计学结果显示,所有功能验证实验均为三次独立重复,P<0.05,具有显著统计学意义。这些Biomarker为蛙病毒感染的诊断提供了潜在靶点,也为抗病毒药物的研发提供了新的方向,例如针对vDPOL或TopII的抑制剂,可有效阻断病毒复制。