1. 领域背景与文献引入
文献英文标题:Causal relationship between gut microbiota and myasthenia gravis: a bidirectional mendelian randomization study;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:神经免疫学(重症肌无力)与肠道微生态
重症肌无力是一种以神经肌肉接头受损为核心的自身免疫性疾病,主要表现为肌肉无力,严重者可出现呼吸衰竭,其发病机制涉及乙酰胆碱受体抗体介导的损伤、CD4+T细胞调控异常等多个层面,但目前仍未完全明确遗传与环境因素的交互作用机制。领域共识:肠道菌群作为人体微生态系统的核心组成,可通过调控免疫稳态、代谢通路等影响远端器官功能,已被证实与系统性红斑狼疮、类风湿关节炎等多种自身免疫病密切相关。现有研究已通过观察性研究发现重症肌无力患者存在肠道菌群组成紊乱,如厚壁菌门丰度降低、变形菌门丰度升高,动物实验也显示重症肌无力小鼠的菌群移植可诱导无菌小鼠出现运动功能障碍,但这些研究仅能证明二者存在关联,无法明确因果关系,且存在混杂因素干扰、动物模型外推性有限等局限性。因此,亟需采用可规避混杂与反向因果的研究方法,明确肠道菌群与重症肌无力的双向因果关联,为发病机制解析与治疗靶点开发提供可靠依据。
2. 文献综述解析
本文献综述部分以“重症肌无力发病机制-肠道菌群与自身免疫病关联-现有重症肌无力菌群研究局限性”为核心逻辑展开评述。作者首先系统梳理了重症肌无力的经典发病机制,包括乙酰胆碱受体抗体、抗MUSK抗体等自身抗体的作用,以及CD4+T细胞及其亚型的调控功能,同时指出肠道菌群在自身免疫病中的调控作用已成为研究热点。随后,作者对现有重症肌无力与肠道菌群的研究进行分类总结:观察性研究层面,多项病例对照研究证实重症肌无力患者与健康人群的肠道菌群多样性、组成存在显著差异,如重症肌无力患者梭菌属丰度仅为健康人群的1/3;动物实验层面,菌群移植实验可诱导重症肌无力样症状,但这些研究均存在局限性,观察性研究无法区分因果关系与反向因果,且易受饮食、用药等混杂因素干扰,动物实验结果难以直接外推至人类群体。基于上述研究空白,作者明确本研究的创新价值:首次采用双向两样本孟德尔随机化方法,利用遗传变异作为工具变量,规避混杂因素与反向因果干扰,精准解析肠道菌群与重症肌无力的双向因果关联,填补领域内因果证据缺失的核心空白。
3. 研究思路总结与详细解析
本研究整体框架为“双向两样本孟德尔随机化分析+多方法验证+敏感性分析”的闭环逻辑,核心科学问题是明确肠道菌群与重症肌无力的双向因果关系,研究目标是筛选与重症肌无力存在因果关联的特定肠道菌群分类单元,为发病机制与治疗策略提供新依据。
3.1 研究设计与数据来源
本环节核心目标是建立符合孟德尔随机化要求的研究体系,确保数据的可靠性与人群匹配性。研究采用两样本孟德尔随机化设计,肠道菌群数据来自MiBioGen联盟的全基因组关联分析(GWAS)数据库,涵盖18340名欧洲人群的门、纲、目、科、属水平菌群数据;重症肌无力数据来自FinnGen研究项目,包含426例重症肌无力患者与373848名健康对照,所有研究对象均为欧洲人群,满足孟德尔随机化的人群同质性要求。研究设计流程与孟德尔随机化核心假设如图1所示。
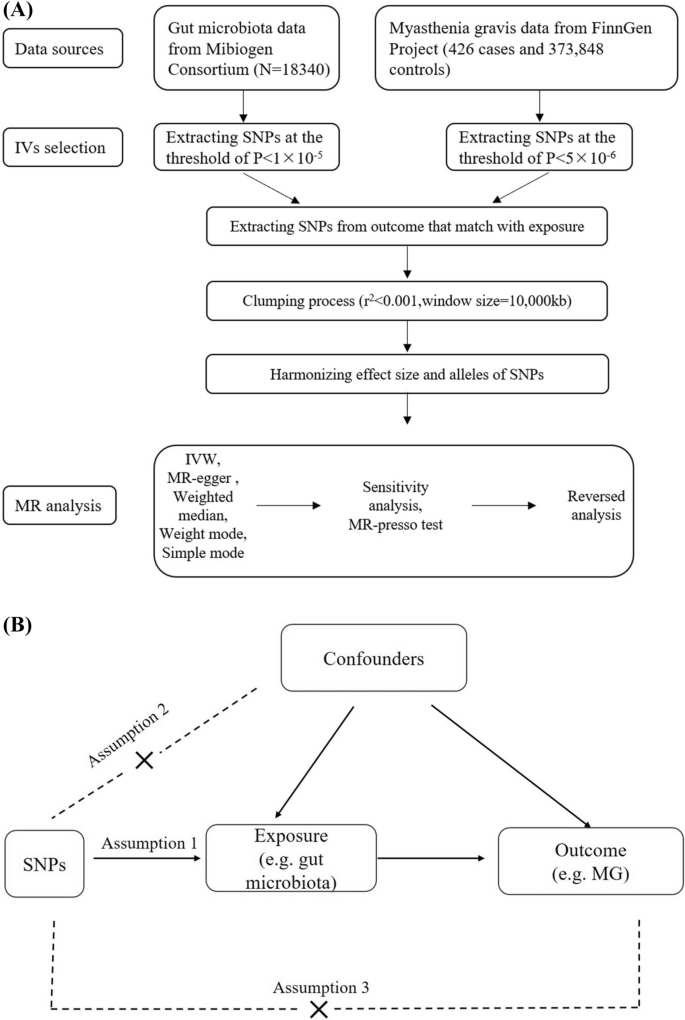
文献未提及具体实验产品,领域常规使用全基因组关联分析(GWAS)公共数据库、R语言统计分析包(如TwoSampleMR、MR-PRESSO)等工具。
3.2 工具变量筛选与有效性验证
本环节核心目标是筛选满足孟德尔随机化三大核心假设的遗传变异作为工具变量(IV),避免弱工具变量干扰。正向分析(肠道菌群→重症肌无力)中,筛选全基因组水平p<1×10^-5的单核苷酸多态性(SNP),通过连锁不平衡分析(r²<0.001,聚类窗口10000kb)确保SNP独立性,校正等位基因 Strand 一致性,计算F统计量验证工具变量强度(F>10为强工具变量);反向分析(重症肌无力→肠道菌群)中,由于仅1个SNP达到全基因组显著性阈值(5×10^-8),故放宽阈值至p<5×10^-6筛选SNP,其余流程与正向分析一致。最终筛选得到的工具变量F统计量均大于10,无弱工具变量,满足孟德尔随机化的核心假设要求。
3.3 双向因果关联分析与验证
本环节核心目标是明确肠道菌群与重症肌无力的双向因果关联,采用多种孟德尔随机化方法交叉验证。正向分析中,以逆方差加权(IVW)法为主要分析方法,结合MR-Egger回归、加权中位数、简单模式、加权模式四种补充方法,结果显示Lachnoclostridium属与重症肌无力风险呈正相关(OR=2.431,95%CI 1.047-5.647,p=0.039),而Clostridiaceae1科(OR=0.424,95%CI 0.202-0.889,p=0.023)、Defluviitaleaceae科(OR=0.537,95%CI 0.290-0.995,p=0.048)、Enterobacteriaceae科(OR=0.341,95%CI 0.135-0.865,p=0.023)及1个未知属(OR=0.407,95%CI 0.209-0.793,p=0.008)与重症肌无力风险呈负相关;反向分析中,IVW法显示重症肌无力与Barnesiella属丰度呈负相关(OR=0.945,95%CI 0.906-0.985,p=0.008),所有补充方法均得到一致结果,因果关联的散点图如图2所示。
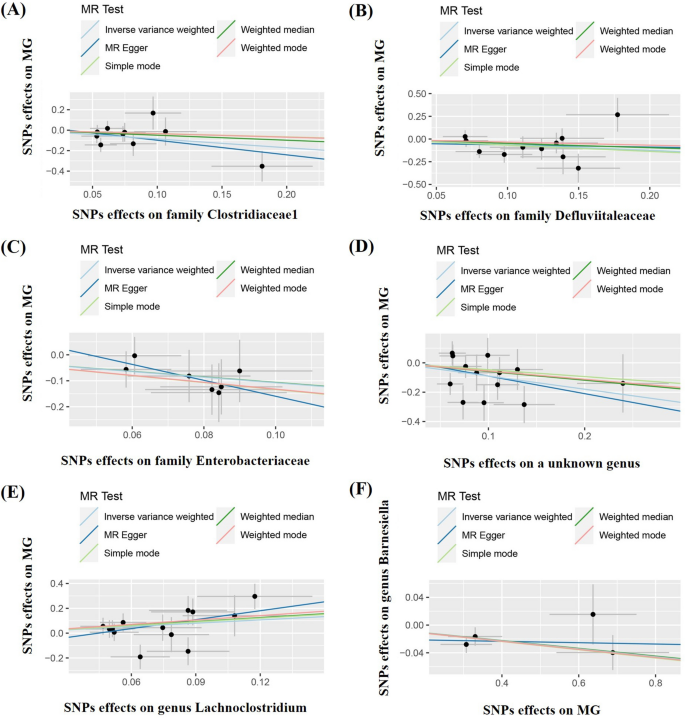
文献未提及具体实验产品,领域常规使用孟德尔随机化统计分析工具、生物信息学分析平台等。
3.4 敏感性分析与结果可靠性验证
本环节核心目标是验证因果关联结果的稳定性,排除异质性、多效性与异常值干扰。采用MR-Egger截距检验评估水平多效性,Cochran"s Q检验评估异质性,MR-PRESSO法检测并校正异常值,留一法分析评估单个SNP对结果的影响。结果显示所有分析的p值均大于0.05,无显著异质性与水平多效性,留一法分析未发现单个SNP可显著影响因果效应估计(图3),进一步证实了研究结果的可靠性。
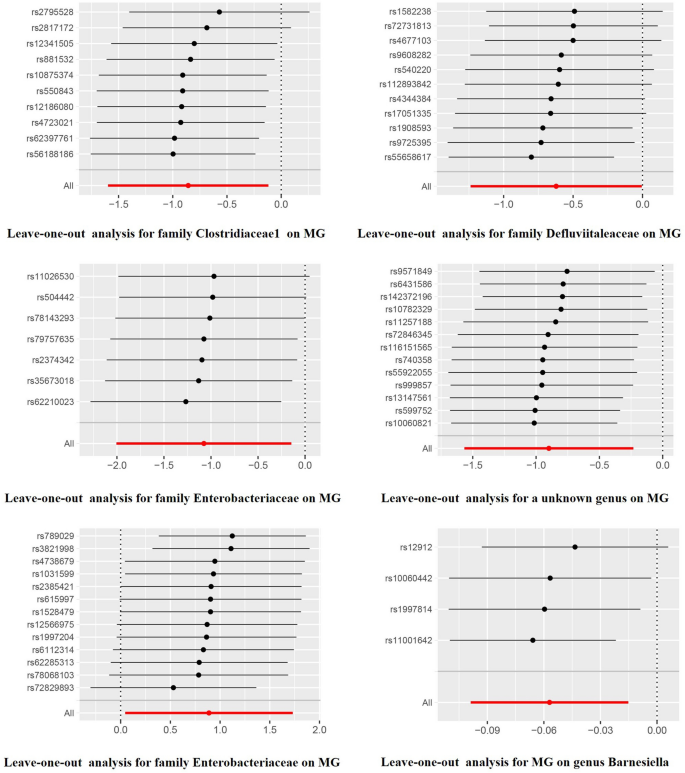
文献未提及具体实验产品,领域常规使用敏感性分析统计方法与工具。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究中涉及的Biomarker为肠道菌群中的特定分类单元,包括Lachnoclostridium属、Clostridiaceae1科、Defluviitaleaceae科、Enterobacteriaceae科、未知属及Barnesiella属。筛选与验证逻辑为:基于大样本GWAS数据库筛选与肠道菌群/重症肌无力相关的遗传变异→通过孟德尔随机化方法验证遗传变异介导的菌群与重症肌无力的因果关联→多方法交叉验证+敏感性分析确认结果可靠性,形成完整的“筛选-验证-确认”链条。
研究过程详述
这些Biomarker的来源为欧洲人群的GWAS数据库,涵盖肠道菌群的科、属水平分类单元。验证方法采用双向两样本孟德尔随机化分析,结合多种统计方法交叉验证:正向分析中,Lachnoclostridium属的因果效应OR值为2.431(95%CI 1.047-5.647,p=0.039),提示其丰度升高可增加重症肌无力风险;Clostridiaceae1科、Defluviitaleaceae科、Enterobacteriaceae科及未知属的OR值均小于1,提示其丰度升高可降低重症肌无力风险;反向分析中,Barnesiella属的OR值为0.945(95%CI 0.906-0.985,p=0.008),提示重症肌无力发病可导致该属丰度降低。所有结果均通过敏感性分析验证,无显著异质性与多效性。
核心成果提炼
本研究首次明确了肠道菌群与重症肌无力的双向因果关联:Lachnoclostridium属是重症肌无力的风险因素,而Clostridiaceae1科、Defluviitaleaceae科、Enterobacteriaceae科及未知属是重症肌无力的保护因素,同时重症肌无力发病可导致Barnesiella属丰度降低。该成果的创新性在于首次采用孟德尔随机化方法规避了混杂因素与反向因果干扰,为肠道菌群在重症肌无力中的调控作用提供了因果证据,突破了现有研究仅能证明关联的局限。此外,研究发现的特定菌群分类单元可作为潜在的重症肌无力发病风险标志物与治疗靶点,为后续机制研究与益生菌/粪菌移植治疗策略开发提供了精准方向。目前暂未获取这些Biomarker的临床诊断特异性与敏感性数据,需进一步开展临床队列研究验证。
