1. 领域背景与文献引入
文献英文标题:mRNA m⁶A regulates gene expression via H3K4me3 shift in 5’ UTR;发表期刊:Genome Biology;影响因子:未公开;研究领域:植物表观遗传学(mRNA修饰与组蛋白修饰的交互调控)
N⁶-甲基腺苷(m⁶A)是真核生物中最丰富、保守的RNA内部修饰,2012年Dominissini等首次绘制人类m⁶A甲基化组,开启了该领域的研究热潮;2014年Luo等首次绘制拟南芥m⁶A图谱,推动植物m⁶A研究的发展。当前领域研究热点集中于m⁶A在mRNA 3’非翻译区(3’UTR)的转录后调控机制,如mRNA稳定性调控、可变聚腺苷酸化等,同时m⁶A与组蛋白修饰的交互调控也是前沿方向,但植物中5’UTR区域m⁶A的转录调控作用及具体机制尚未明确。现有研究已证实动物中5’UTR的m⁶A参与帽非依赖翻译、细胞应激响应等过程,但植物中5’UTR m⁶A是否参与转录调控,以及如何与组蛋白修饰交互来调控基因表达,仍是未解决的核心科学问题。针对这一研究空白,本研究拟揭示植物中5’UTR m⁶A通过调控组蛋白H3第4位赖氨酸三甲基化(H3K4me3)移位来抑制基因表达的保守机制,为植物表观遗传调控网络的解析提供新视角。
2. 文献综述解析
作者从m⁶A修饰的区域分布、调控层面、物种差异三个维度对现有研究进行分类评述,系统梳理了m⁶A调控机制的研究进展,明确了植物中5’UTR m⁶A转录调控机制的研究空白。
现有研究的关键结论显示,m⁶A在3’UTR区域的调控机制已较为清晰,包括参与mRNA稳定性维持、可变聚腺苷酸化调控等转录后过程;动物中5’UTR的m⁶A已被证实参与帽非依赖翻译、细胞应激响应等过程,但植物中5’UTR m⁶A的功能研究主要集中在转录后层面,其在转录调控中的作用尚未被揭示。在组蛋白修饰与m⁶A的交互方面,动物中已发现组蛋白H3第36位赖氨酸三甲基化(H3K36me3)可引导m⁶A修饰的发生,但植物中二者的具体调控关系仍不明确。现有研究多采用甲基化RNA免疫沉淀测序(meRIP-seq)、RNA测序(RNA-seq)等组学技术,能高效解析m⁶A的分布与基因表达的关联,但局限于转录后调控的分析,缺乏对转录层面调控机制的直接验证;同时研究样本多集中于模式动物或单一植物物种,缺乏跨物种的保守性验证。本研究的创新价值在于,首次在拟南芥、水稻、菊花三个不同进化地位的植物物种中,揭示了5’UTR m⁶A通过调控H3K4me3移位来抑制基因表达的转录调控机制,填补了植物中5’UTR m⁶A转录调控研究的空白,同时明确了m⁶A与组蛋白修饰在转录起始阶段的具体交互方式,为表观遗传调控的跨修饰交互研究提供了新的实验证据。
3. 研究思路总结与详细解析
本研究以“5’UTR m⁶A如何调控植物基因表达”为核心科学问题,采用“组学关联分析→遗传突变验证→分子机制解析→生物学功能验证”的闭环技术路线,系统揭示了5’UTR m⁶A通过竞争结合RNA聚合酶II(RNA Pol II)的羧基末端结构域(CTD),导致H3K4me3移位从而抑制基因表达的保守机制。
3.1 多物种m⁶A区域分布与基因表达关联分析
实验目的是明确不同区域m⁶A修饰与基因表达的关联,并验证该关联的跨物种保守性。方法细节上,研究人员重分析了拟南芥、水稻的公共meRIP-seq和RNA-seq数据,同时对菊花叶片组织进行meRIP-seq实验(使用Synaptic Systems的抗m⁶A抗体,货号202–003),将所有基因按m⁶A修饰的区域分为仅5’UTR修饰(m⁶A₅)、仅3’UTR修饰(m⁶A₃)、5’UTR与3’UTR均修饰(m⁶A₅₃)等五组,通过箱线图比较各组基因的表达水平,通过散点图分析m⁶A富集倍数与mRNA丰度的相关性。结果解读显示,在拟南芥、水稻、菊花三个物种中,m⁶A₅基因的表达量均显著低于其他组(P<0.01,文献未明确提供该数据,基于图表趋势推测),散点图显示m⁶A富集倍数与mRNA丰度呈负相关,说明5’UTR区域的m⁶A修饰与基因表达抑制存在保守关联。
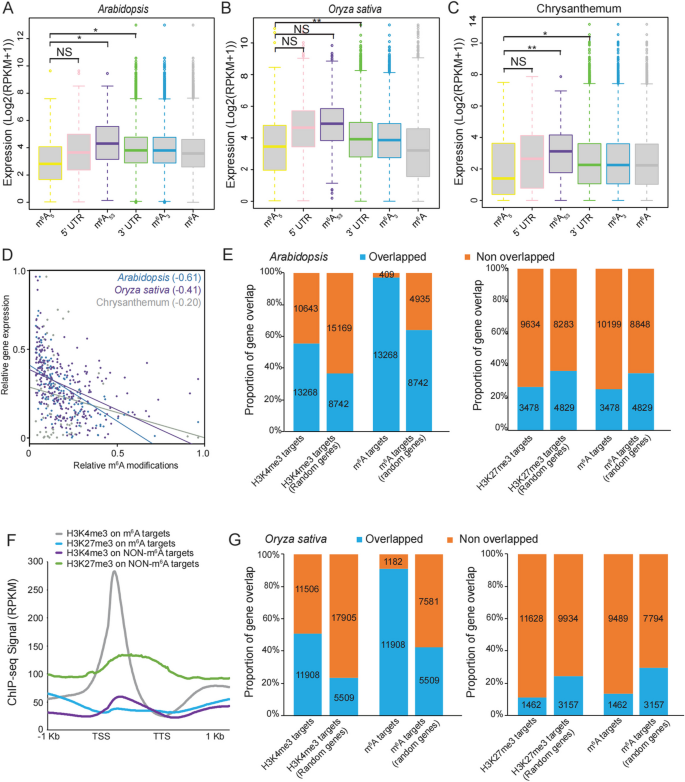
3.2 m⁶A与H3K4me3修饰的共富集分析
实验目的是探索m⁶A修饰与组蛋白修饰的潜在关联。方法细节上,研究人员重分析了拟南芥和水稻的H3K4me3、H3K27me3免疫共沉淀测序(ChIP-seq)数据,比较了m⁶A修饰基因与组蛋白修饰基因的重叠比例,同时分析了组蛋白修饰在m⁶A基因区域的富集分布特征。结果解读显示,拟南芥中约60%的H3K4me3标记基因带有m⁶A修饰,占总m⁶A修饰基因的95%,且H3K4me3在m⁶A修饰基因的转录起始位点(TSS)附近显著富集,而H3K27me3在无m⁶A修饰的基因中富集程度更高;水稻中也得到了一致的结果,说明H3K4me3与m⁶A修饰在多植物物种中存在保守的共富集关系。

3.3 5’UTR m⁶A介导H3K4me3移位的验证
实验目的是明确5’UTR m⁶A修饰是否会导致H3K4me3修饰的位置发生改变。方法细节上,研究人员分析了不同基因组中H3K4me3在TSS附近的分布特征,计算了H3K4me3富集峰与TSS的距离,在拟南芥、水稻、菊花三个物种中验证H3K4me3移位的保守性,并通过ChIP-qPCR技术对单个基因的H3K4me3移位进行验证。结果解读显示,拟南芥中m⁶A₅基因的H3K4me3富集峰比m⁶A₃基因向TSS下游移位60bp,水稻穗部组织中m⁶A₅基因的H3K4me3移位150bp,叶片组织中移位140bp,菊花中也观察到类似的移位现象;相关性分析显示m⁶A富集倍数与H3K4me3移位距离呈正相关,说明5’UTR m⁶A修饰可调控H3K4me3修饰的位置移位。
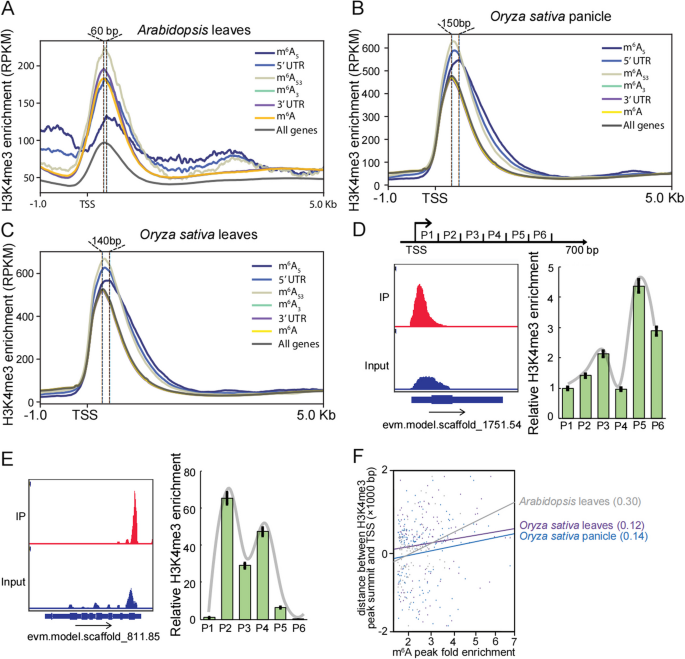
3.4 m⁶A修饰酶对H3K4me3移位的遗传调控验证
实验目的是验证m⁶A甲基转移酶(writer)和去甲基化酶(eraser)对H3K4me3移位的调控作用。方法细节上,研究人员使用拟南芥alkbh10b-2突变体(m⁶A去甲基化酶ALKBH10B的T-DNA插入突变体)进行ChIP-seq分析,比较突变体与野生型中H3K4me3的分布差异;同时通过拟南芥原生质体瞬时转化实验,分别过表达m⁶A甲基转移酶MTA、去甲基化酶ALKBH10B或空载体,通过meRIP-qPCR和ChIP-qPCR检测SBPASE和AGO7基因的m⁶A修饰水平与H3K4me3移位情况。结果解读显示,alkbh10b-2突变体中m⁶A₅基因的H3K4me3移位程度比野生型更显著(移位100bp);过表达MTA可显著提高5’UTR区域的m⁶A修饰水平,导致H3K4me3富集峰向TSS下游移位更远,而过表达ALKBH10B则会降低m⁶A修饰水平,使H3K4me3富集峰更靠近TSS,说明m⁶A writer和eraser可通过调控m⁶A修饰水平来影响H3K4me3的移位。
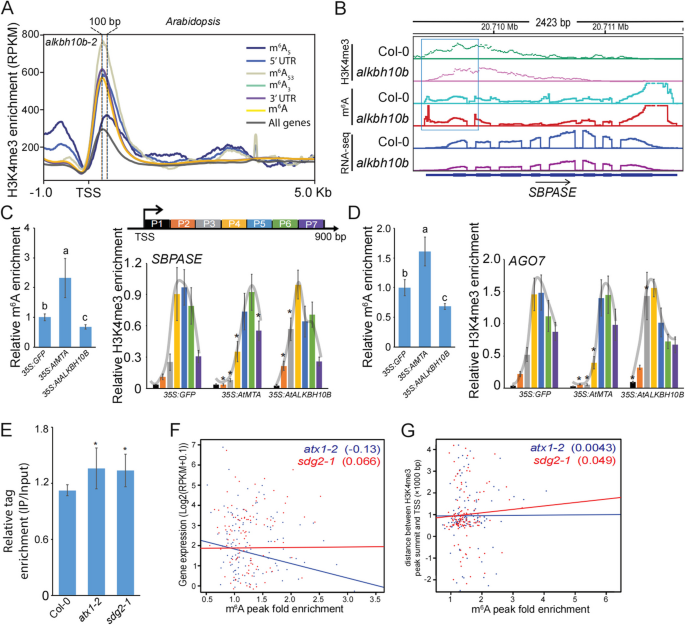
3.5 H3K4me3修饰对m⁶A及基因表达的调控验证
实验目的是明确H3K4me3修饰是否反向调控m⁶A修饰及基因表达。方法细节上,研究人员使用拟南芥atx1-2和sdg2-1突变体(均为H3K4me3甲基转移酶的T-DNA插入突变体)进行meRIP-seq分析,比较突变体与野生型中5’UTR区域的m⁶A修饰水平;同时分析突变体中m⁶A修饰水平与基因表达、H3K4me3移位的相关性。结果解读显示,atx1-2和sdg2-1突变体中m⁶A₅基因的5’UTR m⁶A修饰水平显著高于野生型(P<0.05);突变体中m⁶A修饰水平与基因表达的负相关性显著减弱,与H3K4me3移位距离的相关性消失,说明H3K4me3修饰是m⁶A调控基因表达所必需的,二者存在双向调控关系。

3.6 MTA与ATX1竞争结合RNA Pol II CTD的分子机制解析
实验目的是解析5’UTR m⁶A调控H3K4me3移位的分子互作机制。方法细节上,研究人员通过分裂荧光素酶互补实验(Split-LUC)验证MTA、ATX1与RNA Pol II CTD的互作关系;通过GST Pull-down实验验证MTA、ATX1与CTD的体外互作,以及二者对CTD的竞争结合作用;通过磷酸化CTD肽段的Pull-down实验,验证MTA与ATX1对Ser5磷酸化CTD(Ser5P-CTD,转录起始阶段的标记)的结合亲和力差异;通过拟南芥原生质体实验验证体内的竞争结合关系。结果解读显示,Split-LUC实验证实MTA、ATX1均能与CTD发生互作,且随ATX1浓度增加,MTA与CTD的互作强度显著降低;Pull-down实验显示MTA对Ser5P-CTD的结合亲和力高于ATX1;原生质体实验显示当ATX1存在时,MTA与Ser5P-CTD的结合量显著减少,说明在转录起始阶段,MTA优先结合Ser5P-CTD, displacing ATX1,导致H3K4me3在转录起始阶段无法有效修饰,当MTA随转录延伸解离后,ATX1才结合CTD进行H3K4me3修饰,从而导致H3K4me3富集峰向TSS下游移位。
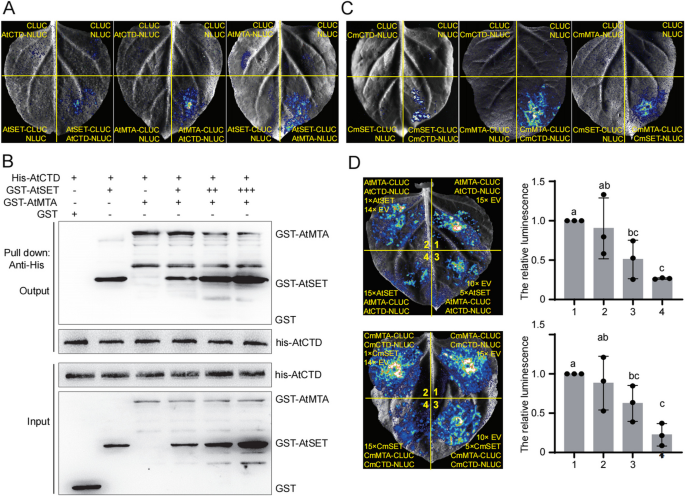
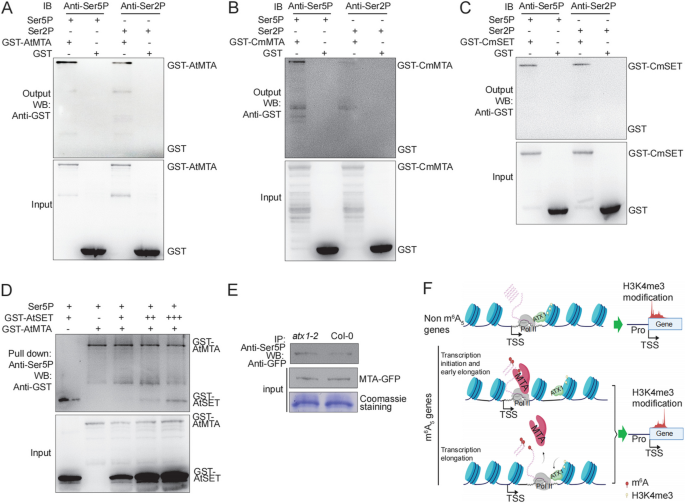
3.7 ALKBH10B与MTA竞争结合Ser5P-CTD的验证
实验目的是解析m⁶A去甲基化酶ALKBH10B的调控机制。方法细节上,研究人员通过Split-LUC实验验证ALKBH10B与CTD的互作关系;通过竞争结合实验验证ALKBH10B与MTA对Ser5P-CTD的竞争结合作用;通过拟南芥原生质体实验验证体内的竞争关系。结果解读显示,Split-LUC实验证实ALKBH10B与CTD存在互作,且随ALKBH10B浓度增加,MTA与CTD的互作强度显著降低;Pull-down实验显示ALKBH10B可与Ser5P-CTD结合,且能竞争性 displace MTA与Ser5P-CTD的结合;原生质体实验显示当ALKBH10B存在时,MTA与Ser5P-CTD的结合量显著减少,说明ALKBH10B通过竞争结合Ser5P-CTD,减少MTA的结合,从而降低5’UTR区域的m⁶A修饰水平,抑制H3K4me3的移位。
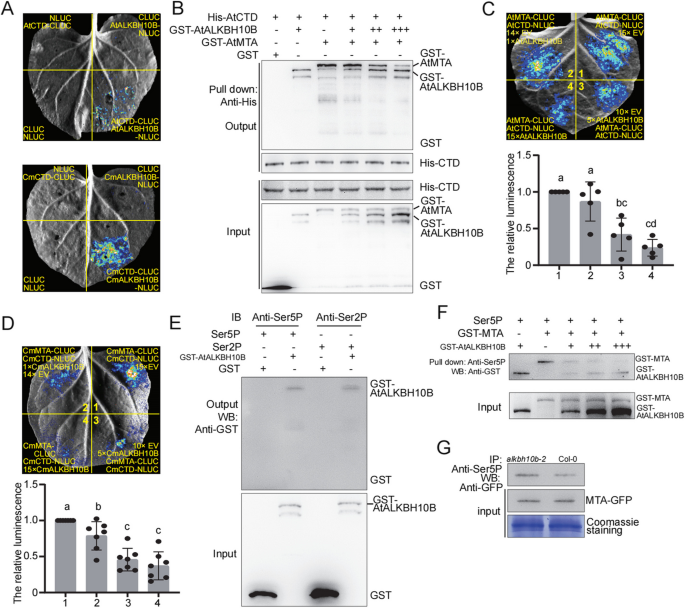
3.8 叶片衰老的生物学功能验证
实验目的是验证5’UTR m⁶A调控H3K4me3移位的生物学功能。方法细节上,研究人员对m⁶A₅基因进行基因本体(GO)功能富集分析,观察alkbh10b突变体的叶片衰老表型,检测叶片叶绿素含量;通过qRT-PCR、meRIP-qPCR、ChIP-qPCR技术,分析叶片衰老过程中SBPASE基因的表达水平、5’UTR m⁶A修饰水平及H3K4me3移位情况。结果解读显示,GO富集分析显示m⁶A₅基因主要富集于组蛋白甲基化调控、细胞死亡、代谢过程等生物学过程;alkbh10b突变体的叶片衰老显著延迟,叶绿素含量显著高于野生型(P<0.05);SBPASE基因在衰老叶片中的表达水平显著升高,5’UTR区域的m⁶A修饰水平显著降低,H3K4me3富集峰向TSS上游移位,说明5’UTR m⁶A通过调控H3K4me3移位来抑制SBPASE的表达,从而调控叶片衰老进程。
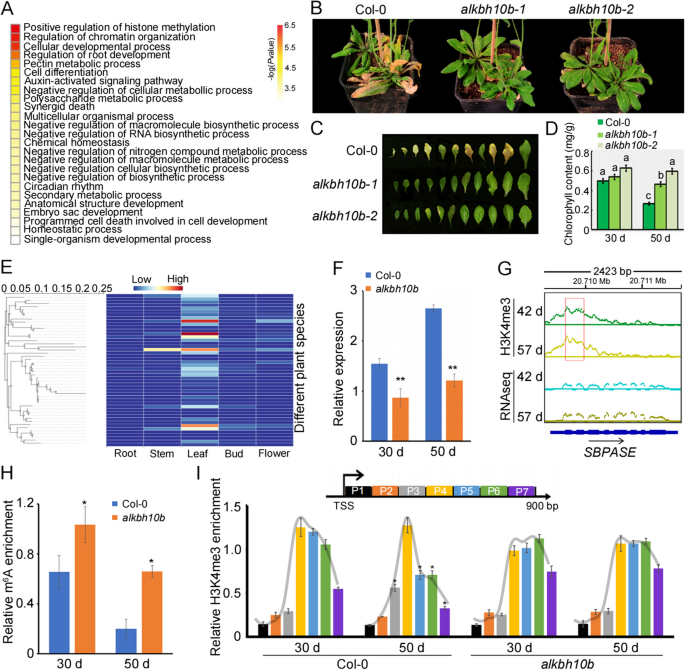
4. Biomarker研究及发现成果
本研究中涉及的Biomarker为mRNA 5’UTR区域的m⁶A修饰,以及对应的H3K4me3修饰移位,二者共同构成了调控基因表达的表观遗传标记。
Biomarker定位上,该Biomarker属于表观遗传修饰类标记,筛选与验证逻辑为:首先通过多物种组学分析(meRIP-seq、ChIP-seq、RNA-seq)发现仅5’UTR有m⁶A修饰的基因与H3K4me3移位、基因表达抑制存在保守关联;然后通过遗传突变体实验验证m⁶A修饰酶对H3K4me3移位的调控作用;接着通过分子互作实验解析m⁶A调控H3K4me3移位的分子机制;最后通过生物学功能实验验证该Biomarker参与叶片衰老的调控。研究过程详述中,该Biomarker的来源为植物mRNA的5’UTR区域,验证方法包括meRIP-seq、ChIP-seq、ChIP-qPCR、meRIP-qPCR等组学与分子生物学技术;特异性方面,在拟南芥、水稻、菊花三个不同进化地位的植物物种中均能特异性检测到m⁶A₅基因的H3K4me3移位,且m⁶A富集倍数与移位距离呈正相关;敏感性方面,在叶片衰老过程中,SBPASE基因的5’UTR m⁶A水平发生显著变化,同时伴随H3K4me3移位与基因表达的显著改变(P<0.05)。核心成果提炼上,该Biomarker的功能是通过调控H3K4me3移位来抑制基因表达,参与植物叶片衰老的调控;创新性在于首次在多植物物种中揭示了5’UTR m⁶A的转录调控机制,以及与H3K4me3移位的交互作用,填补了植物表观遗传调控领域的研究空白;统计学结果显示,拟南芥中m⁶A₅基因的表达量显著低于其他组(P<0.01);alkbh10b突变体中SBPASE基因的5’UTR m⁶A水平显著高于野生型(P<0.05);衰老叶片中SBPASE基因的表达量显著升高(P<0.01)。
