1. 领域背景与文献引入
文献英文标题:Filling the gap: Micro-C accesses the nucleosomal fiber at 100–1000 bp resolution;发表期刊:Genome Biology;影响因子:未公开;研究领域:染色体构象捕获与染色质纤维精细结构研究
2002年染色体构象捕获(3C)技术问世,开启了基因组三维结构研究的新时代,后续衍生的全基因组技术Hi-C实现了基因组尺度的构象分析,在过去十年间为真核与原核基因组的组织原则提供了重要的机械和功能见解,解析了基因环、自接触富集的染色体结构域、大型调控环等多种染色质结构。但传统3C/Hi-C技术存在核心局限性:限制酶切位点在染色体上的分布不均,受GC含量和重复序列影响呈泊松分布,小片段的交联捕获效率远低于大片段,即使使用4碱基切割酶也无法在全基因组实现1kb以下的分辨率,导致核小体纤维的体内精细结构长期无法被解析,成为领域研究的盲区。为填补这一空白,Hsieh等研究者开发了基于微球菌核酸酶(Mnase)的新型染色体构象捕获技术Micro-C,并在酿酒酵母中开展应用研究,本文作为研究亮点文章系统综述并解析了该技术的创新价值与核心成果。
2. 文献综述解析
本文作为研究亮点文章,核心评述逻辑围绕“传统技术局限→新型技术创新→研究成果突破”的主线展开,对现有染色体构象捕获技术进行了分类总结。首先,传统3C衍生技术(3C、Hi-C)的优势在于能够解析基因组尺度的染色质相互作用与大尺度结构,为基因组组织的功能关联提供了重要依据;但这类技术的核心局限性是分辨率受限于酶切位点分布与片段捕获效率,无法突破1kb的分辨率瓶颈,无法触及核小体水平的精细结构,这一盲区长期阻碍了染色质纤维体内结构的研究。针对这一未解决的核心问题,Micro-C技术创新性地采用Mnase替代限制酶,利用核小体在DNA上的规则间距(酵母中为167bp),消化核小体间的连接DNA,实现了100-1000bp的高分辨率,首次将染色体构象捕获的分辨率推进到核小体水平,填补了领域内长期存在的技术盲区,为染色质纤维的体内结构研究提供了全新工具。同时,文章指出Micro-C与传统3C技术具有互补性,前者更聚焦于局部核小体间的相互作用,而后者更适合解析大尺度基因组结构。
3. 研究思路总结与详细解析
本文作为研究亮点文章,系统介绍了Hsieh等团队的核心研究:针对传统3C/Hi-C技术的分辨率盲区,开发并应用Micro-C高分辨率染色体构象捕获技术,在酿酒酵母中解析核小体水平的染色质纤维结构,验证染色质纤维模型,探究影响染色质压缩的分子机制;核心科学问题是如何突破传统构象捕获技术的分辨率限制,解析核小体纤维的体内精细结构与调控机制;技术路线遵循“技术创新→结构解析→模型验证→机制探究”的闭环逻辑。
3.1 Micro-C技术体系构建与应用
实验目的是Hsieh等为突破传统3C技术的分辨率限制,开发能够解析核小体水平染色质结构的新型构象捕获方法。方法细节为:先通过甲醛固定酿酒酵母细胞,使染色质相互作用交联,然后使用微球菌核酸酶(Mnase)消化核小体之间的可及连接DNA,替代传统3C中的限制酶切步骤,后续进行常规构象捕获的连接、纯化与高通量测序分析。结果解读是该技术实现了100-1000bp的分辨率,在酿酒酵母中检测到由1-5个连续基因组成的拓扑结构域,这类结构与细菌中的染色体相互作用域(CID)、哺乳动物中的拓扑关联域(TAD)具有相似性,且Micro-C检测到的长程或染色体间相互作用远少于传统3C(如未检测到着丝粒-着丝粒接触),说明其更聚焦于核小体水平的局部相互作用。产品关联:文献未提及具体实验产品,领域常规使用甲醛固定液、微球菌核酸酶(Mnase)、T4 DNA连接酶、高通量测序平台等试剂与仪器。
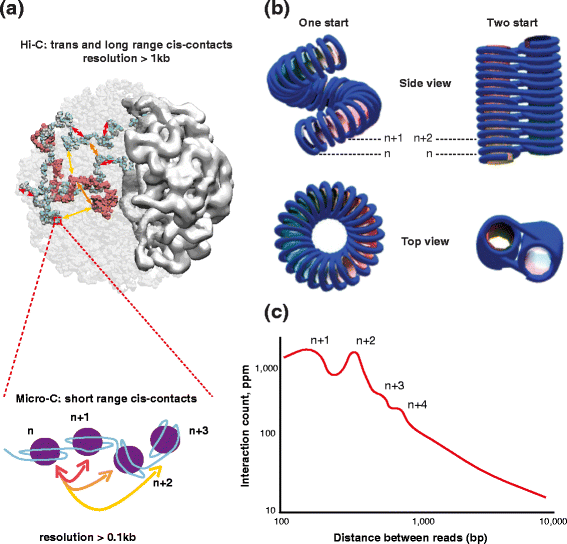
3.2 核小体纤维结构模型验证
实验目的是Hsieh等为评估现有酵母核小体纤维结构模型的合理性,明确体内染色质纤维的真实构象。方法细节为:通过Micro-C实验检测全基因组范围内核小体间的接触频率,重点统计相邻核小体(n与n+1)及间隔一个核小体的核小体(n与n+2)之间的接触数,并分析接触频率的周期性特征。结果解读是实验检测到n与n+1、n与n+2核小体的接触数大致相当,与两种经典核小体纤维模型(柱状堆叠排列、锯齿状排列)均兼容,提示体内染色质纤维可能处于两种结构的动态平衡状态,或不存在高度结构化的稳定纤维;同时未检测到4-6个核小体间距的周期性接触,说明即使存在柱状结构,也未进一步折叠为高阶周期性结构。产品关联:文献未提及具体实验产品,领域常规使用高通量测序数据分析软件(如Hi-C-Pro、Juicer等)进行接触矩阵分析。
3.3 染色质压缩调控机制探究
实验目的是Hsieh等为解析影响染色质压缩水平的分子因素,明确染色质结构与转录活性的关联。方法细节为:首先定义染色质压缩水平为长程接触与短程接触(<300bp)的比值,分析全基因组基因压缩水平与转录活性的相关性;随后在23个染色质结构相关的酿酒酵母突变体中进行Micro-C实验,检测突变体中基因压缩水平的变化;同时使用组蛋白H4变体验证组蛋白修饰对核小体折叠的影响。结果解读是基因压缩水平与转录活性呈负相关,高转录活性基因的压缩水平显著降低,二酰胺处理后上调的基因压缩水平也明显下降,提示转录过程可能通过RNA聚合酶的作用局部破坏核小体纤维;突变体实验显示,RSC染色质重塑复合物和黏连蛋白复合物缺陷会导致基因压缩水平升高,而Mediator或组蛋白去乙酰化酶Rpd3缺陷则导致压缩水平显著降低,且组蛋白H4 N端尾巴对核小体阵列折叠具有重要调控作用。产品关联:文献未提及具体实验产品,领域常规使用酵母基因敲除菌株库、qRT-PCR试剂盒等进行转录活性验证。
3.4 基因环结构的重新评估
实验目的是Hsieh等为验证传统3C技术发现的启动子-终止子基因环结构是否存在于核小体水平。方法细节为:通过Micro-C高分辨率数据检测基因启动子与终止子区域的接触频率。结果解读是未在Micro-C数据中检测到明显的基因环结构,但转录调控蛋白Ssu72(此前被认为是基因环形成的关键因子)突变会导致基因压缩水平轻微但显著降低,提示传统3C检测到的基因环可能需要从染色质可及性等角度重新评估。产品关联:文献未提及具体实验产品,领域常规使用基因组浏览器(如IGV)进行局部接触信号可视化分析。
4. Biomarker研究及发现成果解析
本文中涉及的Biomarker为“染色质压缩水平(长程/短程接触比值)”,作为反映染色质结构状态与转录活性关联的功能性特征,其筛选与验证逻辑基于高分辨率Micro-C技术的全基因组接触分析。
Biomarker定位:染色质压缩水平属于表观遗传结构特征,筛选与验证逻辑为“Micro-C全基因组接触检测→压缩比计算→与转录活性关联分析→突变体功能验证”,完整覆盖了从检测到功能关联的验证链条。研究过程详述:该Biomarker的来源为酿酒酵母的全基因组染色质样本,验证方法包括Micro-C实验检测染色质接触频率、转录组分析关联转录活性、突变体实验验证调控因素;特异性与敏感性方面,高转录活性基因的压缩水平显著降低,二酰胺处理后转录上调的基因压缩水平同步下降,但文献未明确提供ROC曲线、敏感性、特异性的具体数值。核心成果提炼:染色质压缩水平可作为转录活性的关联特征,其调控涉及RSC重塑复合物、黏连蛋白、Mediator、Rpd3去乙酰化酶及组蛋白H4 N端尾巴等多个分子;创新性在于首次通过高分辨率技术揭示了核小体水平的染色质结构域及压缩调控机制,为染色质结构与功能的关联研究提供了新视角;统计学结果方面,突变体中的压缩水平变化具有显著性,但文献未明确提供具体P值、样本量及置信区间数据。
