1. 领域背景与文献引入
文献英文标题:Modified cell cycle status in a mouse model of altered neuronal vulnerability (slow Wallerian degeneration; Wld s);发表期刊:Genome Biology;影响因子:未公开;研究领域:神经退行性疾病与细胞周期调控
神经退行性疾病(如阿尔茨海默病、多发性硬化、运动神经元病等)的发病机制中,轴突和突触等非胞体神经元结构的损伤是疾病起始和进展的核心环节,但目前对这些结构独立的退行性调控机制仍处于研究初期。慢沃勒变性(Wld^s)突变是探索神经元脆弱性调控机制的重要实验工具,该突变能在多种创伤和疾病刺激下延迟轴突和突触的退化,但其神经保护作用的具体机制存在广泛争议。现有研究表明Wld^s可通过多条下游通路发挥作用,包括提升烟酰胺腺嘌呤二核苷酸(NAD)水平、修饰泛素-蛋白酶体系统的定位与活性、改变垂体肿瘤转化基因1(Pttg1)等基因的表达水平,但这些通路研究相对独立,缺乏统一的核心调控机制假说,且部分结论存在矛盾(如Pttg1的mRNA与蛋白表达变化趋势不一致)。针对这一领域空白,本研究旨在探索Wld^s下游的分散变化是否共同作用于细胞周期调控,通过统一的机制假说整合现有研究,揭示神经元脆弱性与细胞周期状态的关联,为神经退行性疾病的保护策略提供新的理论基础。
2. 文献综述解析
作者对Wld^s相关领域现有研究的分类维度为下游调控通路类型,具体分为NAD代谢通路、泛素-蛋白酶体系统通路、基因表达调控通路三类。现有研究的关键结论显示,Wld^s嵌合基因中的烟酰胺单核苷酸腺苷转移酶1(Nmnat1)可通过提升NAD水平激活Sirt1通路,部分调控轴突退化进程;Wld^s能结合含缬酪肽蛋白(VCP/p97),改变泛素-蛋白酶体系统的亚细胞定位与活性;基因组和蛋白质组学研究发现Wld^s可调控包括Pttg1在内的多种基因表达水平。技术方法上,现有研究利用Wld^s突变小鼠模型和细胞系,结合基因组芯片、蛋白质组学等多组学技术,能在体内外系统解析神经保护机制,但各通路研究相对独立,未形成统一的调控网络,且部分实验结论存在矛盾,如Pttg1的mRNA表达被显著下调,但蛋白表达水平却呈现上调趋势。本研究的创新价值在于首次提出Wld^s下游的多种分散变化均汇聚于细胞周期状态的改变,通过细胞周期调控这一核心机制整合现有研究的碎片化结论,为Wld^s的神经保护作用提供了统一的解释框架,解决了现有研究中通路分散、机制矛盾的问题。
3. 研究思路总结与详细解析
本研究的整体框架为:以“Wld^s是否通过调控细胞周期状态改变神经元脆弱性”为核心研究目标,聚焦“Wld^s下游NAD、Pttg1/泛素激活酶E1(Ube1)、VCP通路是否共同介导细胞周期变化,以及细胞周期改变与神经元保护的功能关联”这一核心科学问题,采用“现象发现-通路验证-功能关联”的闭环技术路线,先通过体内外实验检测Wld^s对细胞周期基因和蛋白的影响,再验证各下游通路在细胞周期调控中的作用,最后分析细胞周期变化与细胞增殖、应激通路的关系,系统揭示神经元脆弱性与细胞周期状态的关联。
3.1 体内外细胞周期基因与蛋白表达检测
实验目的:验证Wld^s表达是否改变细胞周期相关基因和蛋白的表达水平及亚细胞定位。
方法细节:体内实验中,选取6-8周龄Wld^s突变小鼠和野生型小鼠的小脑组织,采用细胞周期通路特异性RT² Profiler PCR芯片检测84个细胞周期相关基因的表达,通过定量荧光蛋白免疫印迹(Western Blot)验证蛋白表达水平,同时利用免疫细胞化学(IHC)检测蛋白的核定位情况;体外实验中,将携带增强型绿色荧光蛋白(eGFP)标签的Wld^s载体转染人胚肾293(HEK293)细胞,采用相同的PCR芯片和蛋白免疫印迹技术检测细胞周期基因和蛋白的表达,通过免疫细胞化学验证蛋白核定位。
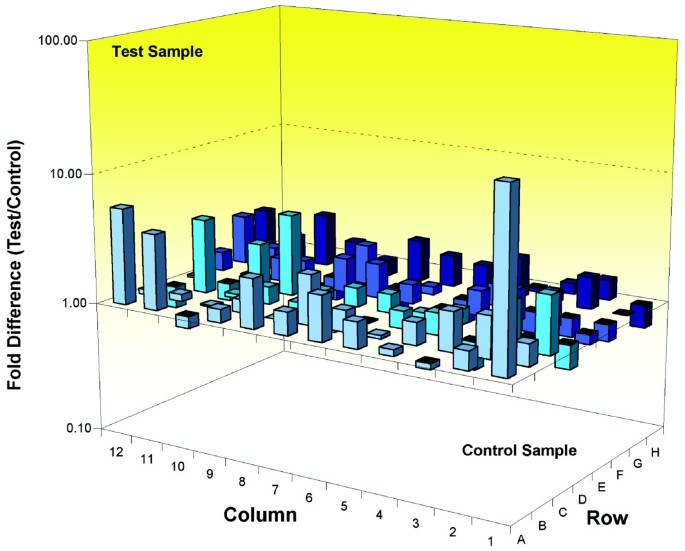
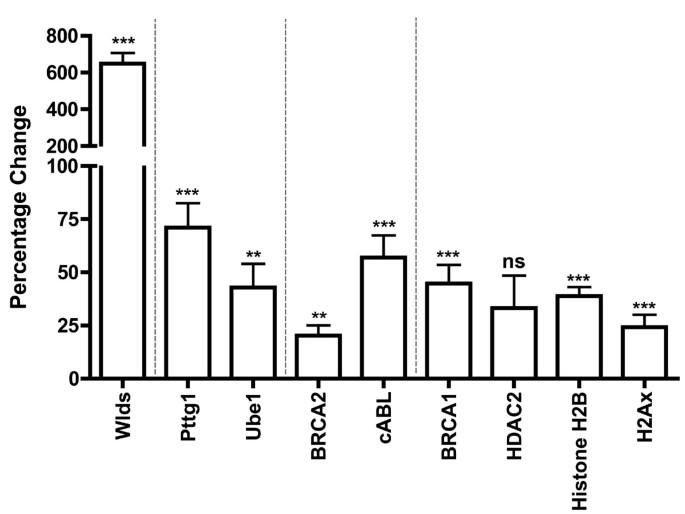
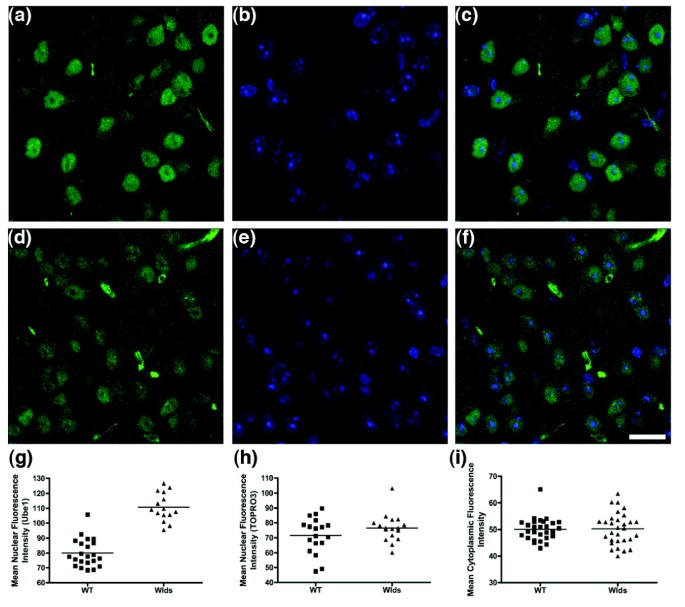
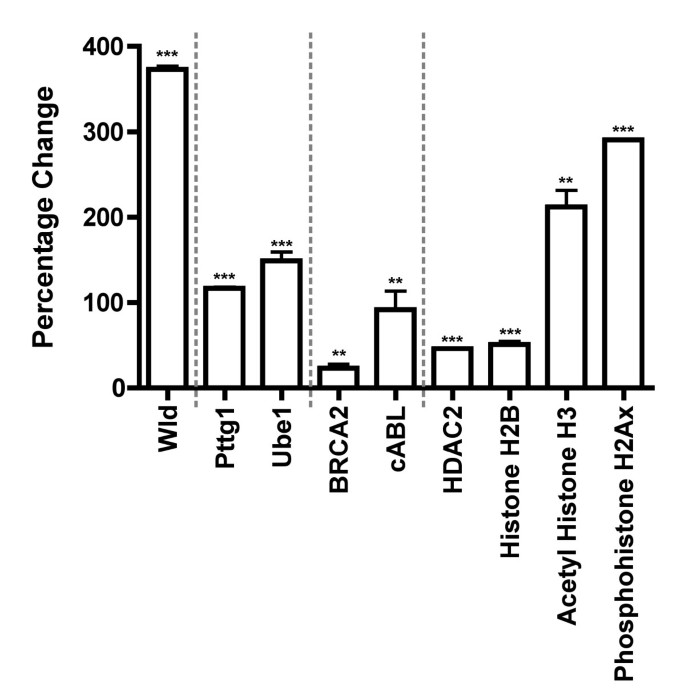
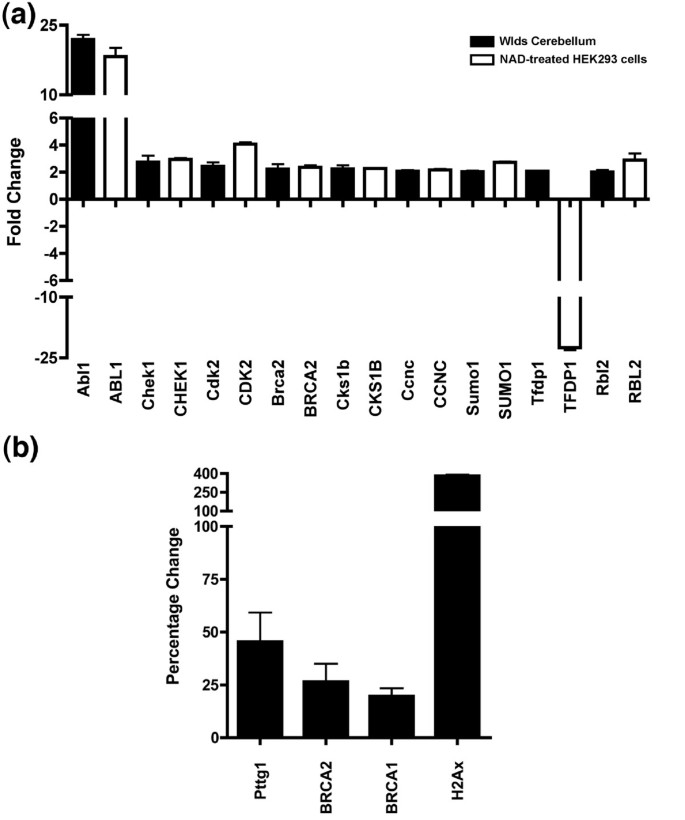
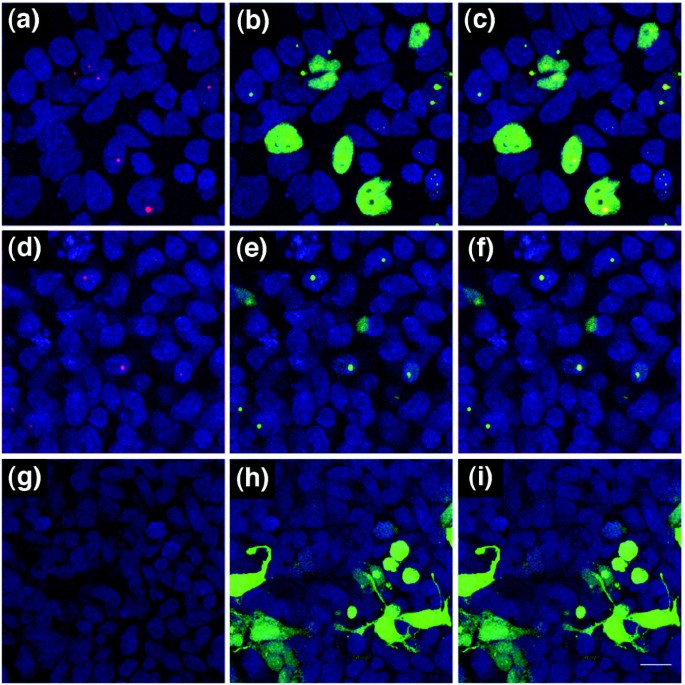
结果解读:体内实验显示,Wld^s小鼠小脑组织中84个细胞周期基因中有17个表达上调超过2倍(n≥3),蛋白免疫印迹验证cABL、Brca2、组蛋白H2B等蛋白表达显著上调(P<0.01);免疫细胞化学结果显示,Ube1在Wld^s小鼠小脑神经元细胞核内的荧光强度显著高于野生型(P<0.001,n≥3)。体外HEK293细胞实验中,转染Wld^s后细胞周期蛋白表达趋势与体内一致,且磷酸化组蛋白H2Ax在转染Wld^s的细胞中100%出现核点状聚集,而对照组无此现象。
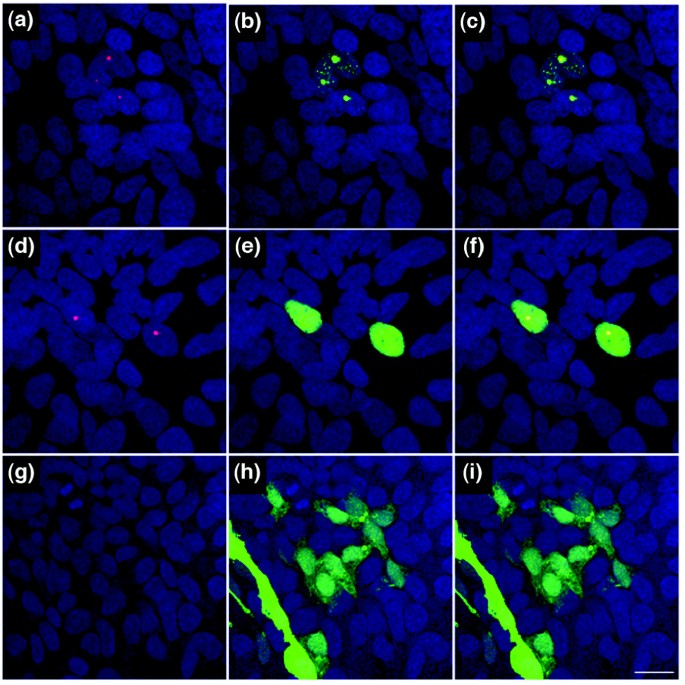
产品关联:实验所用关键产品:RT² Profiler PCR芯片(Tebubio Superarrays)、Odyssey红外成像系统(Li-COR Biosciences)、Ube1一抗(Abcam)、磷酸化组蛋白H2Ax一抗(Upstate)。
3.2 细胞增殖能力检测
实验目的:明确Wld^s诱导的细胞周期变化是否激活细胞有丝分裂后期通路,导致细胞增殖。
方法细节:将Wld^s载体转染人神经元细胞系NT2细胞,设置低、中、高三个剂量组,分别在转染后48h和72h采用MTT(3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐)法检测细胞增殖率,同时在转染后48h采用氚化胸腺嘧啶核苷掺入实验验证DNA合成情况。
结果解读:MTT实验显示,转染Wld^s的NT2细胞在48h和72h的增殖率与对照组无显著差异(n=4,P>0.05);氚化胸腺嘧啶核苷掺入实验也未检测到DNA合成的显著变化,表明Wld^s仅推动细胞向细胞周期再进入方向发展,但不激活有丝分裂后期的增殖通路,细胞周期停滞在早期阶段。
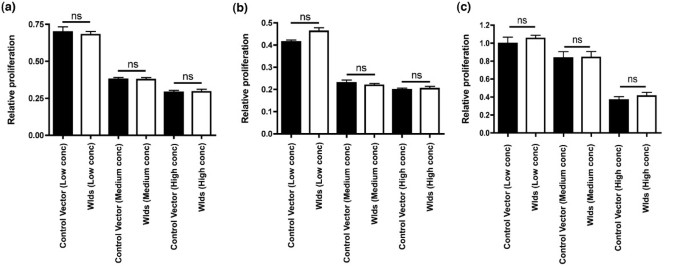
产品关联:文献未提及具体实验产品,领域常规使用MTT试剂盒、氚化胸腺嘧啶核苷试剂、液体闪烁计数仪等。
3.3 下游通路介导细胞周期变化的验证
实验目的:探究Pttg1、NAD、VCP三条通路在Wld^s诱导的细胞周期变化中的具体作用。
方法细节:①Pttg1通路验证:将Pttg1过表达载体和非泛素化Pttg1载体分别转染HEK293细胞,通过蛋白免疫印迹检测细胞周期蛋白表达变化;②NAD通路验证:用1mmol/L NAD处理HEK293细胞和小鼠运动神经元样细胞系NSC34,采用PCR芯片和蛋白免疫印迹检测细胞周期基因和蛋白变化;③VCP通路验证:通过免疫细胞化学检测Wld^s小鼠小脑组织中VCP的核定位情况。
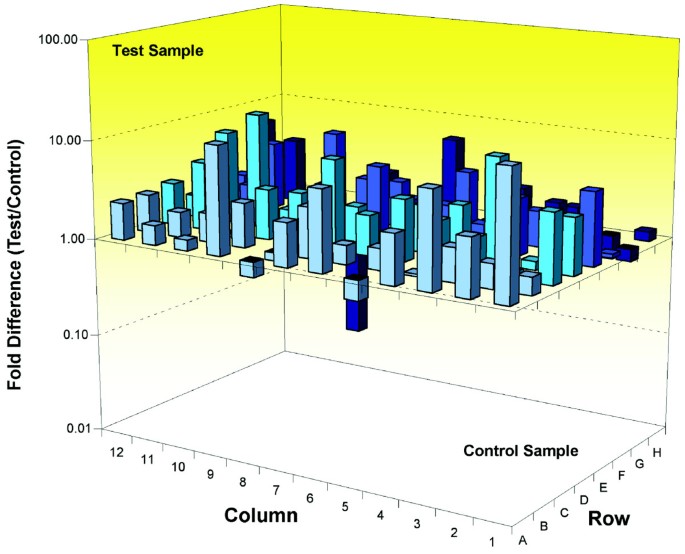
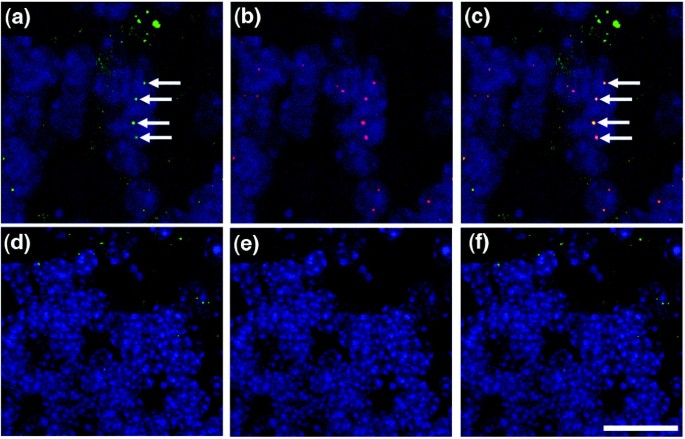
结果解读:①Pttg1过表达可显著上调Ube1蛋白水平,但无法完全模拟Wld^s的所有细胞周期变化,且非泛素化Pttg1载体无法上调Ube1表达,表明Pttg1的泛素化是介导部分细胞周期变化的关键;②NAD处理可使HEK293细胞中48个细胞周期基因表达变化超过2倍,其中47个为上调,且部分基因变化趋势与Wld^s小鼠一致,表明NAD通路可模拟部分Wld^s的细胞周期调控作用;③Wld^s小鼠小脑神经元中VCP呈现明显的核点状聚集,而野生型小鼠中VCP主要位于细胞质,表明Wld^s可诱导VCP核移位,参与细胞周期再进入的早期阶段。
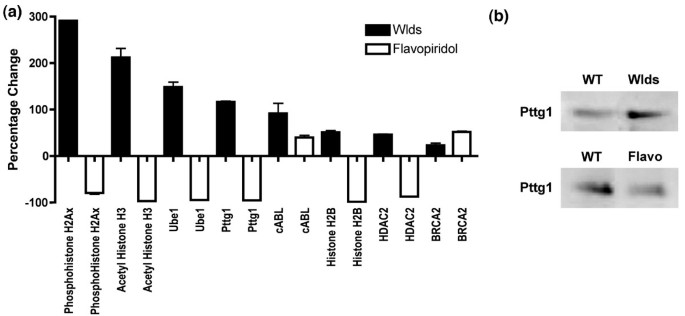
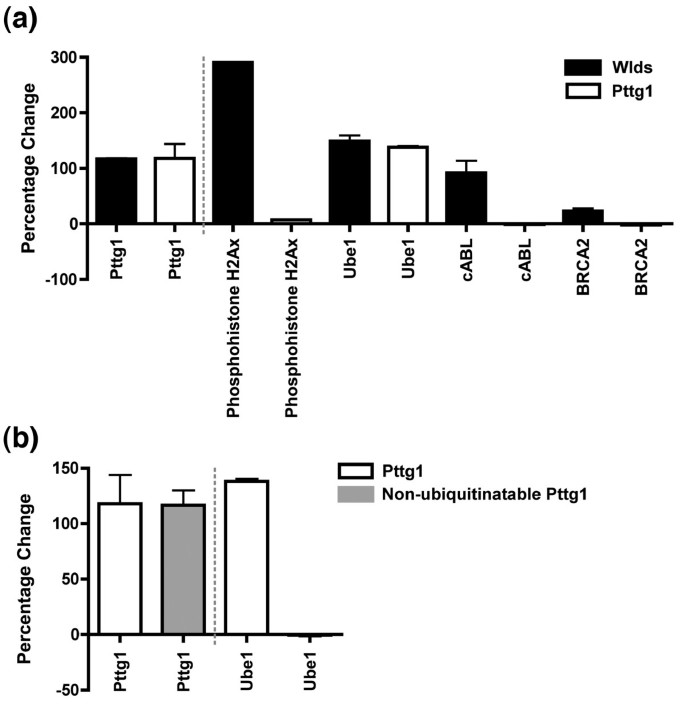
产品关联:实验所用关键产品:NAD(Sigma-Aldrich)、Pttg1过表达载体(已发表构建)、VCP一抗(Abcam)。
3.4 细胞应激通路变化检测
实验目的:分析Wld^s诱导的细胞周期变化是否伴随细胞应激通路的修饰,探索细胞周期与应激通路的关联。
方法细节:采用细胞应激通路特异性RT² Profiler PCR芯片检测Wld^s小鼠小脑组织中84个应激相关基因的表达,通过免疫细胞化学检测HEK293细胞中转染Wld^s后应激诱导蛋白1(STI1)的核定位情况。
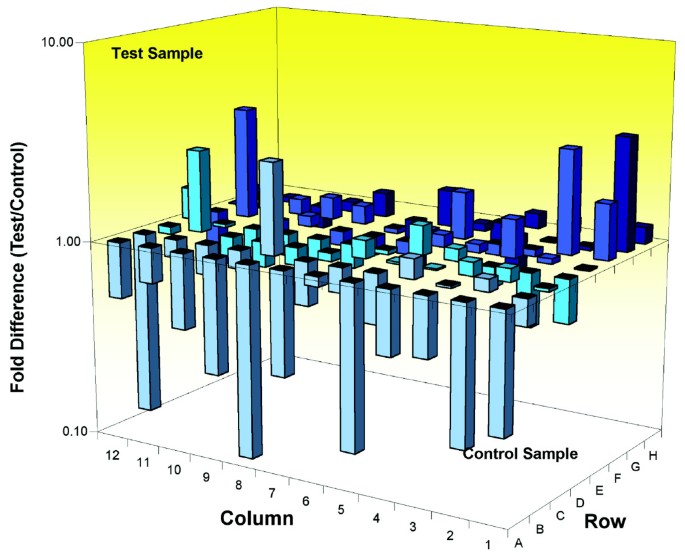
结果解读:Wld^s小鼠小脑组织中14个应激相关基因表达变化超过2倍,既有上调也有下调;免疫细胞化学显示转染Wld^s的HEK293细胞中STI1在细胞核内形成点状聚集,而对照组无此现象,表明细胞周期变化伴随细胞应激通路的修饰,可能共同参与神经元的保护机制。
产品关联:实验所用关键产品:细胞应激通路RT² Profiler PCR芯片(Tebubio Superarrays)、STI1一抗(BD Transduction Laboratories)。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的生物标志物(Biomarker)为细胞周期调控蛋白,包括Ube1、VCP、磷酸化组蛋白H2Ax,其筛选与验证逻辑为:先通过基因组芯片筛选Wld^s调控的细胞周期基因,再通过蛋白免疫印迹和免疫细胞化学验证蛋白表达水平与亚细胞定位变化,最后关联其与Wld^s神经保护表型的关系,形成“基因筛选-蛋白验证-功能关联”的完整链条。
研究过程详述
这些Biomarker的来源为Wld^s小鼠小脑组织和转染Wld^s的HEK293细胞;验证方法包括定量荧光蛋白免疫印迹(检测蛋白表达水平)、免疫细胞化学(检测蛋白核定位);特异性与敏感性方面,Ube1在Wld^s小鼠小脑细胞核内的荧光强度显著高于野生型(P<0.001,n≥3),VCP在Wld^s小鼠小脑神经元中的核定位阳性率显著高于野生型(文献未明确具体数值,基于图表趋势推测),磷酸化组蛋白H2Ax在转染Wld^s的HEK293细胞中100%出现核点状聚集,而对照组无此现象,具有较高的特异性。
核心成果提炼
这些细胞周期蛋白Biomarker与Wld^s的神经保护功能直接相关,其表达和定位变化反映了神经元向细胞周期再进入的状态,但不伴随细胞增殖;本研究的创新性在于首次将细胞周期蛋白作为Wld^s神经保护的潜在标志物,揭示了神经元脆弱性与细胞周期状态的紧密关联,为神经退行性疾病的早期诊断和治疗靶点筛选提供了新方向;统计学结果显示,Ube1核荧光强度差异具有极显著性(P<0.001,n≥3),磷酸化组蛋白H2Ax核聚集阳性率为100%(n≥3),VCP核定位阳性率差异显著(文献未明确具体P值,基于图表趋势推测)。
