1. 领域背景与文献引入
文献英文标题:MiR-1248: a new prognostic biomarker able to identify supratentorial hemispheric pediatric low-grade gliomas patients associated with progression;发表期刊:Biomarker Research;影响因子:未公开;研究领域:儿童神经肿瘤学(儿童低级别胶质瘤)
儿童低级别胶质瘤(pediatric low-grade gliomas,pLGGs)是18岁以下儿童最常见的脑肿瘤,占儿童脑肿瘤的40%,世界卫生组织(WHO)将其分为1级和2级,涵盖毛细胞型星形细胞瘤、节细胞胶质瘤等多种亚型。领域共识:pLGGs的首选治疗方案为安全范围内的完全手术切除,位于小脑或非功能区幕上的肿瘤经完全切除后预后良好,但位于幕上深部或功能区的肿瘤常无法完全切除,约30%的未完全切除患者会出现疾病进展,后续需接受化疗或放疗,而这些治疗手段常导致患者出现癫痫、视力丧失、认知功能障碍等长期后遗症,严重影响生存质量。近年来,pLGGs的分子分型取得进展,比如BRAF基因融合等分子特征已用于风险分层,但目前仍缺乏能够精准预测未完全切除幕上pLGGs患者进展的生物标志物,这是临床亟待解决的核心问题。
针对这一临床空白,本研究旨在筛选pLGGs特异性微小核糖核酸特征,评估其作为预后工具的价值,为未完全切除幕上pLGGs患者的进展风险分层提供可靠的分子标志物,辅助临床决策,推进个性化医疗。
2. 文献综述解析
作者对领域内现有研究的分类维度为“微小核糖核酸在pLGGs中的表达谱研究”和“已报道的pLGGs预后微小核糖核酸研究”两类,通过梳理现有研究的成果与局限性,凸显本研究的创新必要性。
现有研究中,pLGGs的微小核糖核酸表达谱研究显示,不同病理亚型的微小核糖核酸表达存在差异,比如毛细胞型星形细胞瘤中微小核糖核酸-21、微小核糖核酸-34表达上调,微小核糖核酸-124、微小核糖核酸-129表达下调;微小核糖核酸-487b在毛细胞型星形细胞瘤中呈低表达;微小核糖核酸-10b-5p在散发性和神经纤维瘤病1型(NF1)相关的毛细胞型星形细胞瘤中表达降低;微小核糖核酸-20a-5p可调控MAPK/ERK和mTORC1通路,参与部分遗传性星形细胞瘤的发生;微小核糖核酸-125b在多形性黄色星形细胞瘤和节细胞胶质瘤中表达下调;微小核糖核酸-519d和微小核糖核酸-4758可区分节细胞胶质瘤与其他病理亚型。已有的预后微小核糖核酸研究相对有限,一项研究发现微小核糖核酸-29b-3p低表达结合大麻素受体1(CNR1)高表达,可预测未完全切除pLGGs患者的残留疾病消退;另一项研究报道了7个微小核糖核酸组成的特征与化疗反应相关。现有研究的局限性在于,多数研究未聚焦未完全切除的幕上pLGGs人群,且缺乏能够精准预测疾病进展的特异性生物标志物,无法满足临床对进展风险分层的需求。
本研究的创新点在于首次在多中心独立队列中,针对未完全切除的幕上pLGGs患者,筛选并验证了能够预测疾病进展的微小核糖核酸生物标志物,尤其是微小核糖核酸-1248结合肿瘤部位(幕上半球),可实现精准的进展风险分层,填补了该领域的空白,为临床决策提供了新的工具。
3. 研究思路总结与详细解析
本研究的整体框架为“多中心样本收集与分组→微小核糖核酸表达谱筛选→差异微小核糖核酸验证→生物标志物性能评估→功能机制解析”的闭环,研究目标是识别pLGGs特异性微小核糖核酸特征并验证其预后价值,核心科学问题是筛选能够预测未完全切除幕上pLGGs患者进展的预后生物标志物,明确其功能机制。
3.1 多中心样本收集与临床分组
实验目的是建立具有代表性的未完全切除幕上pLGGs患者队列,明确进展与非进展患者的临床病理特征。方法细节:本研究共收集来自4个欧洲儿童神经肿瘤中心的43例幕上未完全切除pLGGs组织样本,分为两个独立队列,队列I包含29例样本(20例毛细胞型星形细胞瘤、9例非毛细胞型星形细胞瘤),来自3个中心;队列II包含9例毛细胞型星形细胞瘤样本,来自德国癌症研究中心。根据术后1个月磁共振成像(MRI)评估切除程度,将患者分为近全切除(NTR,切除50%-90%肿瘤)和活检(切除<50%肿瘤);通过随访期间的MRI评估和临床判断,将患者进一步分为进展组和非进展组;所有患者术前未接受放化疗,研究获得伦理批准,签署知情同意书。结果解读:队列I中62%的患者出现疾病进展,肿瘤分布在幕上半球和中线区域;38%的患者未进展,肿瘤多位于中线结构;队列II中33.3%的患者出现进展,肿瘤均位于中线结构;Kaplan-Meier分析显示,进展组患者的无进展生存期(PFS)显著低于非进展组(文献未明确提供具体数值,基于图表趋势推测)。文献未提及具体实验产品,领域常规使用组织样本保存试剂、MRI成像设备等。
3.2 微小核糖核酸表达谱高通量分析
实验目的是筛选进展组与非进展组患者之间的差异表达微小核糖核酸。方法细节:队列I采用实时定量聚合酶链式反应(RT-qPCR)TaqMan低密度阵列(TLDA)分析754个常见微小核糖核酸的表达水平;队列II采用微小核糖核酸高通量测序技术分析所有已知微小核糖核酸(2656个)的表达谱。分别使用limma检验和DESeq2软件进行差异表达分析,以P<0.05为统计学显著标准;同时进行层次聚类分析,可视化差异表达模式。结果解读:队列I中,非进展组可检测到的微小核糖核酸数量(53%)多于进展组(44%),共筛选出38个差异表达微小核糖核酸,其中9个在进展组上调,29个下调;队列II共筛选出84个差异表达微小核糖核酸,其中32个在进展组上调,52个下调;层次聚类分析显示,进展组与非进展组的微小核糖核酸表达模式可部分区分。
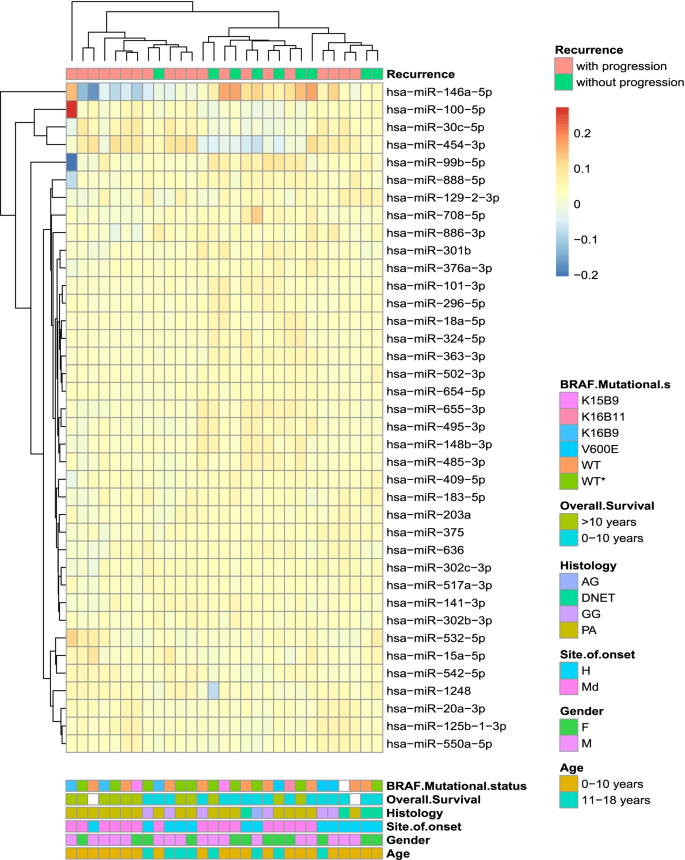
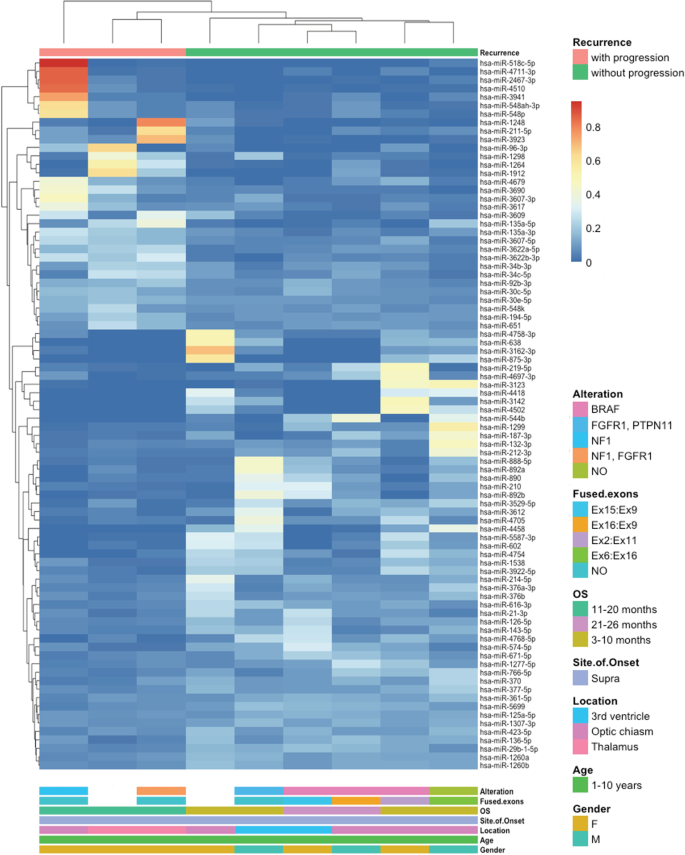
实验所用关键产品:TaqMan Low Density Array(Life Technologies)、高通量测序平台(未明确品牌)。
3.3 跨队列差异微小核糖核酸筛选
实验目的是筛选两个队列中共同的差异表达微小核糖核酸,缩小候选生物标志物范围。方法细节:对队列I和队列II的差异表达微小核糖核酸进行韦恩图分析,取交集得到在两个队列中均存在差异的微小核糖核酸。结果解读:韦恩图分析显示,两个队列的差异微小核糖核酸存在3个交集,分别为微小核糖核酸-1248(进展组上调)、微小核糖核酸-376a-3p(进展组下调)、微小核糖核酸-888-5p(进展组下调)。
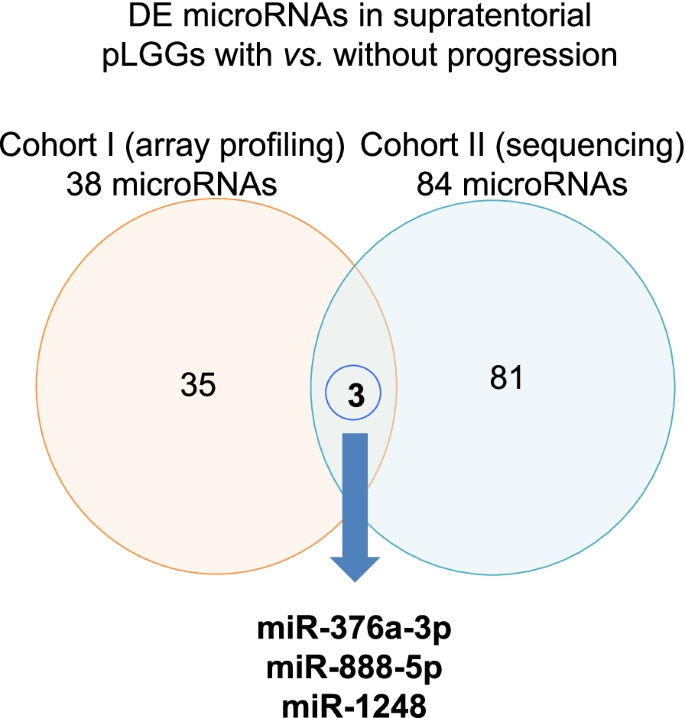
3.4 数字PCR验证差异表达
实验目的是采用绝对定量方法验证候选微小核糖核酸的表达差异,确认其作为生物标志物的可靠性。方法细节:在队列I的32个样本(27个原样本+5个新增样本)中,采用数字PCR(ddPCR)技术检测3个候选微小核糖核酸的表达水平;使用非配对t检验分析进展组与非进展组的表达差异,以P<0.05为统计学显著标准。结果解读:数字PCR结果验证了微小核糖核酸-1248在进展组显著上调(P<0.0001),微小核糖核酸-376a-3p在进展组显著下调(P<0.05),而微小核糖核酸-888-5p的表达差异无统计学意义。
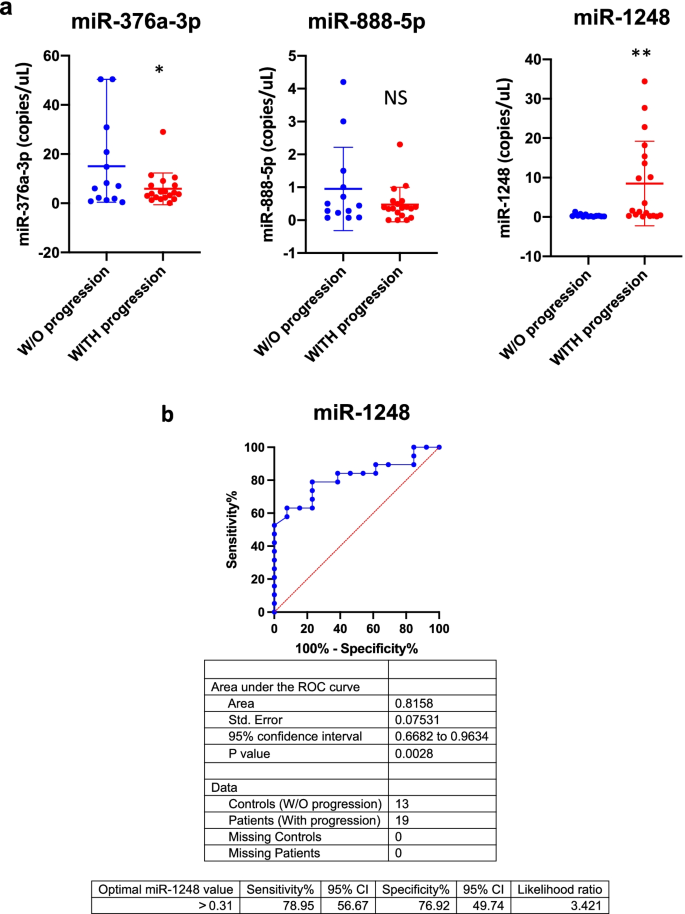
实验所用关键产品:TaqMan™ MicroRNA Assay(Life Technologies)、QX200微滴生成仪(Bio-Rad)、QX200微滴读取仪(Bio-Rad)、QuantaSoft分析软件(Bio-Rad)。
3.5 生物标志物预后性能与临床关联分析
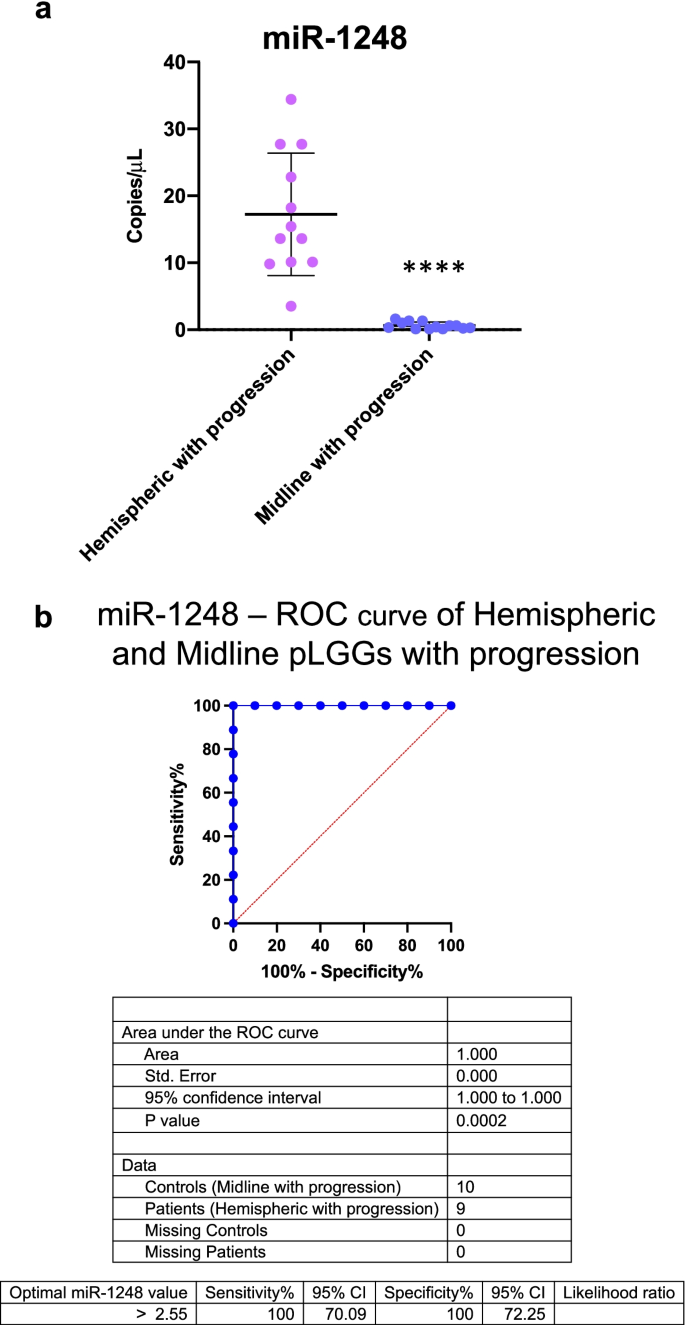
实验目的是评估候选微小核糖核酸的预后诊断效能,分析其与临床病理特征的关联。方法细节:绘制受试者工作特征(ROC)曲线,计算曲线下面积(AUC)评估微小核糖核酸的诊断效能;采用单变量分析评估微小核糖核酸-1248表达与患者临床病理特征(发病部位、病理类型、BRAF状态、年龄、性别、切除程度)的关联;进一步按肿瘤部位(幕上半球/中线)分层,分析微小核糖核酸-1248的表达差异及诊断效能。结果解读:ROC曲线分析显示,微小核糖核酸-1248在所有未完全切除幕上pLGGs患者中的AUC为0.815(95% CI 0.6682-0.9634,P=0.0028),最佳截断值为>0.31 copies/μL;单变量分析显示,微小核糖核酸-1248的表达与肿瘤发病部位(幕上半球)显著相关(P<0.05);分层分析显示,微小核糖核酸-1248仅在幕上半球型进展肿瘤中显著上调,其ROC曲线AUC为1.00(95% CI 1.00-1.00,P=0.0002),最佳截断值为>2.55 copies/μL,可精准识别幕上半球型未完全切除pLGGs的进展患者。
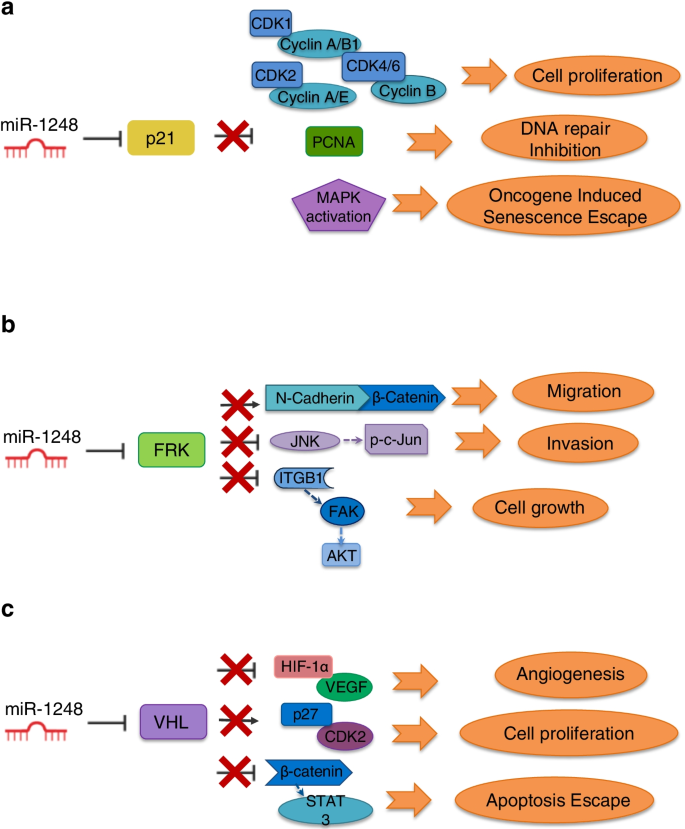
3.6 靶基因筛选与功能机制解析
实验目的是解析微小核糖核酸-1248的致癌功能机制。方法细节:从miRTarBase数据库下载微小核糖核酸-1248的已验证靶基因,与TSGene 2.0数据库中的肿瘤抑制基因取交集;结合已发表文献,分析交集靶基因在胶质瘤中的抑癌功能,推导微小核糖核酸-1248的致癌机制。结果解读:共筛选出10个微小核糖核酸-1248的靶基因,其中5个在胶质瘤中具有明确的抑癌作用,包括细胞周期蛋白依赖性激酶抑制剂1A(CDKN1A,p21)、Fyn相关Src家族酪氨酸激酶(FRK)、斑点型POZ蛋白(SPOP)、von Hippel-Lindau病肿瘤抑制因子(VHL)、S-甲基-5"-硫代腺苷磷酸化酶(MTAP);微小核糖核酸-1248通过下调这些抑癌基因,促进肿瘤细胞增殖、迁移、侵袭,逃逸致癌基因诱导的衰老,激活PI3K/AKT、HIF-1α等致癌通路,从而促进肿瘤进展。
4. Biomarker研究及发现成果解析
本研究的核心Biomarker为微小核糖核酸-1248,是首个针对未完全切除幕上半球型儿童低级别胶质瘤的预后生物标志物,具有精准的进展风险分层能力。
Biomarker定位:本研究发现的Biomarker为微小核糖核酸-1248,属于组织来源的微小核糖核酸;其筛选与验证逻辑为“多中心队列微小核糖核酸表达谱高通量筛选→数字PCR绝对定量验证→临床分层分析确认特异性→生物信息学分析靶基因解析功能”,形成完整的验证链条。
研究过程详述:该Biomarker的来源为未完全切除幕上pLGGs患者的肿瘤组织样本;验证方法采用数字PCR(ddPCR)进行绝对定量检测;特异性与敏感性方面,在所有未完全切除幕上pLGGs患者中,微小核糖核酸-1248的ROC曲线AUC为0.815(95% CI 0.6682-0.9634,P=0.0028),最佳截断值为>0.31 copies/μL;在幕上半球型进展患者中,AUC达到1.00(95% CI 1.00-1.00,P=0.0002),最佳截断值为>2.55 copies/μL,显示出极高的诊断效能。
核心成果提炼:微小核糖核酸-1248是首个能够精准识别未完全切除幕上半球型pLGGs进展患者的预后生物标志物,其高表达与患者疾病进展显著相关;功能机制上,微小核糖核酸-1248通过下调CDKN1A、FRK、VHL等多个抑癌基因,激活致癌通路,促进肿瘤进展;本研究的创新性在于首次将微小核糖核酸表达与肿瘤解剖部位结合,实现了对未完全切除pLGGs患者的精准进展风险分层,为临床医生制定个性化治疗方案提供了可靠依据,填补了该领域缺乏进展预测生物标志物的空白,推进了儿童低级别胶质瘤的个性化医疗进程。
