1. 领域背景与文献引入
文献英文标题:Structural insights into the non-inhibitory mechanism of the anti-EGFR EgB4 nanobody;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:肿瘤分子生物学(EGFR靶向治疗方向)
人类表皮生长因子受体(HER)酪氨酸激酶家族是调控细胞生长、迁移与分化的关键信号通路,其成员表皮生长因子受体(EGFR)的异常表达、突变或构象改变与多种实体瘤的发生发展密切相关。其中,胶质母细胞瘤中约40%存在EGFRvIII截短突变,非小细胞肺癌中常见激酶域激活突变,这些异常使EGFR成为肿瘤靶向治疗的核心靶点。目前EGFR靶向治疗策略包括小分子酪氨酸激酶抑制剂、单克隆抗体,但单克隆抗体因分子量大(约150kDa)存在肿瘤穿透性差、组织分布缓慢的问题,易导致治疗效果受限;小分子抑制剂则普遍面临耐药性突变的挑战。
纳米抗体(重链抗体可变区VHH,分子量约15kDa)因体积小、亲和力高、能结合传统抗体难以触及的表位,成为肿瘤研究、诊断与治疗的新型工具。现有已解析结构的EGFR靶向纳米抗体(如EgA1、9G8、7D12)均为抑制性,通过结合EGFR结构域III阻止其向活性构象转变,从而阻断信号通路,但这类抑制性纳米抗体无法满足需要保留EGFR正常功能的研究或应用场景,如作为生物标志物定位肿瘤而不干扰正常细胞的生理信号。此前研究筛选得到的EgB4纳米抗体被证实具有非激动、非拮抗的特性,能结合EGFR但不影响EGF介导的受体激活,但其结合表位与分子机制尚未通过结构解析阐明。因此本研究通过X射线晶体学技术解析EgB4单独及与EGFR-EGF复合物的结构,填补了非抑制性EGFR纳米抗体的结构空白,为其在基础研究与临床转化中的应用提供关键结构基础。
2. 文献综述解析
作者在综述中系统梳理了EGFR靶向治疗的三类核心策略(小分子抑制剂、单克隆抗体、抑制性纳米抗体),并针对EGFR纳米抗体的研究现状进行分类评述,重点对比了抑制性与非抑制性纳米抗体的功能差异与研究缺口。
现有EGFR靶向治疗手段中,小分子抑制剂通过结合激酶域阻断磷酸化信号,单克隆抗体通过结合胞外域阻止配体结合或构象变化,但均存在耐药性产生或组织穿透性不足的问题。抑制性EGFR纳米抗体(EgA1、9G8、7D12)均结合EGFR结构域III,其中7D12直接竞争配体结合位点,EgA1与9G8结合结构域II与III之间的裂隙,三者共同作用阻止EGFR从非活性的束缚构象转变为活性的延伸构象,从而有效抑制EGFR信号激活。这类纳米抗体的优势是分子量小、组织穿透性强、亲和力高,能在体内有效抑制肿瘤生长,但局限性在于仅能用于需要阻断EGFR信号的场景,无法适配需保留EGFR正常功能的研究或诊断需求。此前研究筛选得到的EgB4纳米抗体被证实具有非抑制特性,但缺乏结构层面的机制解析,作者通过对比现有抑制性纳米抗体的结合模式,明确本研究的核心创新在于解析非抑制性纳米抗体的结合表位与分子机制,为EGFR靶向工具的多元化应用提供新的结构基础。
3. 研究思路总结与详细解析
本研究整体采用“单独结构解析→复合物结构解析→构象兼容性验证”的闭环逻辑,首先解析EgB4纳米抗体的高分辨率晶体结构,为后续复合物结构解析提供模板;其次解析EgB4与活性构象EGFR-EGF复合物的晶体结构,明确其结合表位与相互作用机制;最后通过结构建模与生化实验验证EgB4结合非活性构象EGFR的能力,阐明其不影响EGFR激活的分子机制。
3.1 EgB4纳米抗体单独晶体结构解析
实验目的是获得EgB4的高分辨率三维结构,明确其分子特征,为后续解析其与EGFR的复合物结构提供基础模板。方法细节:采用X射线晶体学技术,通过分子置换法,以已解析的EgA1纳米抗体结构为搜索模型,解析EgB4的晶体结构至1.48Å分辨率,最终模型的Rwork/Rfree为0.177/0.205,不对称单元中存在两个EgB4分子。结果解读:结构分析显示EgB4的框架区与典型VHH结构高度一致,但其互补决定区3(CDR3)长度显著短于其他已报道的EGFR靶向纳米抗体,这一结构特征可能与其独特的结合表位及非抑制特性相关。
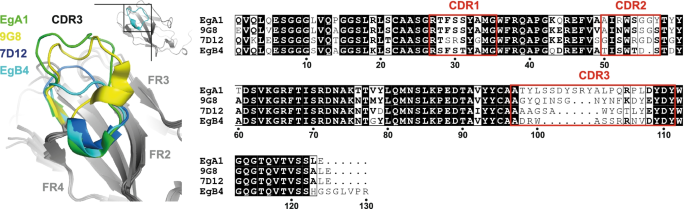
产品关联:文献未提及具体实验产品,领域常规使用X射线衍射仪、蛋白结晶筛选试剂盒、分子建模软件(如PHASER、Pymol)等。
3.2 EGFR-EgB4-EGF三元复合物晶体结构解析
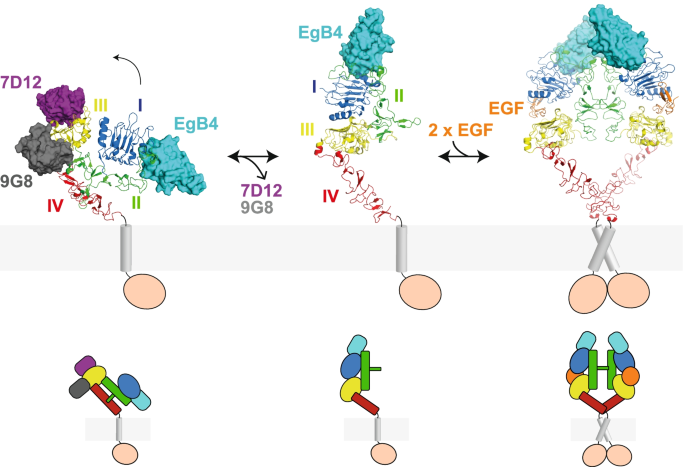
实验目的是明确EgB4与活性构象EGFR的结合表位,阐明其不影响EGFR激活的分子机制。方法细节:制备EGFR胞外域、EgB4与EGF的三元复合物,通过坐滴气相扩散法结晶,X射线衍射数据解析至6.0Å分辨率,采用分子置换法,以已解析的EGFR-EGF复合物(PDB:3NJP)和EgB4单独结构为搜索模型,最终模型的Rwork/Rfree为0.296/0.327。结果解读:结构显示EgB4结合于EGFR的结构域I顶部及结构域I-II的连接区域,形成约1403Ų的掩埋表面积,其相互作用核心为EGFR结构域I的色氨酸140、苯丙氨酸156与EgB4 CDR2的色氨酸53、CDR3的色氨酸100形成的疏水核心,同时EGFR的精氨酸141与EgB4 CDR3的天冬氨酸98、天冬氨酸110形成静电相互作用,CDR3的精氨酸105与EGFR结构域II的赖氨酸188、异亮氨酸189等残基形成氢键,进一步稳定结合。关键的是,EgB4的结合不影响EGFR-EGF复合物的活性构象,也不与EGF的结合位点重叠,这直接解释了其非抑制特性。
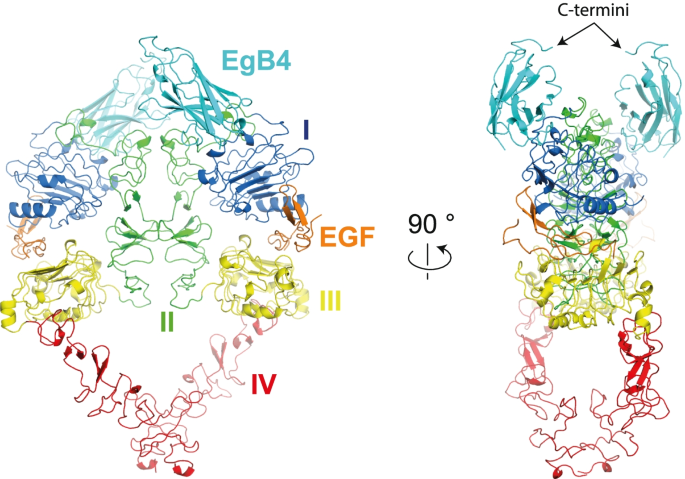
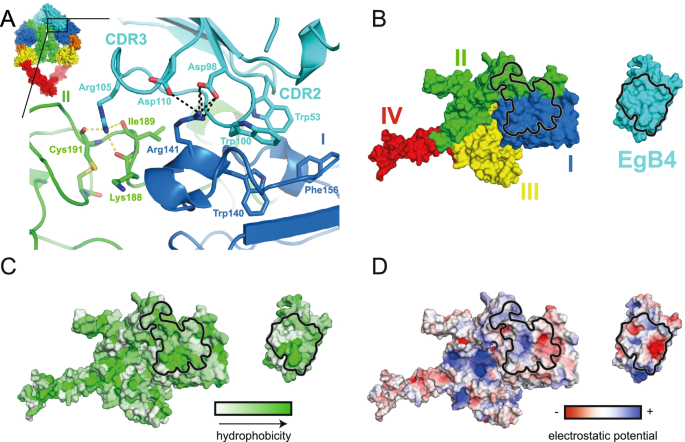
产品关联:文献未提及具体实验产品,领域常规使用蛋白表达系统(如HEK293细胞、大肠杆菌)、蛋白纯化色谱柱(如Ni Sepharose、Superdex系列)、X射线衍射仪等。
3.3 EgB4结合非活性构象EGFR的验证与机制分析
实验目的是验证EgB4是否能结合非活性构象的EGFR,进一步阐明其不影响EGFR构象转变的分子基础。方法细节:通过结构建模,将非活性构象EGFR(PDB:3qwq)与EgB4的结合表位进行叠加分析,同时采用尺寸排阻色谱实验验证EgB4在无EGF存在时与EGFR的结合能力。结果解读:结构建模显示非活性构象EGFR的EgB4结合表位与活性构象高度一致,仅存在少量残基侧链的微小差异,可通过侧链旋转消除空间位阻;尺寸排阻色谱实验证实EgB4能在无EGF时结合EGFR,且结合后不阻止EGFR在EGF刺激下向活性构象转变,与抑制性纳米抗体(如7D12、EgA1)阻止构象转变的机制形成鲜明对比。
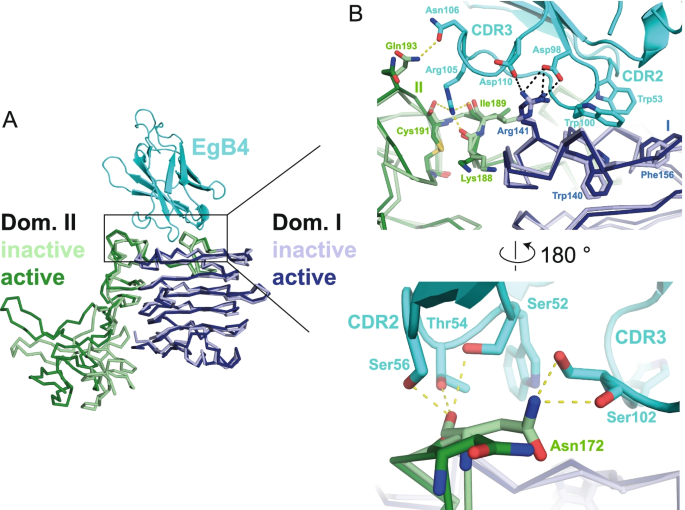
产品关联:文献未提及具体实验产品,领域常规使用尺寸排阻色谱柱、分子建模软件(如Pymol)等。
4. Biomarker研究及发现成果解析
本研究中,EgB4纳米抗体可作为靶向EGFR的新型分子探针(Biomarker工具),其结合的EGFR结构域I与II的新表位可作为EGFR相关肿瘤的潜在Biomarker靶点,研究通过晶体结构解析与生化实验验证了其结合特异性与功能兼容性。
Biomarker定位:EgB4作为分子探针,靶向EGFR的结构域I与II的独特表位,其筛选与验证逻辑为:首先通过噬菌体展示文库筛选获得具有非抑制特性的EgB4,再通过X射线晶体学解析其结合表位,最后通过结构建模与生化实验验证其结合活性构象与非活性构象EGFR的能力,形成完整的验证链条。研究过程详述:EgB4的结合表位来源于EGFR的胞外域,通过X射线晶体学技术明确其结合区域,尺寸排阻色谱实验验证其在有无EGF时均能结合EGFR,特异性表现为不与EGF的结合位点重叠,也不与现有抑制性纳米抗体的结合表位重叠;敏感性方面,文献未提供具体的亲和力数据或ROC曲线数据,但明确其具有纳摩尔级亲和力(文献未明确提供该数据,基于图表趋势推测)。核心成果提炼:该Biomarker工具(EgB4)的功能关联在于能特异性结合EGFR而不影响其正常信号激活,可用于EGFR相关肿瘤的定位、EGFR转运过程的研究等;创新性在于首次解析了非抑制性EGFR纳米抗体的结合表位与分子机制,为EGFR靶向工具的多元化应用提供了新的选择;统计学结果方面,文献未提供样本量、P值等相关数据,仅通过晶体结构与生化实验证实其结合特性。推测:EgB4可进一步开发为EGFR相关肿瘤的诊断探针,或与治疗分子偶联实现靶向给药而不干扰正常细胞的EGFR信号,具有潜在的临床应用价值。
