1. 领域背景与文献引入
文献英文标题:A novel method to derive amniotic fluid stem cells for therapeutic purposes;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:干细胞生物学(羊膜液干细胞分离与临床转化)
领域共识:干细胞治疗是再生医学的核心发展方向,成人组织干细胞存在获取量少、体外增殖能力有限的局限,胚胎干细胞则因伦理争议、畸胎瘤形成风险等问题限制了临床应用。2003年Prusa等首次在羊膜液中发现表达Oct4的多能性细胞,后续研究证实人羊膜液干细胞(hAFS)兼具胚胎干细胞的多能性与成人干细胞的低免疫原性,无畸胎瘤形成风险,可向三胚层细胞分化,且伦理争议小,成为临床干细胞治疗的理想来源。然而现有羊膜液干细胞分离技术存在诸多临床转化障碍:传统方法需耗时数月才能获得足够细胞量,细胞群体异质性高,部分方法依赖动物源抗体磁珠,存在异种污染风险。针对上述研究空白,本文开发了一种无异种污染、快速高效的羊膜液干细胞克隆系分离方法,为羊膜液干细胞的临床转化提供了关键技术支撑。
2. 文献综述解析
本文综述按时间线与技术原理对现有羊膜液干细胞分离方法进行分类评述,明确各类方法的技术优势与临床转化局限,进而凸显本研究的创新性与必要性。
作者将现有研究分为四类:2004年Tsai等的两步培养法,通过非贴壁细胞起始培养,虽实现羊膜液干细胞分离,但细胞群体异质性高,无法满足临床对纯干细胞群体的需求;2006年Tsai等在两步法基础上优化,通过单细胞克隆构建获得高纯度细胞系,但操作步骤繁琐,耗时较长;2007年Kim等采用长期原代培养结合传代筛选的方法,需持续培养至细胞形态均一,细胞倍增时间达3.6天,生产效率极低;2007年De Coppi等的免疫分选法,通过c-Kit抗体磁珠分选阳性细胞,可获得高纯度细胞系,但依赖动物源抗体,存在异种污染风险,不符合临床应用的安全性要求。通过对比现有方法的局限,本文提出的“起始细胞法”将原代培养、干细胞筛选与克隆系构建整合为单一步骤,无需动物源试剂,可在2周内获得10^8级别的纯干细胞群体,细胞倍增时间缩短至0.8天,解决了现有方法的核心痛点,为羊膜液干细胞的临床转化提供了可行路径。
3. 研究思路总结与详细解析
本研究的核心目标是开发适合临床应用的羊膜液干细胞分离技术,核心科学问题为如何快速获取无异种污染、高纯度、高增殖能力的羊膜液干细胞,技术路线遵循“样本收集→起始细胞筛选→克隆系扩增→细胞特性鉴定”的闭环逻辑,通过多维度实验验证新方法的可行性与优越性。
3.1 羊膜液样本收集与起始细胞筛选
实验目的:从临床羊膜穿刺样本中筛选具有高增殖活性的羊膜液干细胞起始细胞,避免异质细胞污染。
方法细节:收集15例16-20周妊娠女性的羊膜液样本(n=15),经离心去除细胞碎片后,采用Chang培养基进行原代培养,37℃、5%CO₂、5%O₂条件下培养3-4天,通过倒置显微镜筛选成纤维样贴壁细胞作为起始细胞,机械去除其他形态的贴壁细胞。
结果解读:14例样本成功筛选到起始细胞(成功率93.3%,n=15),原代培养第3天,85%以上的贴壁细胞为成纤维样干细胞形态,80-100%的单个起始细胞可在体外扩增形成高质量克隆系,有效避免了异质细胞的干扰。
产品关联:实验所用关键产品:Irvine Scientific的Chang培养基、Gibco的α-MEM培养基、PAA的ES-FBS胎牛血清等。
3.2 克隆羊膜液干细胞系构建与扩增
实验目的:通过克隆系扩增获得大量高纯度的羊膜液干细胞,验证新方法的扩增效率。
方法细节:将筛选得到的单个起始细胞在羊膜液干细胞专用培养基(含α-MEM、15%ES-FBS、bFGF等)中培养48小时形成细胞集落,机械挑取单个集落接种至24孔板,待细胞汇合度达70%后,以1:3的比例传代扩增至25cm²、75cm²培养瓶。
结果解读:单个起始细胞培养48小时可形成含100-300个细胞的集落(
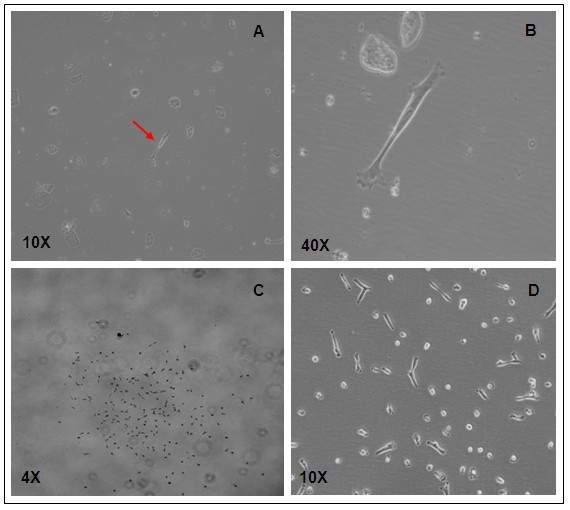
),传代至第2代时可获得10^7级别的细胞,2周内可扩增至10^8级细胞量,而现有方法需耗时2个月才能达到同等细胞量;细胞群体倍增时间为0.8天,是现有方法的2-5倍(文献未明确提供该数据的统计学P值,基于图表趋势推测差异显著)。
产品关联:实验所用关键产品:Chemicon的bFGF、Sigma的谷氨酰胺、Biochrom的青霉素/链霉素等。
3.3 干细胞标志物表达鉴定
实验目的:验证扩增后的细胞是否具有羊膜液干细胞的特异性标志物表达,明确细胞的干细胞特性。
方法细节:采用免疫荧光染色检测核内多能性标志物Oct4a的表达;通过逆转录PCR(RT-PCR)检测Oct4a、Nanog、Sox2、HLA-ABC、HLA-DR等基因的表达;利用流式细胞术检测表面标志物CD29、CD44、CD73、CD105、CD133、CD90、CD34、CD45、SSEA4的表达水平。
结果解读:免疫荧光染色显示,传代18代的克隆细胞系中Oct4a呈阳性表达(
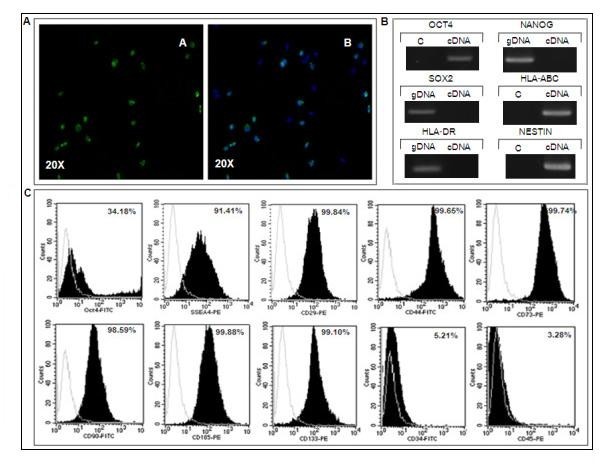
);RT-PCR结果显示,细胞表达Oct4a与HLA-ABC,但不表达Nanog、Sox2与HLA-DR;流式细胞术结果显示,99-100%的细胞表达间充质干细胞标志物CD29、CD44、CD73、CD105,CD133呈高表达,CD90呈低表达,造血干细胞标志物CD34、CD45呈阴性表达;24-41%的细胞表达Oct4a,48-91%的细胞表达SSEA4,证明细胞群体具有高度均一性与干细胞特性。
产品关联:实验所用关键产品:Santa Cruz的Oct4a抗体、Chemicon的SSEA-4抗体、E-bioscience的CD系列抗体、Beckton Dickinson的流式细胞仪等。
3.4 多向分化能力验证
实验目的:验证羊膜液干细胞是否具有向三胚层细胞分化的能力,明确其多能性特征。
方法细节:将传代12代的克隆细胞分别接种至成骨、成脂、神经分化诱导培养基中,37℃、5%CO₂条件下培养,通过碱性磷酸酶染色、Von Kossa染色鉴定成骨分化,油红O染色鉴定成脂分化,TuJ-1免疫染色鉴定神经分化。
结果解读:成骨诱导3周后,细胞碱性磷酸酶染色阳性,Von Kossa染色显示钙沉积;成脂诱导2周后,油红O染色显示细胞内脂滴形成;神经诱导7天后,细胞呈神经样形态,TuJ-1染色阳性(
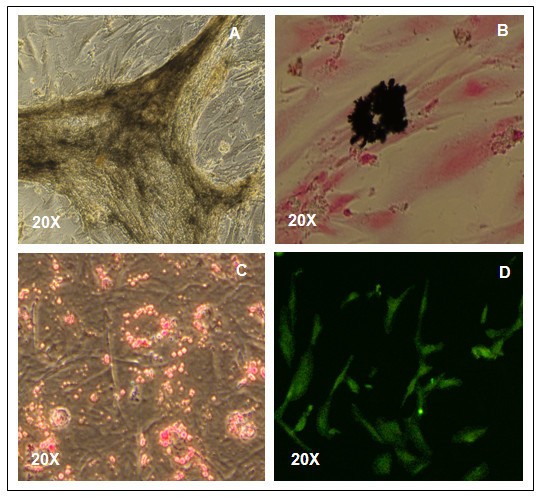
),RT-PCR检测到神经标志物Nestin的表达,证明细胞具有向中胚层(骨、脂肪)与外胚层(神经)分化的能力。
产品关联:实验所用关键产品:Sigma的地塞米松、甘油-2-磷酸、胰岛素、β-巯基乙醇等分化诱导试剂。
3.5 细胞增殖能力与核型稳定性分析
实验目的:验证羊膜液干细胞的长期增殖能力与遗传稳定性,评估其临床应用的安全性。
方法细节:对克隆细胞系进行连续传代培养,记录细胞群体倍增时间;采用Giemsa染色检测传代18代细胞的核型。
结果解读:细胞在传代20代内保持稳定的增殖能力,群体倍增时间维持在0.8天左右(
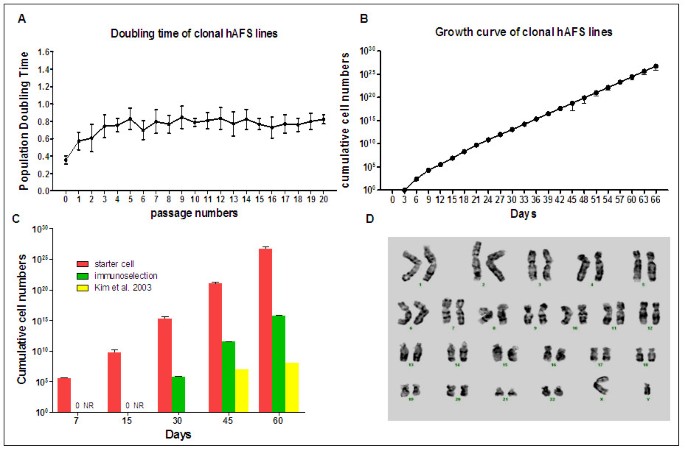
);传代18代的细胞仍保持正常的46XX或46XY核型,无染色体畸变,证明细胞具有良好的遗传稳定性。
产品关联:文献未提及具体核型检测试剂,领域常规使用Giemsa染色液、染色体核型分析系统。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker涵盖羊膜液干细胞的多能性标志物、间充质干细胞标志物与免疫相关标志物,通过“体外筛选→分子鉴定→功能验证”的完整逻辑链条,明确了这些标志物的表达特征与临床意义。
Biomarker定位:本研究的Biomarker包括核内多能性标志物Oct4a、表面多能性标志物SSEA4、间充质干细胞标志物CD29、CD44、CD73、CD105、CD133、免疫相容性标志物HLA-ABC与HLA-DR,筛选与验证逻辑为“原代培养起始细胞→克隆系扩增→免疫荧光/流式/RT-PCR检测→分化功能验证”,确保标志物的特异性与可靠性。
研究过程详述:Biomarker来源于临床羊膜液样本的原代培养起始细胞,验证方法包括免疫荧光染色(Oct4a阳性)、RT-PCR(Oct4a、HLA-ABC阳性,Nanog、Sox2、HLA-DR阴性)、流式细胞术(CD29、CD44、CD73、CD105阳性率99-100%,CD34、CD45阴性,Oct4a阳性率24-41%,SSEA4阳性率48-91%);其中,HLA-ABC阳性、HLA-DR阴性的表达特征,表明细胞具有低免疫原性,适合异体移植应用。
核心成果提炼:这些Biomarker的表达证明,新方法获得的羊膜液干细胞具有典型的间充质干细胞特性,兼具一定的多能性,且遗传稳定(传代18代核型正常,n=10),增殖能力显著优于现有方法(群体倍增时间0.8天,是现有方法的2-5倍,文献未明确提供P值,基于图表趋势推测差异显著);首次通过“起始细胞法”实现了无异种污染的羊膜液干细胞快速扩增,为临床细胞治疗提供了安全、高效的细胞来源,其低免疫原性的特征(HLA-DR阴性)进一步拓展了细胞的异体应用前景。
