1. 领域背景与文献引入
文献英文标题:Tackling an essential problem in functional proteomics of Saccharomyces cerevisiae;发表期刊:Genome Biology;影响因子:未公开;研究领域:酵母功能蛋白质组学、细胞周期与DNA复制
领域共识:酿酒酵母作为经典模式生物,在真核细胞周期调控研究中具有里程碑意义,1970年代Hartwell团队通过温度敏感突变体筛选鉴定了大量细胞分裂周期(CDC)基因,奠定了真核细胞周期调控的理论基础。随着全基因组测序技术的发展,酿酒酵母非必需基因的缺失突变体库已构建完成,但研究发现约18%的酵母基因为必需基因(单倍体缺失后无法存活),其中多数DNA复制相关基因属于必需基因,且仍有大量必需基因功能未被表征。现有必需基因研究方法存在明显局限:传统温度敏感突变体筛选依赖随机突变,部分基因难以获得有效功能缺失突变;基于启动子替换的条件性表达方法虽适合大规模研究,但蛋白表达下调速度慢,易激活细胞周期检查点,掩盖基因的真实功能表型。因此,开发高效、大规模的必需基因产物条件性失活方法,成为解析未表征必需基因功能的核心需求,本文即围绕这一问题介绍了改进的温度敏感降解子(td)系统及其在必需基因功能研究中的应用。
2. 文献综述解析
作者按必需基因条件性失活方法的发展脉络,将现有研究分为三类:传统温度敏感突变体技术、启动子替换调控技术、早期温度敏感降解子(td)技术,系统评述了各类方法的优势与局限性,并突出了本文介绍的改进型td技术的创新价值。
传统温度敏感突变体技术是细胞周期研究的经典方法,通过筛选温度敏感突变菌株成功鉴定了大量CDC基因,推动了真核细胞周期调控机制的解析,但该方法存在明显局限:部分基因产物不易发生温度敏感型结构突变,导致无法通过随机筛选获得有效突变体,且针对单个基因的体外诱变方法不适合大规模基因分析。
基于启动子替换的条件性表达技术通过通用DNA盒替换目标基因的天然启动子,实现了大规模基因功能研究,但该方法的核心问题是蛋白表达下调速度较慢,在细胞周期研究中易激活细胞周期检查点通路,使细胞周期停滞于检查点而非基因功能缺失的真实阶段,限制了对基因功能的精准解析。
早期温度敏感降解子(td)技术通过在目标蛋白N端融合温度敏感降解信号,利用泛素介导的N端规则通路实现温度诱导的蛋白降解,但多数td融合蛋白的降解效率不足,无法快速消除蛋白功能;后续Diffley团队通过过表达N端规则通路的识别因子UBR1,提升了td蛋白的降解效率,但该方法尚未应用于大规模必需基因分析。
本文介绍的Labib团队改进型td技术,通过设计通用同源重组插入盒,实现了快速、大规模构建td融合菌株,解决了现有方法的核心局限,为必需基因的大规模功能解析提供了可行方案。
3. 研究思路总结与详细解析
本研究的核心目标是开发适合大规模分析酿酒酵母必需基因的高效条件性失活方法,鉴定未表征必需基因的生物学功能,尤其是DNA复制相关基因的功能;核心科学问题是如何实现必需基因产物的快速、特异性条件性失活,以及未表征必需基因在细胞周期与DNA复制中的作用;技术路线遵循“工具开发→大规模菌株构建→表型筛选→功能验证”的闭环逻辑,通过改进td降解子系统,成功构建了通用插入盒,实现了大规模必需基因的条件性失活,并鉴定了新的DNA复制相关蛋白复合物。
3.1 改进型温度敏感降解子(td)系统的通用盒构建
实验目的是开发可高效、大规模整合到目标必需基因的td融合系统,实现蛋白的快速条件性降解;方法细节是设计包含KanMX筛选标记(G418抗性)、铜诱导型CUP1启动子、温度敏感降解子(td)编码序列及HA表位标签的通用DNA盒,使用约70nt的基因特异性长引物进行PCR扩增,引物5"端与目标基因N端序列同源,3"端与通用盒序列同源,通过同源重组将通用盒插入到酿酒酵母目标基因的N端,替换天然启动子,构建td融合基因;同时使用携带半乳糖诱导型GAL-UBR1的菌株,以提升td蛋白的降解效率;结果解读:该通用盒可通过同源重组高效整合到目标基因位点,在含铜的培养基中,CUP1启动子驱动td融合蛋白正常表达,细胞可在23℃正常生长;当移除铜并添加半乳糖、将温度升至37℃时,UBR1表达上调,td融合蛋白被快速降解,实现基因功能的条件性失活。
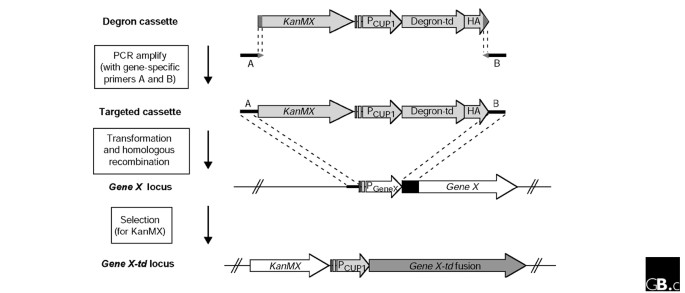
产品关联:文献未提及具体实验产品,领域常规使用PCR扩增试剂盒、酵母转化试剂、G418筛选试剂、HA标签抗体等。
3.2 大规模必需基因td融合菌株的构建与表型筛选
实验目的是筛选具有细胞周期表型的未表征必需基因,鉴定其潜在功能;方法细节是利用上述通用盒,构建了60余个未知功能必需基因的td融合菌株(约占酵母未知功能必需基因的一半);将菌株在23℃含铜和棉子糖的培养基中培养至对数期,随后移除铜、添加半乳糖以诱导UBR1表达,并将温度升至37℃以诱导td融合蛋白降解;通过显微镜观察细胞形态,流式细胞术检测DNA含量,分析菌株的细胞周期表型;结果解读:多数菌株未表现出典型的细胞周期停滞表型,但有少量菌株呈现出CDC表型(细胞形态均一,提示细胞周期停滞),其中3个菌株(CDC101、CDC102、CDC105)的DNA含量分析显示存在明显的DNA复制缺陷。
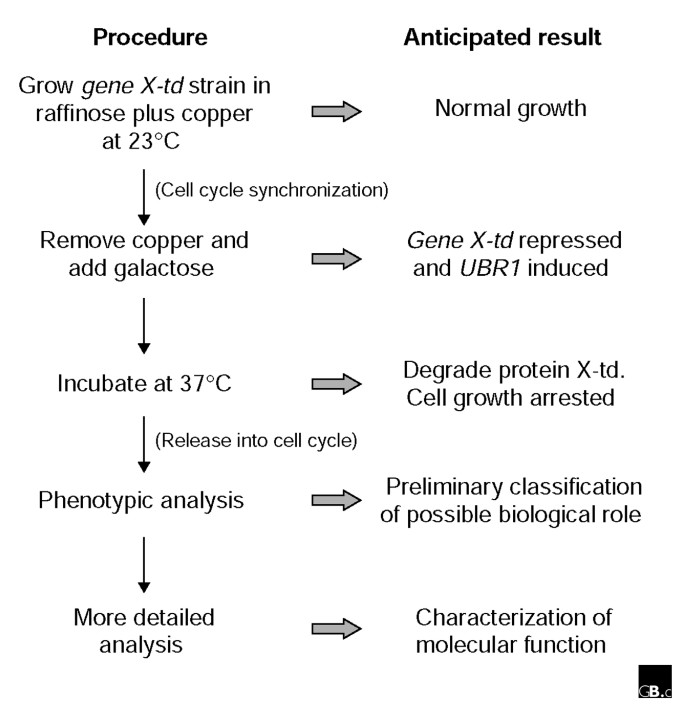
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、荧光显微镜、细胞周期分析软件等。
3.3 DNA复制相关基因的功能验证与蛋白复合物鉴定
实验目的是验证CDC101、CDC102、CDC105的功能及相互作用,明确其在DNA复制中的作用阶段;方法细节:首先参考酵母双杂交数据库的预测结果,通过免疫共沉淀实验验证蛋白间的相互作用;随后采用“执行点”实验,在细胞周期的不同阶段(复制叉建立前后)诱导td融合蛋白降解,分析DNA合成的变化;结果解读:生化分析证实Cdc101、Cdc102、Cdc105与另一个未知功能必需基因产物YOL146W(即Psf3)形成稳定的四蛋白复合物,该复合物与同期报道的酵母及爪蟾GINS复合物完全一致;“执行点”实验显示,在复制叉建立前或后降解Cdc102或Cdc105,均会导致DNA复制缺陷,提示该复合物在DNA复制的起始和延伸阶段均发挥必需作用;此前的温度敏感突变体研究因蛋白失活不充分,未发现该复合物的延伸功能,而本研究的高效td降解系统则明确了其完整功能。
产品关联:文献未提及具体实验产品,领域常规使用免疫共沉淀试剂盒、Western blot检测试剂、DNA合成检测试剂盒等。
4. Biomarker研究及发现成果解析
本研究中鉴定的GINS复合物属于功能型蛋白Biomarker,是真核生物DNA复制的核心调控复合物,其筛选与验证遵循“表型筛选→分子互作验证→功能验证”的完整逻辑链条。
Biomarker定位:GINS复合物是一类保守的DNA复制必需蛋白复合物,属于功能型Biomarker,筛选逻辑为:通过td融合菌株的表型筛选获得DNA复制缺陷菌株→基于蛋白相互作用数据验证复合物形成→通过细胞周期阶段特异性失活实验验证其功能;研究过程详述:该复合物的来源为酿酒酵母的必需基因产物,验证方法包括细胞形态观察、流式细胞术检测DNA含量、免疫共沉淀验证复合物形成、细胞周期“执行点”实验;特异性方面,GINS复合物的失活会特异性导致DNA复制缺陷,细胞停滞于S期,在酵母及爪蟾等真核生物中高度保守;敏感性方面,改进的td系统可快速、高效降解复合物组分,仅需诱导即可检测到明显的复制缺陷(文献未明确提供具体敏感性数值,基于表型趋势推测);核心成果提炼:GINS复合物由Psf1(Cdc101)、Psf2(Cdc102)、Sld5(Cdc105)和Psf3四个亚基组成,是DNA复制起始和延伸阶段的必需功能复合物,其功能缺失会导致DNA复制无法正常启动或进行(文献未明确提供样本量及P值,基于实验表型统计);创新性在于首次通过大规模必需基因分析明确了GINS复合物的完整功能,解决了传统温度敏感突变体因蛋白失活不充分导致的功能表征不全问题,为真核生物DNA复制机制的解析提供了关键依据。
