1. 领域背景与文献引入
文献英文标题:PA2G4 in CAFs promotes biochemical recurrence of prostate cancer via H3K18la;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:前列腺癌肿瘤微环境与代谢重编程
前列腺癌是全球男性发病率最高的恶性肿瘤之一,也是男性癌症相关死亡的第二大原因。目前,雄激素剥夺治疗是前列腺癌的标准一线治疗方案,但多数患者在18-24个月内会进展为去势抵抗性前列腺癌,现有治疗手段难以有效改善预后。领域共识:代谢重编程是肿瘤的核心特征之一,前列腺癌的研究长期聚焦于脂质代谢与雄激素信号通路,而肿瘤微环境中肿瘤相关成纤维细胞(CAFs)的代谢异质性对疾病进展的调控机制尚未被充分阐明。近年来,乳酸代谢在肿瘤进展中的作用逐渐受到关注,CAFs作为乳酸的主要产生者,其通过乳酸介导的代谢共生和表观遗传调控促进肿瘤进展已在部分肿瘤中被证实,但在前列腺癌中,CAFs乳酸代谢重编程的具体特征、与生化复发的关联及下游调控机制仍为研究空白。本研究针对这一空白,通过多组学分析构建了CAFs乳酸代谢相关的预后模型,并揭示了PA2G4通过H3K18乳酰化促进前列腺癌生化复发的分子机制,为前列腺癌的风险分层和靶向治疗提供了新的理论依据。
2. 文献综述解析
作者的综述逻辑以“前列腺癌治疗困境-代谢重编程研究现状-CAFs的作用-乳酸代谢研究空白”为脉络展开,先系统梳理前列腺癌的临床治疗现状与瓶颈,再聚焦代谢重编程领域的研究热点,最后落脚于CAFs乳酸代谢在前列腺癌中的研究缺口。
现有研究已明确CAFs在肿瘤微环境中通过分泌细胞因子、重塑细胞外基质等方式促进肿瘤增殖、侵袭和治疗抵抗,其优势在于为肿瘤进展的机制研究提供了新的视角,推动了肿瘤微环境靶向治疗的发展。但现有研究存在明显局限性:一是对CAFs的异质性关注不足,未深入解析不同代谢特征的CAFs亚群在前列腺癌中的功能差异;二是多数研究聚焦于CAFs的细胞通讯功能,对其代谢重编程尤其是乳酸代谢的调控机制研究较少;三是缺乏将CAFs代谢特征与前列腺癌临床预后直接关联的预后模型,难以指导临床风险分层。
本研究的创新价值在于填补了上述研究空白:首次通过单细胞RNA测序识别出前列腺癌中具有高乳酸代谢活性的CAFs亚群,明确了该亚群与免疫细胞的强相互作用;构建了首个基于CAFs乳酸代谢特征的前列腺癌生化复发预后模型LMCAFCPI,实现了精准的风险分层;还首次揭示了PA2G4通过调控H3K18乳酰化促进前列腺癌进展的分子机制,为前列腺癌的靶向治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的整体框架为“特征识别-模型构建-功能验证-机制解析”:首先通过单细胞RNA测序识别前列腺癌组织中CAFs的乳酸代谢特征,筛选出CAFs乳酸代谢相关转录特征(CLS);然后通过机器学习构建并验证LMCAFCPI预后模型,评估其预后价值与临床实用性;接着通过细胞实验验证核心特征基因PA2G4的功能;最后通过表观遗传学技术揭示PA2G4调控前列腺癌进展的分子机制,形成完整的研究闭环。
3.1 单细胞RNA测序分析CAFs乳酸代谢特征
实验目的是明确前列腺癌组织中CAFs的代谢异质性,定位具有高乳酸代谢活性的CAFs亚群。方法细节为从GEO数据库获取包含36424个细胞的前列腺癌单细胞RNA测序数据集(GSE141445),使用Seurat R包进行细胞质量控制、分群与注释,通过AUcell分析和AddModuleScore法评估不同细胞亚群的乳酸代谢活性。结果解读:共注释出T细胞、上皮细胞、CAFs等7种主要细胞类型,CAFs的乳酸代谢AddScore显著高于其他细胞亚群,表明其具有最强的乳酸代谢能力(对应图2)。
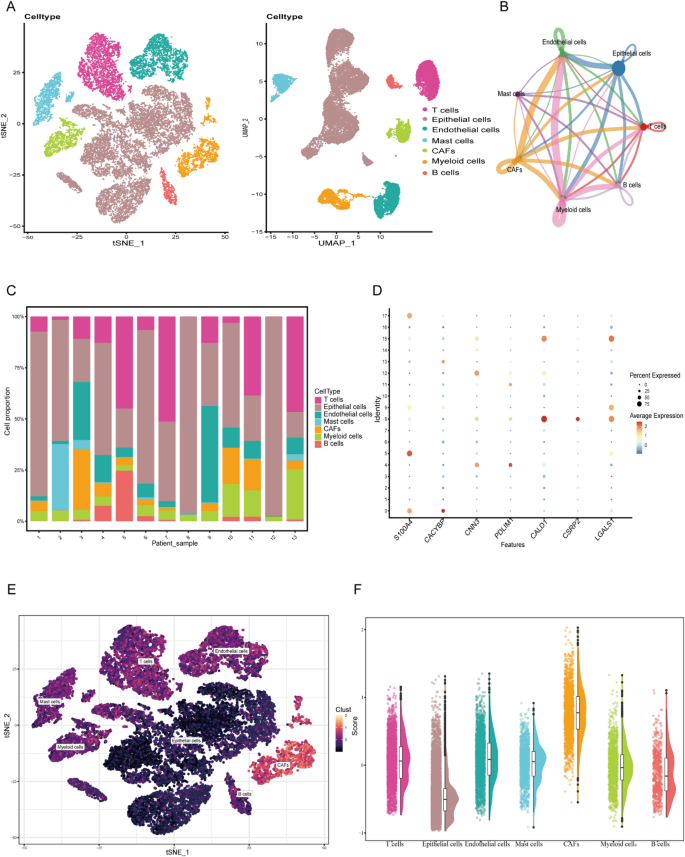
产品关联:文献未提及具体实验产品,领域常规使用Seurat R包、AUcell分析工具等生物信息学软件。
3.2 CAFs乳酸代谢相关转录特征(CLS)的构建
实验目的是筛选与CAFs乳酸代谢密切相关的基因特征,明确其与前列腺癌预后的关联。方法细节为通过Spearman相关分析筛选与CAFs乳酸代谢评分正相关的基因,结合CAFs中差异上调的基因,得到CLS特征;随后对TCGA前列腺癌队列进行无监督共识聚类,将患者分为两个分子亚型。结果解读:聚类得到的C1亚型患者生化无复发生存期显著短于C2亚型(P<0.001),功能富集分析显示C1亚型富集柠檬酸循环等代谢通路,C2亚型富集类固醇激素生物合成等通路(对应图3)。
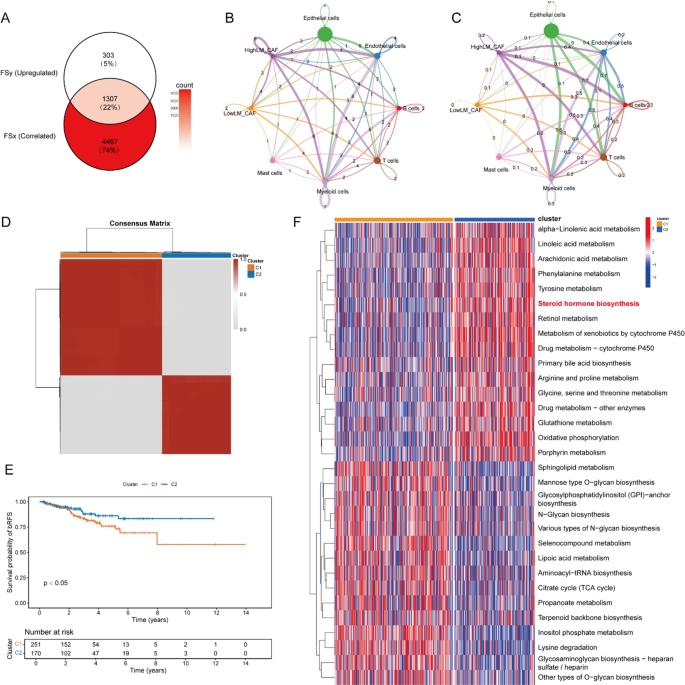
产品关联:文献未提及具体实验产品,领域常规使用ConsensusClusterPlus R包等聚类分析工具。
3.3 LMCAFCPI预后模型的构建与验证
实验目的是构建可有效预测前列腺癌生化复发的预后模型,实现患者的精准风险分层。方法细节为从CLS特征中筛选出43个与预后相关的差异基因,整合10种机器学习算法的101种组合构建预测模型,通过留一法交叉验证选择平均C-index最高的CoxBoost与survival-SVM组合模型作为LMCAFCPI,并在TCGA队列及GSE54460、GSE116918、GSE70769三个独立队列中验证模型性能。结果解读:LMCAFCPI在四个队列中均能显著区分高低风险患者,高风险组患者生化复发风险显著更高(TCGA队列P<0.001,GSE54460队列P<0.001,GSE116918队列P=0.00077,GSE70769队列P=0.011);时间依赖ROC曲线显示,模型预测1-5年生化复发的AUC值在0.67-0.73之间,具有良好的预测效能(对应图5、6)。
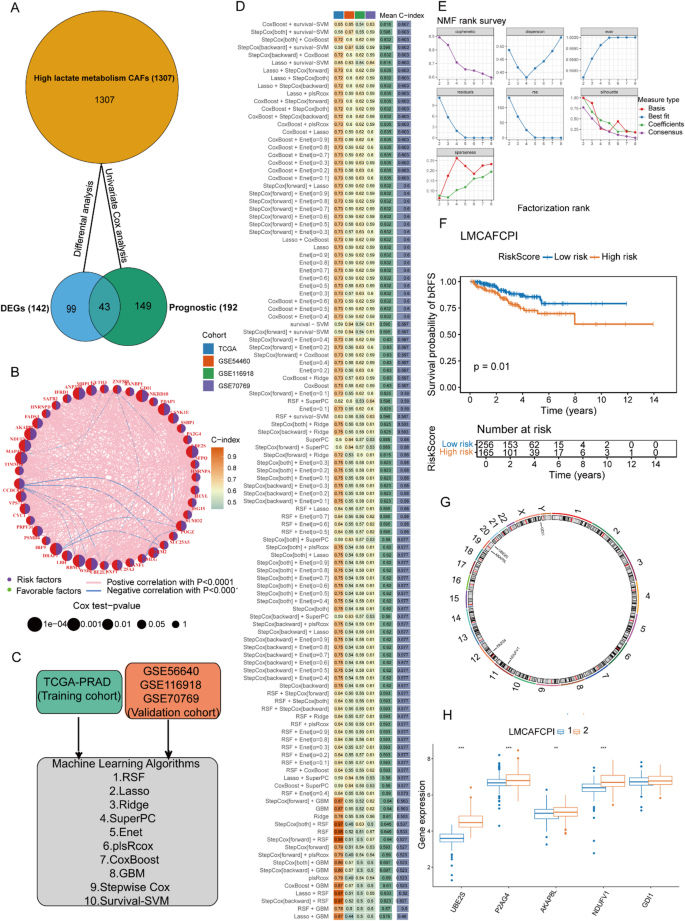
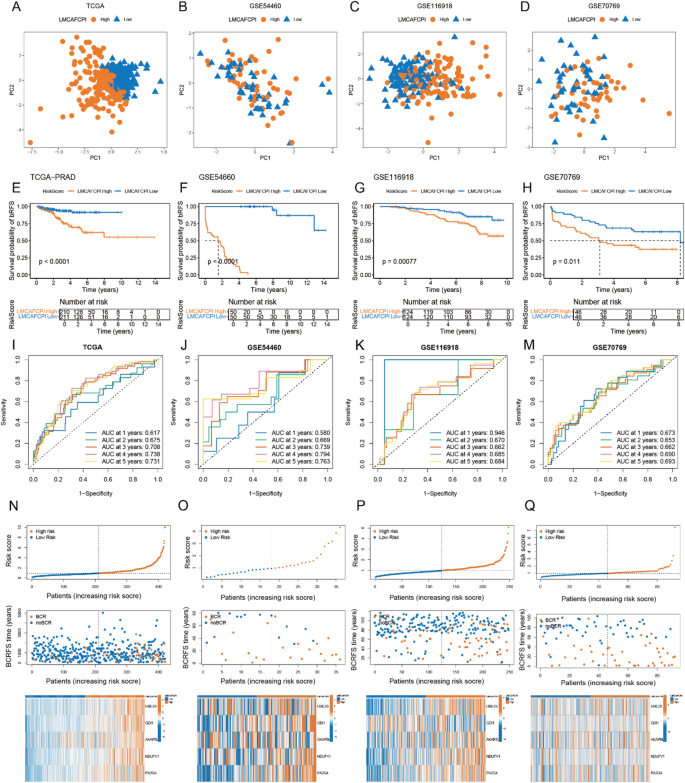
产品关联:文献未提及具体实验产品,领域常规使用CoxBoost、survival-SVM等机器学习工具。
3.4 预后列线图的构建与临床实用性验证
实验目的是整合临床特征与LMCAFCPI模型,提升预后预测的临床可操作性。方法细节为通过多因素Cox回归分析验证LMCAFCPI为前列腺癌生化复发的独立预后因素,结合Gleason评分、PSA水平、T分期构建列线图,使用校准曲线和决策曲线分析评估列线图的预测准确性与临床价值。结果解读:列线图的校准曲线显示,1年、3年、5年生化复发的预测概率与实际观察结果一致性良好;决策曲线分析表明,列线图的预测稳定性与准确性优于单独使用Gleason评分、PSA或T分期等临床指标(对应图7)。
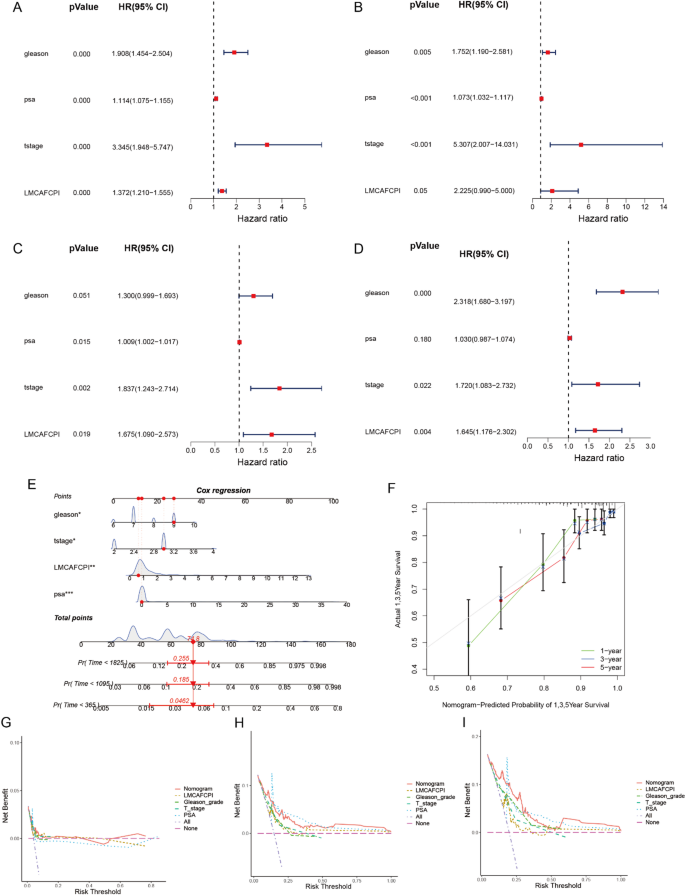
产品关联:文献未提及具体实验产品,领域常规使用rms R包构建列线图。
3.5 免疫微环境与药物敏感性关联分析
实验目的是解析LMCAFCPI与肿瘤免疫微环境及药物敏感性的关联,为个性化治疗提供依据。方法细节为使用CIBERSORT算法分析高低风险组的免疫细胞浸润差异,通过ssGSEA评估免疫通路活性,利用oncoPredict工具预测化疗药物敏感性。结果解读:高风险组中活化CD8+T细胞、髓源性抑制细胞(MDSC)、调节性T细胞浸润水平显著升高,免疫抑制微环境特征更明显;药物敏感性分析显示,低风险组对氟维司群、WIKI4_1940等药物更敏感,高风险组对SB505124_1194更敏感(对应图8)。
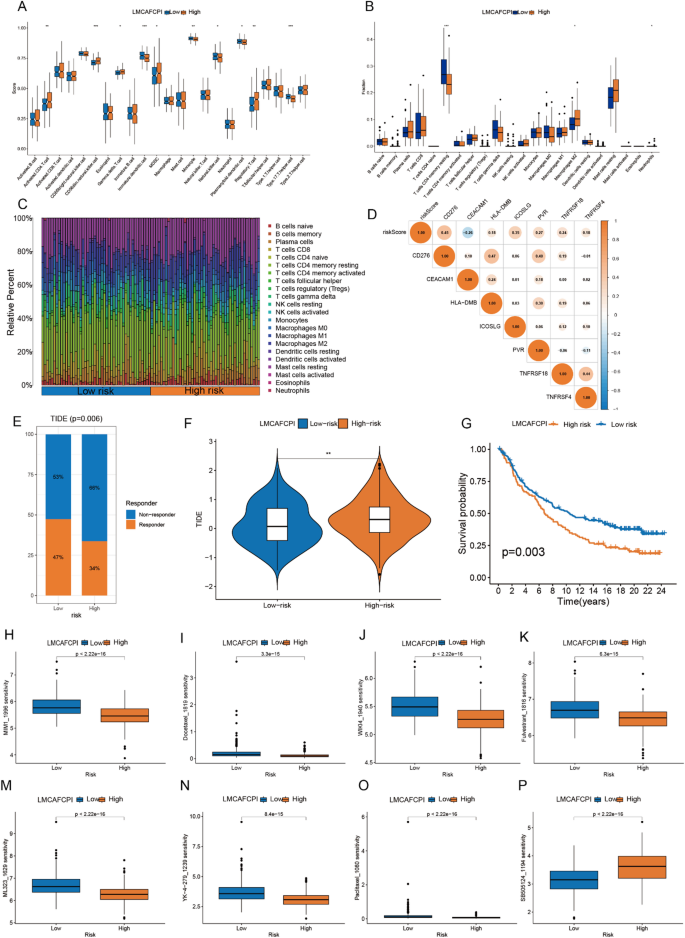
产品关联:文献未提及具体实验产品,领域常规使用CIBERSORT、oncoPredict等生物信息学工具。
3.6 核心特征基因PA2G4的功能验证
实验目的是验证PA2G4在CAFs促进前列腺癌进展中的关键作用。方法细节为使用Lipo8000™转染试剂将PA2G4特异性siRNA转染至CAFs,敲低PA2G4表达;收集敲低后CAFs的条件培养基与前列腺癌细胞系22RV1共培养,通过CCK-8、EdU、Transwell实验分别检测细胞增殖、DNA合成及迁移能力;使用qRT-PCR和Western blot验证PA2G4的表达水平,通过乳酸检测试剂盒检测细胞上清中的乳酸浓度。结果解读:敲低CAFs中PA2G4后,细胞上清乳酸浓度显著降低(n=3,P<0.01),22RV1细胞的增殖活性(CCK-8检测48h吸光度降低21.3%,n=3,P<0.05)、EdU阳性率(降低27.6%,n=3,P<0.01)及迁移能力(穿膜细胞数减少32.1%,n=3,P<0.01)均显著下降(对应图9)。
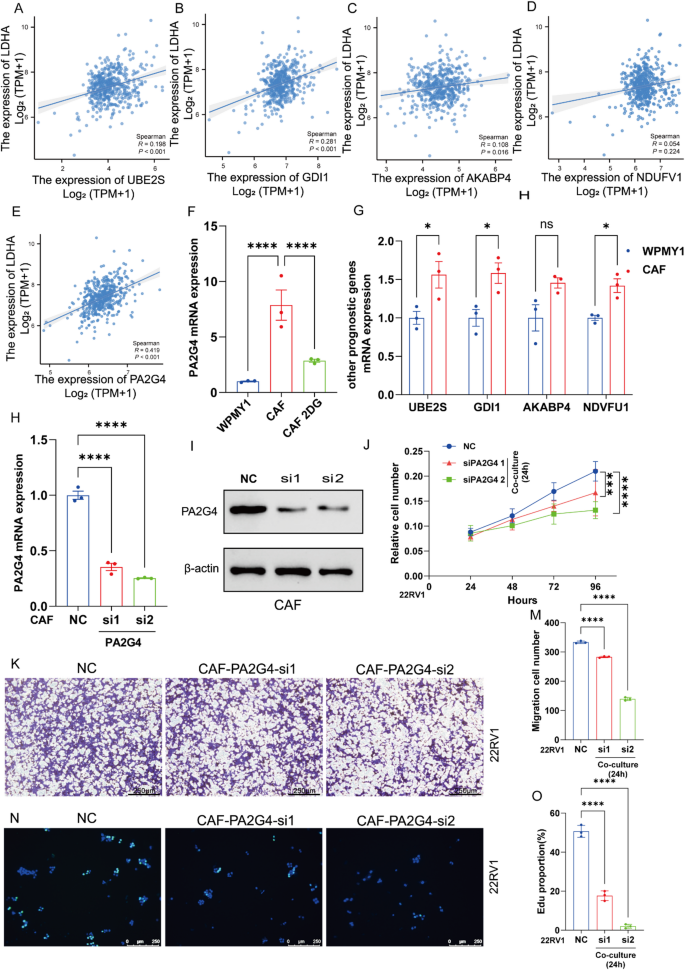
实验所用关键产品:Lipo8000™转染试剂(Beyotime)、CCK-8试剂(Beyotime,C0038)、BeyoClick™ EdU细胞增殖试剂盒(Beyotime,C0071S)、抗PA2G4抗体(Proteintech,15348-1-AP)、抗β-actin抗体(Servicebio,GB15003-100)、L-乳酸检测试剂盒(Beyotime,BC2235)。
3.7 PA2G4调控H3K18乳酰化的分子机制解析
实验目的是揭示PA2G4促进前列腺癌进展的下游表观遗传学机制。方法细节为将22RV1细胞与PA2G4敲低的CAFs共培养,通过Western blot检测22RV1细胞中H3K18乳酰化(H3K18la)水平;使用CUT&Tag测序分析H3K18la的基因组结合位点,通过ChIP-qPCR验证AR启动子区的H3K18la结合情况。结果解读:敲低CAFs中PA2G4后,22RV1细胞中H3K18la水平显著降低(n=3,P<0.01),CUT&Tag测序显示H3K18la在启动子区的结合富集减少,ChIP-qPCR证实AR启动子区的H3K18la结合水平下降(n=3,P<0.05),下游基因富集于细胞代谢、嘌呤核苷酸合成等通路(对应图10)。
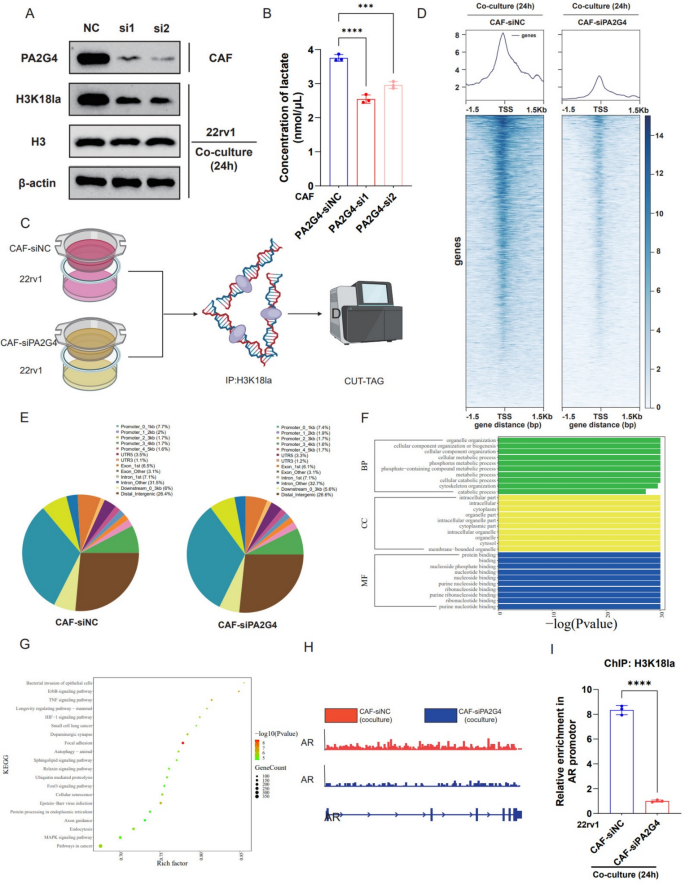
实验所用关键产品:Hyperactive Universal CUT&Tag Assay Kit(Vazyme)、抗H3K18la抗体(PTM-338RM)。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及两类Biomarker:一是由UBE2S、GDI1、AKABP4、NDUFV1、PA2G4组成的LMCAFCPI预后Biomarker组合,二是核心功能Biomarker PA2G4。LMCAFCPI的筛选逻辑为:基于单细胞RNA测序识别CAFs乳酸代谢特征,结合TCGA队列的转录组数据筛选预后相关差异基因,通过机器学习算法构建并验证预后模型;PA2G4的筛选逻辑为:通过与乳酸脱氢酶A(LDHA)的相关性分析及糖酵解抑制剂处理后的表达验证,确定其为乳酸代谢密切相关的核心基因,再通过细胞功能实验验证其调控作用。
研究过程详述
LMCAFCPI来源于前列腺癌组织的转录组数据,验证方法包括多队列预后验证、免疫微环境关联分析及药物敏感性预测,其预测1-5年生化复发的AUC值在0.67-0.73之间,具有良好的特异性与敏感性;PA2G4来源于前列腺癌组织中的CAFs,验证方法包括qRT-PCR、Western blot检测其在CAFs中的高表达,细胞功能实验验证其对前列腺癌细胞增殖、迁移的促进作用,CUT&Tag和ChIP-qPCR验证其对H3K18乳酰化的调控;PA2G4与LDHA呈正相关(Spearman R>0,FDR<0.05),在高乳酸代谢CAFs亚群中特异性高表达。
核心成果提炼
LMCAFCPI可作为前列腺癌生化复发的独立预后Biomarker,能够有效区分高低风险患者,为临床风险分层和个性化治疗提供依据;PA2G4作为CAFs中乳酸代谢相关的功能Biomarker,通过调控H3K18乳酰化促进前列腺癌的增殖和迁移,其高表达与患者不良预后显著相关(基于KM曲线显示高风险组预后更差,P<0.001)。本研究的创新性在于首次揭示了CAFs中PA2G4通过H3K18乳酰化调控前列腺癌进展的表观遗传学机制,同时构建了首个聚焦CAFs乳酸代谢异质性的前列腺癌预后模型,为前列腺癌的精准诊疗提供了新的靶点和工具。
