1. 领域背景与文献引入
文献英文标题:Tumour-specific phosphorylation of serine 419 drives alpha-enolase (ENO1) nuclear export in triple negative breast cancer progression;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:三阴性乳腺癌分子机制与生物标志物研究。
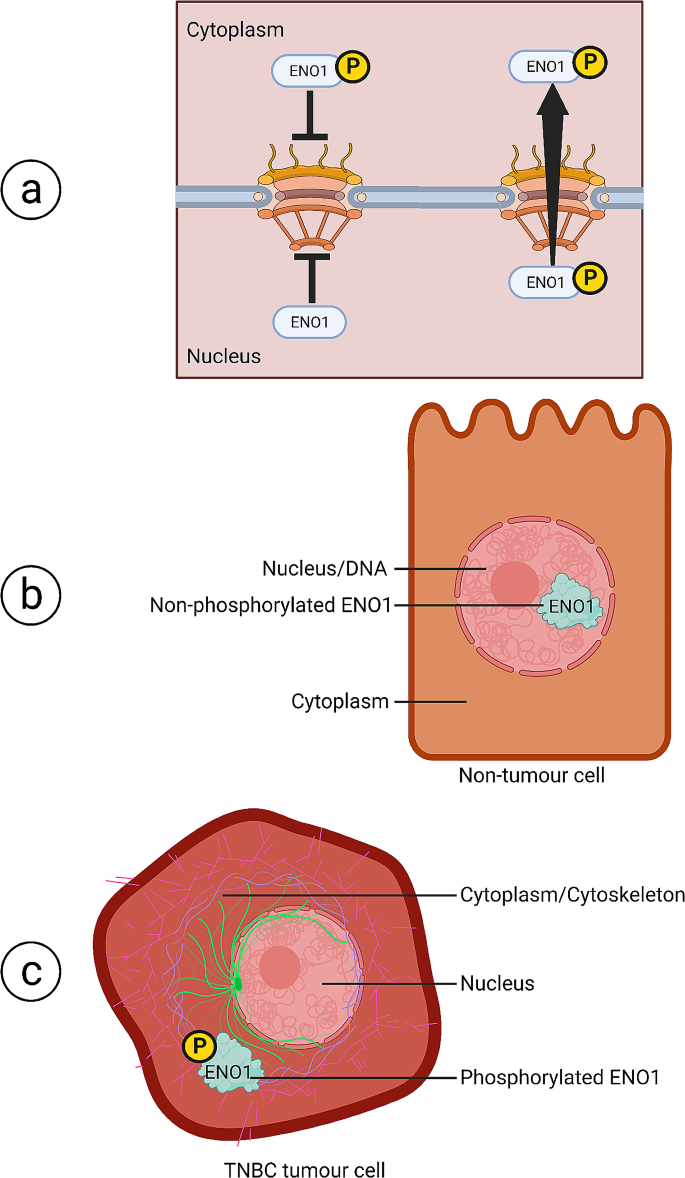
三阴性乳腺癌(TNBC)是乳腺癌中最具侵袭性的亚型,约占所有乳腺癌的10-20%,其核心特征为雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体2(HER2)表达缺失。临床治疗以化疗为主,但存在“三阴性悖论”——尽管化疗病理缓解率高,但患者长期预后极差,转移性TNBC患者确诊后3-5年内死亡率较高,因此亟需挖掘特异性生物标志物及可靶向的调控机制。α-烯醇化酶(ENO1)是糖酵解关键酶,同时作为“兼职”蛋白在18种以上癌症中过表达,已被报道为TNBC的潜在生物标志物。ENO1的亚细胞定位与其功能密切相关,核定位的ENO1/MBP-1在部分癌症中提示良好预后,但TNBC中ENO1核质转运的调控机制尚未明确,这一空白限制了ENO1作为TNBC治疗靶点的开发。本文针对这一问题,探讨了ENO1的肿瘤特异性翻译后修饰对其核输出的调控作用及功能意义,为TNBC的精准诊疗提供新方向。
2. 文献综述解析
作者围绕ENO1的功能多样性、亚细胞定位与癌症预后的关联、翻译后修饰对其调控的研究现状展开综述,核心逻辑为“ENO1的癌症相关功能→亚细胞定位的调控空白→翻译后修饰的潜在作用”。
现有研究证实ENO1在多种癌症中过表达,其糖酵解功能参与肿瘤细胞的Warburg效应,非糖酵解功能则涉及细胞侵袭、转移及化疗耐药等过程;ENO1的亚细胞定位具有组织和肿瘤特异性,核定位的ENO1/MBP-1在卵巢癌及浸润性导管癌中提示良好预后,而胞质定位的ENO1则与TNBC的恶性进展相关;翻译后修饰如甲基化、乙酰化、磷酸化可调控ENO1的亚细胞定位与功能,但现有研究多聚焦于ENO1的酶活调控,未涉及TNBC中ENO1核质转运的特异性调控机制,且未明确S419磷酸化位点在TNBC中的作用。
本文通过对比现有研究的空白,首次明确了TNBC中肿瘤特异性S419磷酸化通过CRM1介导的核输出调控ENO1的胞质定位,进而参与细胞骨架组织的功能,填补了ENO1在TNBC中核质转运调控机制的研究空白,为开发TNBC特异性治疗靶点提供了理论依据。
3. 研究思路总结与详细解析
本文以MCF10系列TNBC进展细胞系为模型,整体研究思路为“验证ENO1表达与定位的肿瘤特异性变化→筛选并验证调控其定位的磷酸化位点→明确核输出通路→解析功能后果”,形成“现象-机制-功能”的完整研究闭环,核心科学问题是TNBC中ENO1的核质转运调控机制及功能意义。
3.1 ENO1在TNBC进展模型中的表达与定位分析
实验目的:明确ENO1的表达水平与亚细胞定位是否随TNBC细胞恶性程度升高发生特异性变化。
方法细节:采用MCF10系列等基因细胞系(MCF10A非肿瘤、MCF10AT癌前、MCF10Ca1h肿瘤、MCF10Ca1a转移),通过实时荧光定量PCR(qRT-PCR)检测ENO1 mRNA表达,蛋白质免疫印迹(Western blot)检测蛋白表达水平,免疫荧光结合共聚焦激光扫描显微镜(CLSM)观察ENO1的亚细胞定位,并计算核质荧光强度比(Fn/c)以量化定位差异。
结果解读:mRNA表达分析显示,ENO1表达随细胞恶性程度升高而显著增加,MCF10Ca1h和MCF10Ca1a细胞的ENO1 mRNA水平分别为MCF10A的3倍(n=3,P<0.001)和3倍(n=3,P<0.0001);蛋白表达在MCF10Ca1h细胞中显著升高2倍(n=3,P<0.01);亚细胞定位方面,MCF10Ca1h细胞的ENO1核质荧光比为0.59(n>30,P=0.03),核定位显著低于MCF10A细胞,而MCF10Ca1a细胞无显著差异;GFP标记的ENO1转染实验进一步证实,MCF10Ca1h细胞中GFP-ENO1的核质荧光比为0.50(n>30,P<0.001),核定位显著降低。
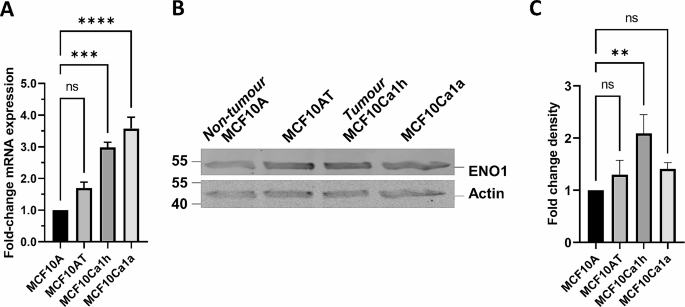
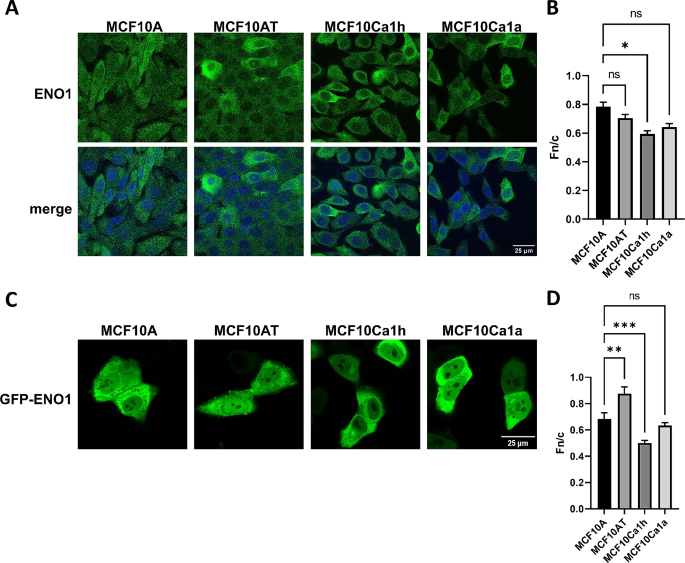
产品关联:实验所用关键产品:Abcam的抗ENO1抗体(货号ab155102)、抗泛磷酸化丝氨酸抗体(货号ab9332),Cell Signaling Technology的抗肌动蛋白抗体(货号3700),Thermo Fisher Scientific的抗V5抗体(货号R960-25)等。
3.2 ENO1磷酸化位点筛选与验证
实验目的:筛选TNBC中调控ENO1亚细胞定位的关键磷酸化位点,并验证其在细胞模型中的存在。
方法细节:分析TCGA数据库中TNBC患者的磷酸化组学数据,筛选ENO1的差异磷酸化位点;在MCF10A和MCF10Ca1h细胞中转染GFP-ENO1,通过GFP-trap免疫沉淀富集ENO1蛋白,再通过蛋白质免疫印迹检测丝氨酸磷酸化水平。
结果解读:从TCGA数据库中筛选到ENO1的11个磷酸化位点,其中丝氨酸419(S419)在TNBC和激素受体阳性乳腺癌中均存在,且TNBC患者样本中S419磷酸化水平有升高趋势;细胞模型验证显示,MCF10A和MCF10Ca1h细胞中的GFP-ENO1均检测到丝氨酸磷酸化信号,证实ENO1在TNBC细胞模型中存在磷酸化修饰。
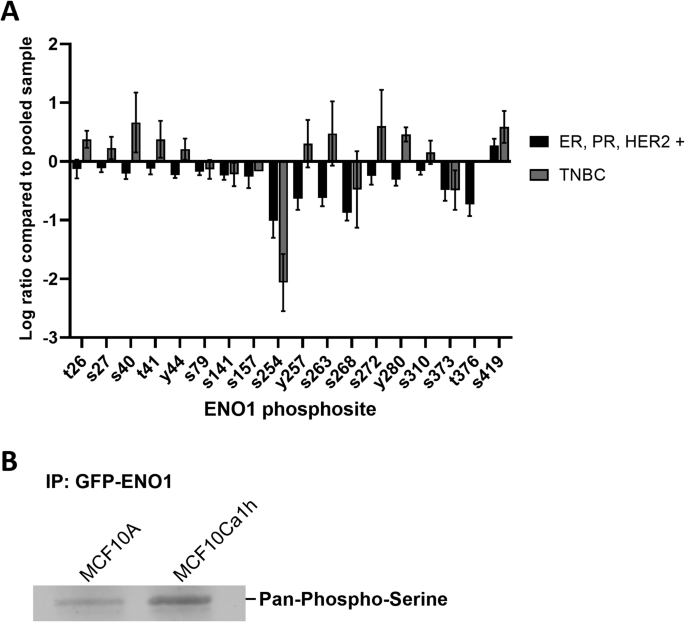
产品关联:实验所用关键产品:Abcam的抗泛磷酸化丝氨酸抗体(货号ab9332),ChromoTek的GFP-Trap树脂等。
3.3 S419磷酸化对ENO1亚细胞定位的调控
实验目的:验证S419磷酸化是否为调控ENO1亚细胞定位的关键位点,并明确其上游激酶。
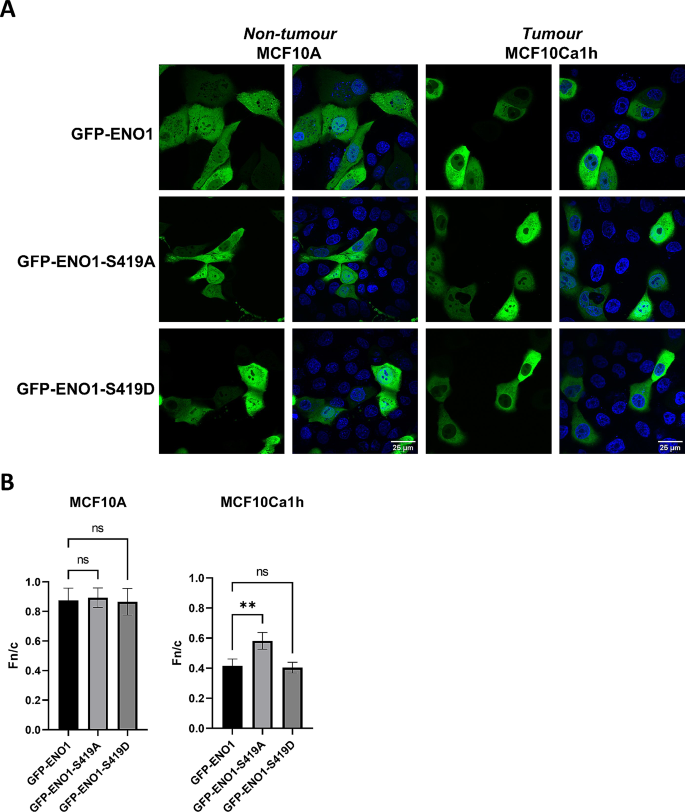
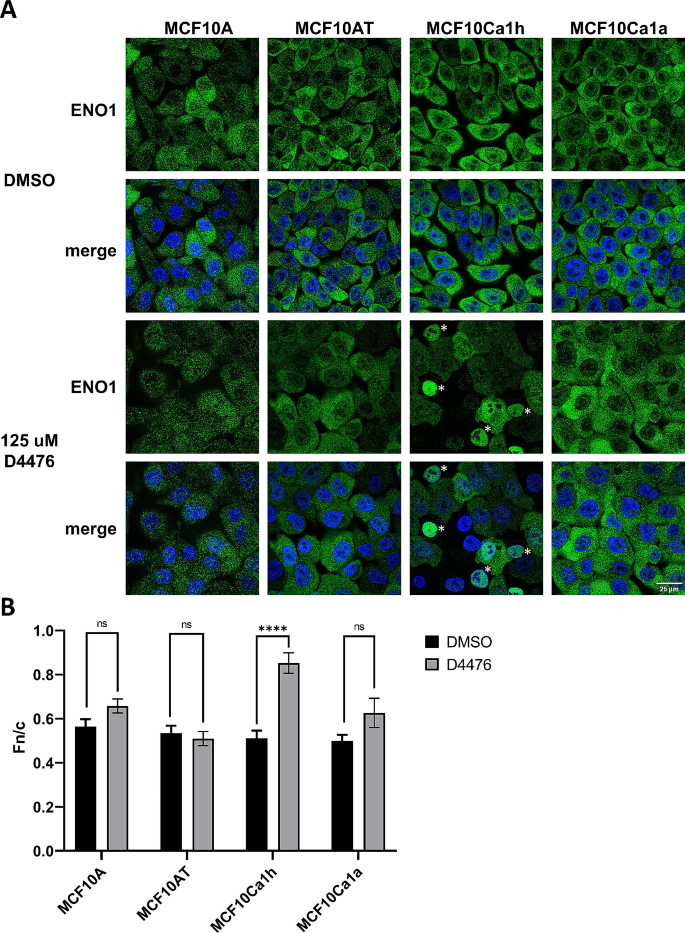
方法细节:构建GFP-ENO1-S419A(磷酸化缺失突变体)和GFP-ENO1-S419D(磷酸化模拟突变体)质粒,转染MCF10A和MCF10Ca1h细胞,通过共聚焦激光扫描显微镜检测亚细胞定位;使用酪蛋白激酶1(CK1)特异性抑制剂D4476处理MCF10系列细胞,检测内源性ENO1的亚细胞定位变化。
结果解读:在MCF10Ca1h肿瘤细胞中,S419A突变体的核质荧光比为0.41±0.04(n>30,P=0.006),核定位显著高于野生型GFP-ENO1;D4476处理后,MCF10Ca1h细胞的ENO1核质荧光比从0.5±0.03升高至0.85±0.04(n>50,P<0.0001),核定位显著增加,约10%的细胞出现ENO1完全核定位,而MCF10A、MCF10AT及MCF10Ca1a细胞无显著变化,证实CK1介导的S419磷酸化特异性调控肿瘤细胞中ENO1的亚细胞定位。
产品关联:实验所用关键产品:Abcam的CK1抑制剂D4476,GenScript构建的GFP-ENO1突变体质粒等。
3.4 ENO1核输出通路的验证
实验目的:明确S419磷酸化调控ENO1核输出的具体通路。
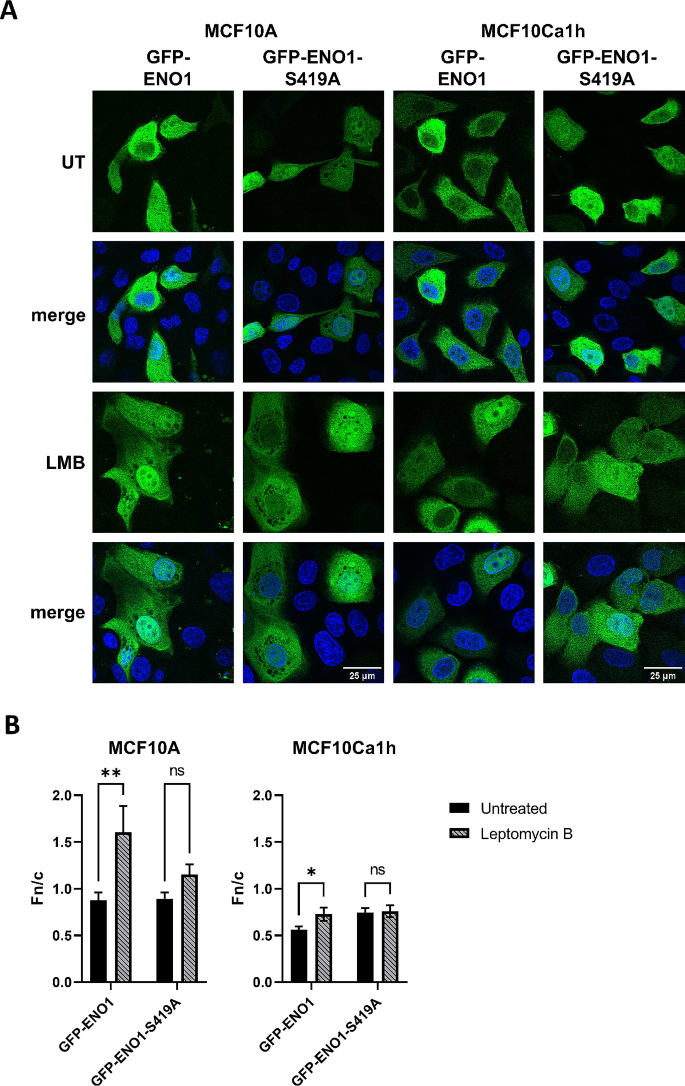
方法细节:使用CRM1(Exportin-1)特异性抑制剂Leptomycin B(LMB)处理转染GFP-ENO1和S419A突变体的MCF10A和MCF10Ca1h细胞,通过共聚焦激光扫描显微镜检测亚细胞定位变化;同时通过蛋白质免疫印迹检测LMB处理对ENO1磷酸化水平的影响。
结果解读:LMB处理后,MCF10Ca1h细胞中野生型GFP-ENO1的核质荧光比从0.56±0.03升高至0.72±0.07(n>30,P=0.0339),核定位显著增加,且与未处理的S419A突变体的核定位水平一致;S419A突变体经LMB处理后核定位无进一步增加,同时蛋白质免疫印迹显示LMB处理不影响ENO1的丝氨酸磷酸化水平,证实S419磷酸化通过CRM1介导的核输出通路调控ENO1的胞质定位。
产品关联:实验所用关键产品:BioAustralis的Leptomycin B等。
3.5 S419磷酸化对ENO1酶活与互作组的影响
实验目的:解析S419磷酸化对ENO1功能的调控作用,明确其非糖酵解功能的分子机制。
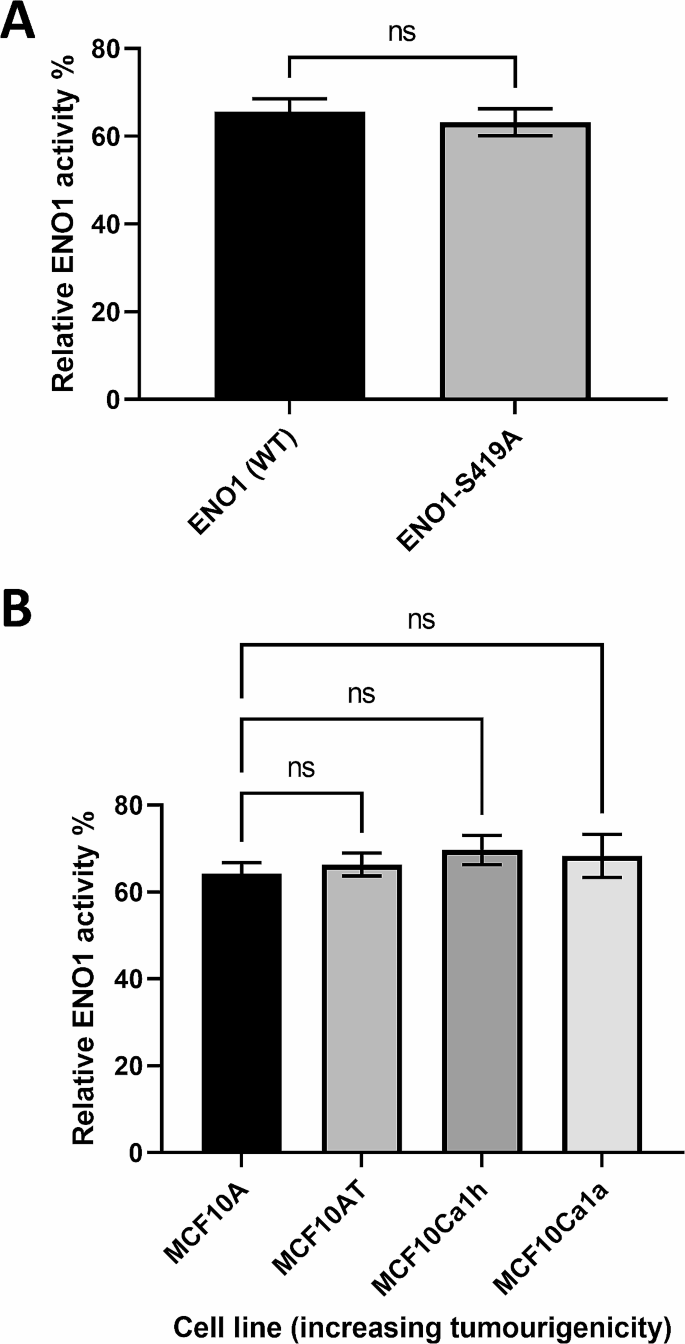
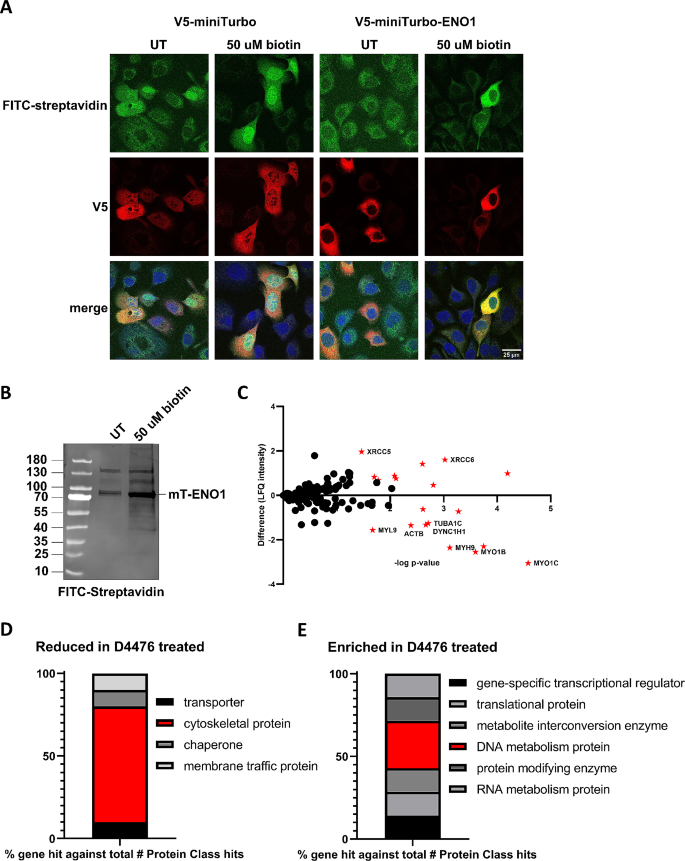
方法细节:重组表达野生型ENO1和S419A突变体蛋白,使用ENO1活性检测试剂盒检测糖酵解酶活;在MCF10Ca1h细胞中表达V5标记的miniTurbo-ENO1,经D4476处理后,通过生物素标记结合LC-MS/MS分析ENO1的互作蛋白组。
结果解读:酶活检测显示,野生型ENO1和S419A突变体的相对酶活分别为61±7%和64±4%(n=3,P>0.05),说明S419磷酸化不调控ENO1的糖酵解酶活;互作组分析显示,D4476处理后,ENO1与细胞骨架调控蛋白(肌球蛋白、微管蛋白、肌动蛋白)的互作显著减少,而与DNA修复、端粒相关蛋白的互作显著增加。
产品关联:实验所用关键产品:Abcam的ENO1活性检测试剂盒(货号ab117994),Thermo Fisher Scientific的抗V5抗体(货号R960-25)等。
4. Biomarker研究及发现成果解析
本文鉴定的核心Biomarker为ENO1的S419磷酸化位点,其筛选与验证逻辑为“TCGA数据库差异筛选→细胞模型表达验证→功能实验机制解析”,为TNBC的恶性程度评估及治疗靶点开发提供了新的候选标志物。
该Biomarker的来源为TNBC患者临床样本及MCF10系列细胞模型,验证方法包括磷酸化组学分析、蛋白质免疫印迹、免疫荧光及功能实验;特异性方面,S419磷酸化仅在TNBC肿瘤细胞中调控ENO1的胞质定位,非肿瘤细胞中虽存在S419磷酸化,但无此调控功能;敏感性方面,MCF10Ca1h肿瘤细胞中,抑制S419磷酸化可导致ENO1核定位显著变化(P<0.0001),提示该位点的磷酸化状态可敏感反映肿瘤细胞的恶性特征。
核心成果提炼:该Biomarker的功能关联在于,S419磷酸化介导的ENO1胞质定位可促进其与细胞骨架调控蛋白的互作,进而参与TNBC细胞的侵袭与转移过程;创新性为首次明确了ENO1的肿瘤特异性核输出调控机制,填补了TNBC中ENO1翻译后修饰与功能调控的研究空白;统计学结果显示,MCF10Ca1h细胞中S419A突变体与野生型的核定位差异显著(P=0.006),D4476处理后的核定位变化也具有高度统计学意义(P<0.0001)。此外,该Biomarker的临床应用潜力在于,ENO1的S419磷酸化状态及亚细胞定位可作为TNBC恶性程度的评估指标,同时针对该位点的磷酸化或CRM1通路的抑制剂可作为TNBC的潜在治疗策略。