1. 领域背景与文献引入
文献英文标题:Hierarchical imaging: a new concept for targeted imaging of large volumes from cells to tissues;发表期刊:BMC Cell Biology;影响因子:3.4(2016年);研究领域:细胞生物学-生物成像技术
在细胞生物学研究中,生物成像技术是解析细胞亚细胞结构、组织空间架构的核心手段。电子显微镜(EM)凭借纳米级分辨率,成为研究细胞超微结构的金标准,但早期EM技术难以实现大体积样本(如完整细胞、组织器官)的三维成像。随着技术发展,体积EM技术逐渐兴起,主要分为块面成像法(如连续块面扫描电镜SBFSEM、聚焦离子束扫描电镜FIBSEM)和阵列断层扫描(AT)两类。块面成像法可直接对树脂包埋样本进行循环成像与切割,无需额外切片处理,适合大体积组织分析,但存在样本破坏性成像、需高金属化染色、产生大量冗余数据等局限性;AT方法通过将连续超薄切片沉积在固体基底上,支持光镜与电镜多模态成像,样本可重复利用,但传统AT设备适配性差,仅能处理小尺寸基底(如TEM铜网),且手动成像效率极低,难以满足大体积样本的高效分析需求。
针对现有体积EM技术的核心缺陷,本研究旨在开发一套高效的层级成像工作流,通过定制化样本处理工具解决连续切片的可靠获取问题,结合自动化靶向成像策略平衡分辨率、数据量与样本利用效率,为从细胞到组织的大体积超微结构研究提供全新技术方案,填补领域内大体积靶向纳米成像的方法学空白。
2. 文献综述解析
本文作者以体积EM技术的技术路径为分类维度,将现有研究分为块面成像技术与阵列断层扫描技术两大方向,系统梳理了两类技术的优势与局限性,并明确了领域内未解决的核心问题。
块面成像技术(SBFSEM、FIBSEM)的核心优势在于无需提前制备切片,可直接对树脂包埋样本进行三维成像,适合完整器官等超大体积样本的结构解析,且成像过程自动化程度较高;但其局限性也十分显著,成像过程具有破坏性,样本会被完全消耗无法重复利用,同时需要对样本进行高浓度重金属染色以提升成像对比度,且由于需对整个块面进行高分辨率成像,会产生海量冗余数据,增加存储与分析成本。阵列断层扫描技术(AT)的优势在于可将连续切片转移至固体基底,支持光镜、电镜多模态成像,样本可重复进行染色与成像,且能实现更高的轴向分辨率;但传统AT设备存在适配性差的问题,仅能兼容TEM铜网等小尺寸基底,无法利用大尺寸基底实现多切片阵列的高效制备,同时手动成像过程耗时极长,难以实现大样本的批量分析。
通过对比现有技术的未解决问题,本研究的创新价值凸显:首次开发了具有7个自由度的定制化基底支架,可适配不同类型的超薄切片机与多种基底材料(硅片、ITO涂层玻璃盖玻片等),实现数百片连续切片的可靠获取与有序排列;结合ZEISS Atlas 5平台构建了自动化层级成像工作流,从低分辨率全景成像到高分辨率靶向成像,仅对感兴趣区域进行高分辨率数据采集,大幅降低数据量,同时实现样本的多模态重复利用,为体积EM技术的实用化提供了关键方法学支撑。
3. 研究思路总结与详细解析
本研究的核心目标是构建一套从样本制备到成像分析的完整层级成像工作流,解决现有体积EM技术的样本处理与数据效率问题;核心科学问题为如何实现连续切片的可靠获取与靶向层级成像,在保证纳米级分辨率的同时控制数据量并提升样本利用率;技术路线遵循“工具开发→方法验证→应用拓展”的闭环逻辑:定制化基底支架设计与优化→连续切片阵列制备→多模态成像验证→细胞群体与组织样本的层级成像分析→技术优势总结。
3.1 定制化基底支架的设计与验证
实验目的:解决传统AT技术中连续切片难以可靠获取、基底适配性差的问题,实现大尺寸基底上多切片条带的有序沉积。
方法细节:设计具有7个平移/旋转轴的基底支架,可适配Leica UC7、RMC Powertome等不同型号的超薄切片机,以及标准振动隔离台与主动振动隔离平台;使用Jumbo钻石刀适配大尺寸基底(最大至载玻片规格),将硅片、ITO涂层玻璃盖玻片等基底固定在载玻片支架上,通过控制支架的多轴移动轨迹,将切片条带引导至基底的干燥区域并附着,完成后通过优化的提升轨迹将基底从刀槽中取出。
结果解读:该支架可在不同实验配置下,可靠沉积由数百片切片组成的多条连续条带(如12条带共约270片切片),支持50nm至1μm厚度的切片处理,且提升基底时不会破坏切片条带的完整性;支架的多轴设计可适配旋转刀位,大幅提升样本制备的灵活性。
产品关联:实验所用关键产品:Jumbo钻石刀(Diatome, Switzerland)、Leica UC7超薄切片机、RMC Powertome PC超薄切片机。

3.2 连续切片阵列的光镜成像与三维重建
实验目的:验证切片阵列在光镜下的成像能力,实现大体积样本的三维结构重建。
方法细节:将拟南芥根样本包埋在Lowicryl HM20亲水性树脂中,制备100nm厚度的连续切片阵列,使用1μg/mL碘化丙啶对切片进行染色,在ZEISS Cell Observer宽场荧光显微镜下采集图像,通过TrakEM2软件对200片切片的图像进行对齐与三维重建。
结果解读:宽场荧光显微镜成像可实现200nm横向分辨率与100nm轴向分辨率,200片切片的三维重建覆盖了约20μm的根组织宽度,可清晰显示根细胞的整体结构与空间分布,且由于切片厚度小于共聚焦显微镜的轴向分辨极限,即使过度染色的样本也能获得高质量图像。
产品关联:实验所用关键产品:Lowicryl HM20树脂、碘化丙啶(Sigma-Aldrich, USA)、ZEISS Cell Observer宽场荧光显微镜。

3.3 电镜层级成像的自动化实现
实验目的:构建自动化层级成像工作流,实现从全景到靶向区域的多分辨率成像,减少冗余数据量。
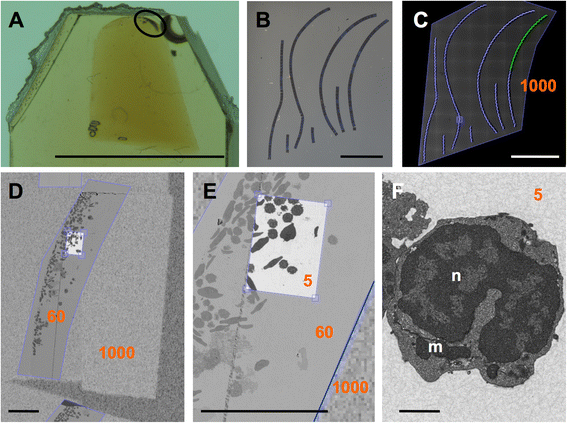
方法细节:将斑马鱼脾脏分离的免疫细胞样本包埋在环氧树脂中,制备连续切片阵列,使用ZEISS Crossbeam 540场发射扫描电镜,结合Atlas 5 Array Tomography平台,先以1000nm像素分辨率成像整个切片阵列,确定样本区域;再以60nm像素分辨率成像样本的完整区域,筛选感兴趣细胞;最后以5nm像素分辨率成像目标细胞的特定区域。
结果解读:实现了从宏观切片阵列到单个细胞亚细胞结构的无缝分辨率切换,仅对感兴趣区域进行高分辨率成像,大幅降低数据存储与处理成本;成像过程完全自动化,可在短时间内完成大样本的多分辨率数据采集。
产品关联:实验所用关键产品:ZEISS Crossbeam 540场发射扫描电镜、ZEISS Atlas 5 Array Tomography平台。
3.4 细胞群体与组织样本的层级成像分析
实验目的:验证层级成像工作流在细胞群体统计与组织极性分析中的应用价值。
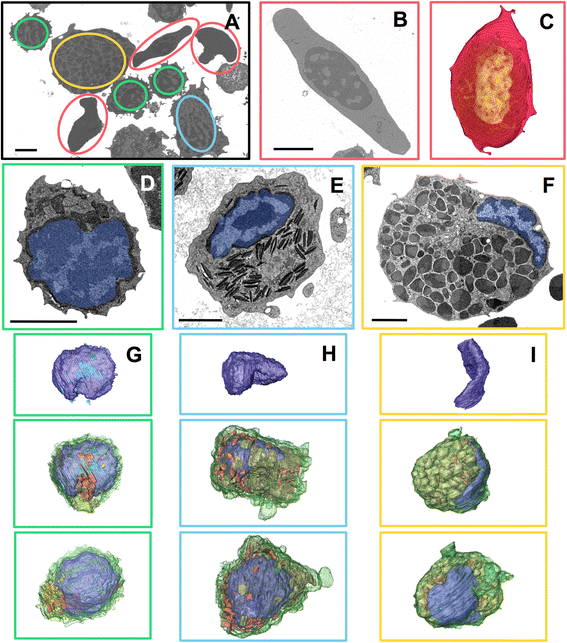
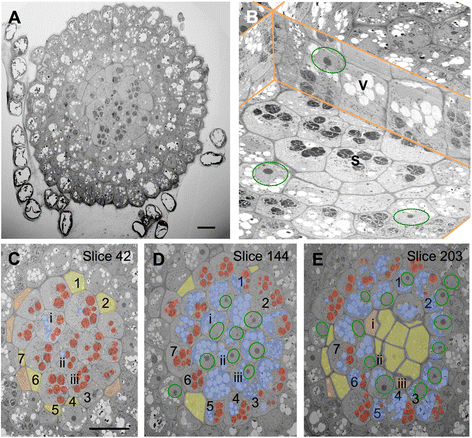
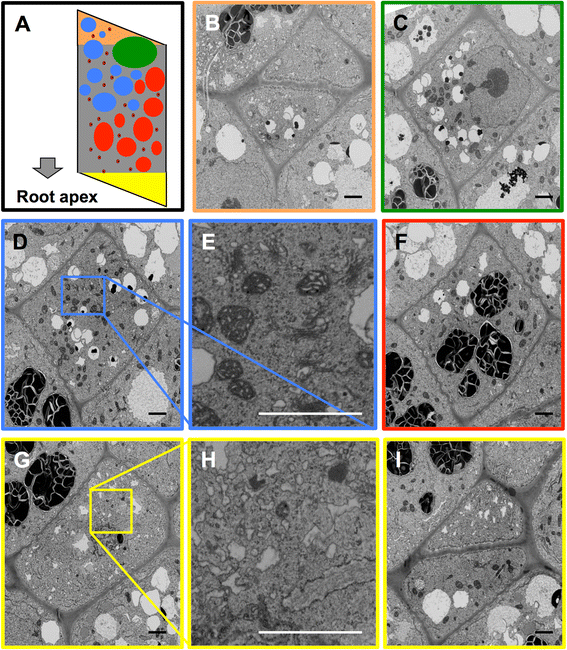
方法细节:对斑马鱼脾脏免疫细胞群体,通过60nm分辨率成像统计239个细胞(n=239)的类型比例,通过5nm分辨率成像对单个细胞进行三维重建与细胞器组成分析;对水芹根冠组织,先以60nm分辨率成像240片切片的完整根冠结构,再以5nm分辨率成像单个细胞,分析细胞器的极性分布特征。
结果解读:在斑马鱼免疫细胞群体中,细胞毒性细胞为主要亚群,不同细胞类型的细胞器组成与形态存在显著差异,可通过细胞器特征进行细胞类型的精准识别;水芹根冠细胞的细胞器呈现明显的极性分布,顶端区域无大型细胞器,仅存在复杂的膜系统,而线粒体、高尔基体等细胞器主要分布在细胞的中下部区域。
产品关联:文献未提及具体实验产品,领域常规使用环氧树脂包埋剂、铀铅染色试剂等。
4. Biomarker研究及发现成果
本文属于生物成像技术方法学研究,未聚焦于疾病相关生物标志物(Biomarker)的筛选与验证,而是开发了一套层级成像技术平台,为细胞与组织的结构特征分析提供新工具,其技术成果可直接应用于结构类Biomarker的可视化与定位研究。
Biomarker定位
本研究中,细胞的细胞器组成与形态特征可作为细胞身份的结构类Biomarker,通过层级成像的高分辨率分析,可基于细胞器的类型、数量与分布模式实现细胞类型的精准识别;同时组织细胞的极性结构特征可作为组织功能的结构Biomarker,反映细胞的功能分工与组织的空间架构。
研究过程详述
针对斑马鱼免疫细胞群体,通过层级成像的60nm分辨率成像统计239个细胞(n=239)的类型比例,结合5nm分辨率成像的细胞器分析,定义了不同免疫细胞类型的结构特征,如细胞毒性细胞的核质比高、细胞质中存在大量分泌溶酶体,粒细胞则具有特征性的颗粒结构;针对水芹根冠组织,通过60nm分辨率成像的全景分析确定细胞的极性分布模式,再通过5nm分辨率成像的单个细胞分析,明确了细胞器的极性分布细节,如顶端区域仅存在膜系统,线粒体等细胞器集中在细胞中下部。
核心成果提炼
本研究建立的层级成像工作流可实现细胞群体的统计分析与单个细胞的纳米级结构解析,其创新性在于通过靶向成像大幅降低数据量,同时实现样本的多模态重复利用;该技术可作为结构Biomarker分析的高效工具,为细胞生物学、发育生物学等领域的结构功能研究提供关键支撑,由于为方法学验证研究,无组间比较的统计学显著性P值。
