1. 领域背景与文献引入
文献英文标题:Discovery and mechanism studies of a novel ATG4B inhibitor Ebselen by drug repurposing and its anti-colorectal cancer effects in mice;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:结直肠癌与自噬靶向治疗
自噬是真核生物维持细胞稳态的关键降解途径,参与代谢应激响应、发育调控等生理过程,其功能异常与肿瘤、神经退行性疾病等密切相关(领域共识)。自噬相关蛋白ATG4B作为半胱氨酸蛋白酶,是自噬通路的核心调控因子,负责LC3B的加工与去脂化,对自噬体的形成与成熟至关重要。近年来研究表明,ATG4B在结直肠癌等多种肿瘤中高表达,敲低ATG4B可抑制结直肠癌细胞周期进程与增殖,成为结直肠癌治疗的潜在靶点。然而,现有ATG4B抑制剂存在效率不足、机制不明确、缺乏体内验证等问题,多数仅完成体外实验,且安全性未得到充分验证,限制了其临床转化应用。针对这一研究空白,本研究通过老药新用策略,从FDA已批准药物库中筛选高效、安全的ATG4B抑制剂,明确其作用机制,并在细胞与动物模型中验证其抗结直肠癌效果,为结直肠癌的靶向治疗提供新的候选药物与理论依据。
2. 文献综述解析
作者围绕ATG4B作为肿瘤治疗靶点的研究现状,从抑制剂筛选方法、抑制剂类型、研究局限性三个维度对现有研究进行分类评述,明确现有研究的核心结论与不足,凸显本研究的创新价值。
现有研究证实,ATG4B在结直肠癌等肿瘤中高表达,是潜在的治疗靶点,已有多种ATG4B抑制剂被报道,包括基于底物肽的共价结合抑制剂(如FMK系列)、天然产物衍生物、虚拟筛选得到的小分子化合物等。这些抑制剂通过不同机制抑制ATG4B活性,部分抑制剂在体外细胞实验中显示出肿瘤生长抑制效果,但多数研究仅停留在体外验证阶段,缺乏体内动物模型的疗效评估,且对抑制剂的作用机制阐释不充分,部分抑制剂的选择性与安全性有待进一步验证。此外,现有抑制剂多为全新合成化合物,面临研发周期长、成本高、临床转化难度大等问题。本研究通过老药新用策略,从FDA已批准药物库中筛选ATG4B抑制剂,既规避了全新药物研发的风险,又能利用已有的安全性数据加速临床转化;同时,本研究首次阐明Ebselen通过共价结合ATG4B的Cys74位点,以及诱导ATG4B在Cys292/Cys361位点形成寡聚体的双重机制抑制ATG4B活性,并在体内外模型中验证其抗结直肠癌效果,弥补了现有研究在机制阐释与体内验证方面的不足。
3. 研究思路总结与详细解析
本研究以“筛选高效安全的ATG4B抑制剂并阐明其抗结直肠癌机制”为核心目标,遵循“高通量筛选→活性与选择性验证→机制阐明→细胞与动物模型验证”的闭环技术路线,通过多组实验明确Ebselen作为ATG4B抑制剂的双重作用机制与抗结直肠癌效果,为老药新用提供了完整的实验证据链。
3.1 ATG4B抑制剂的高通量筛选与活性验证
实验目的:从FDA已批准药物库中筛选具有高效ATG4B抑制活性的化合物。
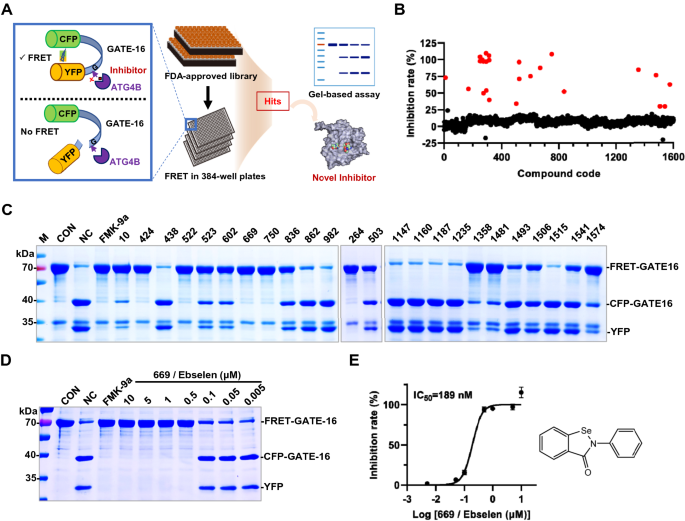
方法细节:构建基于荧光共振能量转移(FRET)的高通量筛选平台,将重组ATG4B蛋白与1600种已批准药物(10μM)共同孵育30分钟后,加入FRET底物FRET-GATE-16,检测抑制率;对初筛得到的24种候选化合物,采用凝胶电泳法验证其对ATG4B底物切割的抑制作用;对9种可商业化的候选化合物进行IC₅₀测定,最终确定活性最优的化合物。
结果解读:FRET筛选共得到24种候选化合物,凝胶验证排除假阳性后,9种化合物进入IC₅₀测定,其中化合物Ebselen的ATG4B抑制活性最强,IC₅₀为189nM(n=3,P<0.05);FRET与凝胶电泳的剂量反应曲线均显示Ebselen对ATG4B的抑制具有剂量依赖性。
产品关联:实验所用关键产品:TargetMol的FDA-approved Drug Screening Library(L1000)、Sigma的Ebselen(E3520)、Proteintech的ATG4B抗体(15131-1-AP)。
3.2 Ebselen对ATG4B的选择性与构效关系分析
实验目的:验证Ebselen对ATG4B的选择性,并初步分析其构效关系。
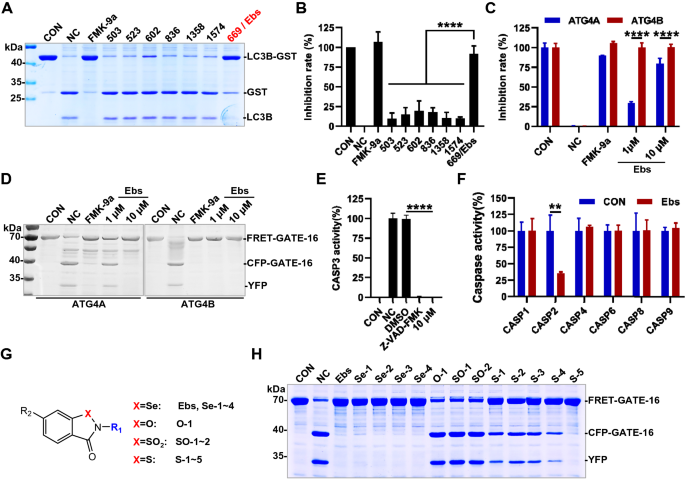
方法细节:采用细胞裂解物中的LC3B-谷胱甘肽-S-转移酶(GST)切割实验验证Ebselen对细胞内ATG4B的抑制活性;通过FRET与凝胶电泳实验检测Ebselen对ATG4A(ATG4家族同源蛋白)的抑制活性;检测Ebselen对半胱氨酸蛋白酶Caspase家族(Caspase-1、2、3、4、6、8、9)的抑制作用;合成Ebselen的结构类似物,分析其构效关系。
结果解读:Ebselen可时间与剂量依赖性地抑制细胞内ATG4B活性;对ATG4A的抑制活性显著弱于ATG4B,1μM Ebselen可完全抑制ATG4B,但仅部分抑制ATG4A;对多数Caspase无显著抑制作用,仅对Caspase-2和Caspase-3有一定抑制;构效关系分析显示,Ebselen母核中的Se原子是其活性关键,替换为O或SO₂原子后活性消失,侧链修饰对活性的影响无明显规律,表明其结构具有优化潜力。
产品关联:实验所用关键产品:Sigma的LC3B抗体(L7543)、Beyotime的Caspase活性检测试剂盒(C1101、C1107等)。
3.3 Ebselen与ATG4B的共价结合机制验证
实验目的:阐明Ebselen与ATG4B的结合方式与关键位点。
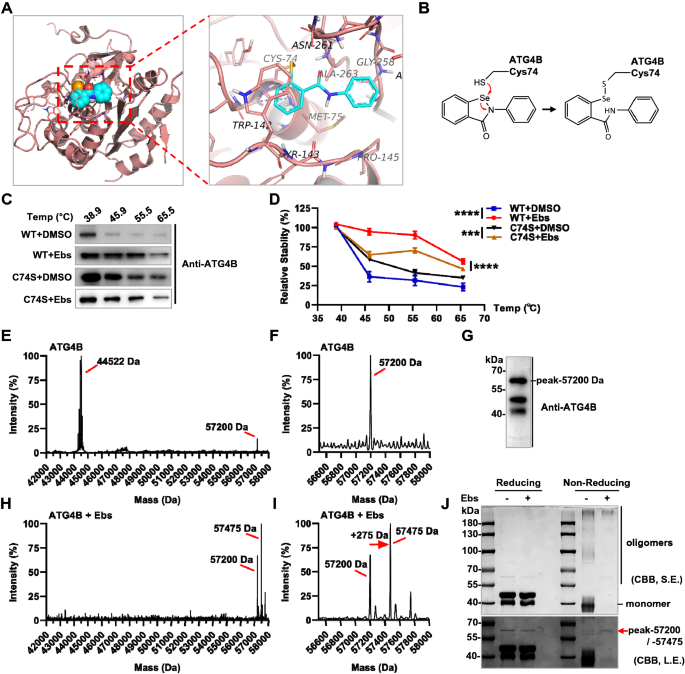
方法细节:采用分子对接模拟Ebselen与ATG4B的结合模式;构建ATG4B的Cys74Ser突变体,通过热位移实验(TSA)验证结合位点;采用变性质谱与非还原电泳验证共价结合。
结果解读:分子对接显示Ebselen可共价结合ATG4B的Cys74位点,并与Trp142等形成π-π堆积与疏水相互作用;热位移实验显示Ebselen可显著提高野生型ATG4B的热稳定性,但对Cys74Ser突变体的热稳定性提升作用显著减弱;变性质谱显示Ebselen处理后ATG4B单体峰消失,出现结合Ebselen的寡聚体峰,非还原电泳显示ATG4B单体减少,寡聚体增加,证实Ebselen与ATG4B的Cys74位点共价结合。
产品关联:实验所用关键产品:Schrödinger的Maestro分子对接软件、Waters的SYNAPT G2-Si质谱仪。
3.4 Ebselen诱导ATG4B寡聚化的机制研究
实验目的:探究Ebselen诱导ATG4B寡聚化的关键位点与生物学意义。
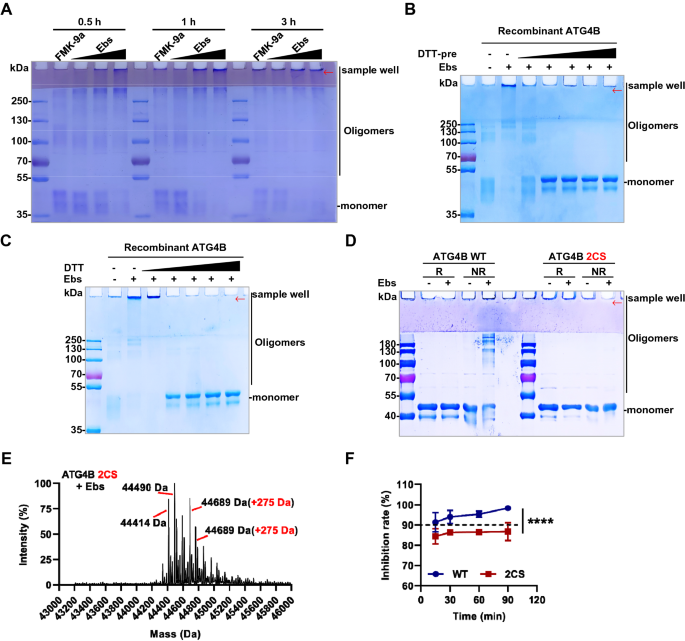
方法细节:将ATG4B与不同浓度Ebselen孵育不同时间,采用非还原电泳检测寡聚化;加入还原剂二硫苏糖醇(DTT)验证寡聚化的可逆性;构建ATG4B的Cys292/361Ser双突变体,检测Ebselen对其寡聚化的影响;通过FRET实验比较Ebselen对野生型与突变体ATG4B的抑制活性。
结果解读:Ebselen可浓度与时间依赖性地诱导ATG4B寡聚化,且该寡聚化可被DTT逆转;Cys292/361Ser双突变体在Ebselen处理后未出现寡聚化,表明寡聚化依赖Cys292与Cys361位点;FRET实验显示Ebselen对野生型ATG4B的抑制率随孵育时间延长而升高,对双突变体的抑制率无明显变化,表明寡聚化可增强Ebselen对ATG4B的抑制作用。
产品关联:文献未提及具体实验产品,领域常规使用DTT、PCR仪等试剂与仪器。
3.5 Ebselen对自噬通量的抑制作用验证
实验目的:验证Ebselen通过抑制ATG4B抑制自噬通量。
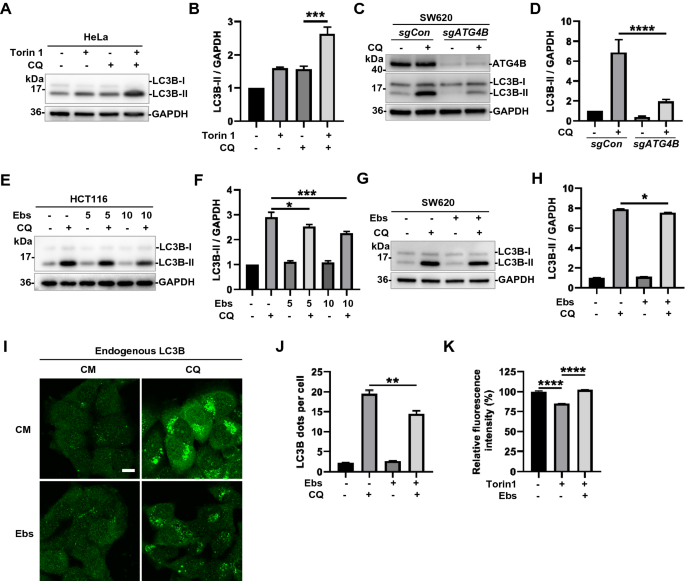
方法细节:采用蛋白质免疫印迹(Western blot)检测自噬标志物LC3B与p62的表达;通过免疫荧光检测LC3B斑点的数量;采用长寿命蛋白降解实验验证自噬通量的变化;构建ATG4B敲低的SW620细胞系,对比Ebselen对敲低细胞与野生型细胞自噬的影响。
结果解读:Ebselen与氯喹(CQ)联合处理后,HCT116与SW620细胞中LC3B-II水平降低,p62水平升高;免疫荧光显示Ebselen处理后LC3B斑点数量减少;长寿命蛋白降解实验显示Ebselen可显著抑制Torin 1诱导的自噬降解;ATG4B敲低细胞的自噬通量显著降低,Ebselen对其自噬的抑制作用减弱,证实Ebselen通过抑制ATG4B抑制自噬通量。
产品关联:实验所用关键产品:MBL的免疫荧光用LC3B抗体(PM036)、ThermoFisher的流式细胞仪(CytoFLEX S)。
3.6 Ebselen抑制结直肠癌细胞增殖的机制验证
实验目的:验证Ebselen通过抑制ATG4B抑制结直肠癌细胞增殖,且不依赖凋亡途径。
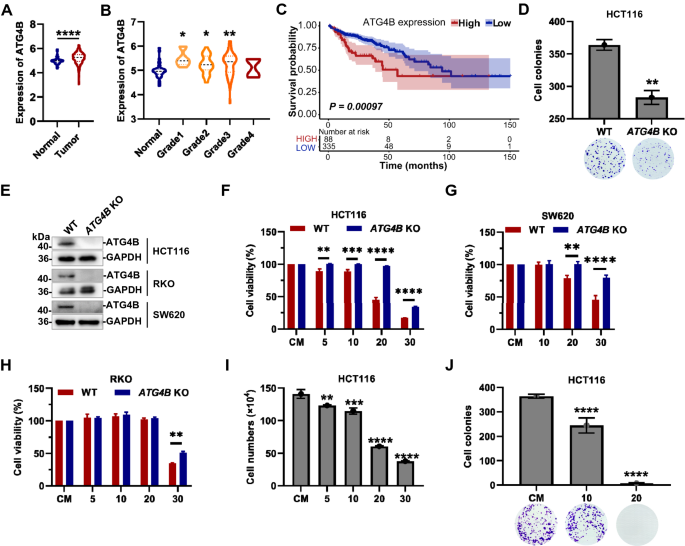
方法细节:通过TCGA数据库分析ATG4B在结直肠癌中的表达与预后的关系;构建ATG4B敲除的结直肠癌细胞系(HCT116、SW620、RKO),采用CCK-8、细胞计数、克隆形成实验检测Ebselen对野生型与敲除细胞的增殖抑制作用;通过Western blot检测凋亡标志物聚腺苷二磷酸核糖聚合酶(PARP)的切割,验证Ebselen是否诱导凋亡。
结果解读:TCGA数据库显示结直肠癌患者ATG4B表达显著高于正常组织(n=288 vs n=41,P<0.05),且高表达与不良预后相关(文献未明确提供HR值,基于生存曲线趋势推测);Ebselen对野生型结直肠癌细胞的增殖抑制作用显著强于ATG4B敲除细胞(HCT116野生型IC₅₀=18.9μM,敲除型IC₅₀=28.1μM,n=3,P<0.05);细胞计数与克隆形成实验显示Ebselen可显著抑制细胞增殖与克隆形成;Western blot显示Ebselen处理后未出现PARP切割,表明其抑制细胞增殖不依赖凋亡途径。
产品关联:实验所用关键产品:Bimake的CCK-8试剂盒(B34304)、Selleckchem的Staurosporine(STS,S1421)。
3.7 Ebselen抑制结直肠癌异种移植瘤生长的体内验证
实验目的:验证Ebselen在体内对结直肠癌的治疗效果与作用机制。
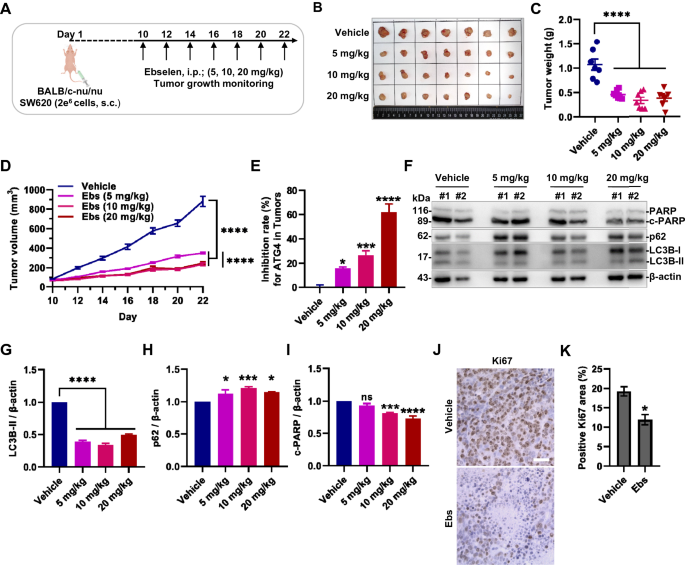
方法细节:将SW620与HCT116细胞接种于裸鼠皮下,建立异种移植瘤模型,待肿瘤体积达60-80mm³时,分别腹腔注射不同剂量Ebselen(5、10、20mg/kg,每两天一次),监测肿瘤体积与小鼠体重;实验结束后,检测肿瘤组织中ATG4B活性、自噬标志物表达、凋亡标志物表达,采用免疫组化(IHC)检测Ki67的表达。
结果解读:Ebselen可剂量依赖性地抑制异种移植瘤生长,10mg/kg剂量下肿瘤体积与重量显著降低(n=7,P<0.05),且小鼠体重无明显变化,未出现肝肾功能损伤;肿瘤组织中ATG4B活性显著降低,LC3B-II水平降低,p62水平升高,自噬通量被抑制;凋亡标志物PARP切割减少,Ki67阳性率显著降低,表明Ebselen通过抑制ATG4B与细胞增殖发挥抗肿瘤作用。
产品关联:实验所用关键产品:Servicebio的免疫组化检测服务、ThermoFisher的BALB/c-nu/nu裸鼠。
4. Biomarker研究及发现成果
本研究将ATG4B作为结直肠癌的预后生物标志物与治疗靶点,通过数据库分析、细胞实验与动物实验系统验证其临床价值,同时明确Ebselen作为ATG4B抑制剂的治疗潜力。
Biomarker定位:ATG4B是自噬通路的关键半胱氨酸蛋白酶,作为结直肠癌的预后生物标志物与治疗靶点,其筛选与验证逻辑为“TCGA数据库临床数据分析→细胞系表达验证→动物模型治疗效果验证”的完整链条。研究过程详述:TCGA数据库分析显示,结直肠癌患者肿瘤组织中ATG4B的mRNA表达水平显著高于正常结肠组织(n=288 vs n=41,P<0.05),且在不同分期的结直肠癌组织中均高表达;细胞系验证显示,结直肠癌细胞系(SW620、HCT116、RKO)中ATG4B的蛋白表达水平显著高于正常结肠上皮细胞系NCM460;动物模型中,Ebselen通过抑制ATG4B活性,显著抑制结直肠癌异种移植瘤的生长,且ATG4B敲除细胞对Ebselen的敏感性降低,证实ATG4B是Ebselen的关键作用靶点。核心成果提炼:ATG4B可作为结直肠癌的预后生物标志物,高表达患者的总体生存率显著低于低表达患者(文献未明确提供HR值,基于生存曲线趋势推测);同时,ATG4B是结直肠癌的有效治疗靶点,Ebselen作为ATG4B抑制剂,可通过共价结合与诱导寡聚化的双重机制抑制ATG4B活性,进而抑制自噬与结直肠癌生长,在体内模型中显示出良好的抗肿瘤活性与安全性,为结直肠癌的靶向治疗提供了新的候选药物。
