1. 领域背景与文献引入
文献英文标题:SAA1 increases NOX4/ROS production to promote LPS-induced inflammation in vascular smooth muscle cells through activating p38MAPK/NF-κB pathway;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:心血管疾病-动脉粥样硬化炎症分子机制
根据世界卫生组织数据,心血管疾病导致的死亡占全球总死亡人数的三分之一,动脉粥样硬化是心血管疾病的主要病理基础,其本质是血管壁的慢性炎症过程。血管平滑肌细胞(VSMC)作为血管壁的主要组成部分,在机械损伤、炎症刺激下发生表型转化,分泌大量炎症因子,参与动脉粥样硬化的起始与进展,这一过程的分子机制是当前研究热点。现有研究表明,血清淀粉样蛋白A1(SAA1)作为急性时相反应蛋白,在炎症状态下可升高1000倍,且与动脉粥样硬化的发生发展密切相关;脂多糖(LPS)作为革兰氏阴性菌细胞壁成分,可诱导多种细胞产生炎症反应;烟酰胺腺嘌呤二核苷酸磷酸氧化酶4(NOX4)是VSMC中活性氧(ROS)的主要来源,ROS可激活下游炎症通路;p38丝裂原活化蛋白激酶(p38MAPK)/核因子κB(NF-κB)是调控炎症因子表达的核心通路。但目前缺乏SAA1介导NOX4/ROS通路与p38MAPK/NF-κB通路串联调控LPS诱导VSMC炎症的直接实验证据,这一机制空白限制了动脉粥样硬化抗炎靶点的开发。因此,本研究旨在明确SAA1在LPS诱导VSMC炎症中的调控作用及分子机制,为动脉粥样硬化的防治提供新的理论依据。
2. 文献综述解析
本文综述部分以“动脉粥样硬化炎症机制-SAA1与炎症的关联-NOX4/ROS通路的作用-p38MAPK/NF-κB通路的调控”为逻辑主线,系统梳理了各组分在VSMC炎症中的研究现状,明确了现有研究的局限性与本研究的创新价值。
现有研究的关键结论包括,LPS可通过与细胞表面受体结合,诱导巨噬细胞、内皮细胞、VSMC等多种细胞表达并释放肿瘤坏死因子-α(TNF-α)、白细胞介素(IL)等炎症因子;SAA1在感染、创伤等炎症状态下由肝脏及局部细胞大量合成,其血清水平与炎症严重程度正相关,且可直接参与细胞的炎症调控;NOX4作为NOX家族成员,在VSMC中持续表达,其激活产生的ROS可介导细胞氧化应激,促进VSMC的增殖、迁移与炎症因子分泌;p38MAPK/NF-κB通路是炎症信号转导的核心通路,多种炎症刺激可通过该通路调控炎症因子的转录表达。现有研究的技术方法优势在于对各单一通路的调控机制研究较为深入,如LPS诱导炎症的信号通路、SAA1的表达调控等均有成熟的实验体系与验证方法,但局限性在于缺乏对SAA1、NOX4/ROS、p38MAPK/NF-κB通路之间串联调控关系的直接验证,无法明确SAA1在LPS诱导VSMC炎症中的具体作用节点。本研究的创新价值在于首次通过细胞实验明确了SAA1通过NOX4/ROS通路激活p38MAPK/NF-κB通路,进而促进LPS诱导VSMC炎症因子释放的完整调控链,填补了该领域的机制空白,为动脉粥样硬化的抗炎治疗提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的整体研究框架为:以LPS诱导的大鼠VSMC炎症模型为研究对象,首先验证处理条件的细胞安全性,明确LPS对SAA1表达的调控规律,随后探究SAA1对NOX4/ROS通路及炎症因子的影响,再通过RNA干扰(siRNA)与通路激活实验验证SAA1调控炎症的通路依赖性,最终明确SAA1介导NOX4/ROS激活p38MAPK/NF-κB通路的分子机制,形成“模型验证→表达调控→功能探究→机制验证”的完整逻辑闭环。
3.1 细胞模型构建与处理条件毒性验证
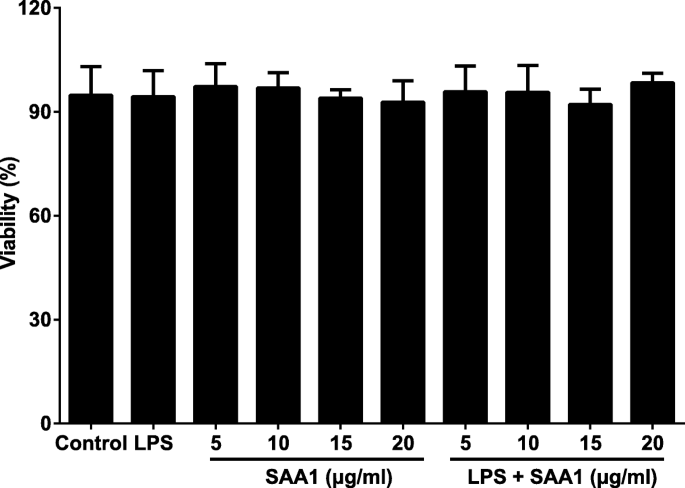
实验目的:确认LPS与重组SAA1蛋白处理对VSMC的细胞毒性,排除细胞死亡对后续实验结果的干扰。方法细节:分离健康雄性SD大鼠胸主动脉VSMC,采用组织块贴壁法培养,传代至5-12代后用于实验;将VSMC分为对照组、不同浓度重组SAA1蛋白处理组(5、10、15、20μg/ml)、重组SAA1蛋白联合1μg/ml LPS处理组,处理24h后采用MTT法检测细胞活力。结果解读:MTT实验结果显示,各处理组的细胞活力与对照组无显著差异(n=3,P>0.05),说明所用浓度的重组SAA1蛋白单独或联合LPS处理均无细胞毒性,可用于后续实验。实验所用关键产品:重组SAA1蛋白(ProSci)、LPS(Sigma);MTT试剂(文献未提及具体品牌,领域常规使用Sigma等品牌的MTT检测试剂盒)。
3.2 LPS对SAA1蛋白表达的浓度与时间依赖性验证
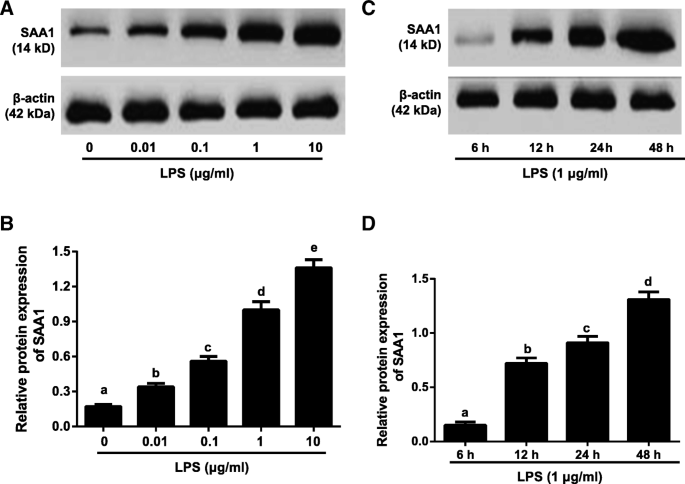
实验目的:明确LPS是否可诱导VSMC中SAA1蛋白的表达,以及表达的浓度与时间调控规律。方法细节:将VSMC分为不同浓度LPS处理组(0、0.01、0.1、1、10μg/ml),处理24h;或1μg/ml LPS处理不同时间组(6、12、24、48h);采用蛋白质免疫印迹(Western blotting)检测SAA1蛋白的表达水平,Image J软件分析条带灰度值。结果解读:蛋白质免疫印迹结果显示,LPS以浓度依赖方式诱导SAA1蛋白表达,1μg/ml LPS处理组的SAA1表达水平显著高于其他浓度组(n=3,P<0.05);同时,1μg/ml LPS处理VSMC后,SAA1蛋白表达随时间延长逐渐升高,24h时达到峰值(n=3,P<0.05),说明LPS可时间和浓度依赖地诱导VSMC中SAA1的表达。实验所用关键产品:蛋白质免疫印迹抗体(Abcam,抗SAA1抗体货号ab171030);凝胶成像系统(Bio-rad Gel Doc EZ Imager)。
3.3 SAA1对LPS诱导VSMC中NOX4/ROS通路的调控作用
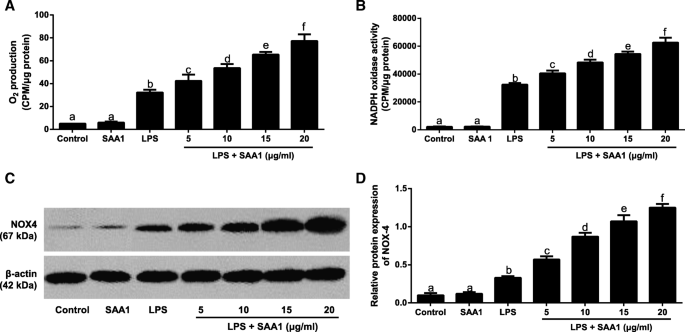
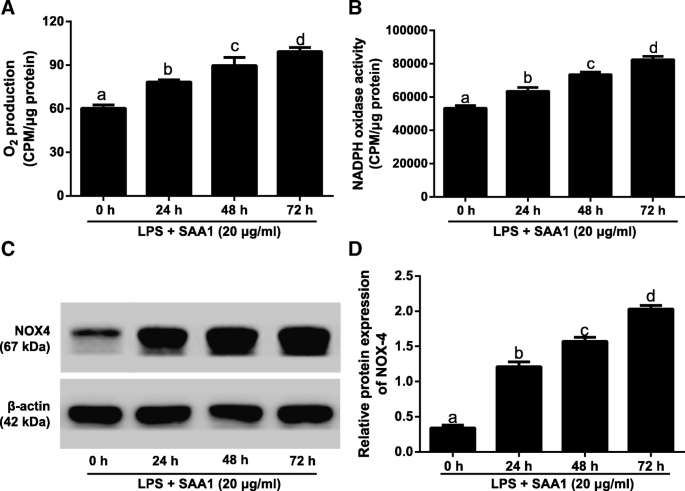
实验目的:探究SAA1对LPS诱导VSMC中NOX4表达及ROS生成的影响。方法细节:将VSMC用不同浓度重组SAA1蛋白(5、10、15、20μg/ml)预孵育24h,再加入1μg/ml LPS处理24h;或用20μg/ml重组SAA1蛋白预孵育不同时间(0、24、48、72h),再加入1μg/ml LPS处理24h;采用光泽精增强化学发光法检测超氧阴离子(O₂⁻)生成与NADPH氧化酶活性,蛋白质免疫印迹检测NOX4蛋白表达。结果解读:实验结果显示,重组SAA1蛋白以浓度依赖方式增加LPS诱导VSMC的O₂⁻生成、NADPH氧化酶活性及NOX4蛋白表达,20μg/ml处理组的上述指标显著高于低浓度组(n=3,P<0.05);同时,20μg/ml SAA1预孵育时间越长,上述指标升高越显著,72h预孵育组达到峰值(n=3,P<0.05);而单独使用20μg/ml SAA1处理的VSMC与对照组相比,上述指标无显著差异(n=3,P>0.05),说明SAA1需在LPS刺激下才能激活NOX4/ROS通路。实验所用关键产品:光泽精(未提及品牌,领域常规使用Sigma);蛋白质免疫印迹抗体(Abcam,抗NOX4抗体货号ab133303)。
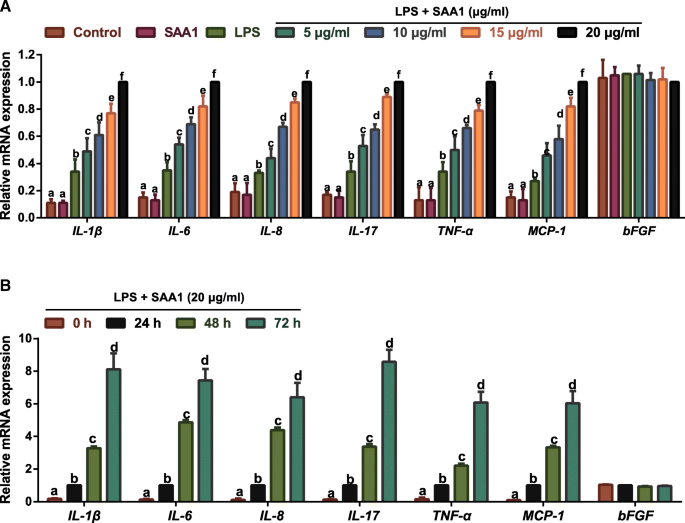
3.4 SAA1对LPS诱导VSMC炎症因子表达的调控作用
实验目的:明确SAA1是否影响LPS诱导VSMC中炎症因子的表达与释放。方法细节:采用上述相同的SAA1预孵育及LPS处理方式,以碱性成纤维细胞生长因子(bFGF)为阴性对照,采用实时荧光定量聚合酶链反应(qRT-PCR)检测IL-1β、IL-6、IL-8、IL-17、TNF-α、单核细胞趋化蛋白-1(MCP-1)的mRNA表达水平,以甘油醛-3-磷酸脱氢酶(GAPDH)为内参,采用2^(-△△Ct)法计算相对表达量。结果解读:实时荧光定量PCR结果显示,重组SAA1蛋白以浓度和时间依赖方式上调LPS诱导VSMC中IL-1β、IL-6、IL-8、IL-17、TNF-α、MCP-1的mRNA表达,20μg/ml处理组及72h预孵育组的上述炎症因子表达显著高于对照组(n=3,P<0.05);而bFGF的mRNA表达在各处理组间无显著差异(n=3,P>0.05),说明SAA1特异性促进LPS诱导的VSMC炎症因子表达。实验所用关键产品:总RNA提取试剂(Takara Trizol);反转录试剂盒(Thermo Fisher);实时荧光定量PCR试剂盒(Takara SYBR Green PCR Master Mix)。
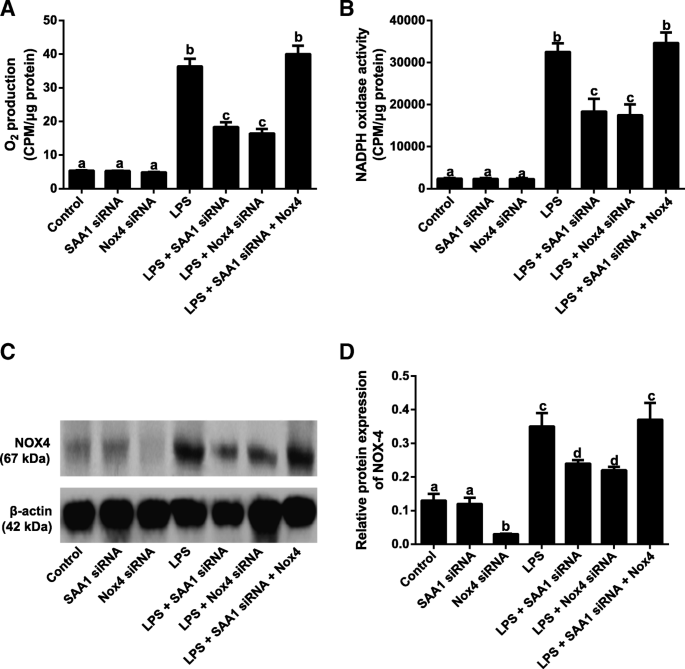
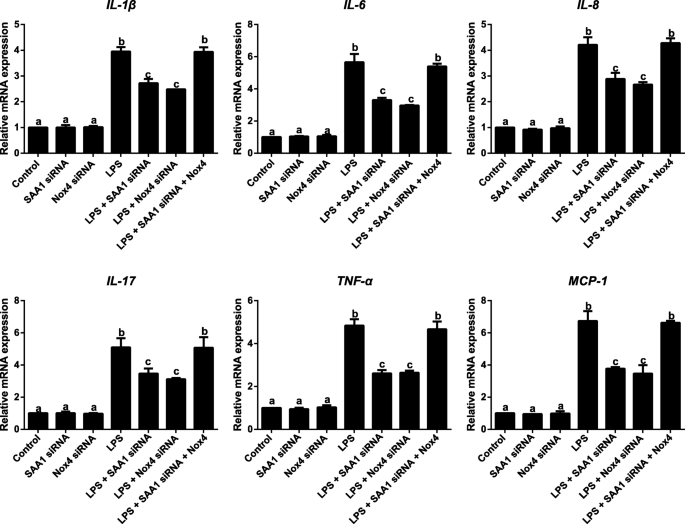
3.5 SAA1介导NOX4/ROS通路调控炎症因子的依赖性验证
实验目的:验证SAA1对LPS诱导VSMC炎症因子的调控是否依赖NOX4/ROS通路。方法细节:将VSMC分为7组:对照组、SAA1 siRNA转染组、NOX4 siRNA转染组、LPS处理组、LPS+SAA1 siRNA组、LPS+NOX4 siRNA组、LPS+SAA1 siRNA+NOX4慢病毒激活组;转染siRNA或慢病毒激活颗粒48h后,用1μg/ml LPS处理24h;检测O₂⁻生成、NADPH氧化酶活性、NOX4蛋白表达及炎症因子mRNA表达。结果解读:与LPS组相比,LPS+SAA1 siRNA组和LPS+NOX4 siRNA组的O₂⁻生成、NADPH氧化酶活性、NOX4蛋白表达及炎症因子mRNA表达均显著降低(n=3,P<0.05);而LPS+SAA1 siRNA+NOX4激活组的上述指标与LPS组无显著差异(n=3,P>0.05),说明SAA1通过NOX4/ROS通路调控LPS诱导的VSMC炎症因子释放,NOX4是SAA1的下游关键靶点。实验所用关键产品:SAA1 siRNA、NOX4 siRNA、NOX4慢病毒激活颗粒(Santa Cruz)。
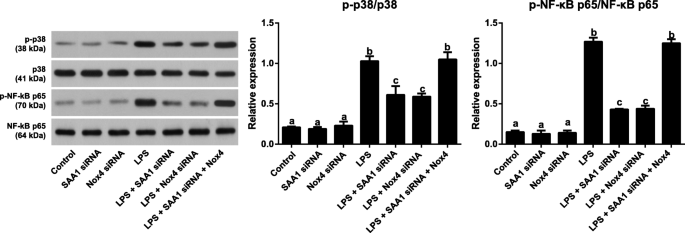
3.6 SAA1通过NOX4/ROS通路激活p38MAPK/NF-κB通路的验证
实验目的:明确SAA1是否通过NOX4/ROS通路激活p38MAPK/NF-κB通路,进而调控炎症因子表达。方法细节:采用上述分组处理方式,蛋白质免疫印迹检测p-p38、总p38、p-NF-κB p65、总NF-κB p65的蛋白表达水平。结果解读:与LPS组相比,LPS+SAA1 siRNA组和LPS+NOX4 siRNA组的p-p38和p-NF-κB p65蛋白表达显著降低(n=3,P<0.05),而总p38和总NF-κB p65的蛋白表达在各组间无显著差异(n=3,P>0.05);LPS+SAA1 siRNA+NOX4激活组的p-p38和p-NF-κB p65表达与LPS组无显著差异(n=3,P>0.05),说明SAA1通过NOX4/ROS通路激活p38MAPK/NF-κB通路的磷酸化,而非调控总蛋白的表达。实验所用关键产品:蛋白质免疫印迹抗体(Abcam,抗p-p38抗体货号ab4822、抗p-NF-κB p65抗体货号ab86299等)。
4. Biomarker研究及发现成果解析
本研究中鉴定的核心Biomarker为血清淀粉样蛋白A1(SAA1),属于细胞内/血清蛋白类功能性Biomarker,其在LPS诱导的VSMC炎症中发挥关键调控作用,为动脉粥样硬化的炎症机制研究与治疗靶点开发提供了新的方向。
Biomarker定位:SAA1作为急性时相蛋白,本研究将其定位为LPS诱导VSMC炎症的调控性Biomarker,其筛选与验证逻辑为:首先在LPS处理的VSMC中验证SAA1的表达呈时间和浓度依赖性上调,随后通过siRNA敲低实验验证SAA1对炎症因子释放的调控作用,再通过NOX4通路激活实验验证其调控的通路依赖性,形成“表达验证-功能验证-机制验证”的完整链条。研究过程详述:SAA1的来源为大鼠VSMC内的内源性蛋白,验证方法包括:采用蛋白质免疫印迹检测LPS诱导下的SAA1蛋白表达水平,明确其表达规律;采用siRNA敲低SAA1表达,观察下游NOX4/ROS通路、炎症因子及p38MAPK/NF-κB通路的变化;采用NOX4慢病毒激活颗粒回补NOX4功能,验证SAA1的调控依赖NOX4通路。特异性与敏感性数据显示,1μg/ml LPS处理VSMC24h后,SAA1蛋白表达水平显著高于对照组(n=3,P<0.05);siRNA敲低SAA1后,LPS诱导的炎症因子mRNA表达水平降低约40%-60%(n=3,P<0.05),p-p38和p-NF-κB p65的蛋白表达水平降低约30%-50%(n=3,P<0.05)。核心成果提炼:本研究首次明确SAA1作为功能性Biomarker,通过NOX4/ROS-p38MAPK/NF-κB通路调控LPS诱导的VSMC炎症因子释放,其功能关联为:SAA1是LPS诱导VSMC炎症的关键调控分子,抑制SAA1表达可显著降低VSMC的炎症反应;创新性在于首次串联了SAA1与NOX4/ROS、p38MAPK/NF-κB通路的调控关系,为动脉粥样硬化的抗炎治疗提供了新的潜在靶点,所有关键实验结果均具有统计学显著性(P<0.05),每组实验样本量为3。
