1. 领域背景与文献引入
文献英文标题:Zyxin is a novel interacting partner for SIRT1;发表期刊:BMC Cell Biology;影响因子:未明确提供;研究领域:细胞生物学(SIRT1介导的蛋白去乙酰化调控与细胞信号转导)
领域共识:SIRT1是酵母沉默信息调节因子2(Sir2)的哺乳动物同源蛋白,属于NAD+依赖的去乙酰化酶家族,2000年左右被发现可调控酵母寿命,后续在秀丽隐杆线虫、黑腹果蝇中证实过表达SIRT1可延长模式生物寿命。在哺乳动物中,SIRT1通过去乙酰化FOXO、p53、NF-κB等关键靶点,参与细胞存活、分化、代谢等多种生理过程,同时在神经保护、发育调控中发挥重要作用,SIRT1敲除小鼠会出现生长迟缓和多组织发育缺陷。当前该领域的研究热点集中在SIRT1在神经退行性疾病、衰老相关疾病中的治疗潜力,但SIRT1在中枢神经系统及发育过程中的具体下游效应分子和调控机制尚未完全阐明,尤其是其与胞质-核穿梭蛋白的相互作用及功能调控仍存在研究空白。
针对SIRT1在中枢神经系统中未知的结合靶点及调控机制问题,本研究通过酵母双杂交技术筛选人类胎脑cDNA文库,旨在鉴定SIRT1的新型互作蛋白,明确两者的相互作用模式及功能调控关系,为解析SIRT1在发育及细胞信号转导中的生物学功能提供新的分子线索。
2. 文献综述解析
作者从SIRT1家族的功能研究和zyxin作为黏着斑蛋白的特性两个维度,系统梳理了领域内现有研究进展,明确了SIRT1下游靶点及zyxin翻译后修饰调控的研究空白,为自身研究的创新性奠定了基础。
关于SIRT1的研究,已证实其作为NAD+依赖的去乙酰化酶,通过修饰多种转录因子和信号分子调控细胞存活、代谢及神经保护,SIRT1敲除小鼠的发育缺陷提示其在胚胎发育中的关键作用,但具体介导这些功能的下游效应分子仍不明确;关于zyxin的研究,已知其作为黏着斑衔接蛋白,参与细胞骨架动态调控和细胞外基质(ECM)到细胞核的信号转导,且能在胞质与细胞核之间穿梭,核内zyxin可与Akt协同发挥抗凋亡功能,但zyxin的翻译后修饰类型及调控机制尚未见报道,现有研究未涉及zyxin与去乙酰化酶的相互作用。
现有研究未揭示SIRT1与zyxin的相互作用,本研究首次发现两者在核内的结合及SIRT1对zyxin的去乙酰化调控,填补了SIRT1下游靶点及zyxin翻译后修饰调控的研究空白,为解析ECM-细胞核信号转导的调控机制提供了新的视角,同时为理解SIRT1在发育过程中的功能提供了新的分子机制。
3. 研究思路总结与详细解析
本研究的整体目标是鉴定SIRT1在中枢神经系统中的新型互作蛋白并明确其功能调控关系,核心科学问题为SIRT1是否与zyxin结合并通过去乙酰化修饰调控其功能,技术路线遵循“筛选验证→定位分析→功能验证”的闭环逻辑,依次通过酵母双杂交筛选、结合区域定位、亚细胞共定位、体内外相互作用验证、表达谱分析及去乙酰化功能验证,逐步阐明两者的相互作用及调控机制。
3.1 酵母双杂交筛选SIRT1互作蛋白
实验目的:从人类胎脑cDNA文库中筛选可与SIRT1相互作用的新型蛋白。
方法细节:构建包含SIRT1去乙酰化酶催化结构域(185-505氨基酸)的诱饵质粒,转化酵母菌株AH109,与含人类胎脑cDNA文库的Y187酵母菌株交配,在缺乏腺嘌呤、组氨酸、亮氨酸、色氨酸的4-DO缺陷培养基上筛选阳性克隆,通过β-半乳糖苷酶实验验证互作活性,并对阳性克隆进行测序鉴定;同时构建不同片段的zyxin缺失突变体质粒,通过酵母双杂交实验定位与SIRT1结合的关键区域。
结果解读:筛选得到5个与zyxin C端片段同源的阳性克隆,结合区域定位实验显示,仅包含zyxin LIM3结构域(501-572氨基酸)的片段可与SIRT1催化结构域结合,而全长zyxin在酵母中未检测到结合信号;推测:全长zyxin的LIM1/2结构域可能处于掩盖状态,需要特定翻译后修饰才能暴露LIM3结构域的结合位点。
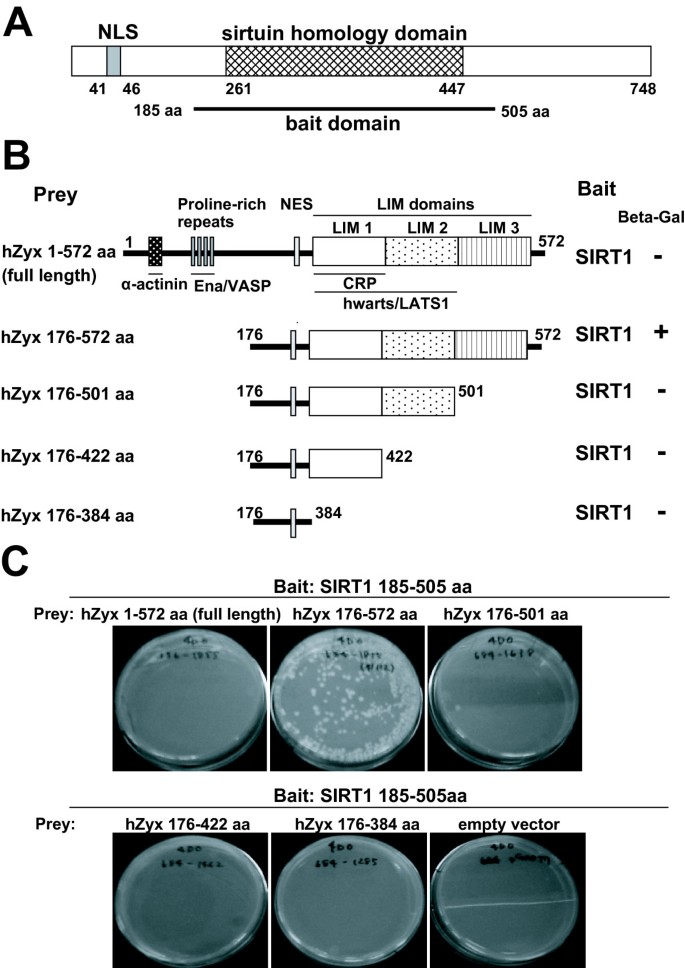
实验所用关键产品:Matchmaker GAL4双杂交系统3(Clontech)、酵母菌株AH109和Y187。
3.2 体外Pull-down实验验证相互作用
实验目的:在体外体系中验证SIRT1与zyxin的相互作用,并进一步确认结合关键区域。
方法细节:原核表达GST-SIRT1融合蛋白并固定于谷胱甘肽琼脂糖珠上,在HEK293T细胞中表达不同片段的HA标签zyxin,将细胞裂解液与GST-SIRT1琼脂糖珠孵育,通过免疫印迹(免疫印迹,WB)检测结合的HA-zyxin片段,同时设置GST蛋白作为阴性对照。
结果解读:免疫印迹结果显示,GST-SIRT1与zyxin的444-572氨基酸片段(包含LIM2-3结构域)结合信号最强,与375-572氨基酸片段结合信号较弱,进一步证实zyxin的C端区域(尤其是LIM3结构域)是与SIRT1结合的关键区域;其中zyxin 375-503氨基酸片段出现非特异性结合,无法评估其与SIRT1的特异性相互作用。
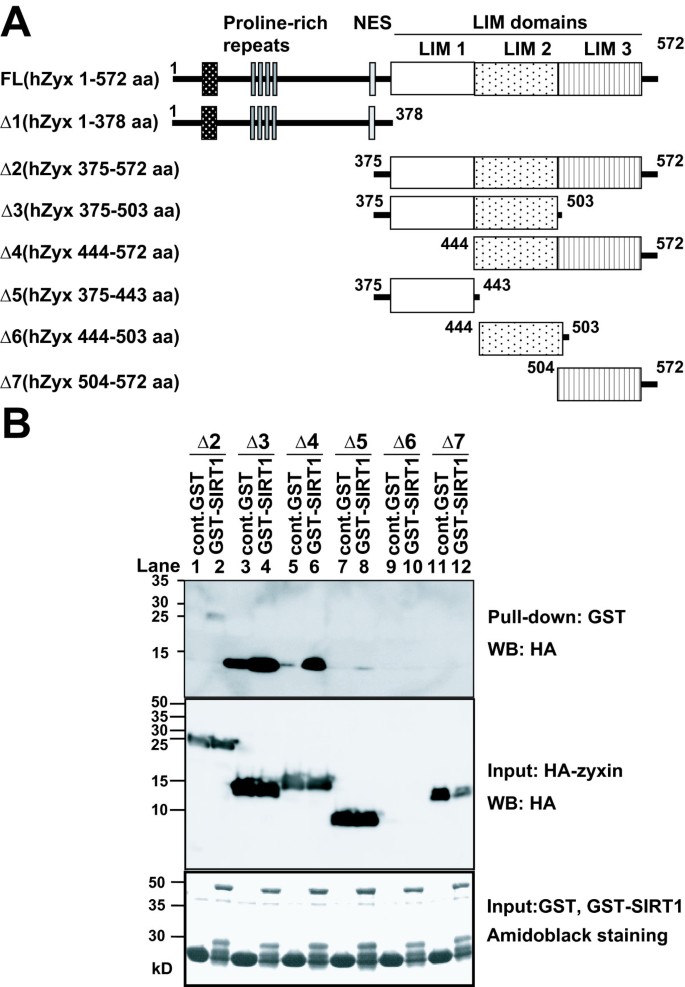
实验所用关键产品:谷胱甘肽琼脂糖珠(GE Healthcare)、HA标签抗体(Sigma-Aldrich)、GST融合蛋白表达载体pGEX-6P-3(GE Healthcare)。
3.3 亚细胞共定位验证
实验目的:观察SIRT1与zyxin在哺乳动物细胞中的亚细胞定位及共定位情况,明确两者的相互作用场所。
方法细节:在COS-7细胞中共转染Myc标签SIRT1和GFP标签zyxin质粒,培养42小时后用核输出抑制剂雷帕霉素B(LMB)处理6小时,通过免疫荧光(免疫荧光,IF)染色标记Myc-SIRT1,利用激光共聚焦显微镜观察蛋白定位,同时统计LMB处理后核内zyxin积累的细胞比例。
结果解读:正常培养条件下,SIRT1主要定位于细胞核,zyxin主要定位于胞质;LMB处理后,zyxin大量积累于细胞核并与SIRT1发生明显共定位,激光共聚焦显微镜的ZX和ZY切面进一步证实两者在核内的共定位;统计显示LMB处理后核内zyxin积累的细胞比例显著升高(文献未明确提供具体数值,基于图表趋势推测)。
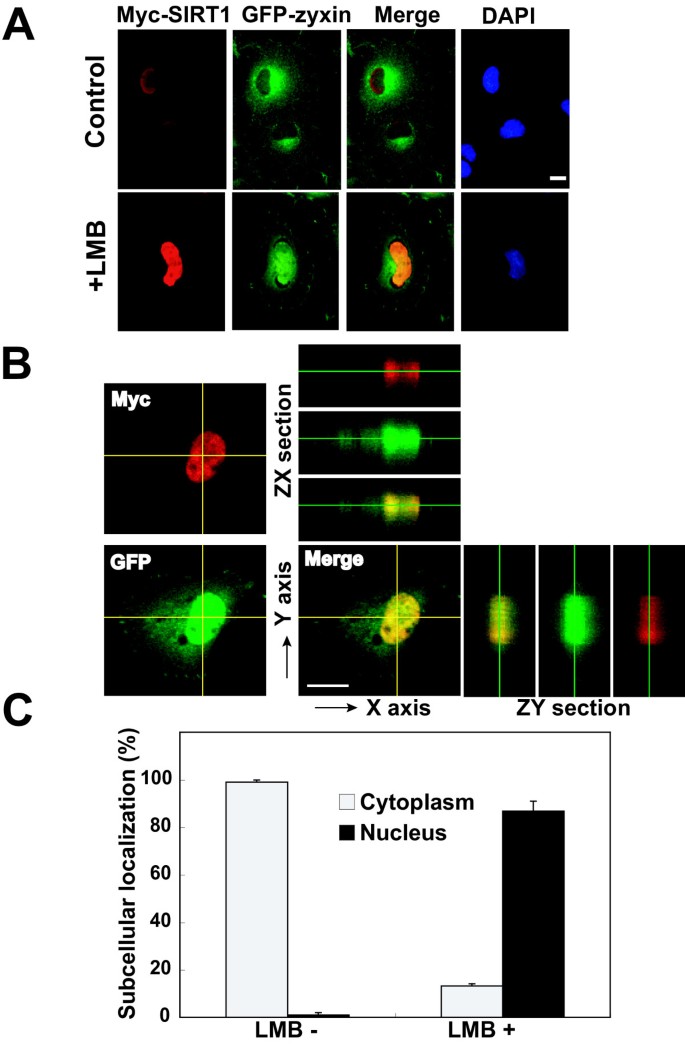
实验所用关键产品:激光共聚焦显微镜Fluoview FV1000(Olympus)、雷帕霉素B(LMB)、Myc标签抗体(Santa Cruz Biotechnology)。
3.4 体内相互作用验证
实验目的:在哺乳动物细胞内验证SIRT1与zyxin的外源性及内源性相互作用。
方法细节:在HEK293T细胞中共转染HA标签SIRT1和GFP标签zyxin质粒,LMB处理6小时后裂解细胞,分别用抗GFP抗体和抗HA抗体进行免疫沉淀,通过免疫印迹检测相互作用的蛋白;同时在HEK293T细胞中单独转染GFP-zyxin质粒,用抗SIRT1抗体免疫沉淀内源性SIRT1,检测其与GFP-zyxin的结合。
结果解读:免疫沉淀实验显示,LMB处理后HA-SIRT1可被抗GFP抗体沉淀,GFP-zyxin也可被抗HA抗体沉淀,说明外源性SIRT1与zyxin在细胞内存在相互作用;内源性免疫沉淀实验显示,抗SIRT1抗体可沉淀内源性SIRT1及结合的GFP-zyxin,证实内源性SIRT1与zyxin也能相互作用,提示两者的相互作用具有生理相关性。
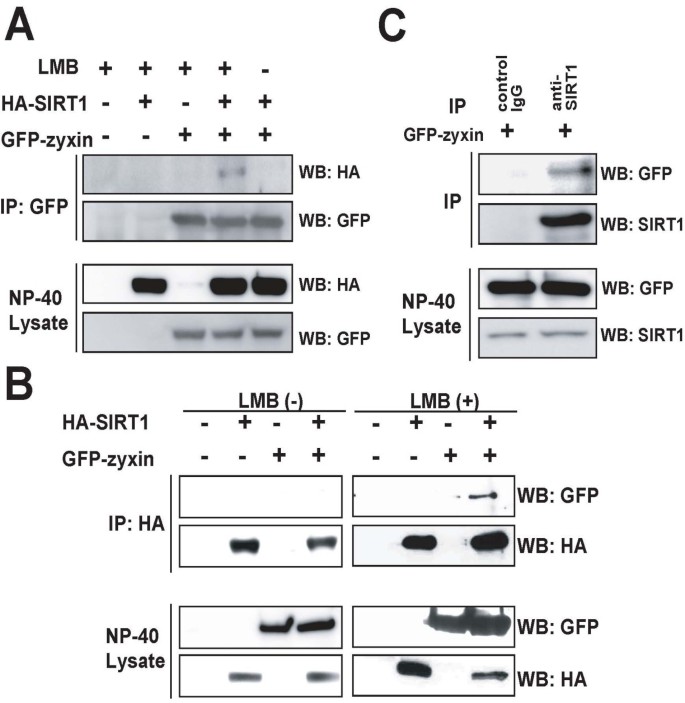
实验所用关键产品:免疫沉淀用rProtein A琼脂糖(GE Healthcare)、SIRT1抗体(Upstate)、GFP标签抗体。
3.5 表达谱分析
实验目的:检测SIRT1与zyxin在小鼠不同组织及发育阶段脑内的表达模式,分析两者表达的相关性。
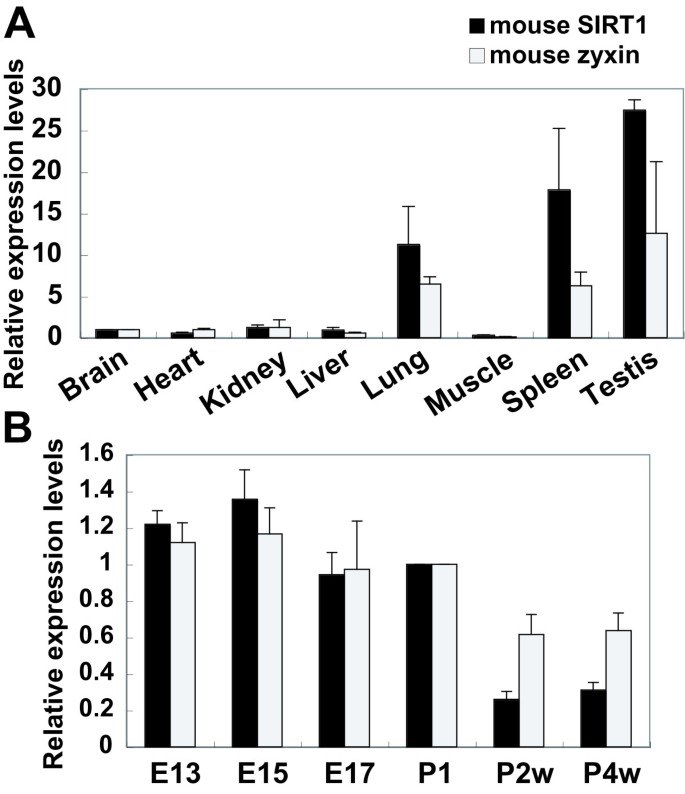
方法细节:提取成年小鼠肺、脾、睾丸等组织及不同发育阶段(胚胎期E13、E15、E17,出生后P1、P2周、P4周)小鼠脑内的总RNA,通过实时荧光定量PCR(实时荧光定量PCR,qRT-PCR)检测SIRT1和zyxin的mRNA表达水平,以GAPDH为内参基因,采用ΔΔCt法计算相对表达量。
结果解读:SIRT1与zyxin在成年小鼠的肺、脾、睾丸组织中表达水平较高,在发育阶段脑内均在E13-P1阶段表达水平最高,两者的表达模式高度一致,提示它们可能在相同的生理过程中发挥协同作用。
实验所用关键产品:Trizol(Invitrogen)、实时荧光定量PCR系统7300(Applied Biosystems)、SYBR GreenER qPCR试剂盒(Invitrogen)。
3.6 SIRT1对zyxin的去乙酰化功能验证
实验目的:验证SIRT1是否能在体内外对zyxin进行去乙酰化修饰。
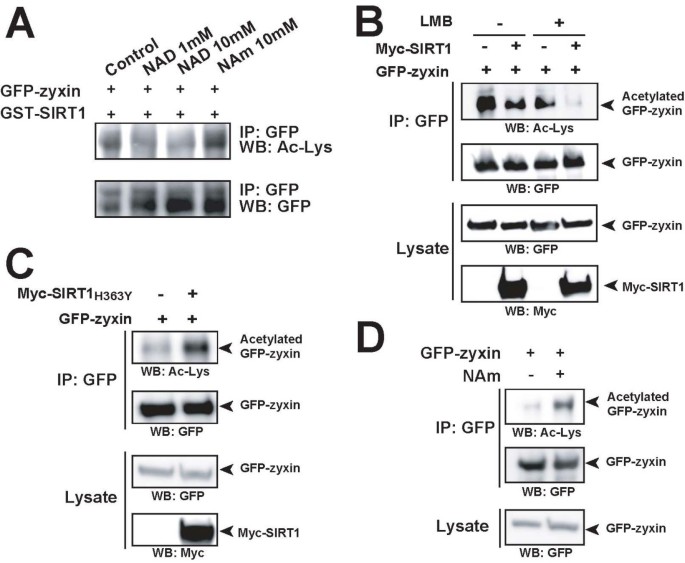
方法细节:体外实验中,免疫沉淀HEK293T细胞中表达的GFP-zyxin,与原核表达的GST-SIRT1在含NAD+或SIRT1抑制剂烟酰胺(NAm)的反应体系中孵育,通过抗乙酰化赖氨酸抗体检测zyxin的乙酰化水平;体内实验中,在COS-7细胞中共转染GFP-zyxin与野生型Myc-SIRT1或功能缺失突变体Myc-SIRT1 H363Y,LMB处理后免疫沉淀GFP-zyxin,检测乙酰化水平;同时用NAm处理表达GFP-zyxin的HEK293T细胞,检测乙酰化水平变化。
结果解读:体外实验显示,NAD+存在时GST-SIRT1可显著降低zyxin的乙酰化水平,NAm处理可完全抑制该效应;体内实验显示,野生型SIRT1可显著降低zyxin的乙酰化水平,而功能缺失突变体SIRT1 H363Y无此作用,NAm处理则显著升高zyxin的乙酰化水平,证实SIRT1可NAD+依赖地特异性去乙酰化zyxin。
实验所用关键产品:抗乙酰化赖氨酸抗体(Cell Signaling Technology)、烟酰胺(NAm)、SIRT1功能缺失突变体质粒(Addgene)。
4. Biomarker研究及发现成果解析
本研究未涉及传统临床诊断或预后生物标志物(Biomarker)的筛选与验证,而是聚焦于分子调控层面的功能Biomarker,即SIRT1的新型下游靶点zyxin,通过系统的筛选与验证流程明确了两者的相互作用及调控关系。
本研究中鉴定的zyxin属于功能型Biomarker,作为SIRT1的新型互作蛋白和去乙酰化底物,其筛选与验证逻辑为:酵母双杂交筛选人类胎脑cDNA文库→体外Pull-down实验验证结合→哺乳动物细胞内免疫共沉淀验证→亚细胞共定位确认相互作用场所→体内外去乙酰化实验验证功能调控,完整的逻辑链条证实了zyxin与SIRT1的功能关联。
zyxin的来源为人类胎脑cDNA文库,通过酵母双杂交筛选获得,后续通过免疫共沉淀、免疫荧光等实验验证了与SIRT1的相互作用,通过去乙酰化实验证实SIRT1可对其进行去乙酰化修饰;本研究未开展zyxin作为疾病Biomarker的相关实验,因此无特异性、敏感性、ROC曲线等临床相关数据。
本研究的核心成果为首次发现zyxin是SIRT1的新型互作蛋白,SIRT1可通过NAD+依赖的去乙酰化修饰调控核内zyxin的功能,两者在小鼠组织及发育脑内的表达模式高度一致,提示它们可能共同参与发育过程中的细胞存活及ECM到细胞核的信号转导调控;该发现的创新性在于首次揭示了SIRT1与黏着斑蛋白zyxin的相互作用及翻译后修饰调控,为解析SIRT1在发育及细胞信号转导中的功能提供了新的分子机制;文献未明确提供相关统计学结果(如P值、样本量、置信区间)。
