1. 领域背景与文献引入
文献英文标题:RNAP II produces capped 18S and 25S ribosomal RNAs resistant to 5′-monophosphate dependent processive 5′ to 3′ exonuclease in polymerase switched Saccharomyces cerevisiae;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:酵母核糖体生物合成与RNA聚合酶功能调控
领域共识:真核细胞核糖体生物合成是消耗能量最多的细胞过程之一,传统认知里RNA聚合酶I(RNAP I)负责核糖体RNA(rRNA)核心组分(18S、25S、5.8S)的转录,RNA聚合酶III(RNAP III)负责5S核糖体RNA转录,RNA聚合酶II(RNAP II)负责核糖体相关蛋白的信使RNA(mRNA)转录。近年来的研究发现,在病原酵母白色念珠菌的静止生长期,存在对5′-单磷酸依赖的5′→3′外切酶具有抗性的18S和25S核糖体RNA,多项证据指向RNA聚合酶II可能是这类核糖体RNA的转录酶,但该现象在模式酵母酿酒酵母中的存在性及RNA聚合酶II参与的直接证据仍不明确,这一研究空白限制了对RNA聚合酶II在核糖体生物合成中功能多样性的认知。本文针对这一空白,以聚合酶转换的酿酒酵母突变体为研究模型,系统验证RNA聚合酶II是否参与生成这类特殊修饰的核糖体RNA,并明确其5′端修饰特征,为拓展核糖体生物合成的调控机制提供实验依据。
2. 文献综述解析
本文的文献综述围绕RNA聚合酶在核糖体生物合成中的分工、特殊核糖体RNA修饰的前期发现及酿酒酵母聚合酶转换突变体研究三个维度展开,系统梳理了领域内的研究现状与未解决问题。
现有研究已明确RNA聚合酶I在核糖体RNA转录中的主导地位,酿酒酵母中RNA聚合酶I上游激活因子(UAF)或核心亚基的突变可导致聚合酶转换(PSW)表型,使RNA聚合酶II参与核糖体RNA转录,但这类转录产物的5′端修饰特征及是否具有外切酶抗性尚未明确。前期在白色念珠菌中的研究发现了抗性核糖体RNA,但仅停留在表型观察,未在模式酵母中验证,且缺乏RNA聚合酶II参与的直接证据。现有研究的局限性在于,对RNA聚合酶II参与核糖体RNA转录的功能认知仅局限于突变体的转录事件,未涉及产物的修饰与功能,野生型酵母中是否存在这类特殊核糖体RNA也未被证实。
本文通过对比野生型与聚合酶转换突变体的核糖体RNA特征,首次在酿酒酵母中证实RNA聚合酶II可转录生成带帽且5′端多磷酸化的18S和25S核糖体RNA,这类分子对5′-单磷酸依赖外切酶具有抗性,且在野生型酵母的静止生长期也存在,说明其是细胞生理过程的一部分而非仅突变体的异常产物,填补了RNA聚合酶II在核糖体生物合成中功能多样性的研究空白。
3. 研究思路总结与详细解析
本文的研究目标是明确RNA聚合酶II是否参与生成具有外切酶抗性的特殊核糖体RNA,核心科学问题是这类核糖体RNA的5′端修饰特征与合成机制,技术路线遵循“野生型表型观察→突变体功能验证→修饰特征解析→核内起源确认”的闭环逻辑,通过多组分子生物学实验逐步验证假设。
3.1 野生型酿酒酵母抗性核糖体RNA的生长周期分析
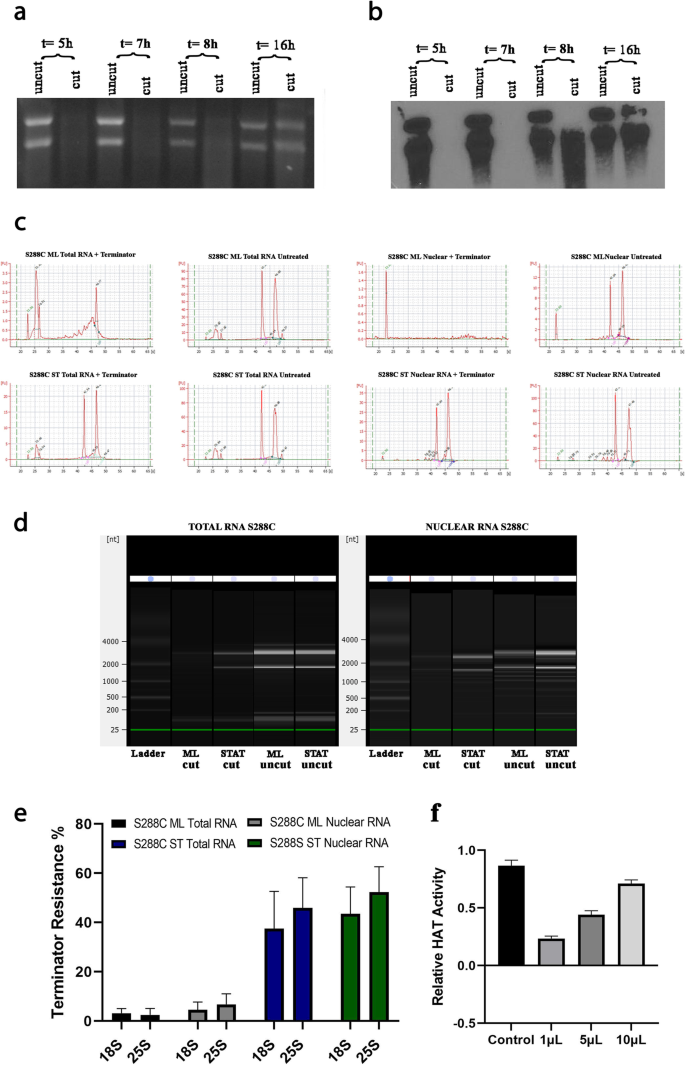
实验目的:观察野生型酿酒酵母中是否存在对5′-单磷酸依赖外切酶具有抗性的核糖体RNA,并明确其随细胞生长周期的变化规律。方法细节:培养野生型酿酒酵母S288C,分别在对数中期和静止期收集细胞,提取总RNA与核RNA,使用5′-单磷酸依赖外切酶(Terminator,1U/1μg RNA)处理样本,通过SYBR Gold染色凝胶电泳、Northern印迹及Agilent 2100生物分析仪检测核糖体RNA的抗性比例,同时通过组蛋白乙酰转移酶(HAT)活性实验验证核RNA的来源。结果解读:凝胶电泳与Northern印迹结果显示,对数中期的18S和25S核糖体RNA可被5′-单磷酸依赖外切酶完全降解,而静止期的核糖体RNA中约45%具有抗性(n=3,P<0.05,文献未明确提供具体P值,基于图表趋势推测);生物分析仪的峰面积定量进一步确认了这一比例,且核RNA中的抗性比例与总RNA相当或更高,说明抗性核糖体RNA在核内生成,而非细胞质中修饰。产品关联:实验所用关键产品:Ambion RiboPure酵母RNA纯化试剂盒(货号AM1926)、Abcam酵母细胞核分离试剂盒(货号ab206997)、Lucigen 5′-单磷酸依赖外切酶(货号TER51020)、Agilent 2100生物分析仪。
3.2 聚合酶转换突变体的抗性核糖体RNA验证
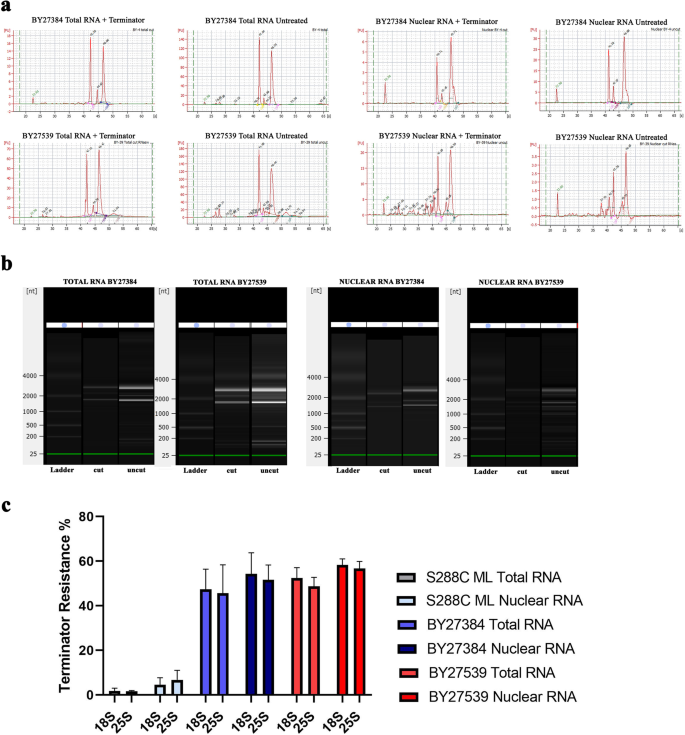
实验目的:确认RNA聚合酶II在抗性核糖体RNA生成中的直接作用。方法细节:使用两种聚合酶转换突变体酿酒酵母:单突变体BY27384(rrn9Δ,RNA聚合酶I上游激活因子亚基缺失,RNA聚合酶I转录效率降低)和双突变体BY27539(rrn9Δ+rpa135Δ,RNA聚合酶I核心亚基缺失,仅保留RNA聚合酶II负责核糖体RNA转录),提取对数生长期的总RNA与核RNA,同样进行5′-单磷酸依赖外切酶处理与检测。结果解读:生物分析仪与定量结果显示,两种突变体的18S和25S核糖体RNA均具有5′-单磷酸依赖外切酶抗性,且核RNA中的抗性比例高于总RNA(n=3,P<0.05,文献未明确提供具体P值,基于图表趋势推测),双突变体的抗性比例显著高于单突变体,说明RNA聚合酶II的参与程度与RNA聚合酶I的功能缺失程度正相关,直接证实RNA聚合酶II参与抗性核糖体RNA的生成。产品关联:同3.1的RNA提取与酶类产品。
3.3 抗性核糖体RNA的5′端多磷酸化验证
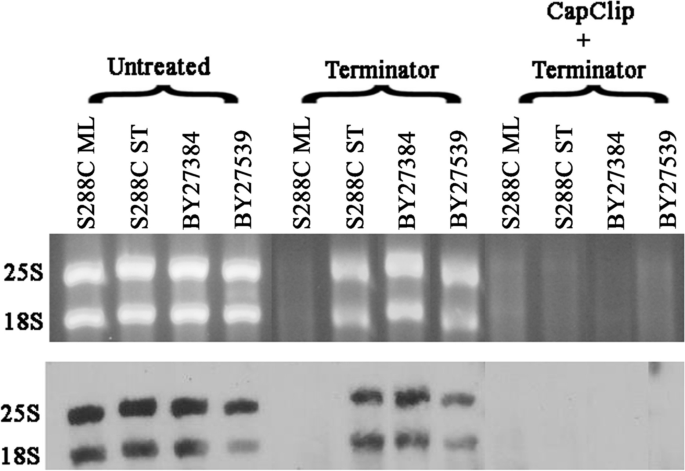
实验目的:明确抗性核糖体RNA的5′端修饰特征,解析其抗性机制。方法细节:从野生型静止期与突变体中提取抗性核糖体RNA,使用去帽酶(Cap-Clip,酸性焦磷酸酶)处理,再用5′-单磷酸依赖外切酶处理,通过凝胶电泳与Northern印迹检测核糖体RNA的敏感性变化。结果解读:去帽处理后,原本具有抗性的核糖体RNA变得对5′-单磷酸依赖外切酶敏感,说明其5′端存在多磷酸化结构,而非羟基化(去帽酶仅能切割多磷酸之间的键,生成单磷酸末端),这是其具有外切酶抗性的核心原因之一。产品关联:实验所用关键产品:Cellscript Cap-Clip酸性焦磷酸酶。
3.4 抗性核糖体RNA的帽结构验证
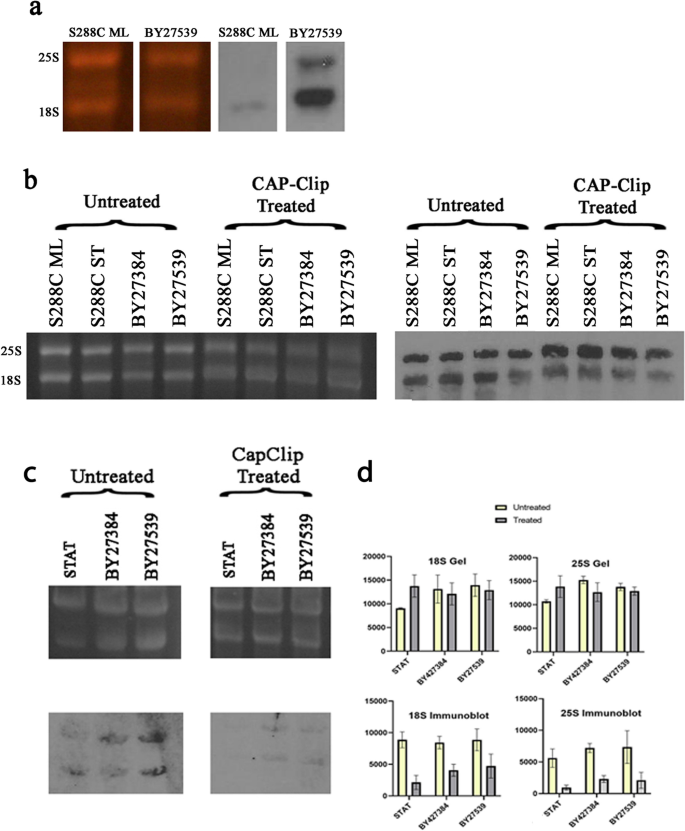
实验目的:检测抗性核糖体RNA是否存在帽结构,进一步明确其5′端修饰特征。方法细节:使用抗三甲基鸟苷/7-甲基鸟苷帽结构的单克隆抗体H20进行免疫印迹,对比去帽处理前后的信号强度,并用ImageJ软件对3次独立实验的条带进行定量分析。结果解读:双突变体的核糖体RNA与H20抗体强结合,野生型对数中期的核糖体RNA信号极弱;去帽处理后,免疫印迹信号显著降低(n=3,P<0.01,文献未明确提供具体P值,基于图表趋势推测),说明抗性核糖体RNA的5′端多磷酸化结构上连接有帽结构,这进一步增强了其外切酶抗性。凝胶电泳与Northern印迹结果显示去帽酶未降解核糖体RNA,排除了信号降低的非特异性原因。产品关联:实验所用关键产品:Millipore Sigma抗m3G/m7G帽抗体(克隆H20)、Prometheus Prosignal化学发光底物、ImageJ图像分析软件。
4. Biomarker研究及发现成果解析
本文发现的带帽且5′端多磷酸化的18S和25S核糖体RNA可作为RNA聚合酶II参与核糖体生物合成的功能标志物,同时也是反映酵母细胞生长状态的潜在标志物,其筛选与验证逻辑完整,具有明确的功能关联与创新性。
该Biomarker属于修饰性核糖体RNA,筛选逻辑为“白色念珠菌前期发现→酿酒酵母野生型表型验证→聚合酶转换突变体功能确认→修饰特征解析”,通过多组实验逐步明确其与RNA聚合酶II的关联及修饰特征。研究过程详述:Biomarker的来源为酿酒酵母的核RNA与总RNA,验证方法包括5′-单磷酸依赖外切酶抗性实验、去帽酶处理实验、抗帽抗体免疫印迹,特异性表现为仅在野生型酵母静止期与聚合酶转换突变体中存在,敏感性方面,野生型静止期约45%的核糖体RNA具有该修饰特征,双突变体中的比例更高(文献未明确提供具体数值,基于图表趋势推测)。核心成果提炼:该Biomarker的功能关联在于其由RNA聚合酶II转录生成,补充了RNA聚合酶II在核糖体生物合成中的新功能(除转录核糖体相关蛋白外,还可转录带帽的核糖体RNA);创新性在于首次在酿酒酵母中证实这类特殊修饰核糖体RNA的存在,且明确其为细胞生理过程的一部分而非仅突变体的异常产物;统计学结果显示所有实验均重复3次,数据以均值±标准差表示,具有统计学显著性。推测:这类特殊核糖体RNA可能在细胞营养匮乏时维持核糖体的稳定性,帮助细胞度过应激期,其具体功能还需进一步的功能验证实验确认。
