1. 领域背景与文献引入
文献英文标题:Skin-permeable gold nanoparticles with modifications azelamide monoethanolamine ameliorate inflammatory skin diseases;发表期刊:Biomarker Research;影响因子:未公开;研究领域:炎症性皮肤病纳米药物递送
银屑病、玫瑰痤疮是全球高发的慢性炎症性皮肤病,患病率高且严重影响患者生活质量。传统局部给药作为无创的自我治疗方式,可避免全身给药的系统副作用,但皮肤角质层的天然屏障导致药物透皮效率极低,长期使用还易引发皮肤萎缩、毛细血管扩张等不良反应,临床治疗需求尚未得到充分满足。氧化应激在炎症性皮肤病的发病机制中起核心作用,过量活性氧(ROS)会激活核因子κB(NF-κB)通路,促进炎症细胞因子分泌;基质金属蛋白酶9(MMP9)在皮损组织中高表达,推动表皮增生与炎症进展。超氧化物歧化酶(SOD)作为关键抗氧化酶,可清除ROS以减轻氧化损伤,但其体内应用稳定性差、递送效率低。纳米颗粒因可控的尺寸、形貌等理化性质,在炎症性疾病治疗中展现出独特优势,其中金纳米颗粒具有天然的类SOD活性,可清除过量ROS,但未修饰的金纳米颗粒易聚集,透皮性与水溶液稳定性差,限制了其局部治疗的应用。因此,开发兼具高透皮性、稳定性与精准抗炎活性的纳米药物成为领域核心需求,本研究通过壬二酸单乙醇胺(MEA)修饰金纳米颗粒,旨在解决上述瓶颈问题,为炎症性皮肤病提供安全有效的局部治疗方案。
2. 文献综述解析
作者按治疗策略将现有研究分为传统局部给药、未修饰纳米药物两类,系统评述了不同方案的临床价值与技术局限,明确了金纳米颗粒在炎症性皮肤病治疗中的潜力与优化方向。传统局部给药如糖皮质激素、钙调磷酸酶抑制剂,优势在于无创、可直接作用于皮损部位,但核心局限是透皮效率低,药物难以到达真皮层发挥作用,且长期使用会破坏皮肤屏障功能,引发多种副作用。纳米药物凭借小尺寸效应与可控表面性质,可提升药物透皮能力,同时通过清除ROS、调控免疫细胞浸润发挥抗炎作用;其中金纳米颗粒因天然的类SOD活性,可有效减轻氧化应激损伤,但其未修饰状态下易聚集沉淀,透皮性差,无法在局部治疗中稳定发挥作用。现有研究虽尝试通过表面修饰提升纳米颗粒的透皮性,但多聚焦于递送效率优化,缺乏针对炎症性皮肤病核心发病机制(氧化应激与MMP9激活)的双重调控策略。本研究首次将MEA修饰金纳米颗粒,既通过表面改性提升了金纳米颗粒的透皮性与水溶液稳定性,又通过调控SOD活性与MMP9活性,实现对氧化应激与炎症反应的双重抑制,填补了领域内兼具透皮递送与精准抗炎的纳米药物研究空白。
3. 研究思路总结与详细解析
本研究以“开发安全有效的炎症性皮肤病局部纳米药物”为核心目标,围绕“MEA修饰如何提升金纳米颗粒的透皮性与稳定性,以及其抗炎的分子机制”这一科学问题,遵循“纳米颗粒合成表征→透皮性验证→体内治疗效果评估→组学与体外实验机制解析→安全性验证”的闭环技术路线,系统验证了Au-MEA NPs的治疗价值与作用机制。
3.1 金纳米颗粒的合成与表征
实验目的:合成柠檬酸盐包被的金纳米颗粒(Au-CA NPs)及MEA修饰的金纳米颗粒(Au-MEA NPs),系统表征其理化性质,验证修饰的成功性及稳定性优势。
方法细节:采用柠檬酸盐还原法合成Au-CA NPs,通过浓度梯度驱动的配体交换法,将MEA替换Au-CA NPs表面的柠檬酸盐配体得到Au-MEA NPs;使用透射电子显微镜(TEM)、X射线衍射仪(XRD)、紫外-可见分光光度计(UV-Vis)、傅里叶变换红外光谱(FTIR)、X射线光电子能谱(XPS)表征颗粒的形貌、晶体结构、表面化学组成;通过静置实验、电感耦合等离子体质谱(ICP-MS)、动态光散射(DLS)评估颗粒的水溶液稳定性。
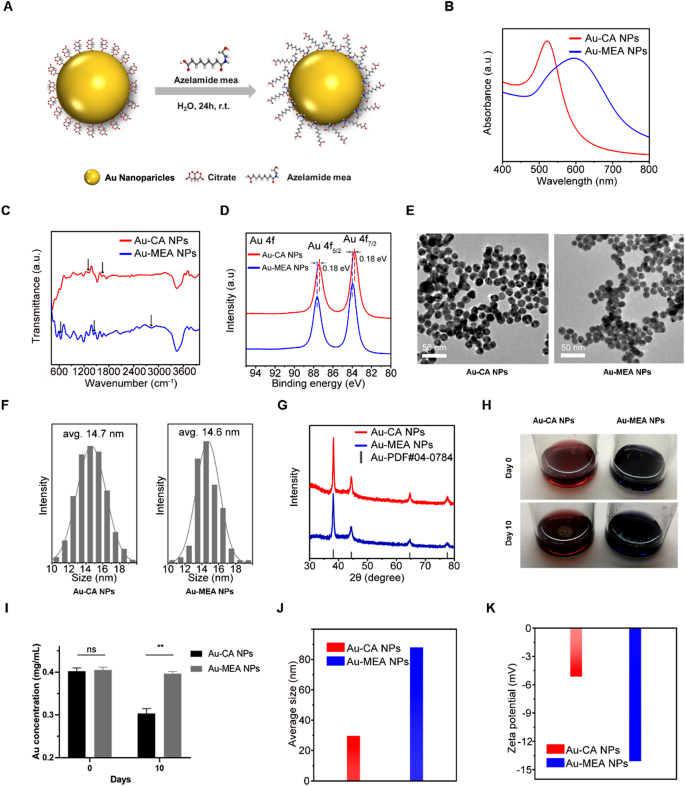
结果解读:UV-Vis光谱显示Au-MEA NPs的特征吸收峰从Au-CA NPs的521nm红移至594nm,FTIR和XPS结果证实MEA成功结合到金纳米颗粒表面;TEM和XRD结果显示两种颗粒均为约15nm的球形高结晶颗粒,修饰后形貌无显著变化;静置10天后,Au-CA NPs出现明显聚集沉淀,而Au-MEA NPs仍保持分散,ICP-MS显示Au-MEA NPs上清液中金含量无显著下降(n=3,P>0.05),DLS显示Au-MEA NPs的水合粒径更大,zeta电位更负(-14.1mV vs Au-CA NPs的-5.15mV),表明其稳定性更强。
产品关联:实验所用关键仪器:JEOL JEM 2100Plus透射电镜、Rigaku Miniflex-600 X射线衍射仪、Thermo Fisher Scientific Nicolet iS20傅里叶变换红外光谱仪、Thermo Fisher Scientific K-Alpha X射线光电子能谱仪、Malvern Zetasizer Nano系列动态光散射仪;文献未提及具体实验试剂品牌,领域常规使用氯金酸、柠檬酸钠等试剂合成金纳米颗粒。
3.2 透皮能力验证
实验目的:验证Au-MEA NPs凝胶的皮肤穿透能力,明确其在皮肤组织中的分布特征。
方法细节:将Au-CA NPs、Au-MEA NPs分别与SEPIMAX ZEN凝胶混合制备纳米颗粒凝胶,通过扫描电子显微镜(SEM)和能量色散X射线光谱(EDS)表征凝胶的形貌与元素组成;将凝胶局部涂抹于小鼠背部皮肤5天后,通过TEM观察皮肤组织中纳米颗粒的分布,ICP-MS检测皮肤组织中的金含量。
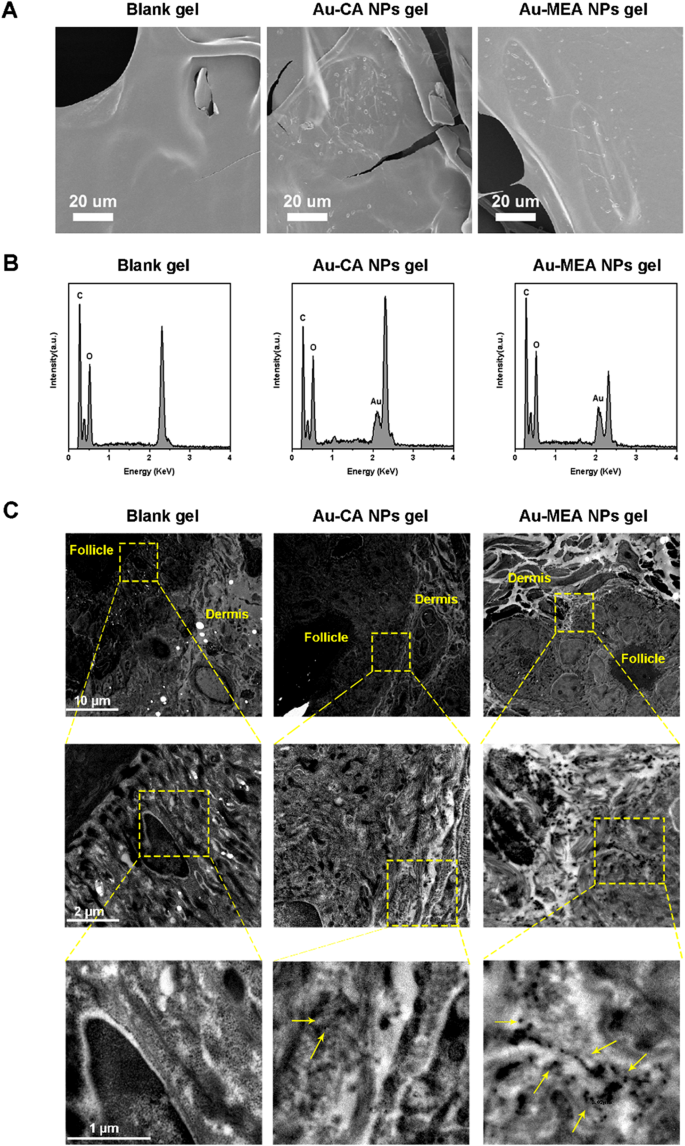
结果解读:SEM显示纳米颗粒凝胶表面呈粗糙颗粒状,EDS检测到金元素,证实纳米颗粒成功嵌入凝胶;TEM结果显示,Au-CA NPs组皮肤中仅少量颗粒分布,而Au-MEA NPs组颗粒在真皮层有明显聚集;ICP-MS显示Au-MEA NPs组皮肤组织中金含量显著高于Au-CA NPs组(n=5,P<0.01),表明Au-MEA NPs具有更强的透皮能力。
产品关联:实验所用关键仪器:Carl Zeiss Sigma HD场发射扫描电镜、Agilent ICP-MS7900电感耦合等离子体质谱仪;文献未提及具体凝胶基质品牌,领域常规使用卡波姆、SEPIMAX ZEN等制备局部给药凝胶。
3.3 动物模型治疗效果评估
实验目的:在咪喹莫特(IMQ)诱导的银屑病模型和LL37诱导的玫瑰痤疮模型中,验证Au-MEA NPs凝胶的治疗效果。
方法细节:构建IMQ诱导的小鼠银屑病模型,每日耳部涂抹5% IMQ乳膏,同时局部涂抹空白凝胶、MEA凝胶、Au-CA NPs凝胶或Au-MEA NPs凝胶,连续给药9天;构建LL37诱导的小鼠玫瑰痤疮模型,背部皮肤连续5天涂抹凝胶,最后2天皮内注射LL37诱导皮损;通过临床评分(耳厚、红斑、鳞屑)、苏木精-伊红(H&E)染色、免疫荧光、实时定量聚合酶链反应(qRT-PCR)评估治疗效果。
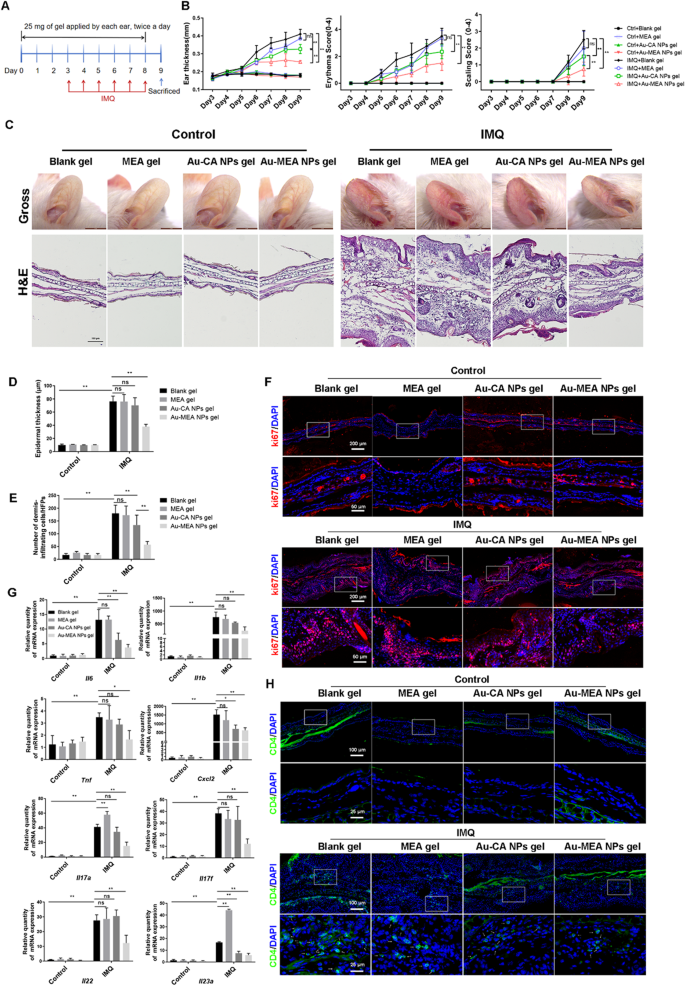
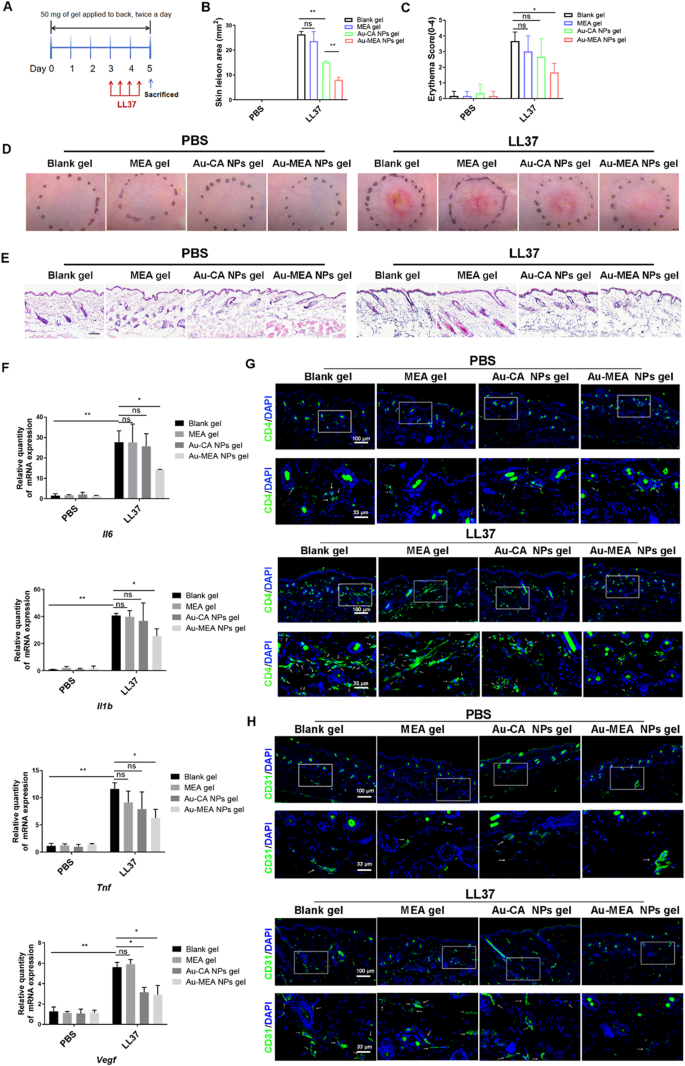
结果解读:在银屑病模型中,Au-MEA NPs凝胶显著降低小鼠耳厚、红斑及鳞屑评分(n=6,P<0.01),H&E染色显示表皮增生减轻、真皮浸润细胞减少(n=6,P<0.01),免疫荧光显示Ki67阳性增殖细胞减少,CD4阳性T细胞浸润减少,qRT-PCR显示IL-6、TNF-α等炎症因子mRNA水平显著下调(n=6,P<0.05);在玫瑰痤疮模型中,Au-MEA NPs凝胶显著降低红斑面积与评分(n=6,P<0.01),H&E染色显示炎症细胞浸润减少,qRT-PCR显示TNF-α、VEGF等因子mRNA水平下调(n=6,P<0.05),免疫荧光显示CD31阳性微血管及CD4阳性T细胞浸润减少。Au-MEA NPs凝胶的治疗效果显著优于Au-CA NPs凝胶,且MEA凝胶与空白凝胶效果无显著差异,证实治疗效果源于修饰后的金纳米颗粒。
产品关联:实验所用关键试剂:5% IMQ乳膏、LL37肽、抗CD4抗体(Thermo Fisher Scientific Cat# 14-0042-85)、抗CD31抗体(BD Biosciences Cat# 558736)、抗Ki67抗体(Thermo Fisher Scientific Cat# 14-5698-80);文献未提及具体qRT-PCR试剂盒品牌,领域常规使用SYBR Green法进行实时定量检测。
3.4 蛋白质组学机制分析
实验目的:通过蛋白质组学分析,揭示Au-MEA NPs治疗炎症性皮肤病的潜在分子通路。
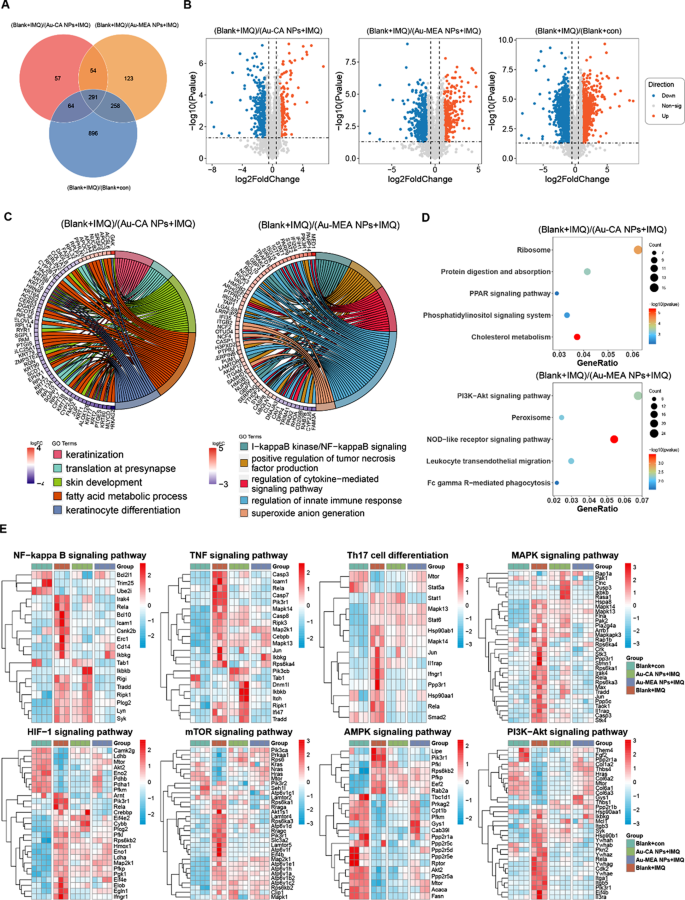
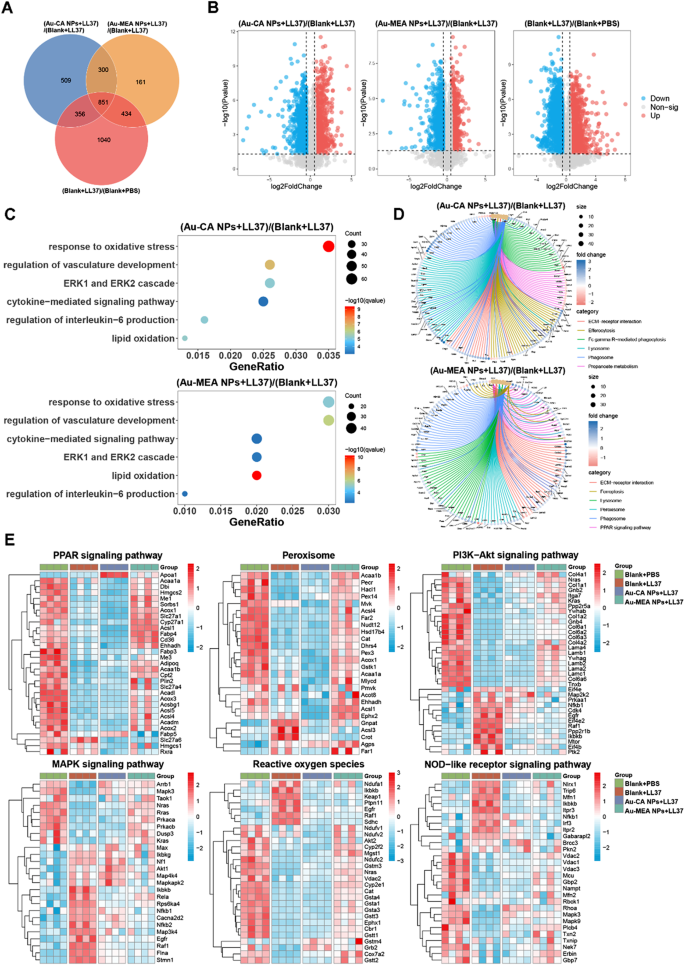
方法细节:收集银屑病和玫瑰痤疮模型中不同处理组的皮肤组织样本,提取蛋白质后进行液相色谱-串联质谱(LC-MS/MS)分析,采用DIA模式采集数据,通过Spectronaut软件分析差异表达蛋白(DEPs),并进行基因本体(GO)和京都基因与基因组百科全书(KEGG)富集分析。
结果解读:在银屑病模型中,与空白凝胶组相比,Au-MEA NPs组有726个DEPs,富集于NF-κB信号通路、TNF信号通路等炎症相关通路;在玫瑰痤疮模型中,Au-MEA NPs组有1746个DEPs,富集于PI3K-Akt信号通路、MAPK信号通路、氧化应激相关通路。聚类分析显示,Au-MEA NPs可逆转炎症和氧化应激相关通路的异常激活,使其接近正常水平,提示其通过调控炎症与氧化应激通路发挥治疗作用。
产品关联:实验所用关键仪器:Thermo Vanquish Neo HPLC系统、Orbitrap Exploris 480质谱仪;文献未提及具体蛋白质组学分析软件的授权信息,领域常规使用Spectronaut、clusterProfiler等工具进行差异蛋白分析与富集。
3.5 体外细胞实验验证抗炎机制
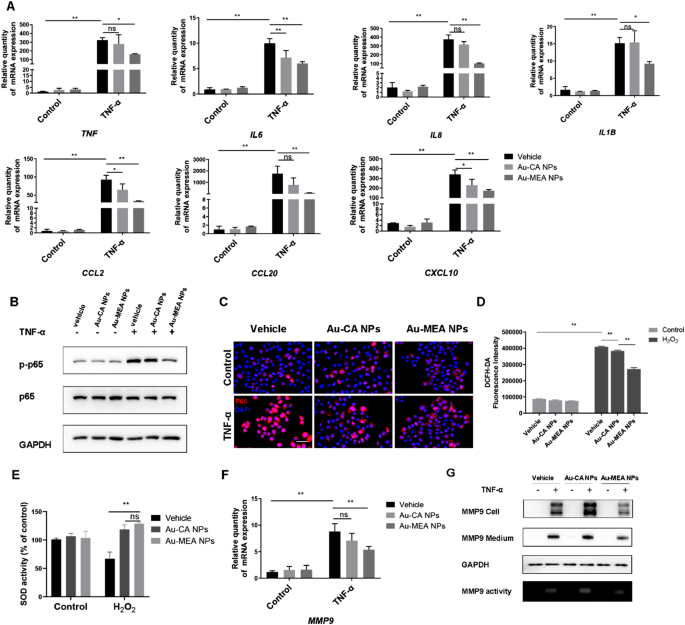
实验目的:在TNF-α诱导的HaCaT角质形成细胞模型中,验证Au-MEA NPs的抗炎机制,明确其对SOD、MMP9及NF-κB通路的调控作用。
方法细节:采用CCK-8实验确定Au-MEA NPs的安全浓度(25μg/mL),将HaCaT细胞预孵育Au-CA NPs或Au-MEA NPs后,用TNF-α或H₂O₂处理;通过qRT-PCR检测炎症因子及MMP9的mRNA水平,蛋白质免疫印迹(Western blot)检测NF-κB p65磷酸化及MMP9蛋白水平,免疫荧光检测p65核移位,DCFH-DA检测ROS水平,凝胶酶谱法检测MMP9活性,SOD活性试剂盒检测SOD活性。
结果解读:Au-MEA NPs显著抑制TNF-α诱导的IL-6、TNF-α等炎症因子mRNA表达(n=3,P<0.05),减少p65磷酸化及核移位(n=3,P<0.01);H₂O₂处理后,Au-MEA NPs显著降低细胞ROS水平(n=3,P<0.01),提升SOD活性(n=3,P<0.05);同时,Au-MEA NPs抑制MMP9的mRNA表达、蛋白水平及活性(n=3,P<0.01),而Au-CA NPs对MMP9活性无显著抑制作用。结果表明Au-MEA NPs通过提升SOD活性清除ROS,抑制MMP9活性,进而阻断NF-κB通路,减少炎症因子分泌。
产品关联:实验所用关键试剂:TNF-α(Thermo Fisher Scientific, 300–01 A)、抗p65抗体(Cell Signaling Technology Cat# 8242)、抗磷酸化p65抗体(Cell Signaling Technology Cat# 3033)、抗MMP9抗体(Abcam Cat# ab76003)、DCFH-DA(Beyotime Institute of Biotechnology);文献未提及具体SOD活性试剂盒品牌,领域常规使用比色法或荧光法试剂盒检测SOD活性。
3.6 体内安全性评估
实验目的:验证Au-MEA NPs凝胶的体内安全性,评估其组织分布及潜在毒性。
方法细节:给药后处死小鼠,收集心脏、肝脏、脾脏、肺、肾脏及皮肤组织,进行H&E染色评估组织形态,ICP-MS检测金元素分布;同时进行溶血实验,评估纳米颗粒对红细胞的毒性。
结果解读:H&E染色显示各主要器官组织形态无异常(n=5,P>0.05),ICP-MS显示金元素主要分布于皮肤组织,各器官中金含量与对照组无显著差异(n=5,P>0.05);溶血实验显示Au-MEA NPs在各浓度下均无显著溶血作用(n=3,P>0.05),表明Au-MEA NPs凝胶局部给药具有良好的安全性。
产品关联:实验所用关键仪器:Agilent ICP-MS7900电感耦合等离子体质谱仪;文献未提及具体H&E染色试剂品牌,领域常规使用苏木精、伊红染色液进行组织染色。
4. Biomarker研究及发现成果
本研究聚焦炎症性皮肤病中的氧化应激与基质金属蛋白酶相关Biomarker,包括超氧化物歧化酶(SOD)、基质金属蛋白酶9(MMP9)及多种炎症细胞因子,通过体内外实验验证了Au-MEA NPs对这些Biomarker的调控作用,明确了其治疗炎症性皮肤病的核心机制。
Biomarker定位:本研究涉及的Biomarker包括酶活性标志物(SOD、MMP9)和炎症细胞因子(IL-6、TNF-α、VEGF等)。筛选与验证逻辑为:首先通过动物模型治疗后的蛋白质组学分析,筛选出氧化应激与炎症相关的差异通路,锁定SOD和MMP9作为核心调控靶点;随后在体外细胞模型中,验证Au-MEA NPs对SOD活性、MMP9表达及活性的调控作用,同时检测炎症细胞因子的表达变化,形成“组学筛选→体内验证→体外机制”的完整逻辑链条。
研究过程详述:SOD作为抗氧化酶Biomarker,其活性在H₂O₂处理的HaCaT细胞中被Au-MEA NPs显著提升,活性水平为对照组的1.8倍(n=3,P<0.05);MMP9作为炎症相关酶Biomarker,其mRNA水平在TNF-α诱导的HaCaT细胞中被Au-MEA NPs下调至对照组的42%(n=3,P<0.01),蛋白表达水平下调至对照组的35%(n=3,P<0.01),凝胶酶谱法显示其活性被显著抑制;炎症细胞因子Biomarker如IL-6、TNF-α的mRNA水平在动物模型中被下调至模型组的30%-50%(n=6,P<0.05)。这些Biomarker的样本来源包括小鼠皮肤组织和HaCaT细胞培养体系,验证方法涵盖qRT-PCR、Western blot、凝胶酶谱法、SOD活性检测等。
核心成果提炼:本研究发现Au-MEA NPs可通过提升SOD活性清除ROS,抑制MMP9的表达与活性,进而阻断NF-κB通路,减少炎症细胞因子的分泌,最终改善银屑病和玫瑰痤疮的皮损症状。该Biomarker调控机制的创新性在于首次将金纳米颗粒的类SOD活性与MMP9抑制作用结合,实现对炎症性皮肤病的双重靶向治疗;其中SOD活性提升与MMP9活性抑制的协同作用,为炎症性皮肤病的治疗提供了新的靶点组合。此外,Au-MEA NPs作为局部给药纳米药物,具有良好的透皮性与安全性,其临床转化价值显著,为炎症性皮肤病的局部治疗提供了新的技术范式。
