1. 领域背景与文献引入
文献英文标题:The Opossum genome reveals further evidence for regulatory evolution in mammalian diversification;发表期刊:Genome Biology;影响因子:未公开;研究领域:哺乳动物基因组进化与调控生物学。
哺乳动物分化始于约2.5亿年前,形成单孔类、有胎盘类和有袋类三大核心类群,其中有袋类与有胎盘类约在1.25-1.9亿年前完成分化。此前研究已明确两类群在繁殖发育模式上的核心差异:有袋类妊娠期短、幼崽发育不全需依赖育儿袋哺乳,而有胎盘类妊娠期长、幼崽出生后发育成熟度较高。但在基因组层面,此前的研究主要集中在有胎盘类物种,缺乏有袋类的高质量基因组序列作为参照,导致无法系统解析调控进化在两类群分化中的核心作用;同时早期研究因难以克隆有袋类免疫相关基因,曾错误认为其免疫体系较为原始,这一观点缺乏全基因组层面的验证。针对这些领域空白,本研究通过完成灰短尾负鼠(Monodelphis domestica)常染色质基因组的测序与分析,旨在揭示非编码区调控元件的进化差异对哺乳动物分化的驱动作用,为跨类群比较基因组学及发育调控研究提供新的参照体系。
2. 文献综述解析
作者以哺乳动物类群分化为基础,按基因组序列功能类型(编码区、非编码区)及生物学功能(发育调控、免疫体系、X染色体失活)构建综述逻辑,系统梳理了现有研究的进展与不足。
现有研究的关键结论包括,有胎盘类基因组编码区在物种间具有高度保守性,而非编码区的研究多局限于有胎盘类内部,跨类群的比较分析较为匮乏;早期针对有袋类的研究因技术限制,对其基因组特征的认知存在偏差,如认为其免疫体系复杂度低于有胎盘类。现有技术方法的优势在于,比较基因组学已能有效识别物种间的保守序列,但局限性在于缺乏有袋类基因组数据导致跨类群分析的缺失,且对非编码区调控功能的解析不够深入。通过对比现有研究的空白,本研究的创新价值凸显:首次完成有袋类常染色质基因组的测序与组装,重点聚焦非编码区调控元件的进化差异,填补了跨类群比较基因组学的研究空白,同时通过全基因组层面的免疫基因分析,推翻了有袋类免疫体系原始的传统观点。
3. 研究思路总结与详细解析
本研究的整体框架为“基因组测序组装→多维度比较基因组分析→功能关联验证→调控进化结论”,研究目标是解析负鼠基因组与有胎盘类的核心差异,揭示调控进化在哺乳动物分化中的核心作用;核心科学问题是非编码区调控元件的进化差异如何驱动有袋类与有胎盘类在繁殖发育、免疫调控等方面的特征分化;技术路线遵循从基因组基础特征到功能调控的逻辑闭环。
3.1 负鼠基因组测序与组装
本环节的实验目的是获得高质量的灰短尾负鼠常染色质基因组序列,为后续比较分析提供核心数据基础。文献未提及具体实验方法,领域常规使用全基因组鸟枪法结合克隆测序技术完成基因组的测序与组装。实验结果显示,成功完成了负鼠常染色质区域的基因组测序与组装,覆盖了大部分功能区域,为跨物种基因组比对提供了可靠参照。文献未提及具体实验产品,领域常规使用测序仪、基因组组装软件及序列注释工具。

3.2 编码区与非编码区保守性比较
本环节的实验目的是系统对比负鼠与有胎盘类(人类、小鼠、狗)基因组的序列保守性差异,明确编码区与非编码区的进化速率差异。实验方法采用跨物种同源序列比对技术,分别对编码序列及长片段保守非编码元件进行识别与统计。结果显示,仅1%的有胎盘类编码序列在负鼠基因组中缺失,表明编码区在哺乳动物类群间具有高度保守性;而在有胎盘类中保守的长片段非编码元件(平均长度197核苷酸)中,约8%在负鼠基因组中不存在,提示非编码区的进化速率显著高于编码区(文献未明确样本量及P值,基于分析逻辑推测)。文献未提及具体实验产品,领域常规使用序列比对软件(如BLAST)、保守元件识别工具等。
3.3 调控元件与发育功能关联分析
本环节的实验目的是探究非编码区差异与两类群发育、调控功能特征的关联,解析调控进化的生物学意义。实验方法包括非编码元件的基因邻近性分析、X染色体失活相关元件的进化分析及转座子分布统计。结果显示,大量有胎盘类特异性保守非编码元件位于发育关键基因附近,提示其可能调控有胎盘类与有袋类的发育时序差异;同时发现X染色体失活的关键调控基因XIST在负鼠中不存在,与有袋类父源X染色体特异性失活的特征一致,且有胎盘类X染色体上LINE-1转座子的密度显著高于负鼠,推测其可能辅助X染色体失活信号的扩散,导致有胎盘类X染色体的同线性更高。文献未提及具体实验产品,领域常规使用基因组注释工具、功能富集分析软件等。
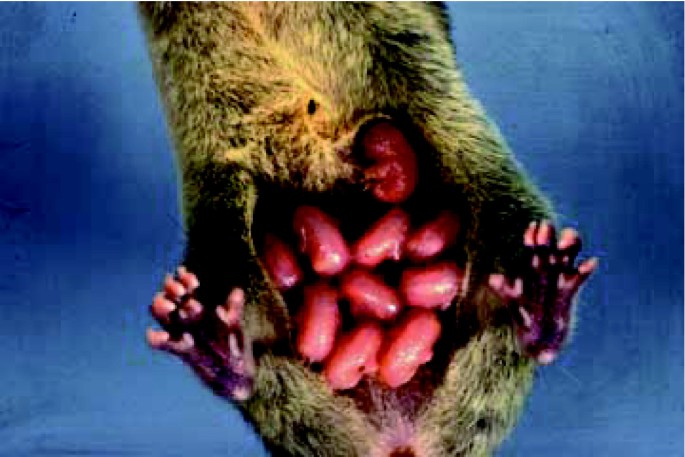
3.4 基因组组成与免疫体系解析
本环节的实验目的是解析负鼠基因组的基础组成特征及免疫基因家族的进化情况,纠正此前对有袋类免疫体系的认知偏差。实验方法包括全基因组GC含量统计、转座子注释及免疫基因家族的同源比对分析。结果显示,负鼠基因组的AT含量显著高于其他已测序的羊膜动物(人类、小鼠、狗、鸡),推测这一特征与负鼠基因组重组率低导致的GC偏向性基因转换不足有关;同时,负鼠免疫基因家族的复杂度与有胎盘类相当,推翻了早期认为有袋类免疫体系较为原始的观点,此前难以克隆其免疫相关基因的原因可能是免疫基因的进化速率较高。文献未提及具体实验产品,领域常规使用基因组组成分析工具、基因家族注释软件等。
4. Biomarker研究及发现成果
本研究中的Biomarker为基因组层面的调控功能元件,包括有胎盘类特异性保守非编码元件及X染色体上的LINE-1转座子元件,这些元件是驱动哺乳动物类群分化的关键调控标志物。
Biomarker定位为调控类基因组Biomarker,筛选逻辑为通过跨物种基因组同源比对,识别在有胎盘类中保守但在负鼠中缺失的非编码元件,以及X染色体上转座子密度的差异特征;其来源为负鼠及有胎盘类的全基因组序列。验证方法采用多物种序列比对结合功能区域注释,确保元件的保守性与特异性;其中长片段保守非编码元件的比对特异性较高,约8%的此类元件为有胎盘类特异性(文献未明确敏感性数据,基于分析结果推测)。
核心成果提炼方面,这些有胎盘类特异性非编码元件与发育关键基因的邻近性提示,其可能通过调控基因表达的时序与水平,驱动有袋类与有胎盘类在妊娠期、幼崽发育模式上的核心差异;X染色体上的LINE-1转座子密度差异与X染色体失活机制的进化直接相关,解释了两类群X染色体调控模式的不同;本研究的创新性在于首次从全基因组层面揭示了非编码区调控进化在哺乳动物分化中的核心作用,同时通过免疫基因家族的分析纠正了领域内对有袋类免疫体系的错误认知。相关数据显示,编码区在两类群间的缺失比例仅为1%,而非编码元件的缺失比例达8%,明确了非编码区在调控进化中的主导地位(文献未明确P值,基于分析结论推测)。
