1. 领域背景与文献引入
文献英文标题:Autophagy in the control and pathogenesis of parasitic infections;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:寄生虫感染与细胞自噬交叉领域
细胞自噬是真核生物中保守的细胞降解与循环过程,1993年Tsukada和Ohsumi首次在酵母中鉴定出15个自噬相关(ATG)基因,奠定了自噬研究的分子基础;2000年后,研究逐渐拓展至宿主-病原体互作领域,发现自噬可通过异噬(xenophagy)清除胞内病原体,同时部分病原体进化出逃逸甚至利用自噬的策略。当前该领域的研究热点聚焦于自噬与免疫通路的交叉调控机制,以及自噬作为抗感染治疗靶点的开发,但仍存在核心问题:不同寄生虫对宿主自噬的调控机制存在显著差异,自噬启动复合物与模式识别受体(PRRs)的精准互作网络尚未完全解析,限制了靶向自噬的抗寄生虫药物研发。这篇综述旨在系统总结近年自噬与寄生虫互作的研究进展,明确关键调控蛋白,为抗寄生虫治疗药物的设计提供理论依据。
2. 文献综述解析
作者以自噬通路的功能分类为核心维度,将现有研究划分为经典自噬与非经典自噬(如LC3相关吞噬作用LAP、疟原虫相关自噬应答PAAR)、自噬与宿主免疫的交叉调控、寄生虫对自噬的逃逸与利用机制、自噬作为治疗靶点的潜力四大模块,系统梳理了自噬在寄生虫感染中的双重作用。
现有研究的关键结论显示,宿主自噬在抗寄生虫感染中具有双向调控作用:一方面,自噬可通过异噬途径将泛素化标记的寄生虫包裹进自噬体,最终在自噬溶酶体中降解;另一方面,疟原虫、弓形虫等寄生虫可通过修饰寄生泡膜(PVM)、分泌调控蛋白等方式逃逸自噬清除,甚至利用宿主自噬获取营养以支持自身生长。技术方法上,现有研究结合了细胞模型(如巨噬细胞、肝细胞系)、动物感染模型(如小鼠疟原虫感染模型)和临床样本分析,能够较为全面地解析自噬与寄生虫的互作机制,但部分研究存在局限性,如针对特定寄生虫的调控机制研究缺乏跨物种验证,自噬与免疫通路的互作研究多集中于单个分子,未形成系统的调控网络。
通过对比现有研究的空白,该综述凸显了其创新价值:首次系统整合了自噬启动复合物(ULK复合物)、PRRs介导的病原体相关分子模式(PAMPs)识别等关键节点在寄生虫感染中的作用,明确了不同自噬通路在抗寄生虫免疫中的特异性功能,同时提出了基于自噬调控蛋白的精准治疗靶点,为后续研究提供了清晰的方向。
3. 研究思路总结与详细解析
作者的整体研究思路是通过系统检索并整合2010-2020年期间自噬与寄生虫感染领域的核心研究成果,围绕“自噬通路-免疫调控-寄生虫逃逸-治疗靶点”的逻辑链条,全面解析宿主自噬与寄生虫的互作机制,最终提炼出具有潜在药物开发价值的关键蛋白。
3.1 自噬核心通路与寄生虫互作机制解析
该环节的核心目标是明确经典自噬与非经典自噬通路在寄生虫感染中的功能差异。作者通过整合现有研究数据,总结了经典自噬的启动依赖ULK复合物(由ATG13、FIP200、ATG101组成)的激活,而异噬清除寄生虫的过程需先对寄生虫进行泛素化标记,再由自噬受体识别并招募LC3蛋白完成自噬体包裹;非经典自噬通路如LAP则无需ULK复合物参与,直接将LC3结合到寄生泡膜上,抑制寄生虫在泡内的生长。结果显示,不同寄生虫对自噬通路的利用存在差异:疟原虫肝脏阶段可利用宿主经典自噬获取营养,同时通过PAAR通路触发宿主的胞内免疫应答;弓形虫则主要通过修饰PVM逃逸自噬清除。文献未提及具体实验产品,领域常规使用自噬检测试剂盒(如LC3抗体、自噬通量检测试剂)、细胞培养体系、动物感染模型等。
3.2 自噬与宿主免疫应答的交叉调控
该环节的目标是解析自噬与宿主免疫通路的互作机制。作者梳理了模式识别受体(PRRs)尤其是 Toll样受体(TLRs)对自噬的调控作用:TLRs可通过识别寄生虫的PAMPs,激活TRIF-p38通路诱导自噬,进而清除寄生虫;同时,干扰素-γ(IFN-γ)可通过调控ATG蛋白的表达,增强自噬对寄生虫的清除能力。此外,作者还总结了自噬在抗原提呈中的作用:自噬可将寄生虫抗原递呈至MHC II类分子,激活CD4+T细胞介导的适应性免疫。文中还展示了胞质dsDNA诱导的STING依赖型免疫应答与自噬的互作机制,STING可调控I型干扰素的表达,同时自噬参与STING依赖的抗微生物应答,而Atg9a可负调控STING依赖的IFN应答。
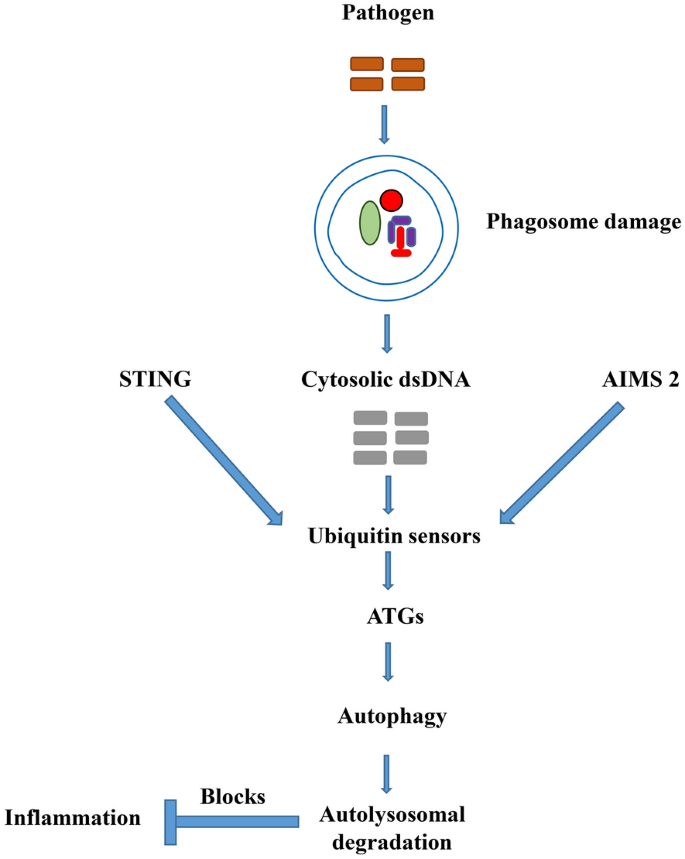
文献未提及具体实验产品,领域常规使用免疫组化(IHC)试剂、流式细胞仪、qRT-PCR检测体系等。
3.3 寄生虫对宿主自噬的逃逸与利用机制
该环节的目标是系统总结寄生虫逃逸或利用宿主自噬的策略。作者指出,寄生虫主要通过三种方式调控宿主自噬:一是抑制自噬启动,如利什曼原虫可通过蛋白酶GP63灭活mTOR,或通过其他机制诱导自噬以获取营养;二是干扰自噬降解通路,如弓形虫通过修饰PVM阻止自噬体与溶酶体融合;三是利用自噬通路获取营养,如疟原虫肝脏阶段可利用宿主经典自噬的氨基酸池支持自身生长。结果显示,疟原虫分泌的UIS3蛋白是其逃逸自噬的关键分子,UIS3可与LC3蛋白结合,阻止LC3与下游效应分子的相互作用,从而抑制自噬通路的激活。文献未提及具体实验产品,领域常规使用基因敲除/过表达细胞系、免疫共沉淀(Co-IP)试剂盒等。
3.4 自噬作为抗寄生虫治疗靶点的潜力分析
该环节的目标是评估自噬相关蛋白作为抗寄生虫治疗靶点的可行性。作者总结了现有研究中具有潜力的靶点:ULK复合物的激活剂可增强宿主自噬对寄生虫的清除能力;PRRs的激动剂可通过诱导自噬激活免疫应答;针对寄生虫逃逸蛋白如UIS3的抑制剂可阻断其对自噬的抑制,恢复宿主的自噬清除功能。此外,作者还提出,将寄生虫抗原靶向递送至自噬体可增强疫苗的免疫原性,如流感病毒抗原与LC3的融合蛋白可显著增强CD4+T细胞应答。结果显示,雷帕霉素(mTOR抑制剂)可通过激活自噬,增强对弓形虫的自噬溶酶体降解,为临床治疗提供了潜在方向。文献未提及具体实验产品,领域常规使用小分子抑制剂、疫苗载体系统等。
4. Biomarker研究及发现成果解析
该综述中涉及的Biomarker主要分为宿主来源的自噬调控蛋白(如LC3、ULK复合物组分、TLRs家族分子)和寄生虫来源的自噬逃逸蛋白(如UIS3),其筛选与验证逻辑基于细胞模型、动物实验及部分临床样本的关联分析,形成了“数据库筛选-细胞系验证-动物模型验证”的完整链条。
Biomarker的来源涵盖宿主细胞(如巨噬细胞、肝细胞)和寄生虫分泌蛋白,验证方法包括免疫印迹、免疫荧光、基因敲除/过表达、免疫共沉淀等。其中,LC3作为自噬激活的核心标志物,其脂化形式LC3-II的表达水平可反映自噬活性,在异噬和LAP通路中均有参与,研究显示LC3与PVM的结合效率可作为评估寄生虫逃逸自噬能力的指标(文献未明确具体数值);UIS3作为疟原虫逃逸自噬的关键Biomarker,通过与LC3的直接结合抑制自噬,在小鼠模型中,UIS3的敲除可显著增强宿主自噬对疟原虫的清除能力,且UIS3作为疫苗候选靶点,在多株小鼠中可诱导抗原特异性CD8+T细胞应答,实现100%无菌保护(文献未明确样本量及P值)。
核心成果提炼显示,这些Biomarker具有重要的功能关联:宿主自噬相关蛋白(如ULK1、TLR9)可作为抗寄生虫治疗的靶点,其激活可增强宿主的抗感染能力;寄生虫来源的UIS3蛋白不仅是疟原虫逃逸自噬的关键分子,还具有疫苗开发潜力。创新性方面,该综述首次系统提出PAAR通路作为疟原虫感染的特异性应答通路,其相关分子可作为新型Biomarker用于疟原虫感染的诊断与治疗监测,为该领域的后续研究提供了新的方向。
