1. 领域背景与文献引入
文献英文标题:Intracellular targeting of Cisd2/Miner1 to the endoplasmic reticulum;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:细胞生物学(内质网与线粒体蛋白定位调控机制)
Cisd家族蛋白是一类含有CDGSH铁硫簇结合域的功能蛋白,其中Cisd1(又称mitoNEET)和Cisd2(又称Miner1/NAF-1)的氨基酸序列与空间结构高度相似,均包含N端跨膜结构域和C端胞质铁硫簇结合域,但二者的亚细胞定位存在显著差异。领域共识:Cisd1稳定定位于线粒体外膜,可作为氧化信号传感器调控细胞死亡与增殖,在肿瘤发生发展中发挥作用,过表达还可导致线粒体聚集;Cisd2的定位则存在争议,部分研究认为其定位于内质网,参与自噬抑制、钙稳态调控,其突变可引发罕见神经退行性疾病Wolfram综合征,也有研究提出Cisd2定位于线粒体,与小鼠早衰表型相关。当前领域未解决的核心问题是,Cisd2靶向并保留在内质网的具体分子基序尚不明确,且结构高度相似的Cisd1与Cisd2为何定位于不同细胞器的分子机制仍不清楚,这限制了对Cisd家族蛋白功能及相关疾病发病机制的深入理解。本研究旨在明确Cisd2靶向内质网的关键结构域,解析其内质网保留的分子机制,并对比Cisd1与Cisd2定位差异的分子基础,为Cisd家族蛋白功能研究及相关疾病干预提供理论依据。
2. 文献综述解析
作者围绕Cisd家族蛋白的定位、功能及潜在定位基序展开现有研究评述,分类维度涵盖蛋白亚细胞定位、生理功能、结构基序的功能推测三个层面。
现有研究的关键结论显示,Cisd1定位于线粒体外膜,可调控铁稳态与氧化信号感知,在肿瘤细胞增殖中发挥双重作用;Cisd2的功能与定位存在分歧,内质网定位的Cisd2可通过与Bcl2互作抑制自噬,参与内质网应激与钙稳态调控,线粒体定位的Cisd2则与衰老相关,其基因敲除可导致小鼠线粒体功能异常与早衰。技术方法层面,现有研究多采用荧光蛋白融合表达或商业抗体进行蛋白定位检测,优势在于可直观观察蛋白亚细胞分布,但局限性在于荧光蛋白融合可能改变蛋白天然构象导致定位 artefact,且部分抗体特异性不足易产生假阳性结果;同时,现有研究未系统解析Cisd2靶向内质网的具体分子基序,对Cisd2 C端KKxx序列的功能未进行直接验证,也未明确Cisd1的类似C端序列为何不发挥内质网定位作用,导致Cisd家族蛋白定位调控机制的研究存在明显空白。本研究的创新价值在于,首次通过构建无标签野生型蛋白及嵌合蛋白,避免了荧光蛋白融合带来的定位偏差,系统验证了Cisd2靶向内质网的N端序列、维持内质网保留的短跨膜结构域与C端KKxx基序,明确了Cisd2与Cisd1定位差异的分子基础,填补了Cisd家族蛋白定位调控机制的研究空白。
3. 研究思路总结与详细解析
本研究的整体研究目标为明确Cisd2靶向并保留在内质网的分子基序,解析其与Cisd1亚细胞定位差异的机制,同时探究Cisd2对细胞器形态的影响;核心科学问题包括Cisd2的哪些结构域负责内质网靶向与保留、Cisd1与Cisd2定位差异的分子基础、Cisd2是否能改变内质网形态;技术路线遵循“假设提出→嵌合/突变体构建→免疫荧光定位验证→蛋白互作实验→超微结构观察”的闭环逻辑,通过多维度实验验证研究假设。
3.1 野生型与嵌合Cisd蛋白的亚细胞定位验证
实验目的:验证Cisd1与Cisd2的N端序列是否为决定其亚细胞定位的关键结构域。
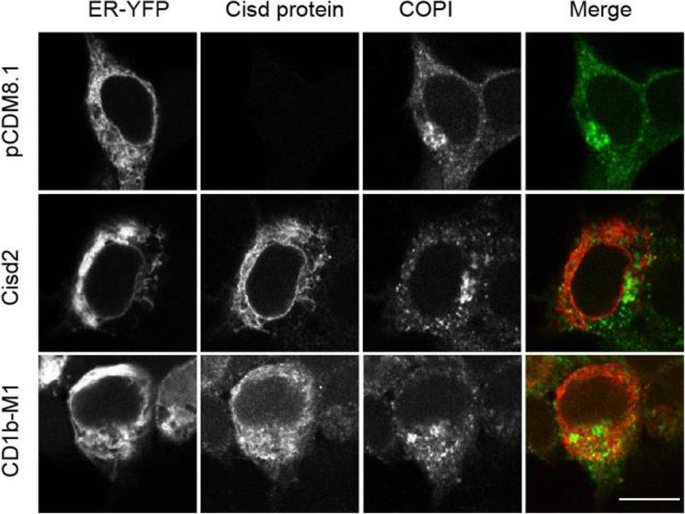
方法细节:在人胚肾(HEK)细胞中共转染野生型Cisd1/Cisd2、内质网靶向黄色荧光蛋白(ER-YFP)及线粒体靶向红色荧光蛋白(mito-RFP),同时构建嵌合蛋白Cisd12(Cisd1 N端序列+Cisd2胞质域)与Cisd21(Cisd2 N端序列+Cisd1胞质域);为避免荧光蛋白融合导致的定位偏差,采用针对Cisd1胞质域的重组抗体RB251与针对Cisd2胞质域的重组抗体RB253进行免疫荧光染色,使用Zeiss LSM700共聚焦显微镜观察蛋白定位。
结果解读:野生型Cisd1与mito-RFP完全共定位,过表达可导致线粒体聚集(箭头所示);野生型Cisd2与ER-YFP共定位,主要分布于核膜及胞质内质网结构,过表达可轻微改变内质网形态;嵌合蛋白Cisd12定位于线粒体并导致线粒体聚集,Cisd21则定位于内质网,表明Cisd1与Cisd2的N端序列是决定其亚细胞定位的关键结构域。
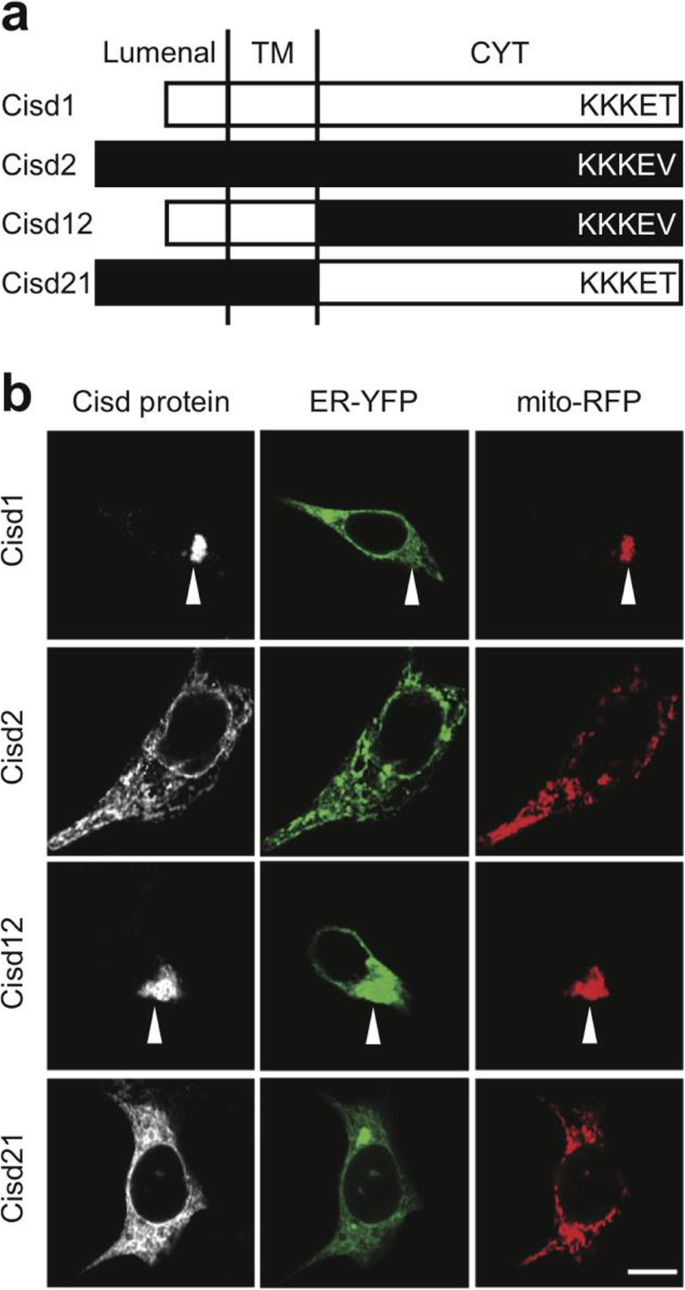
实验所用关键产品:针对Cisd1胞质域的重组抗体RB251、针对Cisd2胞质域的重组抗体RB253,Zeiss LSM700共聚焦显微镜。
3.2 Cisd2内质网保留基序的功能验证
实验目的:明确Cisd2的跨膜结构域(TMD)与C端KKxx基序在内质网保留中的协同作用。
方法细节:构建CD1b与Cisd2不同结构域的融合蛋白,包括CD1b-M1(CD1b信号肽+Cisd2全长)、CD1b-M2(CD1b+Cisd2 TMD+短胞质域)、CD1b-M3(CD1b+Cisd2胞质域)、CD1b-M4/M5(C端KKEV基序突变体,分别将赖氨酸突变为丝氨酸或在C端添加丝氨酸);在HEK细胞中表达上述融合蛋白,通过免疫荧光检测与ER-YFP、高尔基体标志物giantin的共定位,同时采用细胞表面免疫标记结合ImageJ定量分析融合蛋白的细胞表面表达水平,通过Western blot检测融合蛋白的糖基化成熟情况以判断其是否进入分泌通路。
结果解读:CD1b-M1主要定位于内质网,几乎不出现于细胞表面,仅少量蛋白发生糖基化成熟;CD1b-M2部分定位于内质网与高尔基体,约30%的蛋白分布于细胞表面(n=70,文献未明确P值);CD1b-M3主要定位于内质网,少量蛋白出现于细胞表面;突变KKEV基序的CD1b-M4/M5则主要定位于细胞表面,且大部分蛋白发生糖基化成熟,表明Cisd2的短TMD(16个氨基酸)与C端KKEV基序共同发挥内质网保留作用,两者缺一不可。
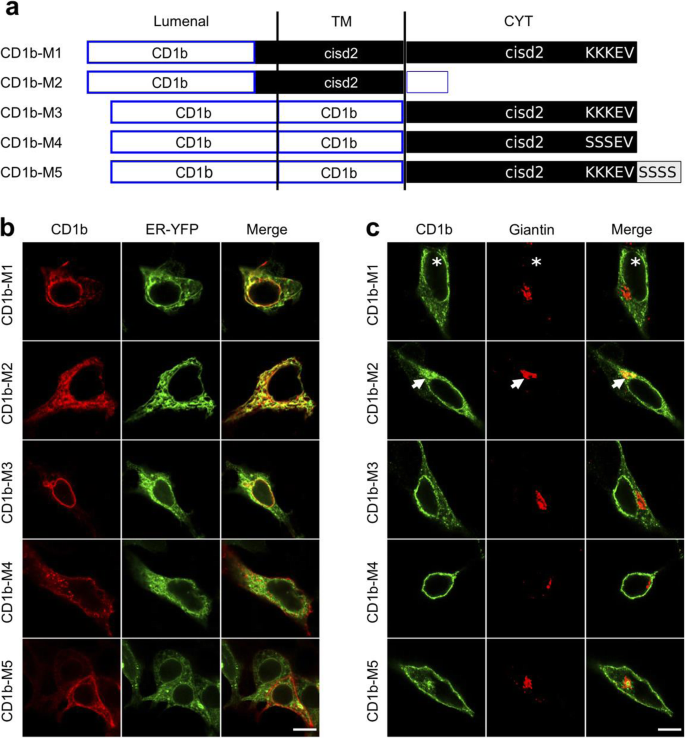
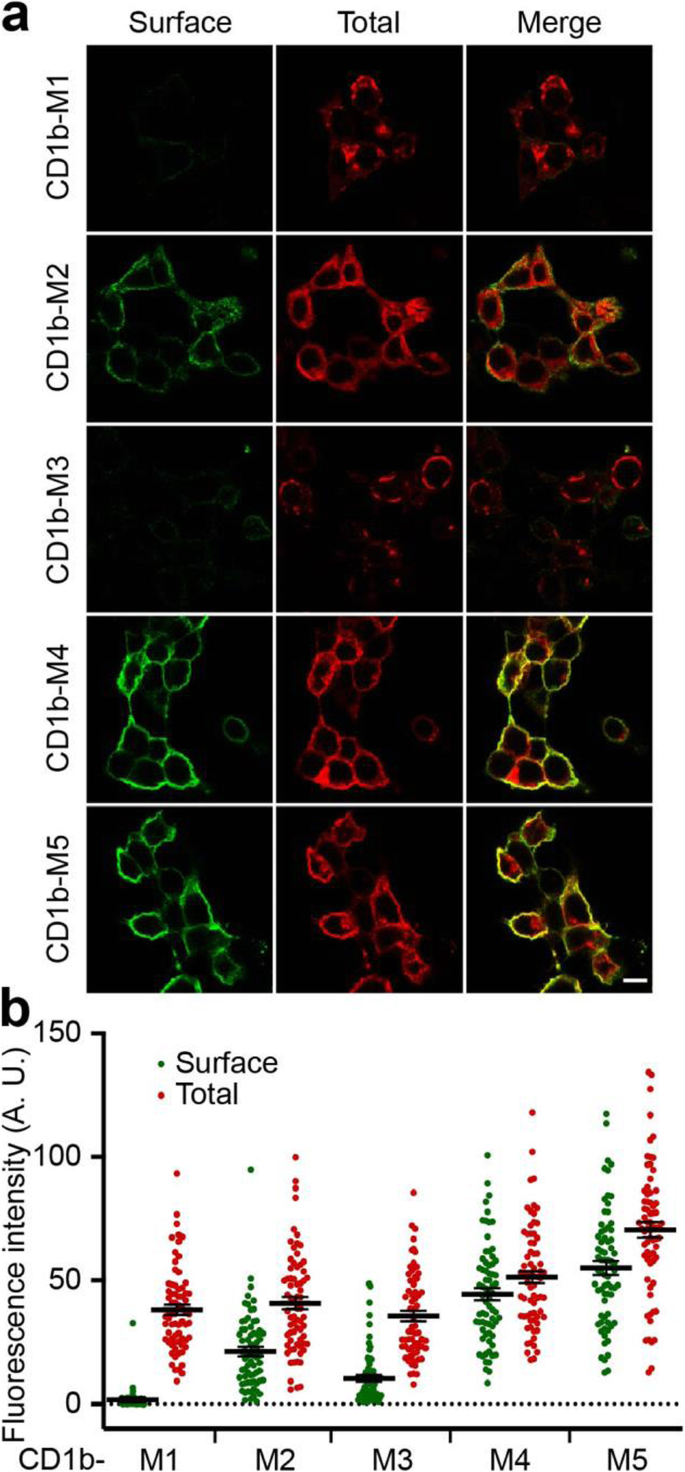
实验所用关键产品:抗CD1b抗体AJ521、抗giantin抗体AA341,ImageJ图像分析软件,iBlot2 Dry blotting蛋白转印系统,Syngene PXi-4凝胶成像系统。
3.3 Cisd2与Cisd1 C端基序的COPI结合能力分析
实验目的:验证Cisd2的KKEV基序是否为功能性COPI结合基序,而Cisd1的KKET基序无此功能的原因。
方法细节:合成Cisd1、Cisd2的C端10个氨基酸的生物素化肽段,同时合成已知的功能性COPI结合基序WBP1的KKxx肽段及突变体WBP1-SS(赖氨酸突变为丝氨酸)作为对照;将肽段固定于Dynabeads® M-280链霉亲和素磁珠上,与COS7细胞裂解液孵育2小时,通过考马斯亮蓝染色与银染检测结合的COPI复合物。
结果解读:WBP1肽段可结合COPI复合物的α、β/β’/γ亚基,WBP1-SS则无结合能力;Cisd2肽段可结合COPI复合物(银染可见亚基条带),但结合效率低于WBP1;Cisd1肽段未检测到COPI结合,表明Cisd2的KKEV是功能性COPI结合基序,而Cisd1的KKET因C端氨基酸差异(苏氨酸 vs 缬氨酸)无法结合COPI,这是两者定位差异的另一关键原因。
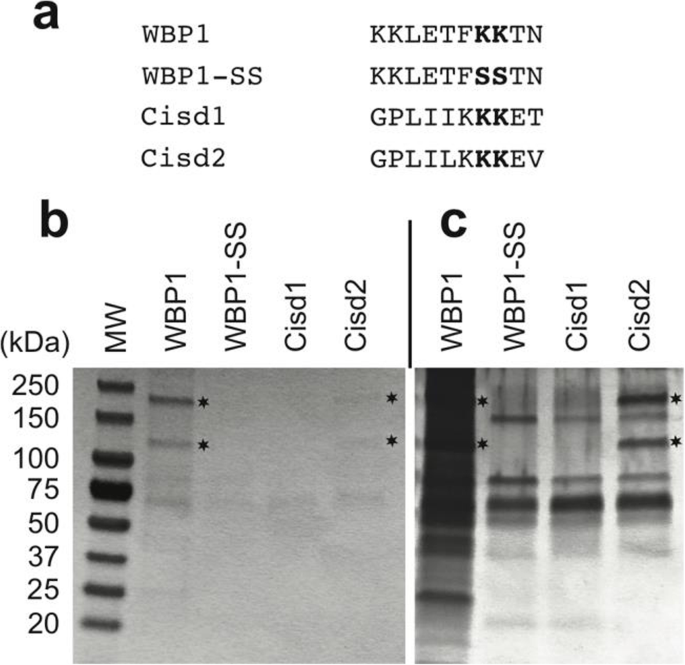
实验所用关键产品:Dynabeads® M-280 Streptavidin磁珠,考马斯亮蓝染色液,银染试剂盒。
3.4 Cisd2过表达对内质网形态及COPI分布的影响
实验目的:探究Cisd2是否能改变内质网形态,以及该过程是否依赖COPI复合物。
方法细节:在HEK细胞中表达CD1b-M1融合蛋白,通过冷冻免疫电镜观察内质网超微结构;同时采用针对COPI复合物的重组抗体RB498,检测过表达Cisd2或CD1b-M1的细胞中COPI的亚细胞分布。
结果解读:电镜结果显示,过表达CD1b-M1的细胞中内质网部分塌陷并与核膜多处连接,形态发生明显改变;但COPI的分布未发生显著变化,仍主要定位于高尔基体周围及胞质点状结构,未在形态异常的内质网区域聚集,推测Cisd2改变内质网形态不依赖COPI复合物,而是通过自身胞质域的二聚体化 tether 相邻内质网膜,与Cisd1改变线粒体形态的机制保守。
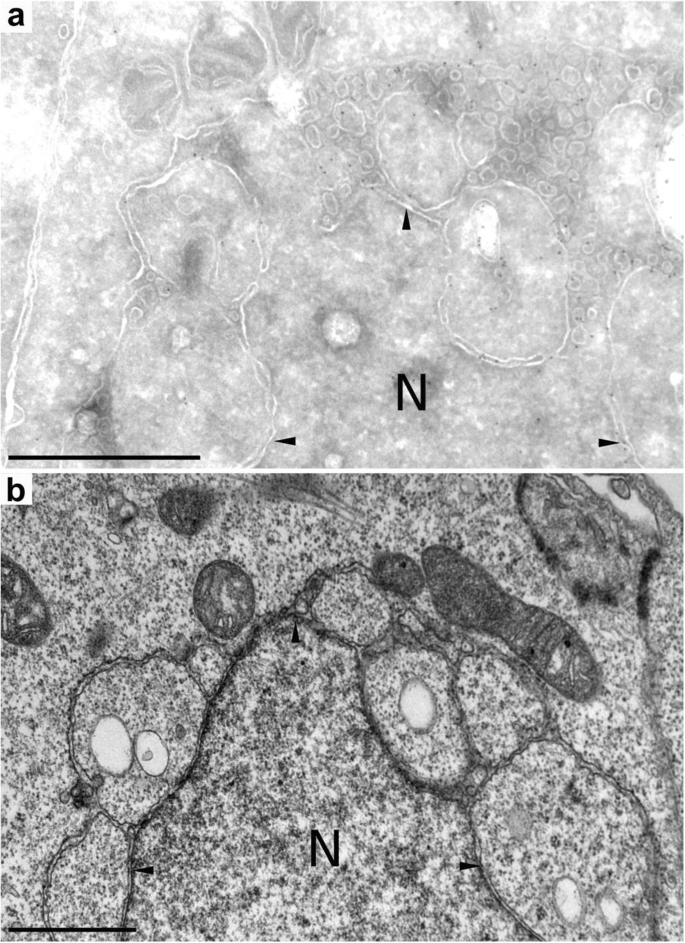
实验所用关键产品:抗COPI复合物的重组抗体RB498,Morgagni电子显微镜,冷冻超薄切片机。
4. Biomarker研究及发现成果
本研究聚焦于Cisd2靶向内质网的功能性分子基序,属于蛋白亚细胞定位调控的分子标志物,通过“序列分析→嵌合/突变体验证→蛋白互作实验”的完整逻辑链,明确了三个关键功能基序及其作用机制。
Biomarker定位:本研究鉴定的功能性分子标志物包括Cisd2的N端内质网靶向基序、短跨膜结构域(TMD)及C端KKEV COPI结合基序;筛选与验证逻辑为,首先通过序列对比推测N端序列可能参与靶向,通过嵌合蛋白实验验证其内质网靶向功能;随后基于短TMD与C端KKxx序列的结构特征,通过突变体实验验证其内质网保留功能;最后通过肽段-蛋白互作实验验证KKEV基序的COPI结合能力。研究过程详述:上述基序均来源于Cisd2的天然氨基酸序列,验证方法包括免疫荧光共定位、细胞表面蛋白定量、Western blot糖基化分析及体外肽段结合实验;特异性方面,Cisd2的N端基序仅介导内质网靶向,而Cisd1的N端序列介导线粒体靶向,Cisd2的KKEV基序可结合COPI,而Cisd1的KKET基因C端氨基酸差异无此功能;敏感性方面,免疫荧光可检测到低表达水平的蛋白定位,银染可检测到低丰度的COPI结合复合物;样本量方面,细胞表面荧光定量分析的样本量为n=70,其余实验样本量文献未明确提供,基于图表趋势推测结果具有统计学意义。核心成果提炼:本研究首次明确了Cisd2靶向并保留在内质网的三个关键分子基序,揭示了Cisd1与Cisd2结构相似但定位不同的分子机制,同时发现Cisd2可通过自身二聚体化改变内质网形态,与Cisd1改变线粒体形态的机制保守;创新性在于首次系统解析了Cisd2的内质网定位调控机制,填补了Cisd家族蛋白定位调控研究的空白,为理解Cisd2在Wolfram综合征、衰老等过程中的作用提供了分子基础;无统计学显著性P值的实验结果,文献未明确提供相关数据。
