1. 领域背景与文献引入
文献英文标题:Visualising single molecules of HIV-1 and miRNA nucleic acids;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-核酸原位可视化技术、病毒学-HIV感染机制研究、分子生物学-微小RNA(miRNA)功能研究
核酸原位可视化技术是细胞生物学领域的核心研究工具之一,可在单细胞水平解析核酸的亚细胞定位、拷贝数与动态变化,为病毒感染、基因表达调控等机制研究提供关键证据。传统荧光原位杂交(fluorescence in situ hybridization, FISH)技术依赖多荧光标记的单探针或单荧光标记的多探针实现信号可视化,虽能常规检测细胞内核酸,但对低拷贝靶标的灵敏度不足,且难以适配小长度核酸。后续发展的滚环扩增(rolling circle amplification, RCA)、分支DNA探针等改进型FISH技术显著提升了信噪比与检测灵敏度,但需要较长的靶标序列,无法应用于miRNA等小核酸的检测;分子信标、MS2-GFP融合蛋白、量子点标记等替代方法虽能实现单分子检测,但存在技术操作复杂、依赖特殊仪器等局限,难以普及。当前领域的核心研究空白是缺乏一种通用、高灵敏、同时兼容低拷贝与小长度核酸的原位可视化方法,因此开发新型技术工具具有重要的学术价值与应用潜力。本文针对这一空白,将邻近连接分析(proximity ligation assay, PLA)与FISH技术结合,开发出寡核苷酸荧光原位杂交(O-FISH)方法,实现了单分子水平的核酸原位检测。
2. 文献综述解析
作者围绕核酸原位可视化技术的发展现状,将现有方法分为三类进行系统评述,明确了不同技术的适用范围与核心局限,为O-FISH方法的创新提供了严谨的逻辑支撑。
传统荧光原位杂交技术是细胞内核酸检测的常规手段,其优势为操作流程成熟、可适配多种细胞样本,但核心局限在于对低拷贝靶标的灵敏度不足,且需要多探针或多荧光标记才能实现信号可视化,无法满足单分子检测需求。基于滚环扩增、分支DNA探针的改进型FISH技术通过信号放大策略提升了信噪比与检测灵敏度,能实现低拷贝核酸的检测,但这类方法需要较长的靶标序列(通常数百nt),无法应用于miRNA(约20nt)等小核酸的原位检测。分子信标、MS2-GFP融合蛋白、量子点标记等替代方法虽能实现单分子核酸检测,但存在技术门槛高、依赖特殊仪器或基因改造等局限,难以作为通用工具普及使用。
通过对比现有技术的核心局限,本文的创新价值凸显:首次将邻近连接分析技术与FISH结合,开发出O-FISH方法,仅需19-26nt的单寡核苷酸探针即可实现低拷贝(1-2个)核酸的特异性原位检测,同时兼容小长度miRNA的检测,填补了通用型高灵敏小核酸原位可视化技术的空白,为细胞生物学、病毒学等领域的研究提供了全新工具。
3. 研究思路总结与详细解析
本研究以开发通用、高灵敏的单分子核酸原位可视化技术为核心目标,针对现有方法无法兼顾低拷贝与小长度核酸检测的问题,构建了O-FISH技术体系,并通过HIV-1病毒模型验证其灵敏度与特异性,进一步拓展至miRNA检测与核酸结构动态分析,形成“方法构建→模型验证→功能拓展”的完整研究逻辑。
3.1 O-FISH技术体系构建与原理验证
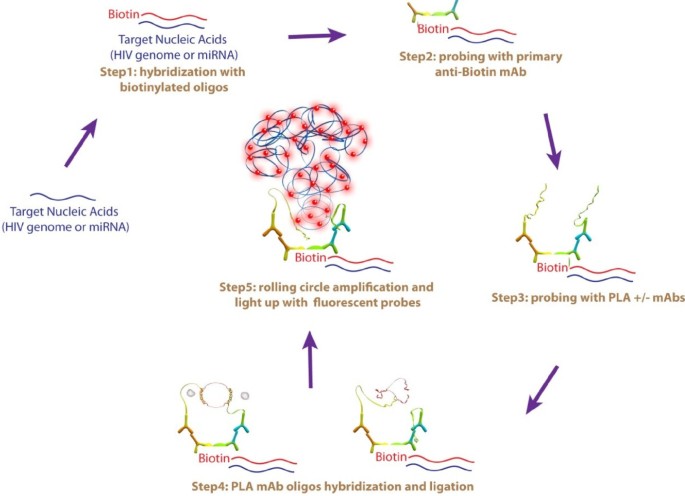
实验目的是改造邻近连接分析技术,使其适配核酸原位检测需求,建立一套高灵敏的单探针核酸可视化方法。方法细节:首先将生物素标记的19-26nt寡核苷酸探针与细胞内靶标核酸杂交,随后结合抗生物素单克隆抗体,再利用PLA探针识别抗体的IgG结构域,通过寡核苷酸连接形成环状DNA,经滚环扩增实现信号放大(约200倍),最终用荧光标记探针检测扩增产物。结果解读:成功构建了完整的O-FISH技术流程,信号放大策略有效提升了单探针的检测灵敏度,可实现单分子核酸的可视化(对应图1)。实验所用关键产品:Sigma-Aldrich的抗生物素单克隆抗体、Olink Bioscience的Duolink II抗小鼠PLA探针及检测试剂盒。
3.2 HIV-1低拷贝核酸检测的灵敏度与特异性验证
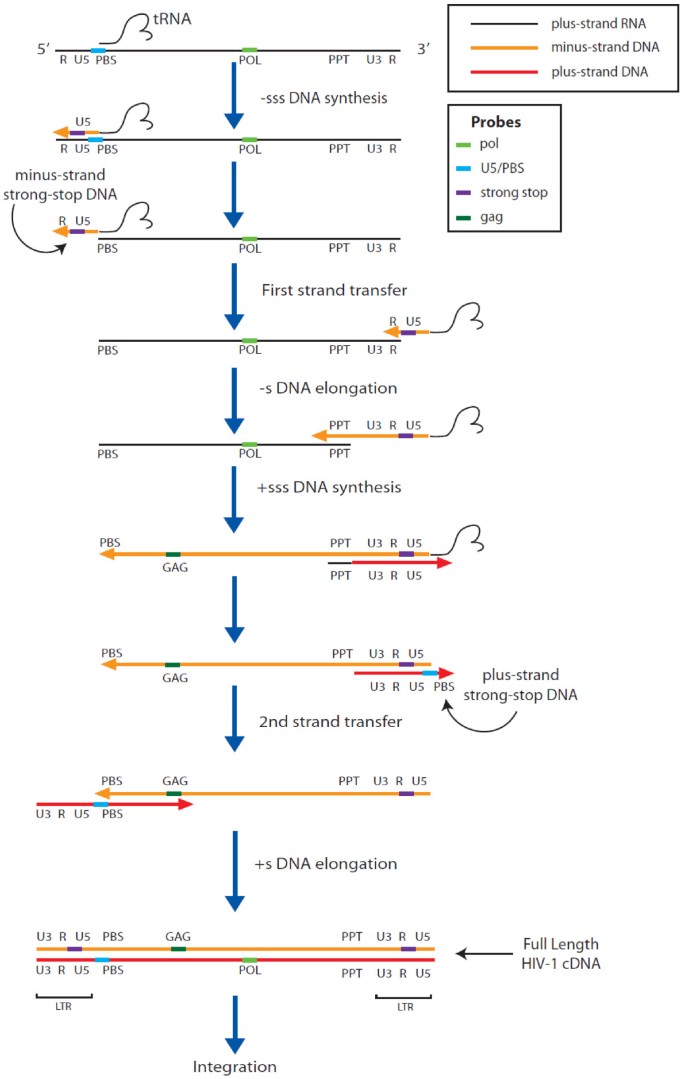
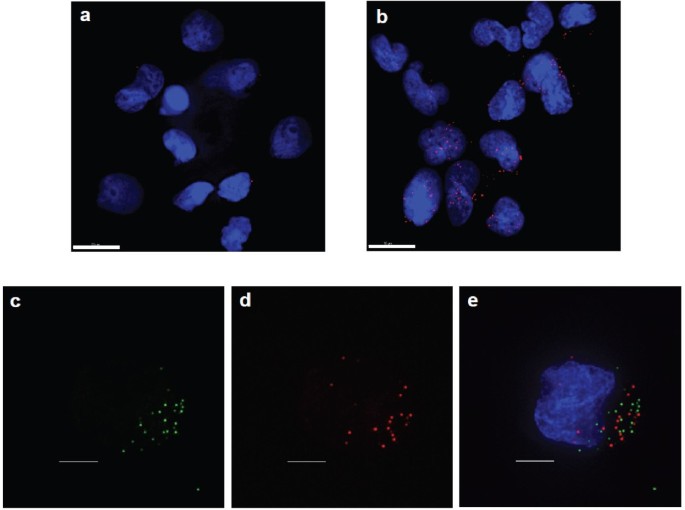
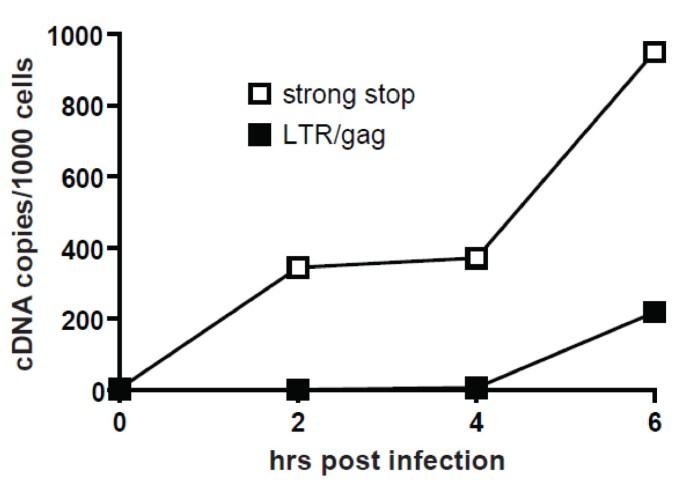
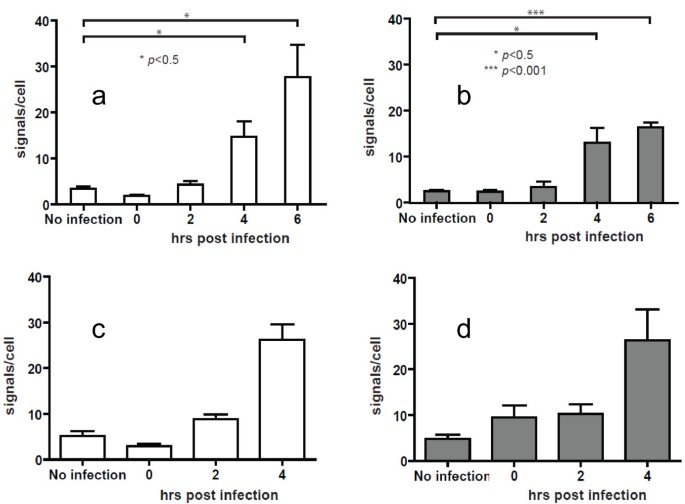
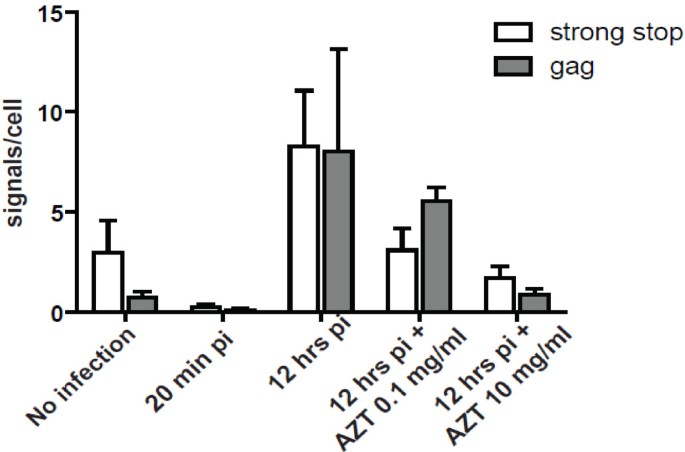
实验目的是验证O-FISH技术对低拷贝核酸的检测能力,利用HIV-1病毒颗粒含2拷贝RNA的特性作为参考模型。方法细节:用HIV-1感染MT-2、Jurkat淋巴细胞,分别针对HIV-1 pol区RNA、早期strong stop cDNA、中期gag cDNA设计26nt生物素探针,进行O-FISH检测;同时采用实时定量PCR(qPCR)检测cDNA水平,并用逆转录抑制剂齐多夫定(AZT)处理验证信号特异性;设置未感染细胞作为阴性对照(对应图2-6)。结果解读:感染细胞中可检测到特异性O-FISH信号,与未感染对照组的背景信号差异显著(文献未明确提供该数据,基于图表趋势推测);qPCR结果显示,O-FISH信号随cDNA合成进程同步增加,AZT处理后信号呈剂量依赖性降低,证明方法特异性良好;进一步通过双色病毒颗粒感染实验,确认信号来自独立的病毒RNA基因组,提示O-FISH可检测低至1-2拷贝的核酸分子。实验所用关键产品:bioMèrieux的Vironostika HIV-1抗原(p24 CA)MicroELISA试剂盒、Sigma-Aldrich的Benzonase核酸酶、Invitrogen的细胞培养基。
3.3 HIV-1 RNA结构动态的原位分析
实验目的是探索O-FISH技术在核酸结构与构象动态研究中的应用潜力,基于HIV-1 RNA在复制周期中存在结构重排的假说进行验证。方法细节:针对HIV-1 RNA 5’非翻译区(UTR)的U5/引物结合位点(PBS)序列设计24nt探针,检测感染后0、2、4小时细胞内的O-FISH信号变化,分析探针结合位点的可及性(对应图7)。结果解读:感染后2小时细胞内的O-FISH信号显著高于0和4小时,提示该时间段内HIV-1 RNA的U5/PBS区域处于暴露状态,而0和4小时因tRNA结合或RNaseH降解导致位点被遮蔽;这一结果为HIV-1 RNA的结构重排假说提供了原位实验证据,证明O-FISH可用于分析核酸构象的动态变化。文献未提及具体实验产品,领域常规使用核酸探针合成服务、共聚焦荧光显微镜成像系统。

3.4 miRNA小核酸的原位检测验证
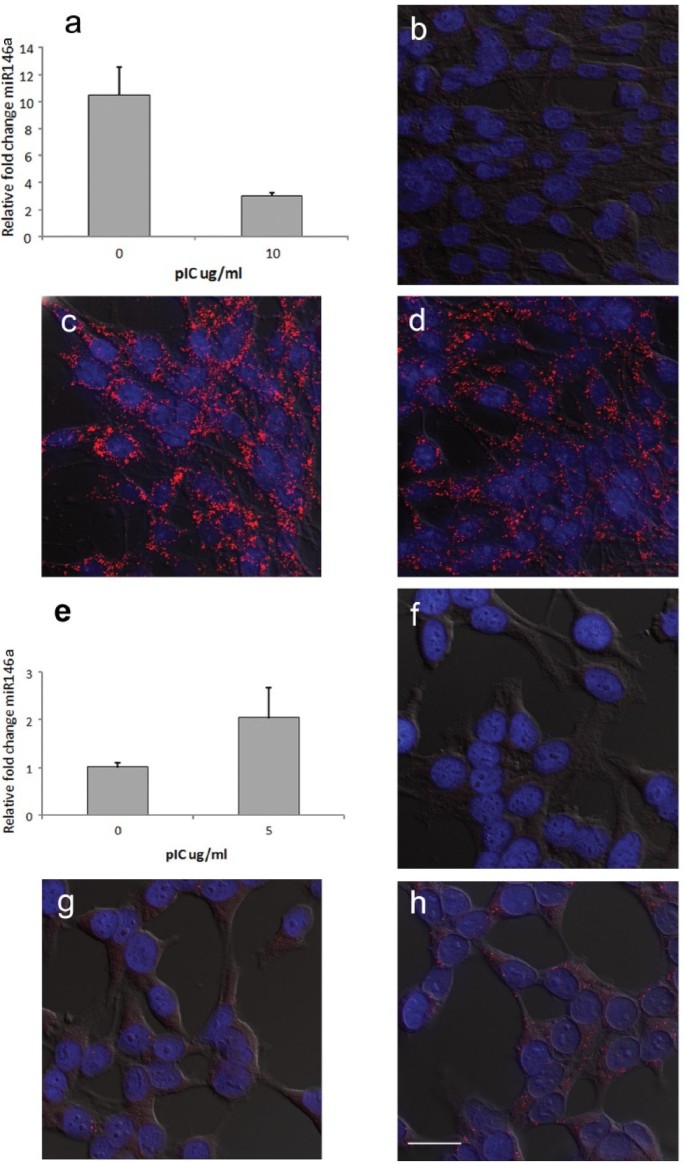
实验目的是验证O-FISH技术对小长度核酸(如miRNA,约20nt)的检测能力,选择miR146a作为靶标,其表达与I型干扰素调控相关。方法细节:用19nt的生物素标记探针检测鸡DF1成纤维细胞和人HeLa细胞中miR146a的表达,采用聚肌苷酸-聚胞苷酸(pIC)处理细胞以调控miR146a水平,同时用qRT-PCR进行定量验证,设置无探针的阴性对照(对应图8)。结果解读:O-FISH检测的miR146a信号变化与qRT-PCR结果完全一致:pIC处理后DF1细胞中miR146a表达下调,HeLa细胞中表达上调;无探针对照组仅检测到极低背景信号,证明O-FISH可特异性检测长度约20nt的miRNA分子。实验所用关键产品:Sigma-Aldrich的Tri-reagent RNA提取试剂、Invitrogen的Lipofectamine 2000转染试剂、Applied Biosystems的SYBR Green qPCR试剂。
4. Biomarker研究及发现成果解析
本研究虽未直接筛选新的疾病Biomarker,但验证了O-FISH技术作为Biomarker原位检测工具的核心能力,可实现低拷贝病毒核酸与功能型miRNA的高灵敏、特异性原位可视化,为Biomarker的细胞水平功能研究提供了技术支撑。
Biomarker定位:研究中涉及的两类靶标分别为HIV-1核酸(包括基因组RNA、strong stop cDNA、gag cDNA)与miR146a。其中HIV-1核酸作为HIV感染的核心Biomarker,筛选逻辑基于病毒复制周期的不同阶段,覆盖从入侵到cDNA合成的关键节点;miR146a作为免疫应答调控的功能Biomarker,筛选逻辑基于其已知的I型干扰素通路调控作用。
研究过程详述:HIV-1核酸的来源为HIV-1感染的MT-2、Jurkat淋巴细胞,采用O-FISH技术进行原位检测,通过未感染细胞对照、AZT抑制实验验证特异性,灵敏度可达1-2拷贝/细胞;miR146a的来源为鸡DF1成纤维细胞和人HeLa细胞,采用O-FISH与qRT-PCR联合验证,无探针对照显示背景信号极低,检测结果与qRT-PCR的一致性证明了方法的准确性(文献未明确提供ROC曲线、敏感性等数据)。
核心成果提炼:O-FISH技术可作为通用型Biomarker原位检测工具,实现低拷贝、小长度核酸Biomarker的可视化;对于HIV-1核酸,可在感染早期原位追踪病毒复制进程,为病毒感染机制研究提供高分辨率工具;对于miR146a,可原位观察其表达水平与亚细胞分布的变化,为免疫应答的细胞异质性研究提供新方法。推测:该技术可进一步拓展至其他疾病相关的低拷贝核酸Biomarker,如循环肿瘤DNA、罕见突变基因的原位检测,为疾病诊断与机制研究提供新的技术路径。
