1. 领域背景与文献引入
文献英文标题:Unveiling the role of CaMKII in retinal degeneration: from biological mechanism to therapeutic strategies;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:视网膜变性与神经退行性疾病。
视网膜变性是一类以感光细胞进行性死亡、视网膜神经元不可逆损伤为核心特征的致盲性疾病,涵盖糖尿病视网膜病变、年龄相关性黄斑变性、视网膜色素变性、青光眼视神经病变等多种亚型,是全球成人失明的主要病因之一。领域共识:当前临床治疗手段以激光光凝、玻璃体切割等侵入性手术为主,缺乏安全有效的靶向分子疗法,且视网膜神经元再生能力有限,疾病进展一旦进入晚期则难以逆转。Ca²⁺/钙调蛋白依赖的蛋白激酶II(CaMKII)作为细胞内关键的钙信号传感器,在阿尔茨海默病等神经退行性疾病中已被证实参与病理过程,但在视网膜变性中的具体作用机制、靶向治疗的可行性仍存在大量研究空白。这篇综述系统整合了近年来CaMKII在视网膜变性中的分子机制、调控通路及治疗策略研究进展,旨在为该领域的基础研究与临床转化提供全面的参考框架。
2. 文献综述解析
作者以“CaMKII的分子基础-视网膜细胞功能-疾病病理机制-治疗策略”为逻辑主线,对现有研究进行分层梳理,明确了CaMKII在视网膜变性中的双重作用及靶向治疗的潜力与挑战。
现有研究的关键结论包括:CaMKII具有四个结构相似但功能不同的亚型,在视网膜不同细胞中呈特异性分布,通过调控血管生成、突触信号转导、细胞存活与凋亡等多种通路参与视网膜变性的病理过程;现有技术方法多基于细胞模型、基因编辑动物模型开展机制研究,能清晰解析分子通路的上下游关系,但局限性在于缺乏大样本临床研究数据支撑,且CaMKII在不同疾病阶段、不同细胞类型中的双重作用(保护/损伤)机制尚未完全阐明,不同亚型的特异性下游靶点仍不明确。
这篇综述的创新价值在于,首次全面系统地整合了CaMKII在视网膜变性领域的全链条研究进展,从分子结构到临床治疗形成完整的知识体系,明确了未来研究的核心方向:一是解析CaMKII不同亚型在视网膜变性中的特异性作用机制,二是开发亚型特异性的CaMKII抑制剂,三是推动临床前研究向临床转化,为视网膜变性的靶向治疗提供新的范式。
3. 研究思路总结与详细解析
综述整体遵循“分子基础-细胞功能-疾病机制-治疗策略”的闭环逻辑,先明确CaMKII的结构与调控机制,再阐述其在视网膜不同细胞中的功能,接着解析在各类视网膜变性疾病中的病理作用,最后总结靶向CaMKII的治疗策略,为该领域的研究提供了清晰的路线图。
3.1 CaMKII的分子结构与调控机制解析
实验目的:明确CaMKII的分子结构特征、激活与失活的调控机制,为后续解析其在视网膜中的功能奠定基础。
方法细节:通过整合结构生物学、分子生物学领域的现有研究数据,系统分析CaMKII四个亚型(α、β、γ、δ)的结构域组成,包括氨基端催化域、中央自调控域、羧基端关联域及可变剪接区域,同时梳理翻译后修饰(磷酸化、氧化、O-糖基化、S-亚硝基化)对其活性的调控机制。
结果解读:CaMKII以12或14个亚基组成的全酶形式发挥功能,自磷酸化(T286位点)可使其在无Ca²⁺/钙调蛋白的情况下保持持续激活状态,氧化修饰(M281/282位点)也可诱导其自主激活;蛋白磷酸酶2A(PP2A)、蛋白磷酸酶1(PP1)等可通过去磷酸化作用抑制CaMKII活性;不同亚型的可变剪接可影响其亚细胞定位与底物特异性。
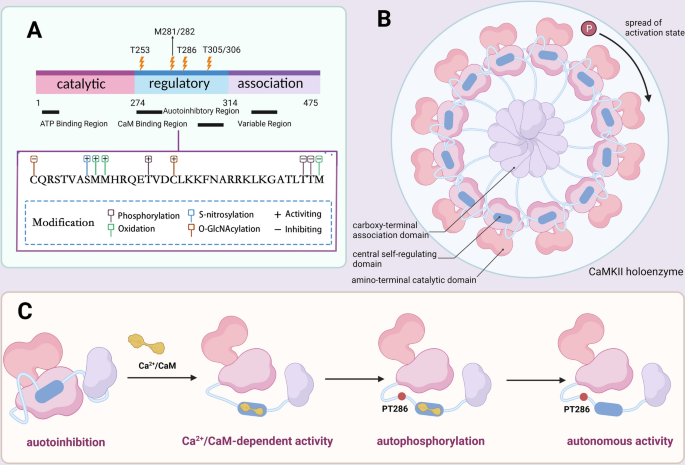
产品关联:文献未提及具体实验产品,领域常规使用蛋白结构分析软件、磷酸化特异性抗体、蛋白激酶活性检测试剂盒等。
3.2 CaMKII在视网膜细胞中的功能解析
实验目的:阐明CaMKII不同亚型在视网膜不同细胞中的分布特征与具体功能。
方法细节:整合免疫组化(IHC)、基因敲除/过表达动物模型、细胞培养等多维度研究数据,分析CaMKII在视网膜神经节细胞、无长突细胞、内皮细胞、视网膜色素上皮细胞中的功能差异。
结果解读:CaMKIIα与β亚型主要表达于视网膜神经节细胞和无长突细胞,参与调控突触信号转导与神经节细胞的存活;CaMKIIγ与δ亚型主要表达于视网膜内皮细胞,通过调控血管内皮生长因子(VEGF)、白细胞介素6(IL-6)等通路促进视网膜血管生成;在视网膜色素上皮细胞中,CaMKII具有双重作用,一方面可通过激活腺苷酸活化蛋白激酶(AMPK)改善线粒体功能、抑制氧化应激,发挥细胞保护作用,另一方面可通过磷酸化动力相关蛋白1(Drp1)诱导线粒体裂变与细胞凋亡,加重细胞损伤。
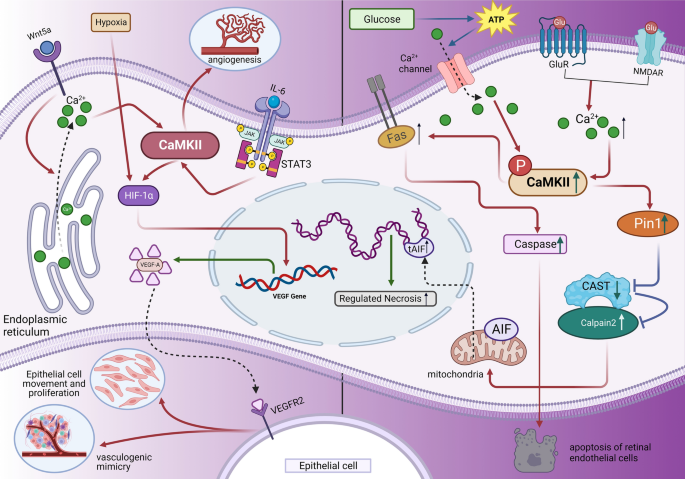
产品关联:文献未提及具体实验产品,领域常规使用免疫组化试剂盒、CRISPR-Cas9基因编辑工具、细胞凋亡检测试剂盒等。
3.3 CaMKII在视网膜变性疾病中的作用机制解析
实验目的:解析CaMKII在各类视网膜变性疾病中的病理作用与调控通路。
方法细节:整合糖尿病视网膜病变、青光眼、视网膜色素变性、年龄相关性黄斑变性等疾病的细胞模型、动物模型及临床前研究数据,分层分析CaMKII在不同疾病中的特异性作用机制。
结果解读:在糖尿病视网膜病变中,CaMKII通过激活核因子κB(NF-κB)通路诱导炎症反应,通过诱导诱导型一氧化氮合酶(iNOS)表达、激活Fas死亡受体通路促进细胞凋亡,同时调控血管内皮细胞功能导致血视网膜屏障破坏;在青光眼中,CaMKII通过环磷酸腺苷激活的交换蛋白1(Epac1)通路诱导视网膜神经节细胞死亡,同时也可通过激活环磷酸腺苷反应元件结合蛋白(CREB)促进神经节细胞存活,呈现双重作用;在视网膜色素变性中,CaMKII过度激活导致phosducin持续磷酸化,影响光信号转导通路,加重感光细胞损伤;在年龄相关性黄斑变性中,CaMKII调控视黄酸信号通路,参与视网膜色素上皮细胞的功能异常与氧化应激损伤。
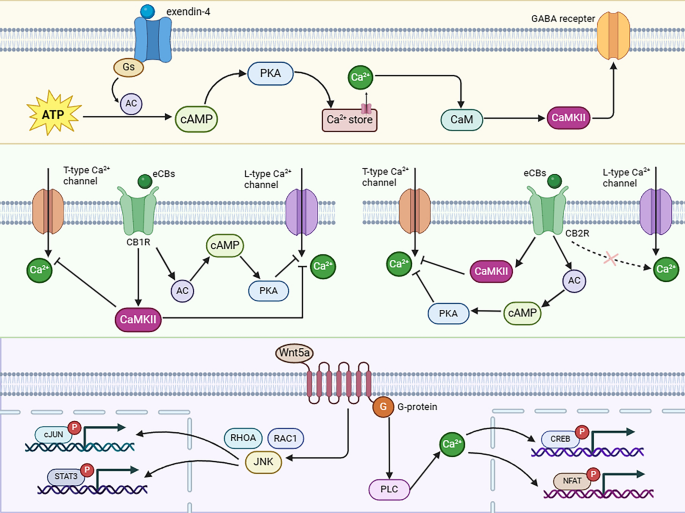
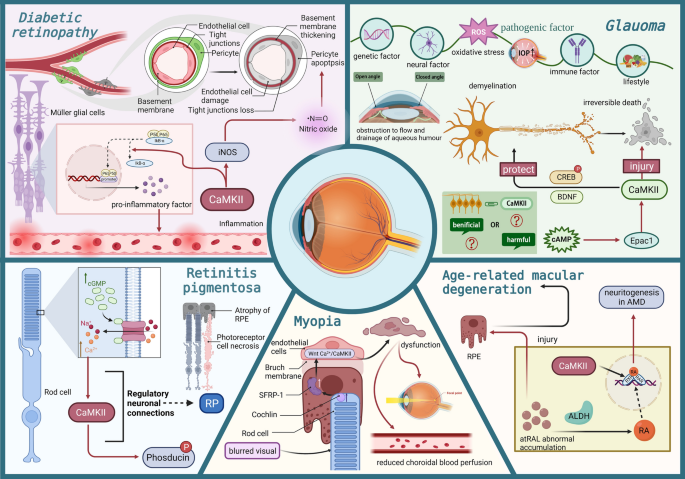
产品关联:文献未提及具体实验产品,领域常规使用疾病动物模型(如链脲佐菌素诱导糖尿病小鼠、青光眼小鼠模型)、炎症因子检测试剂盒、蛋白印迹(WB)试剂盒等。
3.4 靶向CaMKII的治疗策略解析
实验目的:总结现有靶向CaMKII的治疗药物与策略的作用机制、优势与局限性。
方法细节:综述小分子抑制剂、多肽抑制剂、植物来源抑制剂三类靶向CaMKII的治疗手段,分析其临床前研究数据与转化潜力。
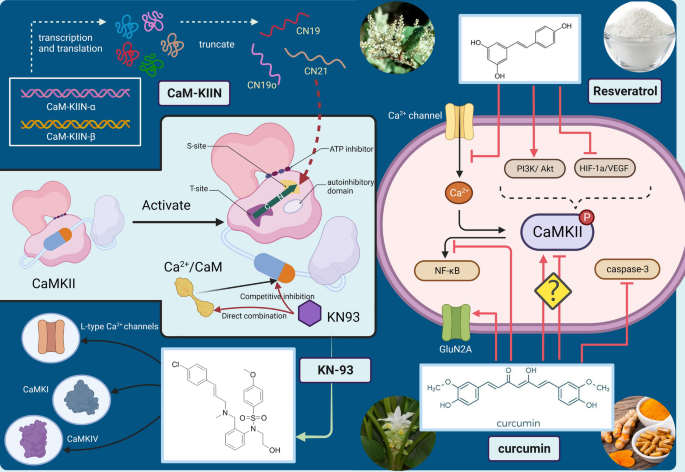
结果解读:KN-93作为经典的小分子CaMKII抑制剂,通过竞争Ca²⁺/钙调蛋白的结合位点抑制CaMKII活性,但存在特异性差的问题,可同时抑制其他激酶与离子通道;CaM-KIIN是天然的特异性CaMKII抑制剂,通过结合CaMKII的T-site阻断底物与催化域的结合,具有高特异性,但生物利用度低,难以穿透血视网膜屏障;白藜芦醇、姜黄素等植物来源抑制剂通过抑制CaMKII活性发挥神经保护作用,具有安全性高的优势,但作用靶点广泛,特异性不足。目前所有靶向CaMKII的治疗策略均处于临床前研究阶段,缺乏临床研究数据支撑。
产品关联:文献未提及具体实验产品,领域常规使用激酶抑制剂筛选平台、体内药物递送系统等。
4. Biomarker研究及发现成果
综述中虽未开展专门的Biomarker筛选与验证研究,但基于现有研究数据,提出了CaMKII相关分子作为视网膜变性潜在Biomarker的可能性,为后续Biomarker研究提供了方向。
Biomarker定位:CaMKII的磷酸化水平、氧化水平及不同亚型的表达水平可作为视网膜变性的潜在Biomarker,其筛选逻辑为“动物模型病理关联-细胞机制验证-临床样本验证”,目前已完成前两个阶段,临床样本验证仍需开展。
研究过程详述:在糖尿病视网膜病变小鼠模型中,CaMKII的磷酸化水平与iNOS表达水平同步升高,与视网膜血管病变程度呈正相关;在青光眼小鼠模型中,视网膜神经节细胞中CaMKII的磷酸化水平显著升高,与神经节细胞死亡数量呈正相关;在视网膜色素变性小鼠模型中,CaMKII的过度激活导致phosducin持续磷酸化,可作为感光细胞损伤的潜在指标。但目前这些数据均来自动物模型,缺乏临床样本的特异性与敏感性验证,无ROC曲线、样本量等具体数据(文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼:CaMKII相关分子作为视网膜变性的潜在Biomarker,其功能关联在于可反映疾病的病理进展程度,创新性在于首次提出CaMKII的亚型特异性表达与磷酸化水平可作为不同视网膜变性疾病的特异性Biomarker,但目前仍处于研究阶段,需进一步开展大样本临床研究验证其临床价值。
