1. 领域背景与文献引入
文献英文标题:A gene-expression program reflecting the innate immune response of cultured intestinal epithelial cells to infection by Listeria monocytogenes;发表期刊:Genome Biology;影响因子:未公开;研究领域:肠道病原菌-宿主相互作用、固有免疫应答
肠道上皮作为宿主抵御肠道病原菌的第一道物理与免疫防线,其对病原菌的识别及应答机制是肠道感染领域的核心研究方向之一。单核细胞增生李斯特菌是一种食源性胞内致病菌,可通过肠道上皮入侵宿主,尤其对新生儿、孕妇及免疫低下人群具有高致病性,其感染依赖于一系列毒力因子(如内化素InlA/InlB、李斯特溶素O LLO、肌动蛋白聚合蛋白ActA)介导的黏附、入侵、胞内逃逸及细胞间扩散。领域共识:此前的研究多聚焦于巨噬细胞、内皮细胞等免疫细胞对李斯特菌的应答机制,证实其毒力因子可激活核因子κB(NFκB)通路引发炎症反应,但肠道上皮细胞作为初始接触病原菌的细胞,其全局转录组应答特征及对病原菌不同毒力阶段的识别能力尚不明确,缺乏系统的转录组学研究数据。本文旨在通过基因芯片技术,分析人肠道上皮细胞系Caco-2对野生型及两种毒力突变体李斯特菌的时间序列转录响应,填补这一研究空白,为肠道上皮固有免疫识别机制提供新的实验依据。
2. 文献综述解析
作者按宿主细胞类型(巨噬细胞、内皮细胞、肠道上皮细胞)与研究技术(传统分子生物学、全基因组转录组学)对现有研究进行分类评述,系统梳理了李斯特菌感染与宿主免疫应答的研究进展。现有研究已证实,李斯特菌的毒力因子如LLO可激活巨噬细胞、内皮细胞的NFκB通路,诱导趋化因子、细胞因子的表达,为病原菌的清除提供信号;基因芯片技术的应用实现了宿主-病原菌相互作用的全局转录组分析,可同时检测数千个基因的表达变化,但其在肠道上皮细胞研究中的应用较为有限。现有研究的局限性在于,多关注免疫细胞的应答,对肠道上皮细胞的研究多集中于单一毒力因子的作用,缺乏对不同毒力阶段病原菌的系统比较,尤其是针对病原菌胞质内运动阶段的宿主转录响应研究较为匮乏。
本文的创新价值在于,首次利用覆盖约一半人类基因组的基因芯片,系统分析肠道上皮细胞对野生型及actA、prfA突变体李斯特菌的时间序列转录响应,通过对比不同毒力菌株的宿主应答差异,明确肠道上皮细胞的固有免疫应答核心通路,且未发现针对病原菌胞质运动或毒力因子的特异性转录应答,为肠道上皮细胞的非特异性固有免疫识别机制提供了直接实验证据,弥补了现有研究在细胞类型覆盖与毒力阶段分析上的不足。
3. 研究思路总结与详细解析
本文的研究目标是解析人肠道上皮细胞对单核细胞增生李斯特菌感染的转录组应答特征,核心科学问题是肠道上皮细胞是否能通过转录组响应区分病原菌的不同毒力阶段,技术路线遵循“细胞感染模型构建→转录组芯片全局分析→突变体应答差异比较→蛋白水平验证”的闭环逻辑,通过多维度实验验证肠道上皮细胞的固有免疫应答机制。
3.1 细胞感染模型构建与形态学验证
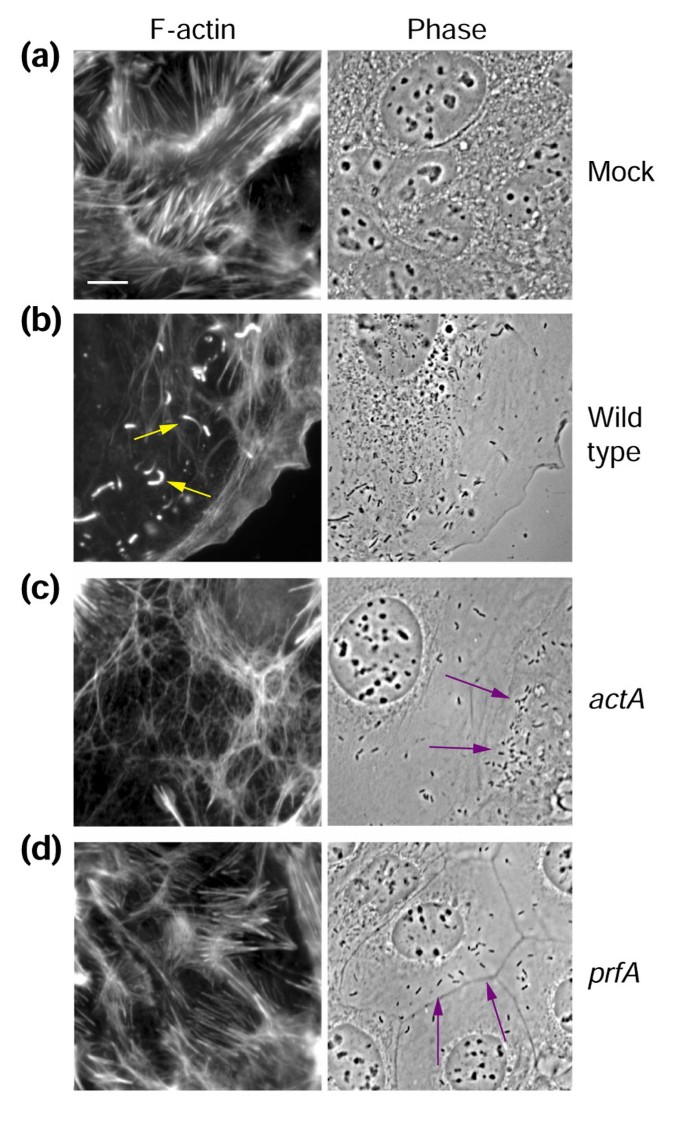
实验目的是建立标准化的肠道上皮细胞感染模型,明确不同毒力李斯特菌在细胞内的行为差异。方法细节为采用人结肠腺癌上皮细胞系Caco-2,分别感染野生型单核细胞增生李斯特菌10403S、actA基因缺失突变体(DP-L1942,丧失肌动蛋白依赖的胞质运动能力)、prfA基因插入突变体(DP-L1075,无法表达所有毒力基因),感染复数约为20,设置0、30、60、120、240、480分钟共6个时间点;在各时间点收集细胞,用3.5%甲醛固定,罗丹明标记的鬼笔环肽染色肌动蛋白骨架,通过荧光显微镜观察细胞内细菌的形态与分布。结果解读显示,野生型细菌在感染后4小时可在胞质内形成肌动蛋白彗星尾结构(图1b),actA突变体无法形成彗星尾,在胞内形成菌落(图1c),prfA突变体无法逃离内体,以单个形式存在(图1d),验证了不同菌株的毒力表型差异。文献未提及具体实验产品,领域常规使用细胞培养培养基、荧光染色试剂、倒置荧光显微镜等。
3.2 转录组芯片分析与数据标准化处理
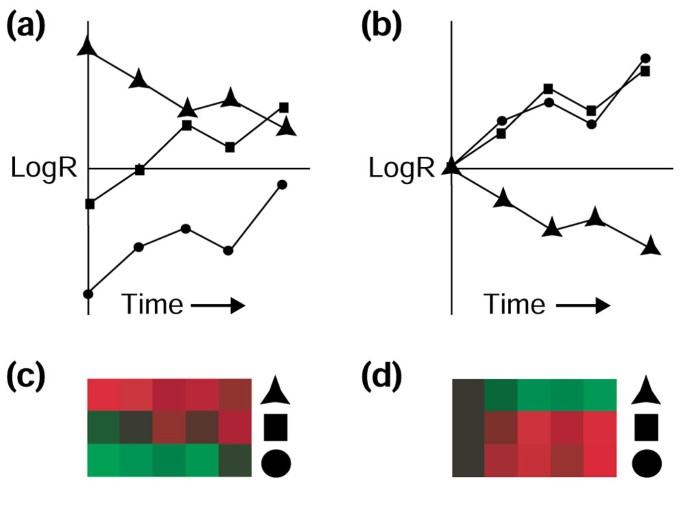
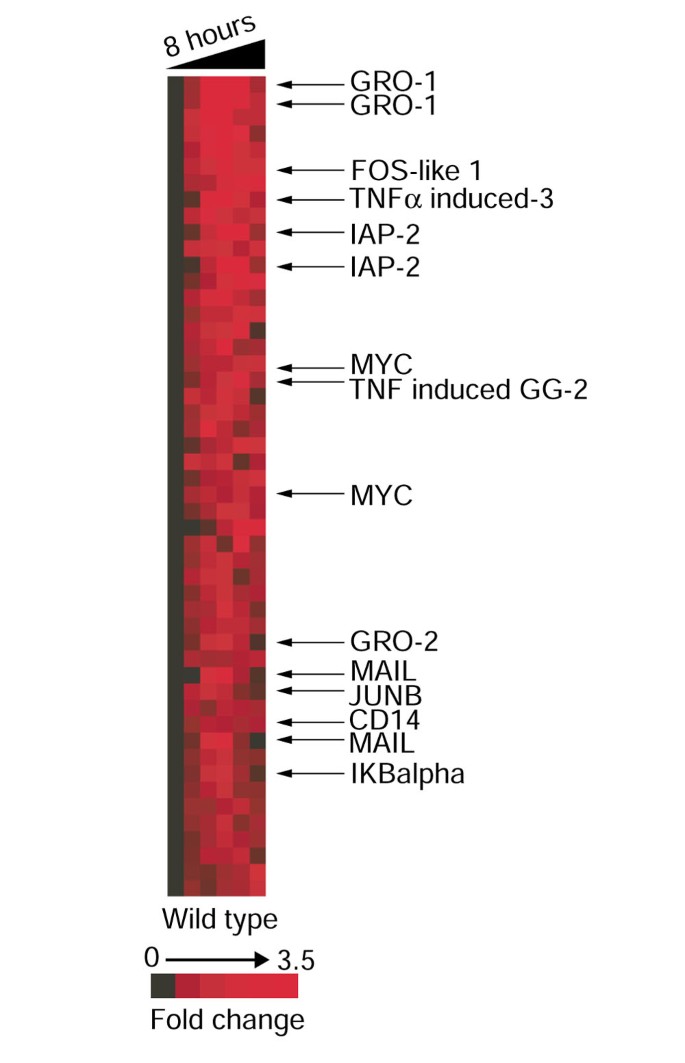
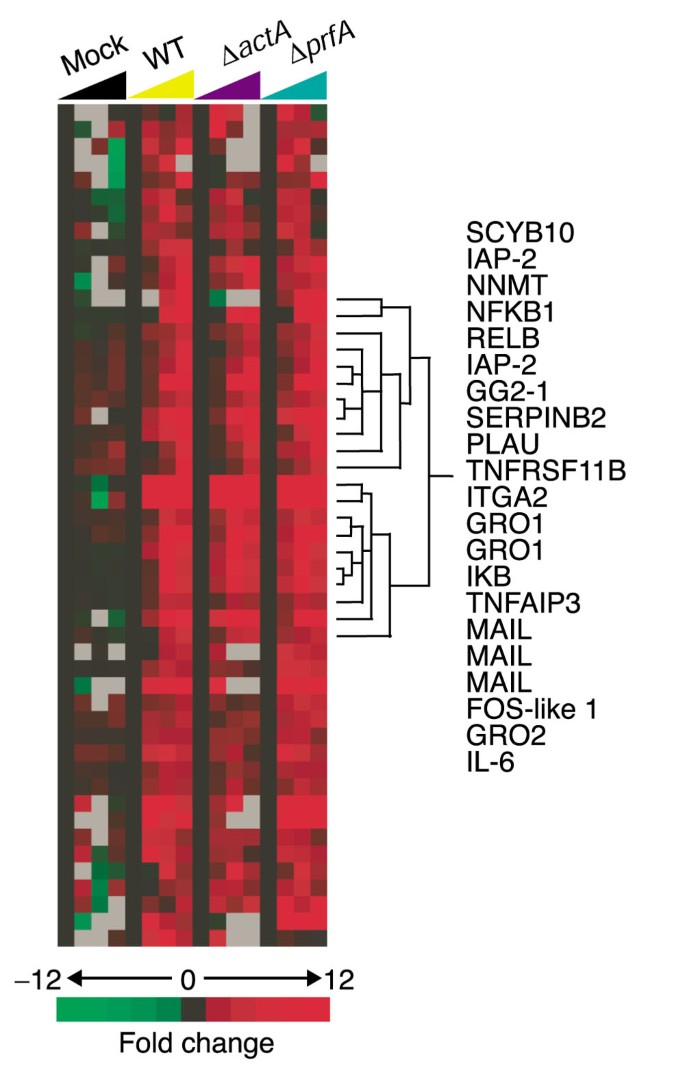
实验目的是全局分析肠道上皮细胞感染后的基因表达动态变化。方法细节为提取各时间点细胞的mRNA,通过反转录合成Cy-5标记的实验样本cDNA,同时以10种不同人类细胞系的混合RNA作为参考样本,合成Cy-3标记的cDNA;将两种标记的cDNA混合后,与包含22594个人类转录本的基因芯片杂交,扫描芯片获取荧光信号,采用时间零点转换法(即各时间点的基因表达水平相对于0时间点的变化)进行数据标准化,通过聚类分析和秩平均法筛选差异表达基因。结果解读显示,感染后大量基因被显著诱导,前50个高诱导基因中20%为核因子κB通路相关基因,包括即刻早期反应基因Fos、Jun,凋亡抑制因子IAP-2,趋化因子Gro-1等(图3);时间序列分析显示基因表达变化呈现动态趋势,核因子κB通路基因在感染后1-4小时持续上调(图2)。文献未提及具体实验产品,领域常规使用基因芯片、荧光标记试剂盒、芯片扫描系统等。
3.3 不同毒力菌株感染的转录响应比较
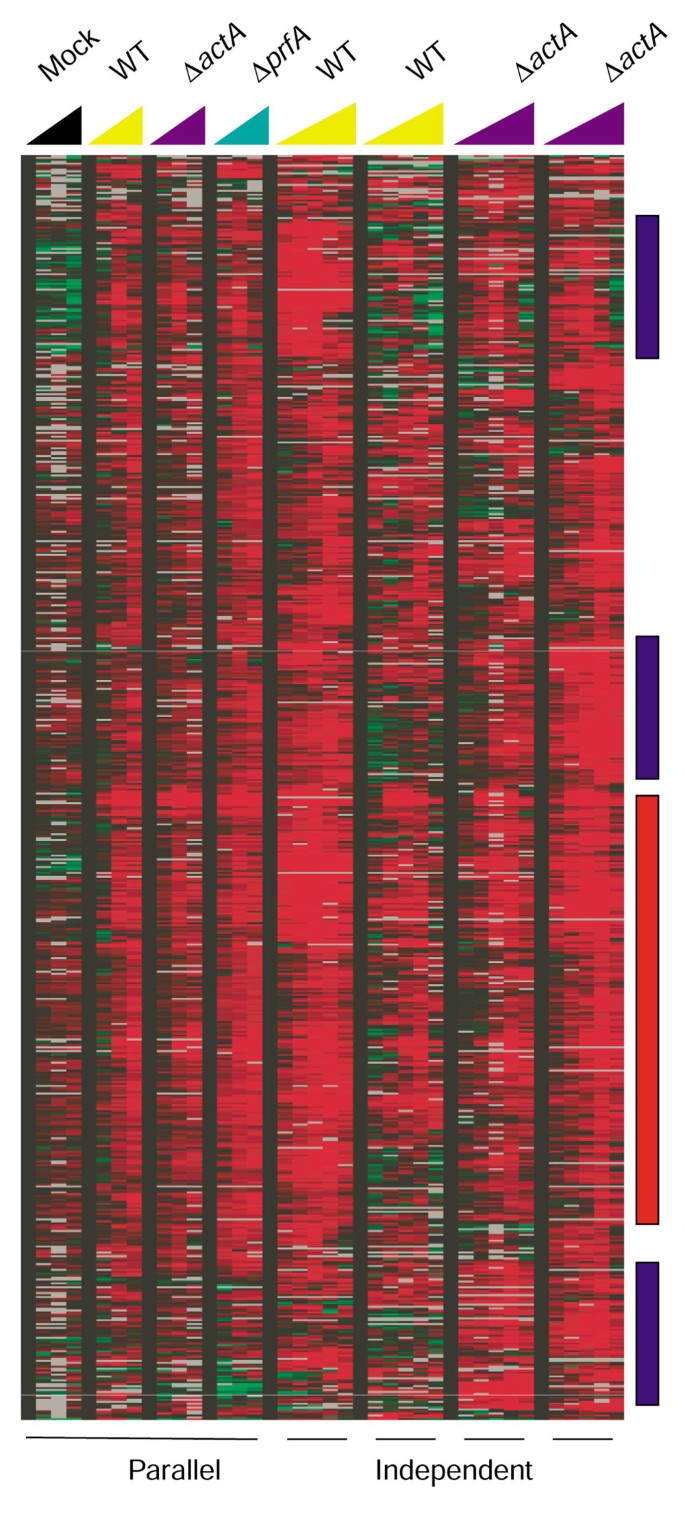
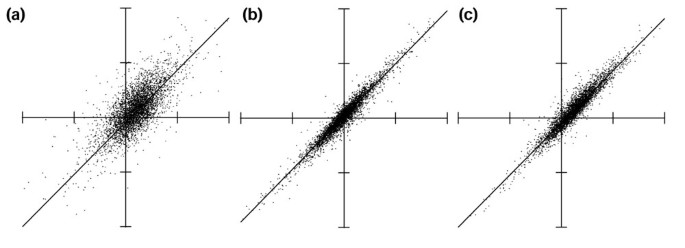
实验目的是验证肠道上皮细胞是否存在针对病原菌特定毒力阶段的特异性转录应答。方法细节为同步进行野生型、actA突变体、prfA突变体的感染实验,设置0、60、120、240分钟时间点,采用显著性分析(SAM)和Excel过滤法,比较三组感染的基因表达差异;同时通过重复实验分析数据变异来源,比较不同批次细胞的转录组相关性。结果解读显示,野生型与两种突变体感染后的转录组响应高度相似,未发现显著差异的基因(图4、5);数据变异主要来源于细胞培养的批次差异,而非芯片技术本身(图5显示同批次细胞的相关性系数为0.94,不同批次为0.74);聚类分析显示核因子κB通路相关基因形成单一聚类,占前50个高诱导基因的40%(图6),进一步证实该通路是主导应答通路。文献未提及具体实验产品,领域常规使用生物信息学分析软件(如SAM、TreeView)等。
3.4 蛋白水平验证与细胞极化状态影响分析
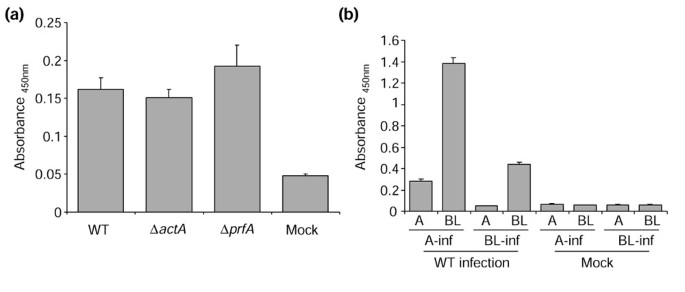
实验目的是验证转录组结果的蛋白水平变化,以及细胞分化状态对免疫应答的影响。方法细节为采用酶联免疫吸附实验(ELISA)检测趋化因子Gro-1的分泌水平,分别检测未极化的Caco-2细胞感染野生型、actA、prfA突变体后的上清液,以及极化的Caco-2细胞(培养于Transwell小室,形成紧密连接)顶端或基底侧感染后的上清液。结果解读显示,未极化细胞中三种感染的Gro-1分泌水平无显著差异(图9a);极化细胞的顶端和基底侧接触细菌后均能分泌Gro-1,且大部分从基底侧分泌(图9b),提示肠道上皮细胞的固有免疫应答不依赖于细胞极化状态,且对病原菌的识别主要基于表面相互作用。文献未提及具体实验产品,领域常规使用ELISA试剂盒、Transwell小室等。
4. Biomarker研究及发现成果解析
本文鉴定的Biomarker为核因子κB通路相关基因(如Gro-1、NFκB1、RelB等),作为肠道上皮细胞对单核细胞增生李斯特菌感染的固有免疫应答标志物,筛选逻辑为通过全基因组转录组分析发现这些基因在感染后显著上调,验证逻辑为结合基因芯片数据与ELISA蛋白检测结果,确认其表达变化的一致性。
该Biomarker的来源为Caco-2细胞感染后的转录组及分泌蛋白,验证方法包括基因芯片技术(全局分析转录水平)和ELISA(检测蛋白分泌水平),特异性与敏感性方面,核因子κB通路基因在感染后1小时即显著上调,Gro-1的分泌水平在感染后4小时达到高峰(文献未明确具体数值,基于图表趋势推测),且对野生型及毒力突变体的响应无差异,提示其为广谱的病原菌响应标志物。
核心成果提炼:首次明确肠道上皮细胞对单核细胞增生李斯特菌的转录应答主要由核因子κB通路介导,且该应答不依赖于病原菌的胞质运动能力或毒力因子表达,说明肠道上皮细胞的初始识别主要基于细菌表面成分与细胞表面受体的相互作用,而非胞内信号;该Biomarker可用于评估肠道上皮细胞的固有免疫激活状态,为肠道感染的早期诊断和治疗靶点筛选提供理论依据,实验重复n=3,数据具有可靠性,文献未明确提供具体统计学P值。推测:该应答机制可能是肠道上皮细胞应对大量共生菌与病原菌的一种适应性策略,通过非特异性的固有免疫应答快速启动防御反应,为后续特异性免疫应答的激活争取时间。
