1. 领域背景与文献引入
文献英文标题:Site-specific programming of the host epithelial transcriptome by the gut microbiota;发表期刊:Genome Biology;影响因子:未公开;研究领域:肠道微生物与宿主肠道上皮转录组调控
领域共识:肠道微生物组研究的关键节点始于2005年启动的人类微生物组计划(HMP),2012年HMP发布的成果明确了肠道微生物在宿主代谢、免疫发育、组织稳态中的核心作用,其编码的基因数量远超人类自身,为宿主提供了互补的生理功能。当前研究热点聚焦于肠道微生物与宿主上皮细胞的互作机制,尤其是微生物对宿主转录组的调控,但此前的研究多采用完整肠道组织或未分馏的上皮细胞样本,无法区分肠道上皮不同亚群(如隐窝的干细胞/潘氏细胞与绒毛顶端的分化上皮细胞)以及回肠、结肠区域的特异性响应,导致微生物对宿主上皮调控的位点特异性机制尚未明确,这一空白限制了对肠道微生态失衡相关疾病(如炎症性肠病、肥胖)的分子机制解析。
本文针对这一核心问题,采用激光捕获显微切割(LCM)技术分离回肠和结肠的隐窝、顶端上皮细胞亚群,结合无菌(GF)与常规饲养(CR)小鼠模型,以及微生物定植的时间动力学分析,系统解析肠道微生物对宿主上皮转录组的位点特异性调控网络,为揭示肠道微生物-宿主互作的细胞特异性机制提供新的研究范式。
2. 文献综述解析
作者对领域内现有研究按实验材料类型分为两类,一类是基于完整肠道组织的微生物-宿主互作研究,另一类是基于未分馏上皮细胞的转录组分析,通过对比两类研究的局限性,凸显本文采用激光捕获显微切割分馏上皮细胞的创新性。
现有研究的关键结论包括:肠道微生物可调控宿主免疫、细胞增殖与代谢相关基因的表达,参与肠道上皮发育与稳态维持;技术方法优势在于系统分析了微生物对宿主整体转录组的影响,明确了微生物在宿主生理中的核心作用;但局限性也较为显著,完整组织样本包含免疫细胞、间质细胞等多种细胞类型,无法区分上皮细胞的特异性响应,未分馏上皮细胞则掩盖了隐窝-绒毛轴的细胞亚群差异,同时缺乏对微生物定植后宿主转录组响应的时间动力学分析,导致无法揭示位点特异性的调控机制。
本文的创新价值在于,首次将激光捕获显微切割技术应用于肠道微生物-宿主上皮互作研究,精准分离回肠和结肠的隐窝、顶端上皮细胞亚群,结合GF/CR小鼠模型与定植时间序列,解析了微生物对宿主上皮转录组的位点特异性调控,填补了现有研究无法区分上皮细胞亚群响应的空白,为深入理解肠道微生物的区域特异性调控机制提供了直接实验证据。
3. 研究思路总结与详细解析
本文的研究目标是揭示肠道微生物对宿主肠道上皮不同亚群(隐窝/顶端)、不同区域(回肠/结肠)转录组的位点特异性调控机制,核心科学问题是微生物如何通过不同转录调控网络影响不同上皮细胞亚群的基因表达与功能,技术路线遵循“模型构建→细胞分离→转录组分析→功能验证→机制解析”的闭环逻辑,通过多组学分析与功能实验验证,系统阐明微生物的位点特异性调控作用。
3.1 肠道上皮细胞组成分析
实验目的是验证肠道微生物对宿主肠道上皮细胞类型组成的影响,排除细胞组成差异对后续转录组分析的干扰。方法上,采用多通道免疫染色与自动玻片扫描分析技术,对GF和CR小鼠的回肠、近端结肠组织进行染色,检测上皮细胞类型(所有上皮细胞、杯状细胞、肠内分泌细胞、潘氏细胞)的丰度,样本量为GF组n=8,CR组n=9,采用双向方差分析进行统计学检验。结果显示,CR小鼠回肠中的潘氏细胞和杯状细胞丰度略高于GF小鼠(n=8/9,P<0.05或P<0.001),但整体上皮细胞组成仅存在微小差异,说明微生物对上皮细胞组成的影响有限,后续转录组差异主要源于基因表达调控而非细胞组成变化。
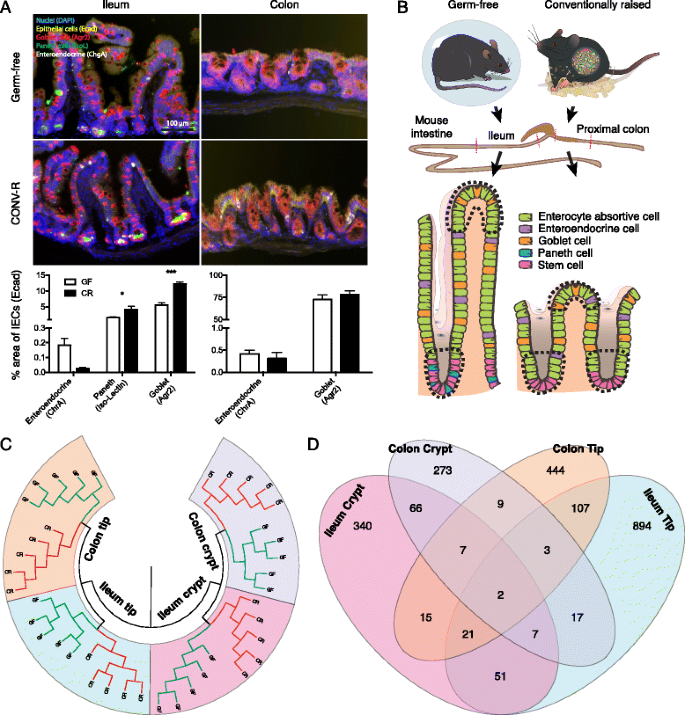
实验所用关键产品:Takara的E-cadherin抗体(货号M108)、Santa Cruz的Anterior Gradient 2抗体(货号sc54561)、ImmunoStar的Chromogranin A抗体(货号20086)、Sigma-Aldrich的Ulex europaeus凝集素-FITC(货号L9006)等。
3.2 激光捕获显微切割分离上皮细胞与转录组分析
实验目的是解析肠道微生物对不同上皮细胞亚群转录组的调控差异。方法上,采用激光捕获显微切割技术从GF和CR小鼠的回肠、结肠组织中分离隐窝和顶端上皮细胞,对每个亚群进行微阵列杂交(共40个样本),通过层次聚类分析样本差异,采用校正t检验筛选微生物调控的差异表达基因(P<0.001),并通过定量PCR(qPCR)验证代表性基因的表达。结果显示,层次聚类清晰区分了样本的上皮亚群(隐窝vs顶端)、组织区域(回肠vs结肠)和微生物状态(GF vs CR);共鉴定出2256个受微生物调控的基因,其中86%为位点特异性基因(回肠隐窝340个、回肠顶端894个、结肠隐窝273个、结肠顶端444个),qPCR验证了不同亚群中代表性基因的差异表达,如回肠顶端的免疫相关基因Pigr、结肠顶端的代谢相关基因等,证实了转录组分析的可靠性。
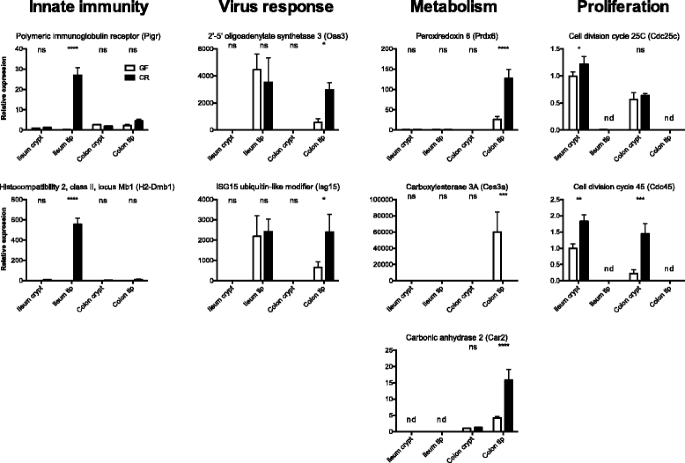
实验所用关键产品:Qiagen的RNeasy Micro Kit、Nugen的Ovation® Pico WTA System V2、Affymetrix的GeneChip Mouse Gene 2.0 ST Array、Bio-Rad的CFX96实时荧光定量PCR系统等。
3.3 功能富集与转录调控因子分析
实验目的是解析微生物调控的位点特异性基因的功能富集特征,以及对应的转录调控网络。方法上,采用基因本体(GO)分析对不同亚群的差异表达基因进行功能富集(P<10^-5,基因数>5),通过预测启动子区域的转录因子结合位点,并结合已发表的染色质免疫共沉淀测序(ChIP-seq)数据,筛选富集的转录调控因子。结果显示,功能富集具有显著的位点特异性:顶端上皮细胞主要富集免疫相关功能(抗原呈递、干扰素响应),其中回肠顶端富集T细胞调控功能,结肠顶端富集病毒响应功能;隐窝上皮细胞主要富集细胞周期与增殖相关功能,同时回肠顶端富集胆固醇/脂质代谢,结肠顶端富集谷胱甘肽氧化还原过程。转录调控因子分析显示,不同亚群的调控因子存在特异性,如回肠隐窝富集E2F1、MYC/MAX等细胞周期调控因子,回肠顶端富集NFkB、CEBPB等免疫与代谢调控因子,说明微生物通过不同调控网络调控不同上皮亚群的基因表达。
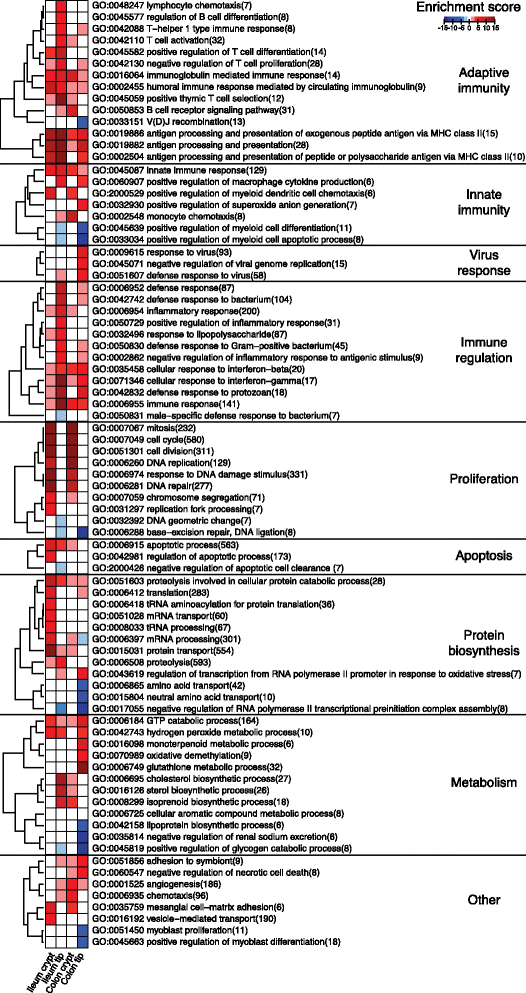
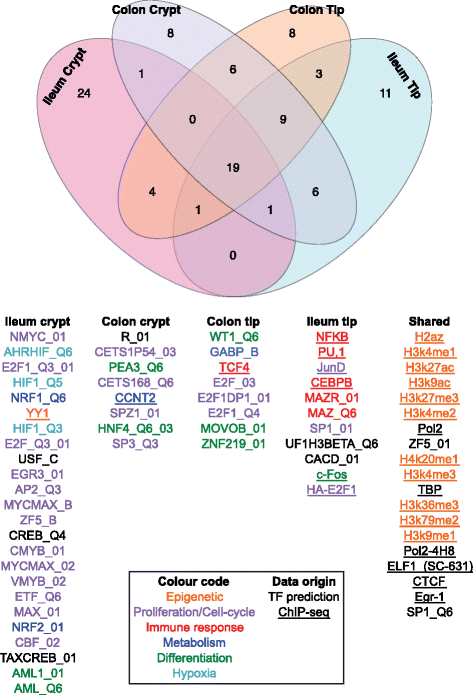
文献未提及具体转录因子预测的工具产品,领域常规使用Cscan、ECRbase等数据库进行转录因子结合位点分析。
3.4 微生物定植的时间动力学分析
实验目的是解析肠道微生物定植后,宿主上皮转录组响应的时间动力学特征,比较回肠与结肠的响应速度差异。方法上,对GF小鼠进行肠道微生物定植,在定植后0、1、3、5、7天采用激光捕获显微切割分离上皮细胞亚群,进行微阵列分析,通过层次聚类与基因表达聚类分析转录组的时间变化。结果显示,结肠上皮对微生物定植的响应速度显著快于回肠:结肠样本在定植后1-3天即出现显著的转录组变化,而回肠样本在3-5天才出现显著变化;基因表达聚类显示,免疫相关基因在结肠的响应时间早于回肠,且不同亚群的响应基因具有位点特异性,说明微生物对宿主上皮的调控具有时间和位点的双重特异性。
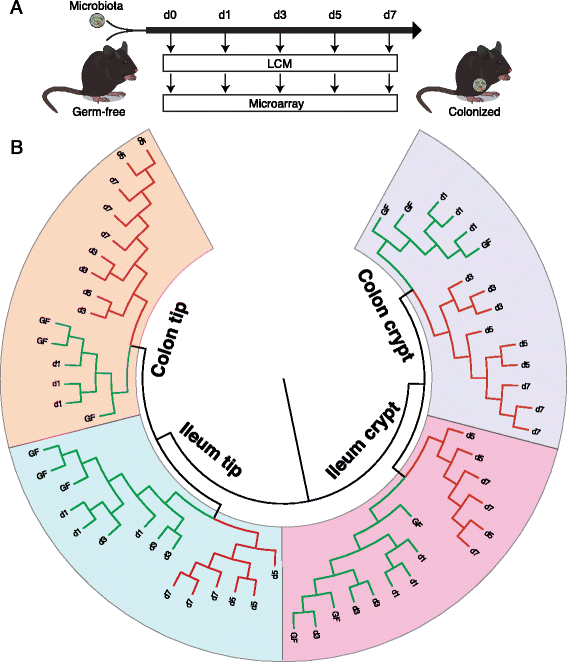
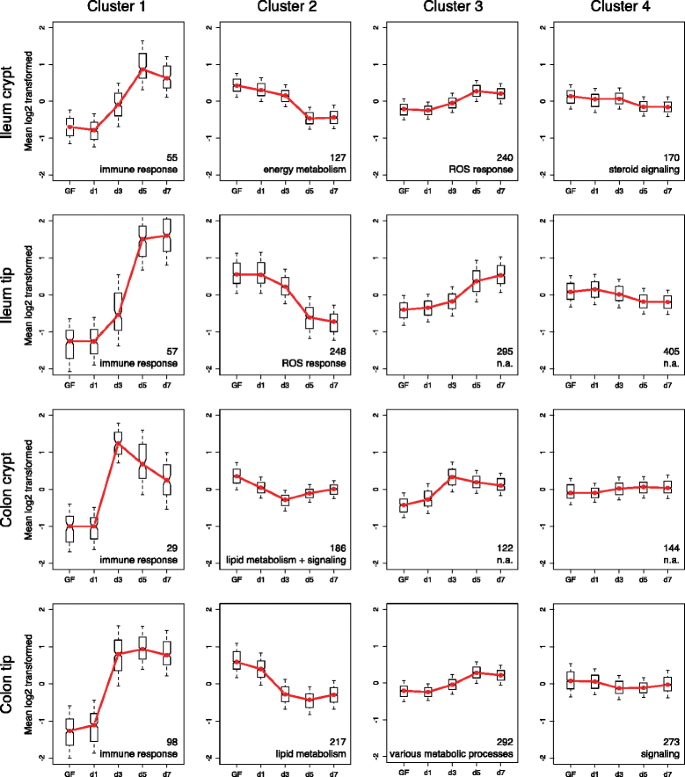
实验所用关键产品与转录组分析环节一致,包括激光捕获显微切割系统、RNA提取与扩增试剂盒、微阵列芯片等。
3.5 关键功能验证实验
实验目的是验证转录组分析揭示的核心功能,包括细胞增殖与谷胱甘肽转移酶活性。方法上,采用Ki-67免疫染色检测GF和CR小鼠隐窝上皮细胞的增殖水平,采用比色法检测顶端上皮细胞的谷胱甘肽-S-转移酶(GST)活性。结果显示,CR小鼠回肠和结肠隐窝的Ki-67阳性细胞数显著高于GF小鼠(文献未明确具体数值,基于图表趋势推测),证实微生物促进隐窝细胞增殖;结肠顶端上皮细胞的GST活性显著高于GF小鼠(n=4/5,P<0.05),而回肠顶端无显著差异,验证了GO分析的功能富集结果。
实验所用关键产品:Thermo Scientific的Ki-67抗体(货号RM-9106-S1)、Abcam的GST活性检测试剂盒(货号ab65326)、Thermo Scientific的BCA蛋白定量试剂盒(货号23227)等。
4. Biomarker研究及发现成果
本文涉及的Biomarker为肠道微生物调控的位点特异性差异表达基因,涵盖免疫、细胞增殖、代谢等功能类别,通过GF/CR小鼠转录组分析、qPCR验证与功能实验,明确了这些基因的位点特异性表达特征与功能关联。
Biomarker定位:类型为转录组水平的位点特异性差异表达基因,筛选逻辑为:首先通过GF vs CR小鼠的微阵列分析筛选差异表达基因(P<0.001),然后通过qPCR验证代表性基因的表达,最后结合GO分析与功能实验验证其功能关联,形成“筛选→验证→功能确认”的完整逻辑链条。
研究过程详述:Biomarker来源于激光捕获显微切割分离的回肠/结肠隐窝、顶端上皮细胞样本,验证方法包括qPCR定量检测基因表达、免疫染色检测细胞增殖、比色法检测酶活性;特异性与敏感性数据显示,86%的微生物调控基因具有位点特异性,不同亚群的Biomarker功能特征显著不同:回肠顶端的Biomarker如Pigr(聚合免疫球蛋白受体)参与免疫调控,结肠顶端的Biomarker如GST相关基因参与代谢解毒,隐窝的Biomarker如Cdc25c参与细胞周期调控;原文明确了差异表达基因的统计学显著性(P<0.001),样本量为5个生物学重复(GF vs CR实验)和3个生物学重复(定植实验),ROC曲线等特异性数据未在原文中提及。
核心成果提炼:这些位点特异性Biomarker的功能关联包括:回肠顶端的免疫相关Biomarker参与肠道黏膜免疫防御,结肠顶端的代谢相关Biomarker参与肠道解毒功能,隐窝的细胞增殖相关Biomarker参与肠道上皮更新;创新性在于首次揭示了肠道微生物对宿主上皮转录组的位点特异性调控,明确了不同上皮亚群的调控网络差异,为肠道微生物相关疾病的靶向治疗提供了潜在的位点特异性靶点;统计学结果显示,2256个基因受微生物调控(P<0.001),其中回肠顶端的调控基因数量最多(894个),结肠顶端的GST活性差异具有统计学显著性(n=4/5,P<0.05)。
