1. 领域背景与文献引入
文献英文标题:Sex-dependent neuronal effects of α-synuclein reveal that GABAergic transmission is neuroprotective of sleep-controlling neurons;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:神经科学(帕金森病与睡眠障碍)
帕金森病(PD)是全球范围内最常见的神经退行性疾病之一,男女发病风险比约为2:1,性别已被明确为PD发病的重要影响因素。近二十年来的研究证实,睡眠障碍如REM睡眠行为障碍(RBD)、日间过度嗜睡(EDS)是PD前驱期的核心生物标志物,可早于运动症状出现数年至数十年,但其潜在细胞机制尚未完全阐明。α-突触核蛋白(α-syn)的异常聚集是PD的病理标志,此前多数研究聚焦于寡聚体或纤维体形式α-syn的神经毒性,而单体α-syn(α-syn_M)的作用被认为相对良性,直至近年研究发现其可调控上丘背侧被盖核(LDT)雄性神经元的功能并诱导神经毒性。LDT是调控睡眠-觉醒周期与REM睡眠肌张力的关键核团,其胆碱能神经元退变与PD前驱睡眠障碍密切相关,但此前研究仅关注雄性LDT神经元,α-syn_M对雌性LDT神经元的效应及性别差异机制仍是空白。针对这一研究缺口,本研究旨在探讨α-syn_M对雌雄LDT神经元膜兴奋性、细胞内钙水平及细胞活力的性别差异效应,并揭示GABA能传递在其中的神经保护作用,为PD前驱睡眠障碍的性别差异提供细胞水平机制依据。
2. 文献综述解析
本文综述部分以α-syn的存在形式、脑区特异性及性别差异为核心分类维度,系统梳理了现有研究对α-syn神经毒性、睡眠障碍与PD关联的认知,明确了现有研究的局限性与本研究的创新价值。
现有研究中,关于α-syn的神经毒性,多数研究聚焦于寡聚体和纤维体形式,证实其可干扰细胞内多种功能并诱导神经元死亡,而针对单体α-syn的研究相对较少,早期观点认为其神经毒性较弱甚至无毒性,但近年研究发现α-syn_M可影响LDT雄性神经元的膜兴奋性与细胞活力,提示其可能参与PD前驱期病理过程。关于睡眠障碍与PD的关联,研究表明LDT胆碱能神经元退变是PD患者RBD发生的重要原因,且PD男性前驱睡眠障碍的发生率显著高于女性,但性别差异的细胞机制尚未明确。现有研究的局限性主要体现在三个方面:一是缺乏对单体α-syn在不同性别神经元中效应的对比研究;二是未明确GABA能传递等神经环路机制在α-syn_M神经毒性中的性别特异性调控作用;三是对LDT等睡眠调控核团的研究未充分考虑性别因素。本研究的创新点在于首次揭示了α-syn_M对LDT神经元的性别差异效应,发现雌性LDT神经元中存在GABA能传递介导的内源性神经保护机制,同时证实激活GABA能传递可有效缓解雄性LDT神经元的α-syn_M诱导神经毒性,为PD前驱睡眠障碍的性别差异提供了全新的细胞机制解释。
3. 研究思路总结与详细解析
本研究以“α-syn_M对LDT神经元的性别差异效应及GABA能传递的调控作用”为核心科学问题,采用“假设提出→细胞功能检测→机制验证→神经保护效应确认”的闭环技术路线,通过膜片钳电生理、钙成像、细胞死亡组织化学三种核心技术,系统解析了α-syn_M对雌雄LDT神经元的多维度效应及GABA能传递的调控机制。
3.1 脑片制备与实验模型构建
实验目的:构建稳定的雌雄小鼠LDT和黑质(SN)脑片模型,为后续电生理、钙成像及细胞活力检测提供实验载体,同时制备高纯度单体α-syn用于干预实验。
方法细节:选用12-30日龄NMRI小鼠,经异氟烷麻醉后断头取脑,快速制备250μm厚度的LDT和SN脑片,在含氧人工脑脊液(ACSF)中37℃孵育15min后室温平衡至少1h;通过原核表达系统重组表达人源α-syn,经离子交换层析和分子筛层析分离纯化得到单体组分,以100nM终浓度通过灌流或孵育方式施加于脑片;使用河豚毒素(TTX)、GABA_A受体拮抗剂SR-95531、GABA_B受体拮抗剂CGP55845、甘氨酸受体拮抗剂士的宁、GABA_A受体激动剂蝇蕈醇、GABA_B受体激动剂巴氯芬等药物进行干预实验。
结果解读:成功制备的脑片可维持神经元功能稳定至少8h,α-syn_M单体纯度经验证符合实验要求,药物干预可特异性阻断或激活相应神经信号通路,为后续实验提供可靠基础。
产品关联:实验所用关键产品:河豚毒素(TTX,Tocris, UK)、SR-95531(Sigma, Denmark)、CGP55845(Tocris, UK)、士的宁(Sigma, Denmark)、蝇蕈醇(Sigma, Denmark)、巴氯芬(Sigma, Denmark)、Fura-2 AM钙指示剂、碘化丙啶(PI,Sigma-Aldrich)、4",6-二脒基-2-苯基吲哚(DAPI,Sigma-Aldrich)。
3.2 α-syn_M对雌雄LDT和SN神经元膜电流的性别差异效应
实验目的:明确α-syn_M对雌雄LDT和SN神经元膜兴奋性的调控作用,验证性别差异与脑区特异性。
方法细节:采用全细胞膜片钳技术,在电压钳模式下记录神经元基线膜钳制电流,施加100nM α-syn_M 3-4min后,检测膜电流的变化幅度与方向。
结果解读:雄性LDT神经元中,α-syn_M诱导内向电流,与此前研究结果一致;而雌性LDT神经元中,α-syn_M诱导外向电流,幅度为54.8±11.3pA(n=14),与雄性效应完全相反。雌雄SN神经元中,α-syn_M均诱导外向电流,幅度分别为雌性47.2±16.0pA(n=11)、雄性与雌性无显著差异(p=0.3847),表明α-syn_M的效应具有LDT特异性性别差异,而SN中无性别差异。
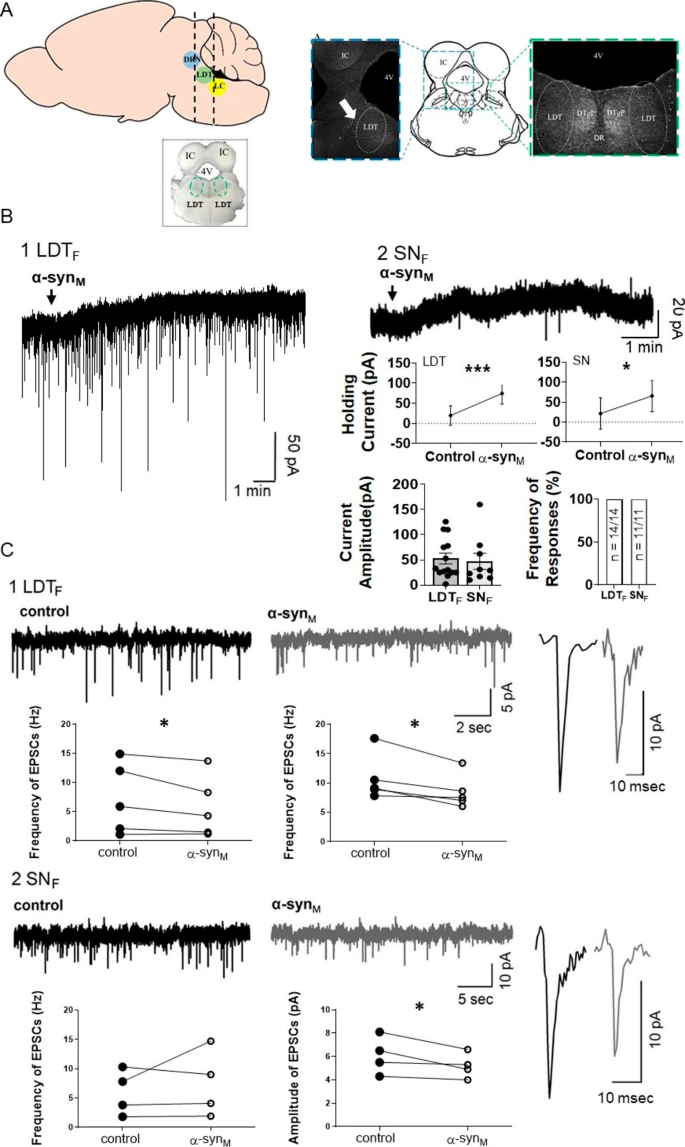
3.3 α-syn_M对雌雄LDT和SN神经元突触传递的调控作用
实验目的:检测α-syn_M对雌雄LDT和SN神经元兴奋性突触传递的影响,进一步验证性别差异效应。
方法细节:在膜片钳电压钳模式下,记录自发兴奋性突触后电流(sEPSCs)的幅度与频率,对比α-syn_M处理前后的变化。
结果解读:雌性LDT神经元中,α-syn_M使sEPSCs频率降低约20%(对照组7.2±2.7Hz,处理组5.8±2.3Hz,n=5,p=0.0475),幅度降低21%(对照组10.8±1.7pA,处理组8.5±1.3pA,n=5,p=0.0253);雌性SN神经元中,sEPSCs幅度降低14%(p=0.0483),频率无显著变化;雄性SN神经元中,sEPSCs幅度降低10%(p=0.0449),频率无显著变化。结果进一步证实LDT神经元对α-syn_M的突触传递效应存在性别差异,而SN中无性别差异。
3.4 α-syn_M对雌雄LDT神经元细胞内钙水平的性别差异影响
实验目的:解析α-syn_M对雌雄LDT神经元细胞内钙稳态的调控作用,明确钙变化的性别差异特征。
方法细节:采用Fura-2 AM负载钙成像技术,记录神经元基线钙荧光强度,施加α-syn_M后检测钙荧光强度变化(ΔF/F%),分析钙变化的方向与比例。
结果解读:雄性LDT神经元中,97.4%的神经元出现钙变化(n=38/39),其中76.3%为钙水平升高(n=29/38);雌性LDT神经元中,100%的神经元出现钙变化(n=89/89),其中58.4%为钙水平降低(n=52/89),雌雄钙变化方向的比例差异显著(p=0.0004),表明α-syn_M对LDT神经元钙稳态的调控具有明显性别差异。
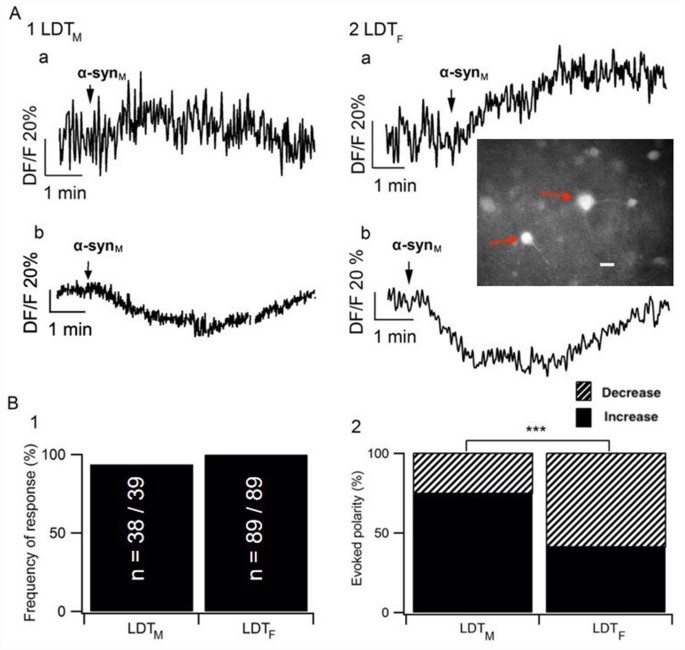
3.5 GABA能传递在α-syn_M诱导雌性LDT神经元效应中的机制解析
实验目的:探讨GABA能传递对α-syn_M诱导雌性LDT神经元膜电流与钙变化的调控机制,明确突触传递的作用。
方法细节:分别在TTX阻断动作电位、低钙溶液阻断突触传递、或GABA_A/GABA_B/甘氨酸受体拮抗剂存在的条件下,记录α-syn_M对雌性LDT神经元的膜电流效应;在GABA/甘氨酸受体拮抗剂存在下,检测钙降低幅度的变化。
结果解读:TTX或低钙溶液处理后,α-syn_M在雌性LDT神经元中由诱导外向电流转为诱导内向电流(-7.7±2.0pA,n=4);GABA/甘氨酸受体拮抗剂处理后,同样诱导内向电流(-16.3±5.2pA,n=3);钙降低幅度在拮抗剂处理后显著减小,由对照组的57.1±3.0%ΔF/F(n=52)降至36.2±2.3%ΔF/F(n=49,p=0.0001)。结果表明,α-syn_M对雌性LDT神经元的抑制效应依赖于GABA能突触传递,内源性GABA能传递掩盖了α-syn_M的直接兴奋性效应。
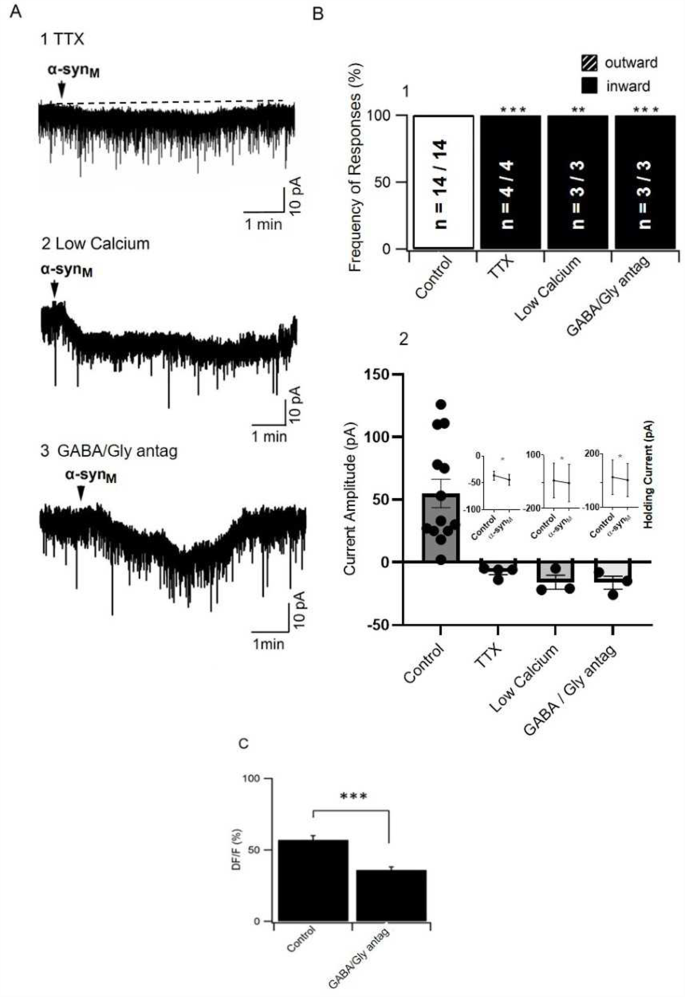
3.6 α-syn_M对雌雄LDT神经元兴奋性的功能影响
实验目的:检测α-syn_M对雌雄LDT神经元动作电位发放频率的影响,明确其对神经元输出功能的性别差异调控。
方法细节:在膜片钳电流钳模式下,将神经元膜电位钳制在-45mV以诱导持续动作电位发放,对比α-syn_M处理前后的发放频率。
结果解读:雌性LDT神经元中,α-syn_M使动作电位发放频率降低36.5%(对照组0.41±0.05Hz,处理组0.26±0.08Hz,n=3,p=0.0498);而此前研究显示雄性LDT神经元中发放频率显著升高,表明α-syn_M对LDT神经元兴奋性的调控具有完全相反的性别差异效应。
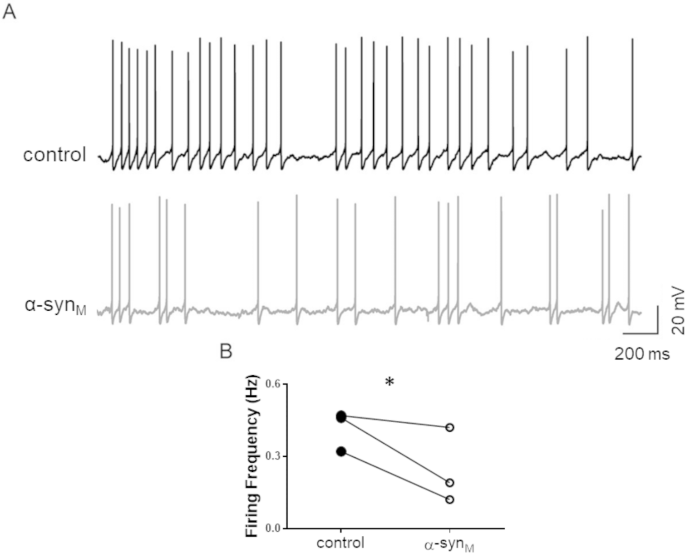
3.7 GABA能传递介导的性别特异性神经保护效应验证
实验目的:验证GABA能传递对α-syn_M诱导LDT神经元死亡的性别特异性调控作用,明确其神经保护功能。
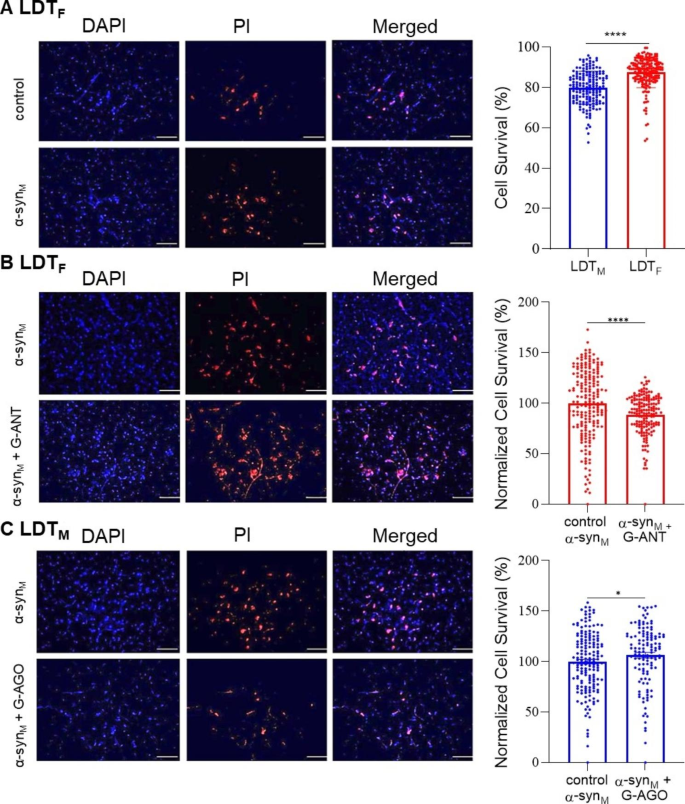
方法细节:采用PI/DAPI双染色法,检测LDT脑片在α-syn_M孵育7h后的细胞存活率;分别在雌性LDT中加入GABA/甘氨酸受体拮抗剂、雄性LDT中加入GABA受体激动剂,检测存活率的变化。
结果解读:雌性LDT神经元的存活率为87.4±0.6%(n_a=183/n_40=48),显著高于雄性的79.9±0.6%(n_a=168/n_40=66,p<0.0001);雌性LDT中加入GABA/甘氨酸受体拮抗剂后,存活率显著降低(p=0.0001);雄性LDT中加入GABA受体激动剂后,存活率显著升高(p=0.0334)。结果证实,内源性GABA能传递介导雌性LDT的神经保护作用,而激活GABA能传递可有效缓解雄性LDT神经元的α-syn_M诱导神经毒性。
4. Biomarker研究及发现成果解析
本研究聚焦于神经环路功能层面的Biomarker——GABA能传递功能(包括GABA_A、GABA_B受体介导的信号通路),通过“细胞功能差异观察→机制验证→神经保护效应确认”的完整逻辑链条,证实其作为PD前驱期性别特异性神经保护机制的核心Biomarker价值。
Biomarker定位:本研究中的核心Biomarker为GABA能传递功能,其筛选逻辑基于α-syn_M对雌雄LDT神经元的性别差异效应:首先通过电生理和钙成像实验发现雌性LDT神经元的抑制效应依赖于GABA能传递,进而通过细胞活力实验验证其神经保护作用,最终形成“细胞功能差异→机制解析→临床关联”的完整验证链条。
研究过程详述:该Biomarker的来源为小鼠LDT脑片的神经环路功能,验证方法包括膜片钳电生理检测膜电流与突触传递变化、钙成像检测细胞内钙稳态变化、PI/DAPI染色检测细胞存活率变化;特异性方面,该Biomarker的调控效应具有严格的性别特异性:仅在雌性LDT中表现为内源性神经保护,在雄性LDT中需外源性激活GABA能传递才能发挥保护作用;敏感性方面,阻断GABA能传递可使雌性LDT神经元的存活率降低约11.2%(p=0.0001),激活GABA能传递可使雄性LDT神经元的存活率升高约6%(p=0.0334),表明其对α-syn_M神经毒性的调控效应具有统计学显著性。
核心成果提炼:该Biomarker的功能关联在于,它是PD前驱期睡眠障碍性别差异的关键细胞机制:雌性LDT中内源性GABA能传递可拮抗α-syn_M的神经毒性,从而降低PD前驱睡眠障碍的发生风险;而雄性LDT中GABA能传递功能相对不足,激活该通路可成为潜在的神经保护治疗靶点。其创新性在于首次发现GABA能传递介导的性别特异性神经保护机制,突破了此前对α-syn_M神经毒性无性别差异的认知;统计学结果方面,雌雄LDT神经元存活率差异p<0.0001,GABA/甘氨酸受体拮抗剂对雌性存活率的影响p=0.0001,GABA受体激动剂对雄性存活率的影响p=0.0334,所有数据均具有明确的统计学显著性。
