1. 领域背景与文献引入
文献英文标题:mTOR hypoactivity leads to trophectoderm cell failure by enhancing lysosomal activation and disrupting the cytoskeleton in preimplantation embryo;发表期刊:Cell Biosci;影响因子:未公开;研究领域:胚胎发育与生殖生物学(植入前胚胎mTOR信号通路调控)
植入前胚胎发育是妊娠成功的关键起始阶段,约30%的早期妊娠丢失源于此阶段的发育异常,营养代谢稳态是维持胚胎正常发育的核心因素。领域共识:mTOR(哺乳动物雷帕霉素靶蛋白)作为整合细胞内外营养、生长信号的核心激酶,在生殖系统中参与卵泡发生、卵母细胞成熟、胚胎细胞增殖等多个过程,mTOR全基因敲除小鼠胚胎因细胞增殖障碍在植入后迅速致死,提示其对胚胎发育的必需性。但现有研究多聚焦于mTOR整体敲除的胚胎致死效应,针对植入前胚胎阶段mTOR低活性的特异性影响及分子调控机制仍存在空白,尤其是mTOR信号对滋养外胚层(TE)细胞命运决定的下游效应通路尚未明确,无法为早期妊娠丢失的机制提供精准的分子靶点。本文通过体内外药物抑制mTOR活性的模型,结合多组学分析与细胞功能实验,旨在揭示mTOR低活性对植入前胚胎8-细胞到囊胚转化的影响及分子机制,填补该领域的研究空白。
2. 文献综述解析
作者以mTOR在生殖系统的作用阶段为分类维度,系统梳理了现有研究在卵泡发生、卵母细胞成熟、胚胎发育三个层面的进展与局限性,明确了植入前胚胎阶段mTOR低活性调控滋养外胚层细胞功能的研究空白。
现有研究支持mTOR是生殖发育过程中的关键调控激酶,在卵泡发生中mTOR参与颗粒细胞增殖与卵母细胞成熟启动,在胚胎发育中mTOR敲除胚胎因细胞增殖障碍在植入后致死,部分研究发现mTOR通过氨基酸信号调控滋养外胚层细胞分化,但现有研究存在明显局限性:一是多采用mTOR全基因敲除模型,导致胚胎早期致死,无法解析植入前阶段mTOR低活性的特异性效应;二是未揭示mTOR低活性对8-细胞到囊胚转化这一关键节点的调控作用;三是缺乏对mTOR下游分子通路(如溶酶体激活、细胞骨架紊乱)与滋养外胚层细胞功能异常的关联分析。本文的创新价值在于首次采用第三代双价mTOR抑制剂Rapalink-1构建体内外mTOR低活性模型,结合转录组、甲基化组测序与细胞功能验证,明确了mTOR低活性通过增强溶酶体激活和破坏细胞骨架导致滋养外胚层细胞功能异常的分子机制,填补了植入前胚胎阶段mTOR调控滋养外胚层细胞命运的研究空白,为早期妊娠丢失的机制提供了新的理论依据。
3. 研究思路总结与详细解析
本文的研究目标是明确mTOR低活性对植入前胚胎发育的影响及分子机制,核心科学问题是mTOR如何调控8-细胞到囊胚转化及滋养外胚层细胞功能维持,技术路线采用“体内外药物抑制模型构建→胚胎发育表型检测→细胞命运与功能验证→多组学分子机制解析→关键通路功能验证”的闭环逻辑,系统揭示mTOR低活性的生物学效应与分子靶点。
3.1 体内外mTOR抑制模型构建与胚胎发育表型检测
实验目的:验证mTOR抑制对植入前胚胎囊胚形成、植入能力及后续胚胎发育的影响。
方法细节:体内模型选用ICR品系妊娠小鼠,在0.5和1.5 dpc(交配后天数)分别腹腔注射1.5 mg/kg第三代mTOR抑制剂Rapalink-1,对照组注射玉米油,后续检测3.5 dpc囊胚形成率、5.5 dpc植入位点数量、13.5 dpc胎儿发育情况及出生体重;体外模型收集1-细胞或8-细胞胚胎,在KSOM培养基中分别加入50、100、200 nM Rapalink-1、200 nM雷帕霉素(mTORC1特异性抑制剂)、5 μM JR-AB2-011(mTORC2特异性抑制剂),在37℃、5%CO₂培养箱中培养,观察胚胎发育阶段,将培养得到的囊胚移植至假孕小鼠子宫,检测7.5 dpc植入位点数量与大小。
结果解读:体内mTOR抑制后,胚胎中mTORC1下游靶点p-4E-BP1和mTORC2下游靶点p-AKT的磷酸化水平显著降低(n=3,P<0.05),囊胚形成率从对照组的95%降至41%(n=3,P<0.01),5.5 dpc植入位点数量从14个降至7个(n=12,P<0.01),13.5 dpc胎儿数量减少,出生体重显著降低(n=127/131,P<0.05);体外培养中,Rapalink-1处理的1-细胞胚胎囊胚形成率呈浓度依赖性降低,8-细胞胚胎处理后70%停滞在桑椹胚阶段,囊胚形成率从对照组的92%降至30%(n=7,P<0.01),胚胎移植后植入率从50%降至10%(n=14,P<0.01),植入位点大小显著减小(n=10,P<0.05)。
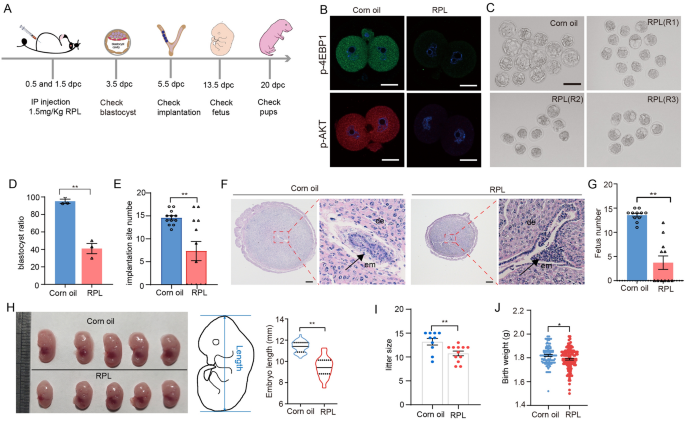
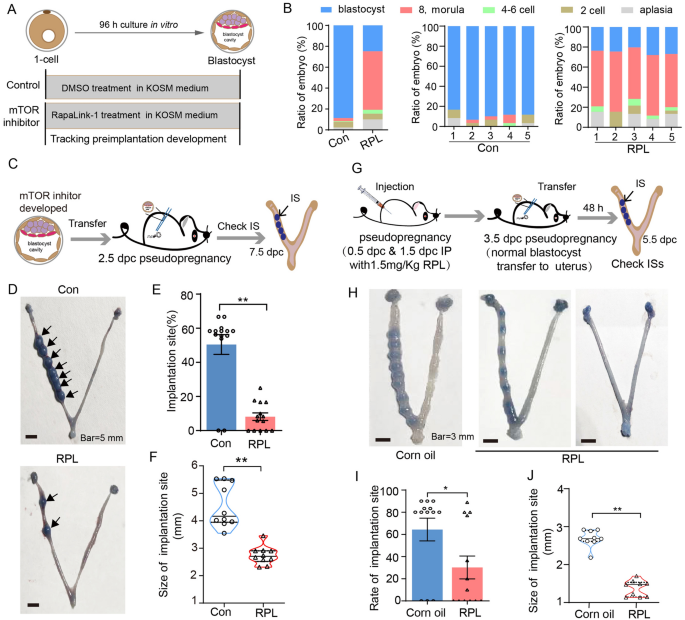
产品关联:实验所用关键产品:Rapalink-1(APExBIO)、雷帕霉素(LC Laboratories)、JR-AB2-011(MCE)、KSOM培养基(Millipore,货号MR-107-D)、Chicago Sky Blue(Sigma)。
3.2 植入前胚胎细胞命运与囊胚质量检测
实验目的:明确mTOR抑制对囊胚内细胞团(ICM)、滋养外胚层细胞分化及细胞凋亡的影响。
方法细节:采用免疫荧光染色技术,检测内细胞团标记物SOX2、滋养外胚层标记物CDX2,以及内细胞团进一步分化的上胚层(EPI)标记物NANOG、原始内胚层(PrE)标记物SOX17;通过TUNEL染色检测囊胚细胞凋亡情况;利用激光共聚焦显微镜获取囊胚3D荧光图像,结合IMARIS软件进行细胞计数与定位分析。
结果解读:mTOR抑制后,囊胚总细胞数、内细胞团细胞数、滋养外胚层细胞数均显著减少(n=7,P<0.05),CDX2+滋养外胚层细胞比例从对照组的~60%降至~35%(n=7,P<0.01),SOX2+内细胞团细胞比例无显著变化;原始内胚层标记物SOX17+细胞数及比例显著降低(n=7,P<0.05),上胚层标记物NANOG+细胞数及比例无显著变化;TUNEL阳性凋亡细胞数是对照组的5倍(n=10,P<0.01),表明mTOR抑制主要影响滋养外胚层与原始内胚层细胞的分化,导致囊胚质量下降与细胞凋亡增加。
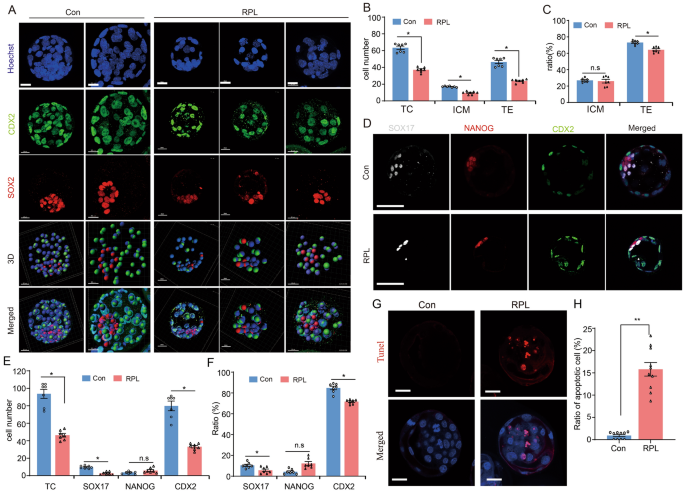
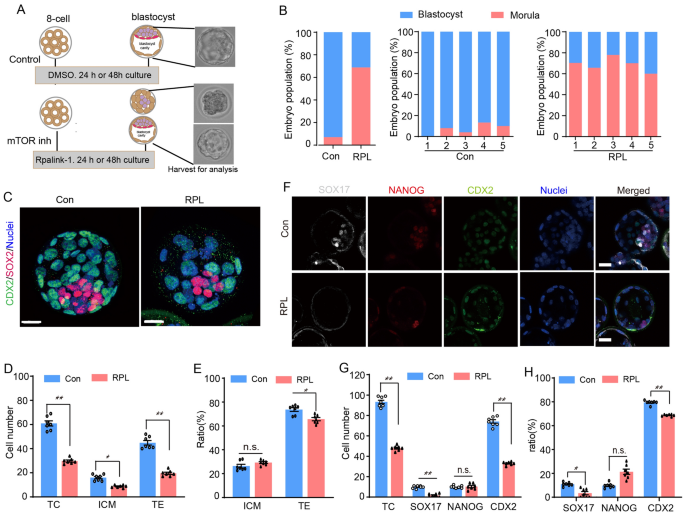
产品关联:实验所用关键产品:SOX2抗体(Abcam)、CDX2抗体(Biogenex)、NANOG抗体(Abcam)、SOX17抗体(R&D)、TUNEL细胞凋亡检测试剂盒(Roche)、IMARIS软件(Bitplane,版本9.0.2)。
3.3 转录组与甲基化组测序分析
实验目的:解析mTOR抑制后植入前胚胎的转录组变化与表观遗传调控机制。
方法细节:收集Rapalink-1处理组与对照组的囊胚,采用Smart-seq2方法构建单细胞转录组文库,进行Illumina HiSeq2500测序;采用全基因组亚硫酸氢盐测序(BS-seq)检测基因组DNA甲基化水平;通过DESeq2分析差异表达基因(DEGs),DAVID工具进行GO/KEGG富集分析,GSEA进行基因集富集分析;整合转录组与甲基化组数据,分析差异甲基化区域(DMRs)与DEGs的关联。
结果解读:转录组分析共鉴定出1145个DEGs,其中716个基因下调,429个基因上调;下调基因显著富集于滋养外胚层细胞分化、Wnt信号通路等生物学过程,上调基因显著富集于溶酶体组织、代谢过程等;GSEA分析显示滋养外胚层分化相关基因(如Cdx2、Hand1、Eomes)显著下调,溶酶体通路相关基因显著上调;甲基化组分析显示Rapalink-1处理组全基因组平均甲基化水平从3.57%升至4.84%(n=3,P<0.05),共鉴定出5250个DMRs,其中90.8%为高甲基化区域;整合分析发现157个重叠基因,高甲基化且下调的基因富集于细胞骨架组织、细胞形态调控等通路,高甲基化且上调的基因富集于溶酶体、mTOR信号通路等。
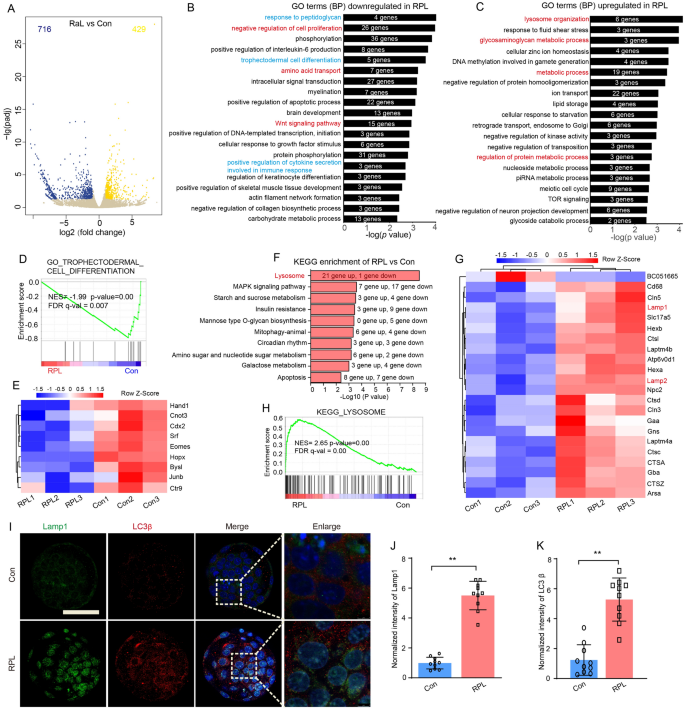
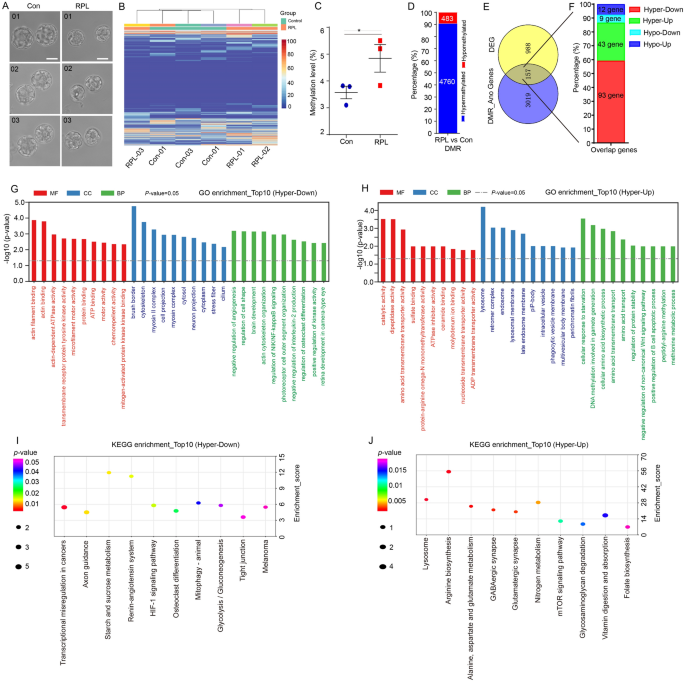
产品关联:实验所用关键产品:Smart-seq2建库试剂盒、EZ DNA Methylation-Gold Kit(Zymo Research)、Illumina HiSeq2500测序平台、DESeq2软件、DAVID功能注释工具。
3.4 溶酶体激活与细胞骨架紊乱的功能验证
实验目的:验证mTOR抑制导致的溶酶体激活与细胞骨架紊乱是滋养外胚层细胞功能异常的关键机制。
方法细节:采用LysoTracker Green染色检测囊胚溶酶体活性,免疫荧光染色检测溶酶体标记物LAMP1、LAMP2与自噬标记物LC3β的表达;采用FITC-鬼笔环肽染色检测F-肌动蛋白的分布,免疫荧光检测E-钙粘蛋白的表达,观察细胞骨架与细胞连接的变化。
结果解读:Rapalink-1处理后,囊胚的LysoTracker Green荧光强度显著升高(n=10,P<0.01),LAMP1、LAMP2、LC3β的免疫荧光强度显著增加(n=10,P<0.05),表明mTOR抑制增强了溶酶体激活与自噬活性;F-肌动蛋白分布紊乱,部分卵裂球出现细胞骨架网络聚集,E-钙粘蛋白表达异常,细胞连接破坏,部分卵裂球出现胞质分裂失败(n=7,P<0.05),表明mTOR抑制导致细胞骨架紊乱与细胞连接异常,进而影响滋养外胚层细胞功能。
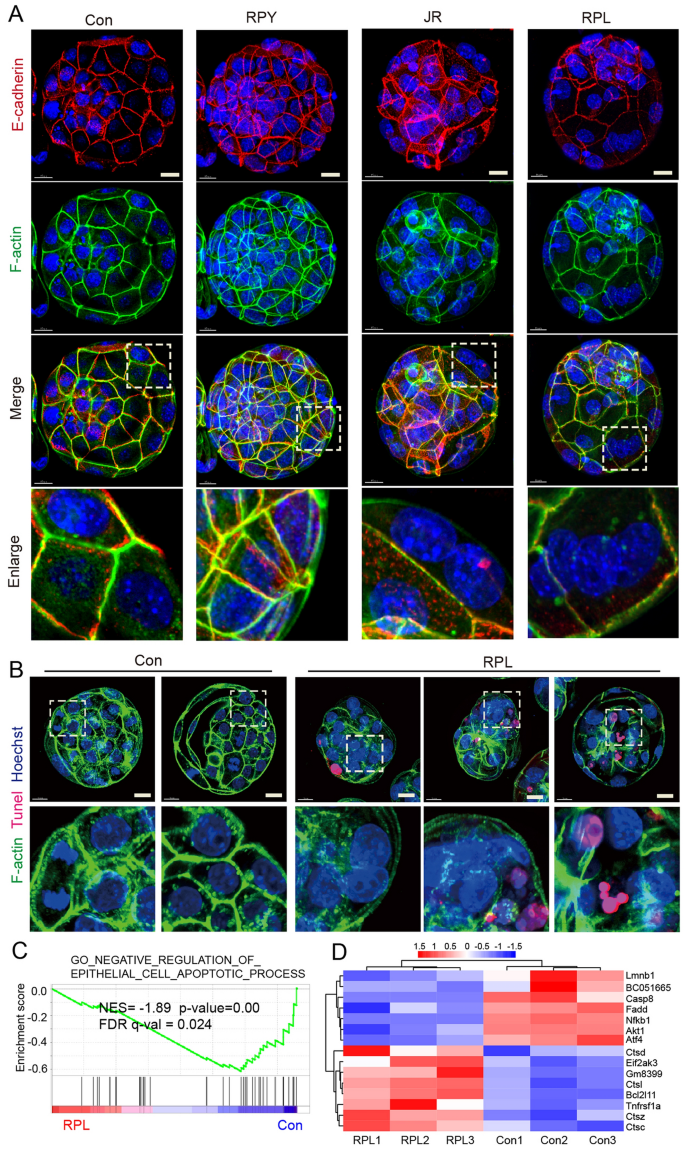
产品关联:实验所用关键产品:LysoTracker Green(Invitrogen)、LAMP1抗体、LAMP2抗体、LC3β抗体、FITC-鬼笔环肽(Sigma)、E-钙粘蛋白抗体(R&D)、激光共聚焦显微镜(Zeiss LSM880)。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括滋养外胚层细胞分化相关基因(Cdx2、Hand1、Eomes)、溶酶体激活相关基因(Lamp1、Lamp2、Ctsd)及细胞骨架相关基因(如肌动蛋白结合基因),筛选与验证逻辑采用“多组学测序筛选→细胞水平免疫荧光验证→功能实验验证”的完整链条,明确了这些Biomarker与mTOR低活性及滋养外胚层细胞功能异常的关联。
Biomarker定位
滋养外胚层细胞分化相关基因(Cdx2等)是mTOR低活性导致滋养外胚层细胞功能异常的核心效应分子,筛选逻辑为通过转录组测序发现mTOR抑制后显著下调的滋养外胚层分化基因,经免疫荧光验证蛋白表达变化,甲基化组分析显示其启动子区域高甲基化;溶酶体激活相关基因(Lamp1等)是mTOR低活性的下游效应分子,筛选逻辑为转录组测序发现显著上调的溶酶体基因,经LysoTracker染色与免疫荧光验证溶酶体活性增强;细胞骨架相关基因是mTOR低活性导致细胞连接破坏的关键分子,筛选逻辑为转录组-甲基化组整合分析发现高甲基化且下调的细胞骨架基因,经免疫荧光验证细胞骨架分布紊乱。
研究过程详述
滋养外胚层分化相关基因Cdx2的来源为囊胚细胞的转录组数据,验证方法为免疫荧光染色,特异性表现为mTOR抑制后CDX2+滋养外胚层细胞比例从~60%降至~35%(n=7,P<0.01);溶酶体相关基因Lamp1的来源为囊胚细胞的转录组数据,验证方法为LysoTracker染色与免疫荧光,敏感性表现为LAMP1免疫荧光强度上调2.1倍(n=10,P<0.05);细胞骨架相关基因的来源为转录组-甲基化组整合分析数据,验证方法为FITC-鬼笔环肽染色,显示F-肌动蛋白分布紊乱,细胞连接破坏。
核心成果提炼
滋养外胚层分化基因Cdx2作为关键Biomarker,其表达下调与mTOR低活性导致的滋养外胚层细胞功能异常直接相关,风险比表现为mTOR抑制后滋养外胚层细胞比例降低41.7%(n=7,P<0.01),囊胚植入率降低80%(n=14,P<0.01);溶酶体激活相关基因Lamp1的表达上调是mTOR低活性的下游效应,其荧光强度上调2.1倍(n=10,P<0.05),提示溶酶体激活是滋养外胚层细胞功能异常的关键通路;本文的创新性在于首次揭示了mTOR低活性通过表观遗传调控滋养外胚层分化基因表达、增强溶酶体激活、破坏细胞骨架导致滋养外胚层细胞功能异常的分子机制,为早期妊娠丢失的Biomarker筛选提供了新的候选靶点,所有结果均来自动物与细胞实验,无临床样本数据。
