1. 领域背景与文献引入
文献英文标题:Efficacy of a novel double-controlled oncolytic adenovirus driven by the Ki67 core promoter and armed with IL-15 against glioblastoma cells;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:神经肿瘤学(胶质母细胞瘤靶向免疫治疗)
胶质母细胞瘤(GBM)是中枢神经系统恶性程度最高的肿瘤之一,领域共识:尽管手术联合放疗、化疗的综合治疗方案已应用数十年,但患者中位生存期仅约15个月,预后极差。其核心困境在于肿瘤细胞的高度异质性、治疗耐药性,以及肿瘤微环境中存在的强免疫抑制状态——肿瘤细胞表达的多种蛋白可导致T细胞功能障碍,转化生长因子-β(TGF-β)、白细胞介素-10(IL-10)等因子进一步诱导局部及全身免疫抑制。近年来,溶瘤腺病毒因能选择性在肿瘤细胞内复制并裂解肿瘤,同时可搭载治疗基因调节免疫微环境,成为胶质母细胞瘤治疗的研究热点。然而,现有溶瘤腺病毒存在靶向特异性不足、免疫激活效果有限等问题,且尚未有研究探索Ki67核心启动子调控的双调控溶瘤腺病毒搭载IL-15的治疗潜力。针对这一研究空白,本研究构建了Ki67核心启动子驱动E1A基因、CMV启动子调控IL-15表达的双调控溶瘤腺病毒,旨在实现精准靶向胶质母细胞瘤细胞的同时,激活免疫应答增强抗肿瘤疗效,为胶质母细胞瘤的新型治疗策略提供实验依据。
2. 文献综述解析
作者从溶瘤病毒的靶向调控策略、免疫修饰基因的应用两个维度对领域内现有研究进行分类评述。现有研究表明,溶瘤腺病毒可通过肿瘤特异性启动子调控病毒关键复制基因(如E1A),实现对肿瘤细胞的选择性杀伤,避免损伤正常组织;表达免疫共刺激因子(如OX40L)或细胞因子(如IL-4)的溶瘤腺病毒,可通过激活淋巴细胞、增强免疫细胞浸润等方式提升抗肿瘤效果。但现有研究仍存在局限性:部分溶瘤病毒的肿瘤靶向特异性不足,对正常组织存在潜在毒性;单一的免疫修饰基因激活免疫应答的能力有限,难以有效打破胶质母细胞瘤的免疫抑制微环境;缺乏将精准靶向调控与强效免疫激活相结合的协同治疗策略。
与现有研究相比,本研究的创新点在于首次构建了Ki67核心启动子驱动的双调控溶瘤腺病毒并搭载IL-15,通过Ki67启动子的肿瘤特异性实现病毒在胶质母细胞瘤细胞内的选择性复制,同时利用IL-15激活小胶质细胞等免疫细胞,从直接杀伤肿瘤、激活免疫应答、抑制血管生成三个层面协同发挥抗肿瘤作用,为胶质母细胞瘤的治疗提供了全新的协同策略。
3. 研究思路总结与详细解析
本研究的核心目标是构建并验证Ki67核心启动子驱动的双调控溶瘤腺病毒搭载IL-15对胶质母细胞瘤的治疗效果,核心科学问题是该双调控病毒如何实现精准靶向杀伤、免疫激活及抗血管生成的协同作用,技术路线遵循“构建载体→体外验证靶向性→验证免疫激活效应→验证抗血管生成作用”的闭环逻辑。
3.1 重组双调控溶瘤腺病毒的构建
实验目的是构建以Ki67核心启动子调控E1A基因、CMV启动子调控IL-15基因表达的双调控溶瘤腺病毒载体。方法细节为通过分子克隆技术,将5型腺病毒的E1A内源性启动子替换为Ki67启动子,构建Ad5-Ki67载体;在此基础上,分别将GFP基因和IL-15基因插入E3区域,由CMV启动子调控表达,得到Ad5-Ki67/GFP和Ad5-Ki67/IL-15;将构建好的质粒与骨架质粒共转染293T细胞,通过噬斑纯化获得纯化病毒。结果解读显示,成功构建了三种重组腺病毒Ad5-GFP、Ad5-Ki67/GFP、Ad5-Ki67/IL-15,滴度分别为1×10¹² vp/ml、1.3×10¹² vp/ml、1×10¹² vp/ml,载体构建的正确性经分子鉴定确认。实验所用关键产品:Gibco的磷酸盐缓冲液(PBS)、胰酶、杜尔贝科改良伊格尔培养基(DMEM),Invitrogen的胎牛血清,ATCC的细胞系,Lonza的人脐静脉内皮细胞(HUVEC)。
3.2 病毒感染特异性与肿瘤杀伤能力验证
实验目的是验证双调控溶瘤腺病毒对胶质母细胞瘤细胞的选择性感染与杀伤能力,同时评估其对正常细胞的安全性。方法细节为将三种病毒以感染复数(MOI)40分别感染胶质母细胞瘤细胞(GL261、U251、U87、原代BT-01)及正常小胶质细胞(HMC3、BV2),72小时后通过荧光显微镜观察GFP表达水平;采用细胞计数试剂盒-8(CCK-8)检测不同MOI及不同时间点的细胞活力。结果解读显示,荧光显微镜结果显示Ad5-Ki67/GFP对胶质母细胞瘤细胞的感染效率显著高于Ad5-GFP,GFP表达强度显著增强(n≥3,P<0.05),而对正常小胶质细胞HMC3、BV2无感染能力(
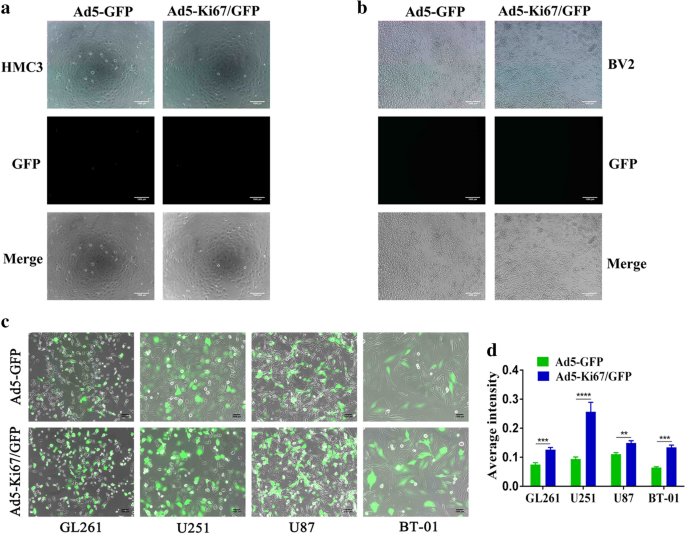
)。CCK-8结果显示,Ad5-Ki67/GFP和Ad5-Ki67/IL-15对胶质母细胞瘤细胞的增殖抑制作用显著强于Ad5-GFP,且呈剂量依赖性和时间依赖性,而对正常小胶质细胞的活力无显著影响(n=3,P<0.01)(
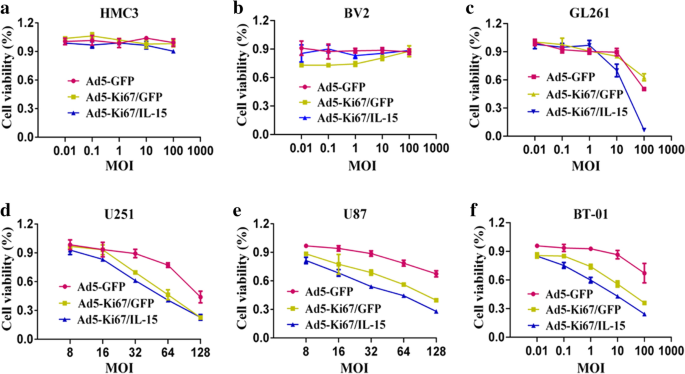
、
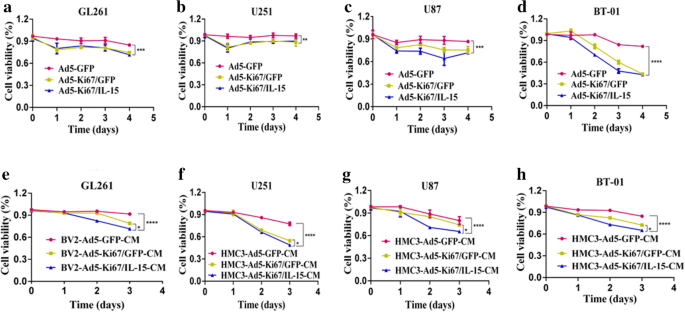
)。实验所用关键产品:Olympus荧光显微镜,Dojindo的CCK-8试剂盒,PerkinElmer的酶标仪。
3.3 IL-15表达与免疫激活效应验证
实验目的是验证双调控溶瘤腺病毒介导的IL-15表达及对小胶质细胞的激活效应。方法细节为用Ad5-Ki67/IL-15感染胶质母细胞瘤细胞,在24、48、72、96小时收集细胞上清,采用酶联免疫吸附试验(ELISA)检测IL-15浓度,采用逆转录聚合酶链反应(RT-PCR)检测IL-15基因表达水平;将病毒感染后的小胶质细胞条件培养基加入胶质母细胞瘤细胞培养体系,CCK-8检测肿瘤细胞活力。结果解读显示,ELISA结果显示Ad5-Ki67/IL-15感染后,胶质母细胞瘤细胞上清IL-15浓度随时间升高,96小时时GL261细胞上清为10.325 pg/ml、U251为12.97 pg/ml、U87为19.32 pg/ml(n=3,P<0.001),原代BT-01细胞上清在72小时达到9.71 pg/ml(n=3,P<0.001);RT-PCR结果显示IL-15基因表达上调超过200倍(n=3,P<0.001)(
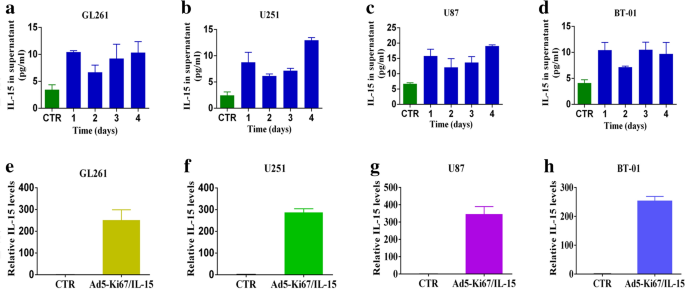
)。经Ad5-Ki67/IL-15处理的小胶质细胞条件培养基能显著抑制胶质母细胞瘤细胞增殖(n=3,P<0.001),表明IL-15有效激活了小胶质细胞的抗肿瘤活性。实验所用关键产品:Neobioscience的IL-15 ELISA试剂盒,Applied Biosystems的RT-PCR系统。
3.4 抗血管生成作用及机制验证
实验目的是验证双调控溶瘤腺病毒对胶质母细胞瘤血管生成的抑制作用及机制。方法细节为采用管形成实验,将病毒感染后的胶质母细胞瘤细胞上清加入HUVEC培养体系,观察管形成能力;采用ELISA检测细胞上清中血管内皮生长因子(VEGF)的浓度;通过外源性添加VEGF验证其对管形成的逆转作用。结果解读显示,管形成实验结果显示病毒感染后的胶质母细胞瘤细胞上清能显著抑制HUVEC的管形成能力,管段长度和管数量显著减少(n=3,P<0.001)(
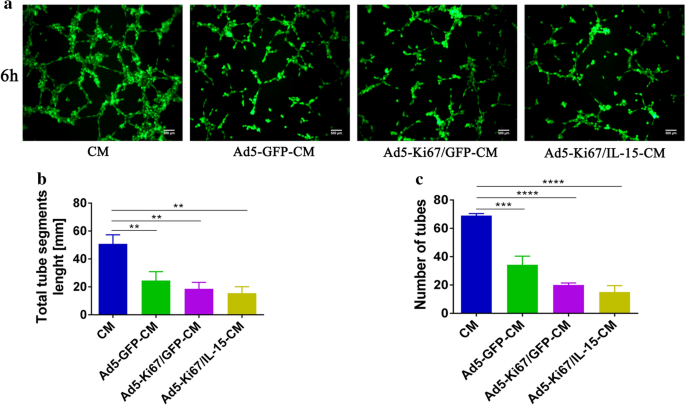
、
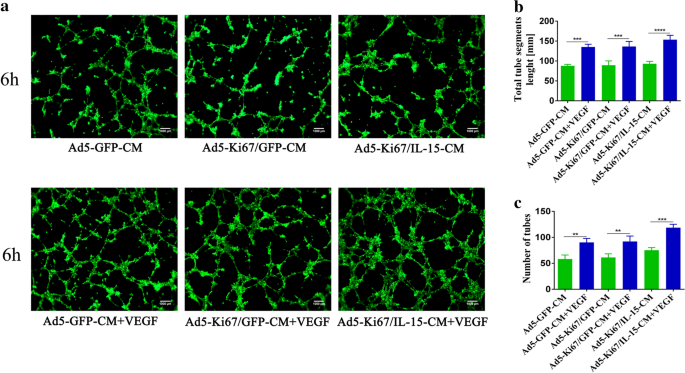
);ELISA结果显示病毒感染后胶质母细胞瘤细胞的VEGF分泌水平显著降低(n=3,P<0.01)(
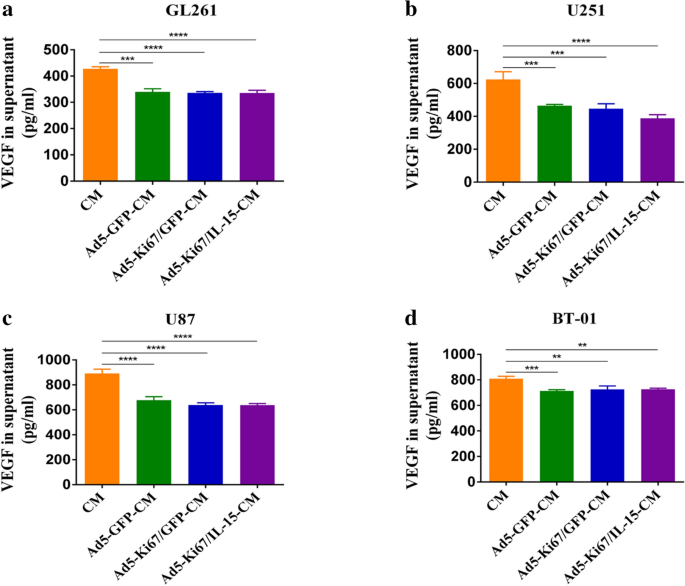
);外源性添加VEGF可部分逆转病毒上清对管形成的抑制作用,表明病毒通过降低VEGF分泌发挥抗血管生成作用。实验所用关键产品:BD的基质胶(Matrigel),Peprotech的重组VEGF蛋白。
4. Biomarker研究及发现成果
本研究中的核心Biomarker为Ki67,属于增殖类生物标志物,其筛选与验证逻辑基于Ki67在胶质母细胞瘤细胞与正常脑组织中的表达差异:Ki67是与细胞增殖密切相关的核蛋白,在胶质母细胞瘤细胞中高表达,而在正常脑组织中表达水平极低,且其表达水平与胶质母细胞瘤的恶性程度及不良预后正相关。
研究过程中,作者利用Ki67的表达差异,将Ki67核心启动子用于调控溶瘤腺病毒的E1A基因,实现病毒在高表达Ki67的胶质母细胞瘤细胞内的选择性复制。通过荧光显微镜验证,该双调控病毒仅感染高表达Ki67的胶质母细胞瘤细胞(GL261、U251、U87、原代BT-01),而不感染低表达Ki67的正常小胶质细胞(HMC3、BV2),特异性显著(n≥3,P<0.05);通过CCK-8实验验证,病毒仅对胶质母细胞瘤细胞具有杀伤作用,对正常细胞无显著毒性,进一步证实了Ki67作为靶向调控Biomarker的有效性。
核心成果方面,Ki67作为靶向调控Biomarker,为溶瘤腺病毒提供了精准的肿瘤特异性复制开关,结合IL-15的免疫激活作用,实现了精准靶向杀伤、免疫激活、抗血管生成的协同抗肿瘤效果。该研究首次证实了Ki67启动子与IL-15联合应用的协同治疗潜力,为胶质母细胞瘤及其他实体瘤的精准治疗提供了新的Biomarker与治疗策略,具有重要的临床转化价值。
