1. 领域背景与文献引入
文献英文标题:Cold stress induces enhanced chromatin accessibility and bivalent histone modifications H3K4me3 and H3K27me3 of active genes in potato;发表期刊:Genome Biology;影响因子:未公开;研究领域:植物表观遗传学(马铃薯冷胁迫响应的表观调控)
植物非生物胁迫响应的表观调控是当前生命科学研究的热点方向之一,早期研究已证实组蛋白甲基化、乙酰化等修饰参与植物对干旱、低温等胁迫的响应,随着DNase-seq、ATAC-seq等染色质开放状态鉴定技术的发展,全基因组水平解析染色质动态与基因表达的关联成为研究重点。目前,作物胁迫响应的表观调控研究多集中于单个基因的修饰变化,全基因组层面染色质可及性与组蛋白修饰的协同调控机制仍不明确;双价组蛋白修饰(H3K4me3/H3K27me3)在哺乳动物干细胞中调控发育基因的静息状态,但植物中仅在少数基因或特定发育阶段被报道,其在非生物胁迫响应中的功能及调控机制尚未揭示。马铃薯作为全球重要的非粮食作物,冷储存过程中会发生冷诱导糖化(CIS),导致加工产品品质下降并产生潜在致癌物丙烯酰胺,而CIS的表观调控机制尚未被系统解析。
针对上述研究空白,本研究以双单倍体马铃薯为材料,通过多组学联合分析,系统解析冷胁迫下马铃薯块茎染色质可及性和组蛋白修饰的动态变化,揭示双价组蛋白修饰在冷胁迫响应中的调控作用,为马铃薯CIS的表观遗传改良提供理论依据。
2. 文献综述解析
本文献综述从染色质开放状态的鉴定与功能、组蛋白修饰在植物胁迫响应中的作用、双价组蛋白修饰的研究现状三个维度展开,系统梳理了领域内现有研究的进展与不足,为自身研究的创新点奠定了基础。
染色质开放区域(DNase I超敏感位点,DHSs)作为顺式调控元件的富集区域,已在拟南芥、水稻等模式植物中被全基因组鉴定,其分布与基因表达水平密切相关,但冷胁迫下作物全基因组DHSs的动态变化特征及与差异表达基因的关联研究较为匮乏。组蛋白修饰中,H3K4me3作为活性转录标记,H3K27me3作为转录抑制标记,在植物胁迫响应中的作用已有报道,但多集中于单个胁迫响应基因的修饰变化,全基因组层面的修饰动态与基因表达的调控网络尚未构建。双价组蛋白修饰(H3K4me3/H3K27me3)在哺乳动物干细胞中被证实调控发育基因的静息状态,而植物中仅在拟南芥的少数发育基因或干旱胁迫记忆基因中被报道,且存在实验样本细胞异质性导致的结果争议,其在冷胁迫响应中的功能及调控机制完全未知。
与现有研究相比,本研究首次在马铃薯中开展冷胁迫下全基因组DHSs和双价组蛋白修饰的联合分析,揭示了活性基因在冷胁迫下染色质可及性增强及双价修饰富集的特征,填补了植物冷胁迫表观调控中染色质动态与双价修饰功能研究的空白;同时,本研究明确了基因区DHSs与温度响应基因表达的关联,为作物胁迫响应的表观调控机制提供了新的研究视角。
3. 研究思路总结与详细解析
本研究以解析马铃薯冷胁迫下染色质动态与基因表达的关联为目标,围绕“冷胁迫如何通过染色质状态和组蛋白修饰调控基因表达”这一核心科学问题,采用“样本制备→多组学测序→生物信息学分析→实验验证→模型构建”的闭环技术路线,系统揭示了冷胁迫下马铃薯块茎的表观遗传调控机制。
3.1 实验样本制备与测序文库构建
实验目的:获取不同温度处理的马铃薯块茎及叶片样本,构建高质量的DNase-seq、RNA-seq、ChIP-seq及Sequential ChIP-seq文库,为后续全基因组分析提供可靠材料。
方法细节:选用双单倍体马铃薯克隆DM1-3 516 R44作为实验材料,温室条件下种植70天后同步采集叶片和块茎,块茎随机分为两组,分别置于室温(22℃)和4℃环境中处理14天,所有样本采集后立即液氮研磨并保存于-80℃。DNase-seq文库构建采用核提取、DNase I梯度消化(0.04-4单位)、脉冲场凝胶电泳(PFGE)评估消化效果,文库构建后进行Illumina HiSeq单端测序(50nt);RNA-seq文库采用RNeasy Plant Mini Kit提取总RNA,经DNase I去除基因组DNA后,使用TruSeq mRNA-seq kit构建文库并测序;ChIP-seq使用针对H3K27me3、H3K4me3等组蛋白修饰的特异性抗体,通过MNase消化核小体、免疫沉淀获取目标染色质片段,构建文库后测序;Sequential ChIP-seq采用Re-ChIP-IT kit,依次使用H3K4me3和H3K27me3抗体进行免疫沉淀,反向顺序实验作为对照,验证双价修饰的共定位。
结果解读:成功构建6个DNase-seq文库(室温块茎、冷处理块茎、叶片各2个生物学重复),各样本比对到马铃薯参考基因组的唯一读长比例分别为45%、46%、51%,生物学重复间的测序数据相关性较高,表明实验重复性良好;RNA-seq和ChIP-seq文库均获得高质量测序数据,读长质量和覆盖度满足后续生物信息学分析的要求。
产品关联:实验所用关键产品:RNeasy Plant Mini Kit(Qiagen, Cat. # 74904)、TruSeq mRNA-seq kit(Illumina)、H3K27me3抗体(Millipore 07-449)、H3K4me3抗体(Abcam 8580)、Re-ChIP-IT kit(Active Motif, Cat # 53016)。
3.2 全基因组DHSs鉴定与分布特征分析
实验目的:全基因组鉴定不同样本中的DNase I超敏感位点(DHSs),分析其基因组分布特征及与基因表达的关联,揭示冷胁迫下染色质开放状态的动态变化。
方法细节:使用自主开发的Popera软件(FDR<0.05)独立鉴定每个生物学重复中的DHSs,仅保留两个重复中共同存在的DHSs用于后续分析;通过计算DHSs在启动子、外显子、内含子、基因间区等基因组特征区域的分布比例,采用z检验比较室温与冷处理块茎间的分布差异;结合RNA-seq数据,分析温度特异性DHSs与差异表达基因的关联程度。
结果解读:室温块茎中鉴定到50531个DHSs,冷处理块茎中鉴定到61986个,叶片中鉴定到81603个;DHSs在染色体上富集于远端区域,着丝粒区域分布较少,且与基因密度呈正相关(Pearson相关系数r=0.82,p<2.2e-16),与转座子密度呈负相关(r=-0.68,p<2.2e-16)。冷处理块茎中外显子和内含子区域的DHSs比例(14.2%、11.8%)约为室温块茎的2倍(7.7%、6.1%,z检验p<0.0002),且冷特异性基因区DHSs对应的7314个基因中,69%为差异表达基因,以上调为主(中位倍数变化1.7,Wilcoxon秩和检验p=1.15e-15);进一步分析显示,基因区DHSs与温度响应的差异表达基因关联更显著,而非基因区DHSs与组织特异性表达基因关联更显著。
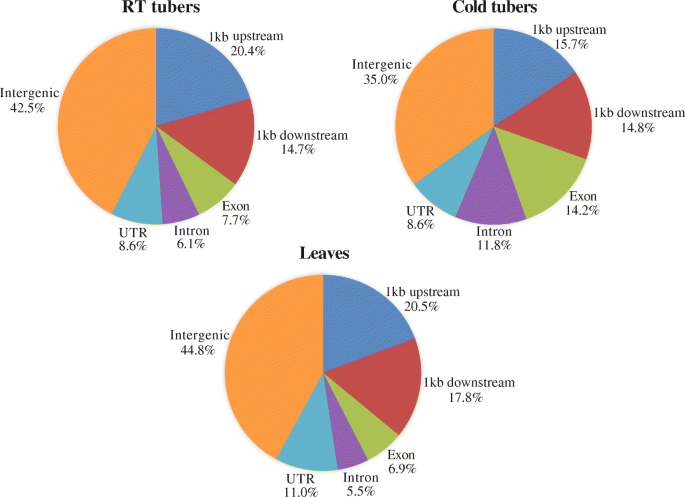
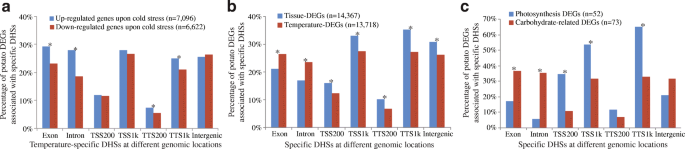
产品关联:文献未提及具体实验产品,领域常规使用DNase I、脉冲场凝胶电泳系统等试剂与仪器。
3.3 冷胁迫下染色质可及性与组蛋白修饰动态分析
实验目的:分析冷胁迫下不同表达水平基因的染色质可及性变化,检测组蛋白修饰的动态分布特征,揭示染色质状态与组蛋白修饰的协同变化规律。
方法细节:将基因按表达水平(FPKM)分为不同组别,比较室温与冷处理块茎中基因区域及侧翼区域的DNase I敏感性差异;通过ChIP-seq检测H3K27me3、H3K4me3、H4K5,8,12,16ac等组蛋白修饰的分布模式,采用Wilcoxon秩和检验比较不同样本间的修饰水平差异。
结果解读:冷胁迫下,在室温与冷处理中均表达的基因(FPKM>1)的基因体区域DNase I敏感性显著升高(Wilcoxon秩和检验p<2.2e-16),而启动子和终止子区域的敏感性则有所降低;冷处理块茎中,活性基因的基因体区域显著富集H3K27me3,其水平显著高于组成型沉默基因(p<2.2e-16),而室温块茎中活性基因的H3K27me3水平与基因间区相似;H3K4me3在冷处理块茎中从基因5"端向基因体中部广泛分布,且在组成型沉默基因中也出现沉积;H4K5,8,12,16ac的分布模式与H3K4me3类似,但未在组成型沉默基因中检测到沉积。
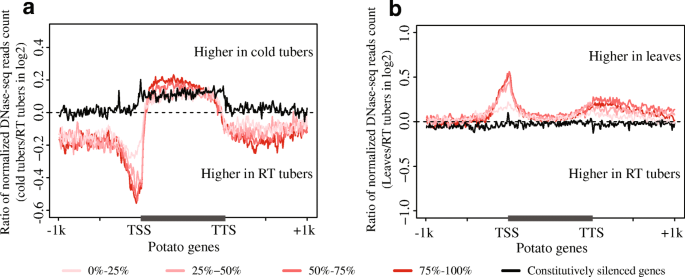
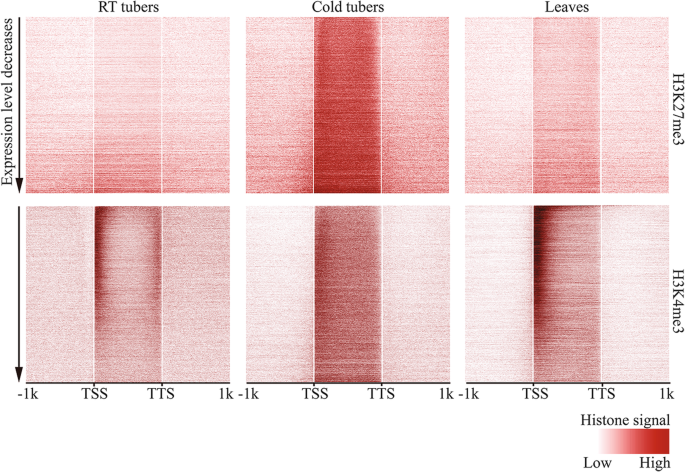
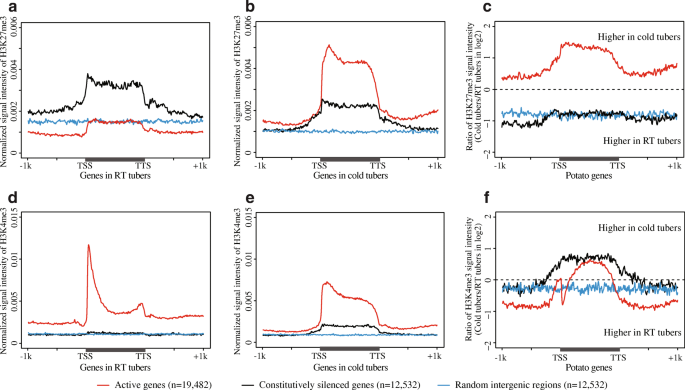
产品关联:实验所用关键产品:H3K27me3抗体(Millipore 07-449)、H3K4me3抗体(Abcam 8580)、H4K5,8,12,16ac抗体(Millipore 06-598)。
3.4 双价组蛋白修饰的验证与功能分析
实验目的:验证冷胁迫下活性基因中H3K4me3与H3K27me3双价修饰的存在,分析其与基因表达及功能的关联,揭示双价修饰在冷胁迫响应中的调控作用。
方法细节:采用Sequential ChIP-seq技术,先使用H3K4me3抗体免疫沉淀,再使用H3K27me3抗体进行二次沉淀,同时设置反向顺序沉淀作为对照,验证两种修饰在同一核小体上的共定位;分析双价修饰关联基因的表达水平变化,通过BLASTp比对拟南芥同源基因,使用agriGO工具进行Gene Ontology(GO)功能富集分析;比较双价修饰关联基因与其他活性基因的染色质可及性差异。
结果解读:Sequential ChIP-seq结果证实,冷处理块茎中6442个活性基因(占总活性基因的33%)的基因体区域存在H3K4me3与H3K27me3的双价修饰;这些基因中,47.5%在冷胁迫下上调表达,31%下调表达,21.5%组成型表达,双价修饰的信号强度与基因表达变化的方向无关;GO功能富集分析显示,上调的双价修饰关联基因主要富集于胁迫响应相关功能,而下调的基因则富集于发育过程;与其他活性基因相比,双价修饰关联基因的染色质可及性在冷胁迫下的升高幅度显著更高(Wilcoxon秩和检验p<2.2e-16)。
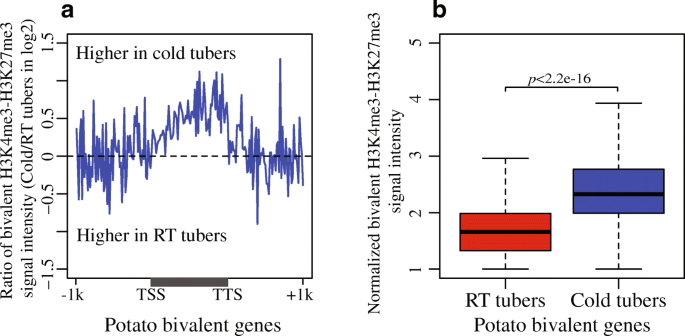
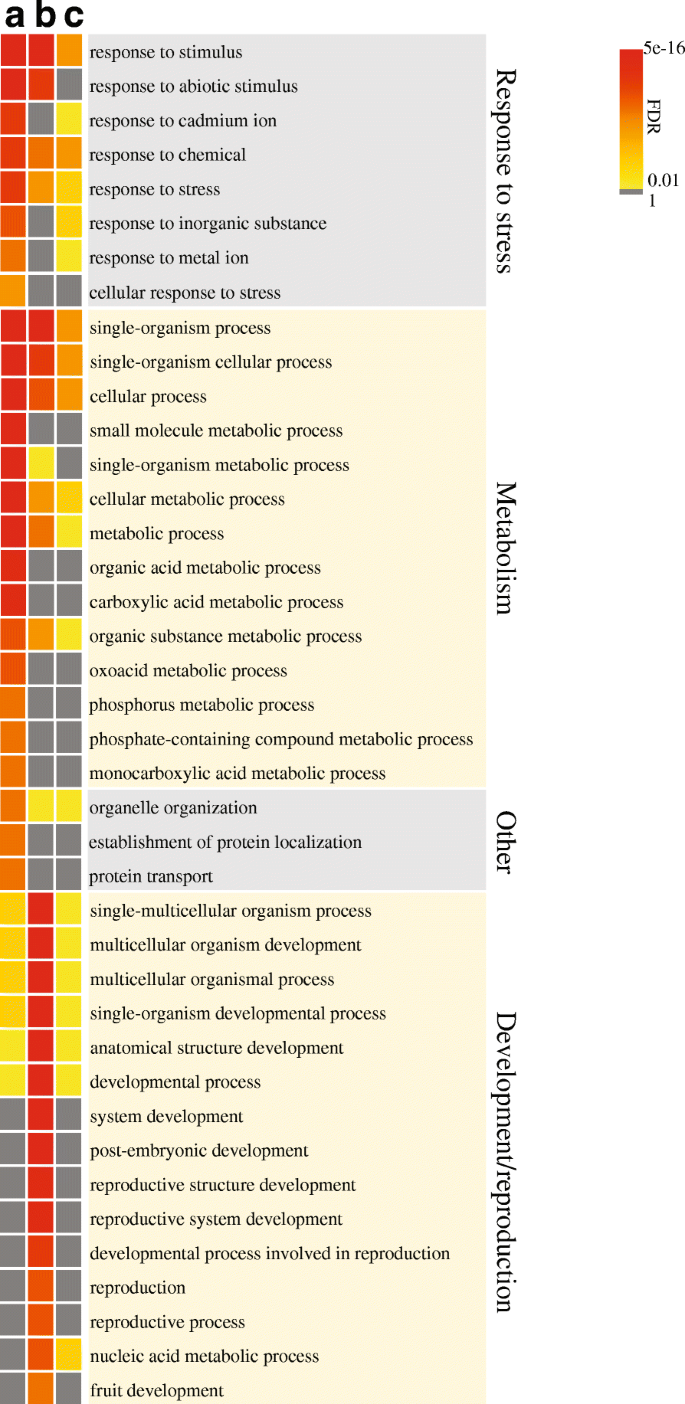
产品关联:实验所用关键产品:Re-ChIP-IT kit(Active Motif, Cat # 53016)、H3K4me3抗体(Abcam 8580)、H3K27me3抗体(Millipore 07-449)。
3.5 冷胁迫响应的表观调控模型构建
实验目的:整合所有实验结果,构建冷胁迫下马铃薯块茎染色质动态与基因表达的调控模型,系统阐释表观遗传修饰在冷胁迫响应中的作用机制。
方法细节:基于染色质可及性、组蛋白修饰及基因表达的关联分析结果,总结冷胁迫下马铃薯块茎的表观调控规律,提出可视化调控模型。
结果解读:提出的调控模型显示,在室温条件下,活性基因的启动子区域染色质处于开放状态,基因5"端富集H3K4me3,而基因体区域染色质关闭且无H3K27me3沉积;当遭遇冷胁迫时,活性基因的基因体区域染色质可及性增强,同时沉积H3K4me3与H3K27me3双价修饰,其中H3K4me3有助于维持染色质的开放状态,H3K27me3则通过与Polycomb-group(PcG)蛋白(如LHP1)互作,根据基因的功能特性调控其上调或下调,从而实现对冷胁迫的响应。
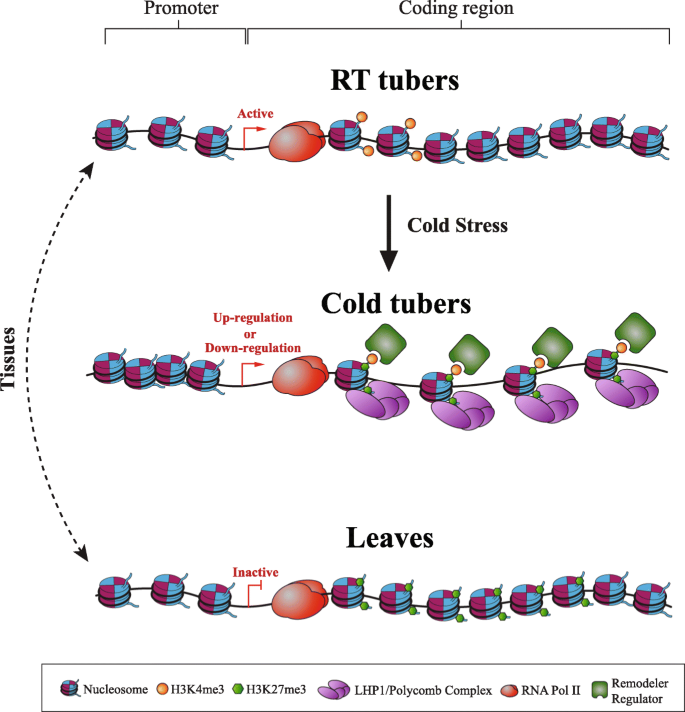
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析软件(如R、Perl等)进行数据整合与模型构建。
4. Biomarker研究及发现成果解析
本研究鉴定的表观遗传Biomarker包括冷诱导的基因区DNase I超敏感位点(DHSs)和H3K4me3/H3K27me3双价组蛋白修饰,这些标记可作为马铃薯冷胁迫响应的表观调控指标,为作物胁迫响应的分子机制研究及遗传改良提供新的靶点。
Biomarker定位:明确Biomarker类型分为两类,一类是染色质开放标记(冷特异性基因区DHSs),另一类是组蛋白修饰标记(H3K4me3/H3K27me3双价修饰);筛选与验证逻辑为:通过DNase-seq全基因组筛选冷胁迫下特异性出现的基因区DHSs,利用ChIP-seq检测组蛋白修饰的全基因组变化,采用Sequential ChIP-seq验证H3K4me3与H3K27me3在同一核小体上的共定位,结合RNA-seq数据关联其与基因表达功能的关系,形成完整的筛选与验证链条。
研究过程详述:Biomarker的来源为马铃薯块茎经4℃冷处理14天后的染色质样本;验证方法包括:DNase-seq鉴定冷特异性DHSs的存在,ChIP-seq定量组蛋白修饰的富集水平,Sequential ChIP-seq证实双价修饰在同一核小体上的共定位;特异性与敏感性方面,冷特异性基因区DHSs与冷胁迫差异表达基因的关联率达69%,其中上调基因的中位倍数变化为1.7(Wilcoxon秩和检验p=1.15e-15),双价修饰关联基因中47.5%为冷上调的胁迫响应基因,31%为冷下调的发育基因,具有明确的功能特异性。
核心成果提炼:该Biomarker的功能关联为:冷特异性基因区DHSs作为顺式调控元件的富集区域,直接调控冷胁迫下差异表达基因的表达;H3K4me3/H3K27me3双价修饰作为冷胁迫响应的表观调控标记,通过调控染色质可及性和基因表达,参与马铃薯块茎中胁迫响应基因的激活和发育基因的抑制;创新性在于首次在植物冷胁迫响应中发现活性基因广泛存在H3K4me3/H3K27me3双价修饰,且该修饰与染色质可及性增强密切相关,打破了传统认为双价修饰仅存在于静息状态基因的认知,为作物胁迫响应的表观调控机制提供了新的范式;统计学结果显示,双价修饰关联基因占活性基因的33%(n=6442/19482),冷上调基因中双价修饰关联基因的比例为47.5%(n=3064/6442),Wilcoxon秩和检验证实双价修饰关联基因的染色质可及性升高幅度显著高于其他活性基因(p<2.2e-16)。
