1. 领域背景与文献引入
文献英文标题:Connective Tissue Growth Factor (CTGF/CCN2) enhances lactogenic differentiation of mammary epithelial cells via integrin-mediated cell adhesion;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:乳腺上皮细胞泌乳分化调控
领域共识:乳腺腺泡发育与泌乳分化是多因素协同调控的复杂过程,既受催乳素、糖皮质激素等系统性激素的调控,也依赖乳腺上皮细胞与细胞外基质、局部生长因子的相互作用。其中,β1整合素介导的细胞-基质黏附是激活催乳素下游Stat5通路、诱导β-酪蛋白等泌乳相关基因转录的关键环节。前期研究发现,结缔组织生长因子(CTGF/CCN2)在乳腺泌乳分化过程中呈糖皮质激素依赖地上调,且瞬时过表达CTGF可促进β-酪蛋白转录,但CTGF调控乳腺上皮细胞泌乳分化的具体分子机制尚未明确,尤其是其与整合素信号通路的关联仍需深入解析。本研究针对这一空白,通过构建可诱导的CTGF过表达细胞模型,系统解析了CTGF通过整合素介导的细胞黏附、存活信号调控泌乳分化的分子机制,为乳腺泌乳调控的研究提供了新的靶点与理论依据。
2. 文献综述解析
作者以乳腺泌乳分化的调控网络为核心,从激素信号、细胞外基质-整合素互作、局部生长因子三个维度梳理了领域内现有研究。现有研究已明确催乳素通过激活Jak2-Stat5通路直接调控β-酪蛋白等泌乳相关基因的转录,细胞外基质中的层粘连蛋白、胶原蛋白通过结合β1整合素复合物,激活黏着斑激酶(FAK)等下游信号,为Stat5通路的激活提供必要的细胞内环境;技术方法上,HC11小鼠乳腺上皮细胞系和MCF10A三维腺泡模型已成为模拟乳腺泌乳分化的经典体系,可在体外精准复现体内泌乳分化的关键表型。但现有研究仍存在局限性,即对局部生长因子如何协同细胞外基质-整合素信号调控泌乳分化的机制解析不足,尤其是CTGF作为泌乳分化过程中上调的关键生长因子,其具体作用靶点与信号传导路径尚未明确。
本研究通过构建四环素诱导的CTGF过表达细胞模型,首次明确CTGF可通过两种机制促进乳腺上皮细胞泌乳分化:一是直接结合α6β1整合素复合物,激活整合素介导的存活信号;二是诱导细胞外基质蛋白(如纤连蛋白、层粘连蛋白)的表达,增强整合素的功能活性。这一发现填补了CTGF调控乳腺泌乳分化机制的空白,为理解局部生长因子与细胞外基质信号的协同作用提供了新的实验证据。
3. 研究思路总结与详细解析
本研究的核心目标是解析CTGF促进乳腺上皮细胞泌乳分化的分子机制,围绕“CTGF是否通过整合素介导的细胞黏附调控泌乳分化”这一核心科学问题,采用“细胞模型构建→表型验证→信号通路解析→机制验证”的闭环技术路线,通过多维度实验明确了CTGF的作用靶点与调控路径。
3.1 四环素诱导CTGF过表达细胞系构建与泌乳分化表型验证
实验目的:构建可诱导的CTGF过表达HC11细胞系,验证CTGF对乳腺上皮细胞泌乳分化的促进作用。
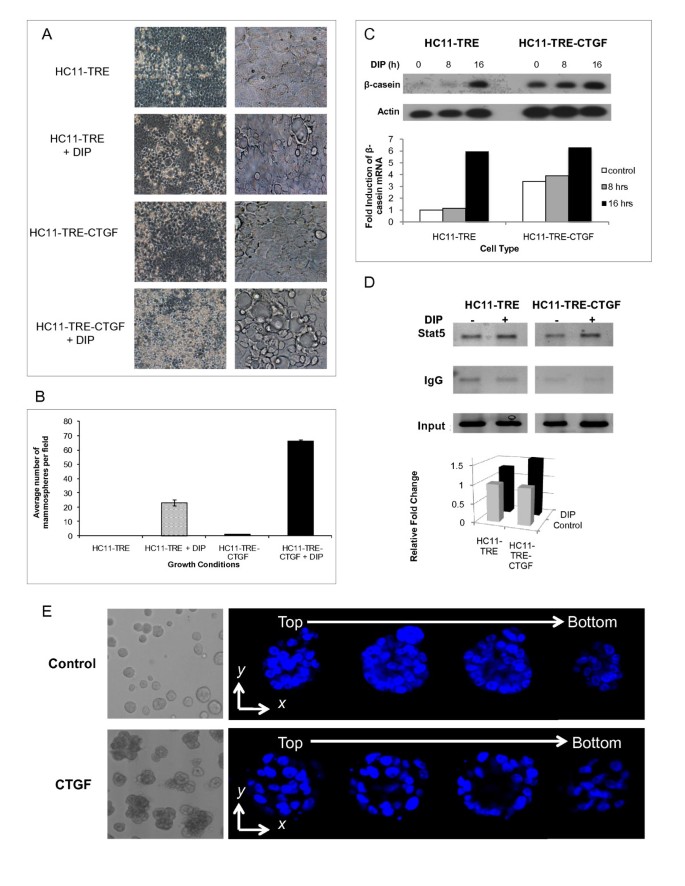
方法细节:利用四环素调控的表达系统,构建HC11-TRE-CTGF细胞系,通过去除培养基中的强力霉素诱导CTGF过表达;将细胞培养至汇合后,用含地塞米松、胰岛素、催乳素(DIP)的分化培养基处理5天,通过相差显微镜观察乳腺球形成并计数;在0、8、16小时提取细胞RNA,通过Southern blot检测β-酪蛋白转录水平;同时采用MCF10A细胞三维培养体系,在Matrigel中添加外源性CTGF(50 ng/ml),培养20天后通过共聚焦显微镜观察腺泡结构。
结果解读:HC11-TRE-CTGF细胞的乳腺球数量和大小均显著高于HC11-TRE对照组,5个低倍视野的平均乳腺球数量较对照组增加(n=5,P<0.05);DIP处理8小时后,HC11-TRE-CTGF细胞的β-酪蛋白转录水平较对照组显著上调,且在无DIP处理时也检测到低水平的β-酪蛋白表达;MCF10A细胞在CTGF处理后,腺泡数量和体积增加,且形成具有中空 lumen的极化腺泡结构,表明CTGF可促进三维培养体系中乳腺上皮细胞的分化。
产品关联:实验所用关键产品:Sigma的小鼠抗β-肌动蛋白抗体、Santa Cruz Biotechnology的山羊抗CTGF抗体、BD Biosciences的LSRII流式细胞仪、Promega的CellTiter96 MTT检测试剂盒、Roche的TUNEL凋亡检测试剂盒。
3.2 CTGF对细胞外基质依赖的β-酪蛋白转录的调控
实验目的:验证CTGF是否通过调控细胞外基质-细胞相互作用影响β-酪蛋白转录。
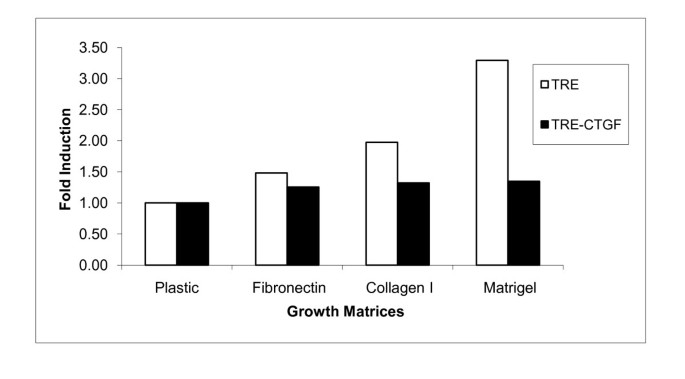
方法细节:将HC11-TRE和HC11-TRE-CTGF细胞接种于纤连蛋白、胶原蛋白I、Matrigel包被或未包被的培养板,在无血清条件下培养至汇合后,用DIP处理48小时;提取细胞总RNA,通过Northern blot检测β-酪蛋白转录水平,并以肌动蛋白为内参进行归一化分析。
结果解读:HC11-TRE对照组细胞在纤连蛋白、胶原蛋白I或Matrigel包被的培养板上,β-酪蛋白转录水平较未包被组上调3倍以上;而HC11-TRE-CTGF细胞在不同包被条件下,β-酪蛋白转录水平无显著差异,表明CTGF可部分替代外源性细胞外基质,降低乳腺上皮细胞对细胞外基质的依赖,从而促进β-酪蛋白转录。
产品关联:文献未提及具体细胞外基质包被试剂品牌,领域常规使用Corning的Matrigel基质胶、Sigma的纤连蛋白与胶原蛋白I试剂。
3.3 CTGF对HC11细胞增殖与存活的调控
实验目的:探究CTGF对乳腺上皮细胞增殖能力与存活信号的调控作用。
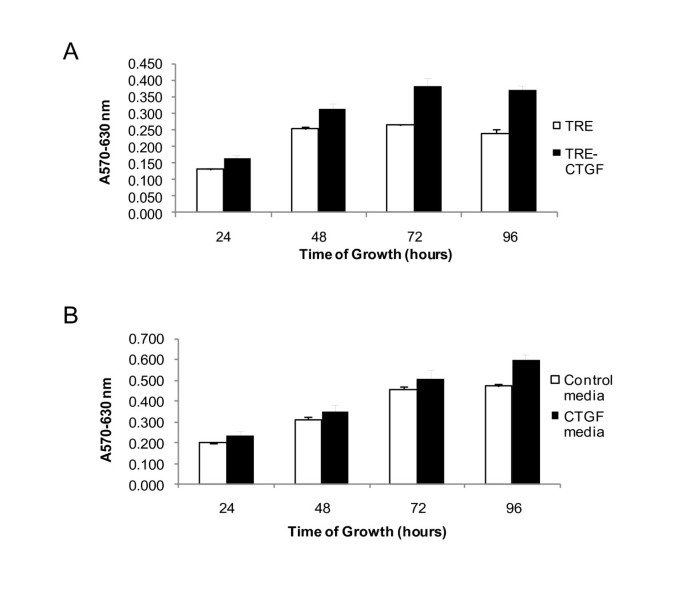
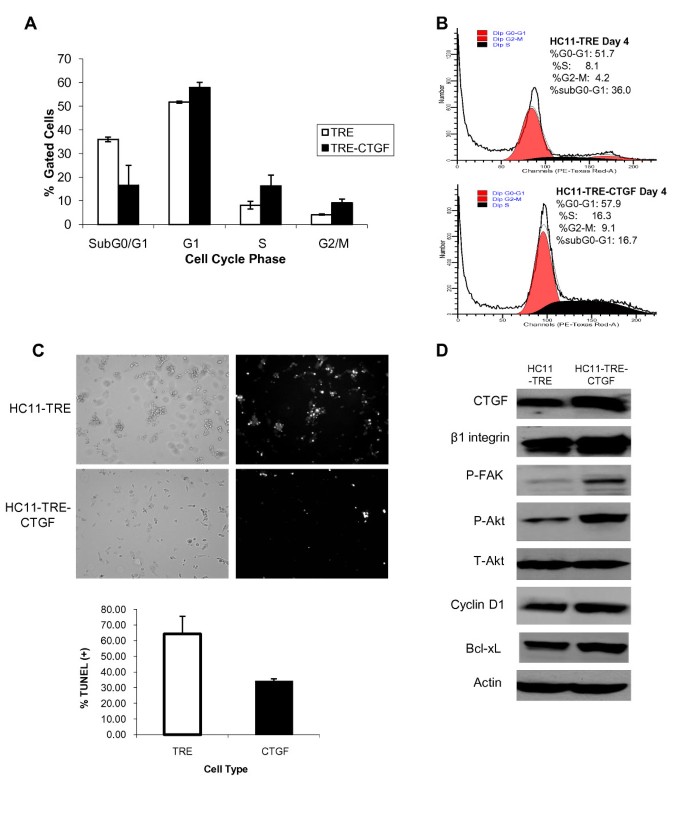
方法细节:采用MTT法检测无血清条件下HC11-TRE和HC11-TRE-CTGF细胞在24、48、72、96小时的增殖能力;收集HC11-TRE-CTGF细胞的无血清条件培养基,按1:1比例与新鲜无血清培养基混合处理HC11细胞,检测增殖变化;用流式细胞术分析96小时无血清培养后细胞的周期分布,TUNEL法检测细胞凋亡水平;提取细胞蛋白,通过Western blot检测β1整合素、磷酸化FAK、磷酸化Akt、Bcl-xL等存活相关蛋白的表达。
结果解读:HC11-TRE-CTGF细胞在无血清条件下的增殖能力显著高于对照组,96小时时吸光度值较对照组升高(n=4,P<0.005);CTGF条件培养基处理的HC11细胞增殖能力显著高于对照组条件培养基处理组,96小时时差异最显著(n=4,P<0.005);细胞周期分析显示,HC11-TRE-CTGF细胞的S期和G2/M期细胞比例高于对照组,而亚G0/G1期(凋亡)细胞比例低于对照组;TUNEL检测显示,对照组细胞的TUNEL阳性率显著高于CTGF过表达组;Western blot结果显示,CTGF过表达细胞中β1整合素、磷酸化FAK、磷酸化Akt、Bcl-xL和Cyclin D1的表达水平均显著上调。
产品关联:实验所用关键产品:BD Transduction的小鼠抗β1整合素抗体、Cell Signaling Technology的兔抗磷酸化Akt抗体、Santa Cruz Biotechnology的兔抗Bcl-xL抗体。
3.4 CTGF对整合素表达与功能的调控
实验目的:明确CTGF对整合素表达及细胞黏附功能的调控作用。
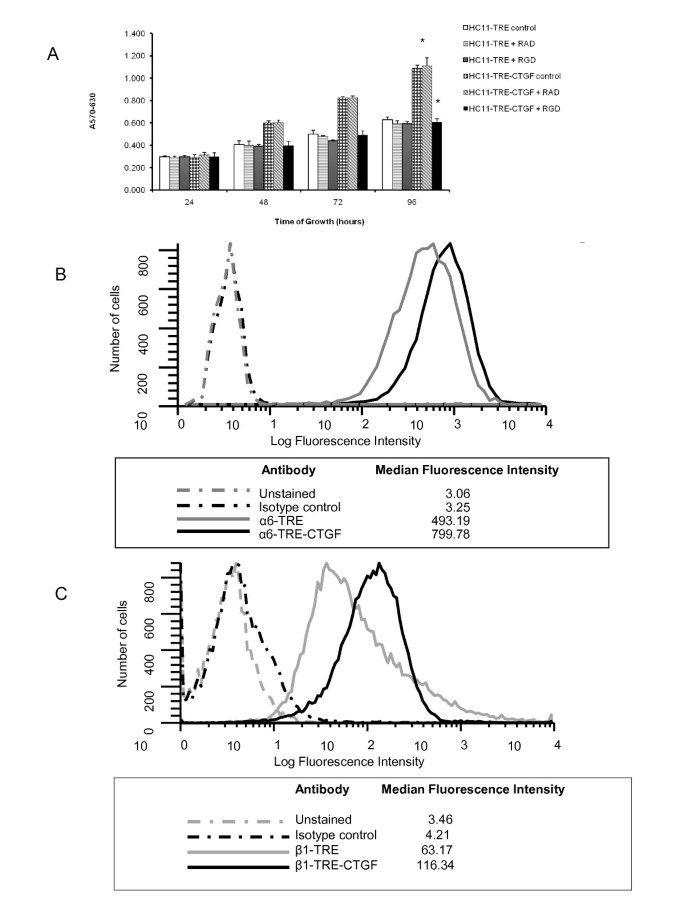
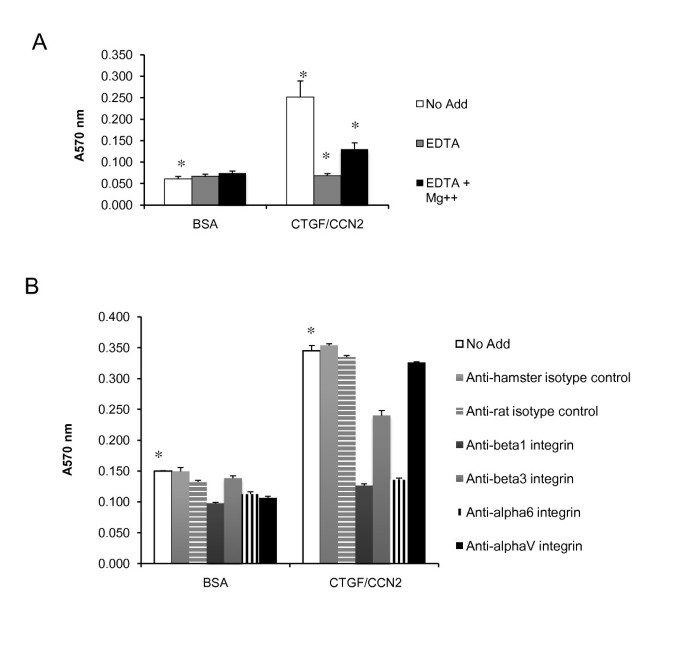
方法细节:在无血清培养基中添加RGD肽(整合素竞争性抑制剂)或RAD肽(对照肽),用MTT法检测细胞增殖变化;收集无血清培养4天的细胞,用抗β1整合素、抗α6整合素抗体染色,通过流式细胞术检测细胞表面整合素的表达水平;将HC11细胞接种于重组CTGF包被的培养板,添加EDTA、Mg²+或整合素阻断抗体,培养4小时后检测细胞黏附能力。
结果解读:RGD肽处理后,HC11-TRE-CTGF细胞的增殖能力下降38%,而RAD肽处理无显著影响,对照组细胞增殖仅下降7%(n=4,P<0.005);流式细胞术显示,HC11-TRE-CTGF细胞表面β1和α6整合素的表达水平显著高于对照组;HC11细胞可黏附于CTGF包被的培养板,EDTA可抑制该黏附,添加Mg²+可恢复黏附;抗α6或β1整合素抗体可完全阻断CTGF介导的细胞黏附,抗β3抗体部分阻断,抗αV抗体无显著作用。
产品关联:实验所用关键产品:BD Biosciences的抗β1、α6整合素抗体、Santa Cruz Biotechnology的抗αV、β3整合素抗体。
3.5 CTGF对黏着斑复合物形成的调控
实验目的:验证CTGF对乳腺上皮细胞黏着斑复合物形成的促进作用。
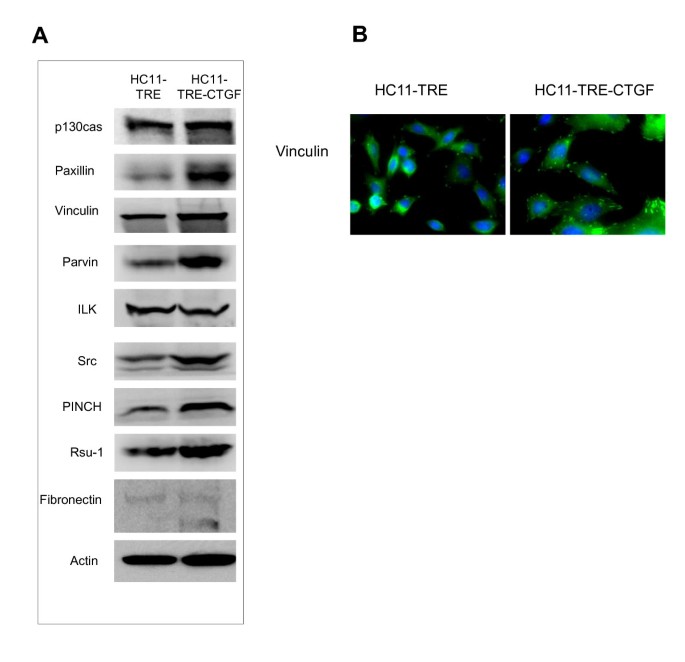
方法细节:提取HC11-TRE和HC11-TRE-CTGF细胞的蛋白,通过Western blot检测paxillin、p130CAS、vinculin、parvin等黏着斑相关蛋白的表达;将细胞接种于盖玻片,培养4天后用抗vinculin抗体染色,通过免疫荧光显微镜观察黏着斑的形态与数量。
结果解读:Western blot结果显示,CTGF过表达细胞中paxillin、p130CAS、vinculin、parvin、PINCH1、Rsu-1等黏着斑相关蛋白的表达水平均显著上调;免疫荧光染色显示,HC11-TRE-CTGF细胞的黏着斑数量更多、体积更大,表明CTGF可促进黏着斑复合物的形成与成熟。
产品关联:实验所用关键产品:Sigma的小鼠抗vinculin抗体、BD Transduction的小鼠抗PINCH1抗体、Invitrogen的AlexaFluor 488标记二抗。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为结缔组织生长因子(CTGF/CCN2),属于分泌型生长因子类Biomarker,其筛选与验证遵循“前期研究发现→细胞系功能验证→信号通路解析→临床相关模型验证”的完整逻辑链条。
CTGF是乳腺上皮细胞泌乳分化过程中糖皮质激素依赖上调的关键生长因子,本研究通过前期转录组学研究发现其在泌乳分化中的表达变化,随后通过细胞系过表达、外源性添加等实验验证其功能,并通过整合素阻断实验明确其作用靶点为α6β1整合素复合物。CTGF的来源为乳腺上皮细胞的分泌产物,验证方法包括四环素诱导的细胞系过表达、无血清条件培养基处理、MCF10A三维培养体系外源性添加;特异性数据显示,CTGF可特异性结合α6β1整合素复合物,抗α6或β1整合素抗体可完全阻断CTGF介导的细胞黏附;敏感性数据显示,低水平的CTGF表达即可诱导β-酪蛋白的转录(无DIP处理时仍可检测到低水平β-酪蛋白表达);ROC曲线等数据文献未明确提供。
CTGF作为乳腺上皮细胞泌乳分化的调控Biomarker,其功能关联为通过激活α6β1整合素介导的存活信号,促进细胞增殖与存活,并协同细胞外基质信号调控β-酪蛋白转录,最终促进泌乳分化;创新性在于首次明确CTGF通过直接结合整合素复合物与诱导细胞外基质蛋白表达的双重机制调控泌乳分化,为乳腺泌乳调控的研究提供了新的靶点;统计学结果显示,CTGF过表达组的乳腺球数量、β-酪蛋白转录水平、细胞增殖能力均显著高于对照组(n=4或5,P<0.05或P<0.005),细胞凋亡率显著低于对照组。
