1. 领域背景与文献引入
文献英文标题:CellSIUS provides sensitive and specific detection of rare cell populations from complex single-cell RNA-seq data;发表期刊:Genome Biology;影响因子:未公开;研究领域:单细胞RNA测序数据分析、稀有细胞类型鉴定、神经发育体外模型研究。
单细胞RNA测序(scRNA-seq)技术自2009年首次实现单个小鼠卵裂球的转录组分析以来,伴随商业化平台的普及与技术迭代,通量已从单个细胞提升至百万级细胞,成为解析复杂组织细胞异质性、发现新型及稀有细胞类型的核心技术。当前领域内已发展出涵盖无监督聚类、发育轨迹分析、差异表达分析等多类工具,但针对占比<1%的稀有细胞的精准鉴定仍存在方法学缺口:现有聚类方法在细胞比例失衡时性能显著下降,无法有效区分稀有细胞与背景噪声,且多数方法难以同步获取稀有细胞的功能相关转录组特征,限制了对稀有细胞在健康与疾病中功能的解析。
针对这一未解决的核心问题,本研究开发了CellSIUS(Cell Subtype Identification from Upregulated gene Sets)算法,通过“初始粗聚类+稀有亚群精细鉴定”的两步分析策略,实现对复杂单细胞RNA测序数据中稀有细胞类型的高灵敏度、高特异性鉴定,并同步输出其功能特征基因集,为领域内稀有细胞的研究提供了全新的技术范式。
2. 文献综述解析
作者通过构建已知细胞组成的基准单细胞RNA测序数据集,系统对比现有特征选择与聚类方法的性能,明确了稀有细胞鉴定中的方法学瓶颈,进而论证了CellSIUS算法研发的必要性与创新性。
现有单细胞RNA测序数据分析工具可分为细胞中心型与基因中心型两类,细胞中心型工具包括用于细胞类型鉴定的无监督聚类算法(如SC3、Seurat)、解析发育路径的轨迹分析工具(如Monocle)、针对稀有细胞的鉴定方法(如RaceID3、GiniClust2)等,基因中心型工具则以差异表达分析为主。特征选择方法中,基于均值-方差趋势的高变异基因(HVG)选择策略对低表达基因的捕获能力不足,而基于深度调整负二项模型的NBDrop方法能更有效保留与细胞类型相关的特征基因,对细胞类型方差的解释率可达47%。聚类方法在细胞比例均衡的数据集上表现较好,多数方法能实现完美聚类,但在包含占比<1%的稀有细胞的数据集上,所有方法均无法正确识别稀有细胞,仅DBSCAN能将其标记为离群点,但存在大量假阳性离群点的问题。现有稀有细胞鉴定工具中,RaceID3假阳性率高,易产生大量无意义小簇;GiniClust2采用双聚类融合策略,但对低丰度稀有细胞的检测灵敏度不足,且无法输出具有明确功能关联的特征基因集。
与现有方法相比,CellSIUS的核心创新在于通过强制特征基因的簇特异性有效规避技术噪声干扰,同时利用基因共表达网络分析直接输出稀有细胞的功能特征基因集,解决了现有方法“能鉴定稀有细胞但无法解析其功能”的缺陷;在合成与真实数据集的验证中,CellSIUS的灵敏度与特异性均显著优于RaceID3与GiniClust2,填补了稀有细胞精准鉴定与功能解析的方法学空白。
3. 研究思路总结与详细解析
本研究以“解决稀有细胞鉴定的方法学瓶颈”为核心目标,围绕“基准数据集构建→现有方法性能评估→CellSIUS算法开发→多数据集验证→神经发育模型应用”的闭环技术路线展开,通过系统的实验设计与计算分析,验证了CellSIUS在稀有细胞鉴定中的性能优势,并展示了其在解析复杂生物系统细胞异质性中的应用价值。
3.1 基准数据集构建与现有方法性能评估
实验目的:构建已知细胞组成的单细胞RNA测序基准数据集,系统评估现有特征选择与聚类方法的性能,明确稀有细胞鉴定的核心方法学缺口。
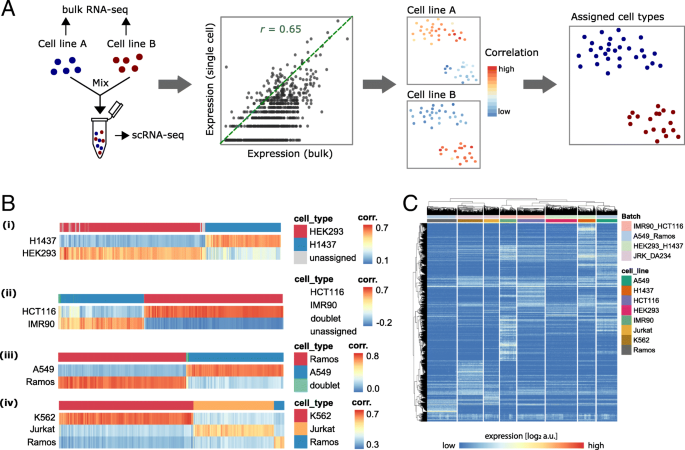
方法细节:选取8种人类细胞系(A549、H1437、HCT116、HEK293、IMR90、Jurkat、K562、Ramos),通过10X Genomics Chromium平台构建包含约12000个单细胞转录组的数据集,同时对每种细胞系进行bulk RNA测序作为细胞类型注释的金标准;构建模块化分析流程,涵盖质量控制、标准化、特征选择、聚类、标记基因鉴定五个模块,对比HVG、NBDisp、NBDrop三种特征选择方法对细胞类型方差的解释能力,随后选取7种聚类方法(SC3、Seurat、pcaReduce、hclust、mclust、DBSCAN、MCL)在细胞比例均衡的完整数据集、比例失衡的子集1(细胞占比2%-32%)、含极稀有细胞的子集2(稀有细胞占比<1%)中进行性能评估,通过调整兰德指数(ARI)衡量聚类结果与真实细胞类型注释的一致性。
结果解读:特征选择分析显示,NBDrop方法对细胞类型方差的解释率最高(47%),显著优于HVG的10%,而NBDisp方法选择的基因多为低表达基因,存在明显局限性;聚类方法在完整数据集上多数能实现完美聚类(ARI=1),但在子集2中,所有方法均无法正确识别占比<1%的稀有细胞,仅DBSCAN将其标记为离群点,但同时产生大量假阳性离群点,这一结果明确了现有方法在稀有细胞鉴定中的核心瓶颈。
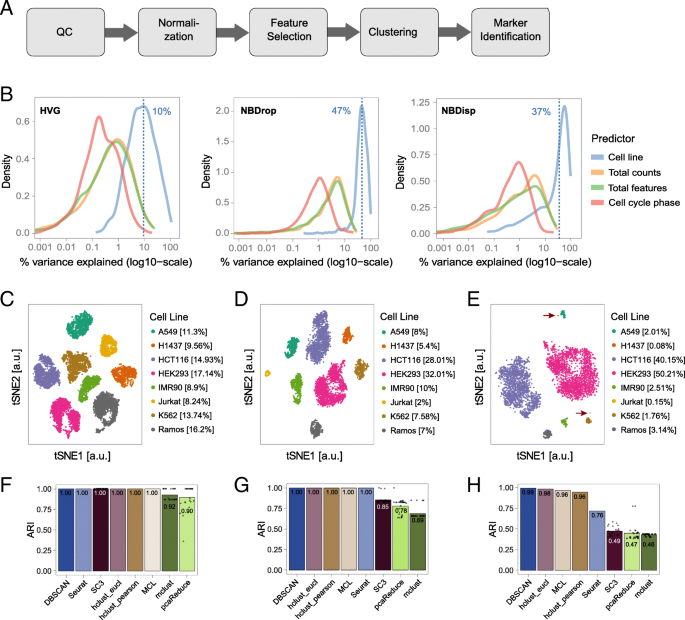
产品关联:实验所用关键产品:10X Genomics Chromium Single Cell平台、Illumina HiSeq2500测序平台、R语言scater、scran、M3Drop、irlba等分析包。
3.2 CellSIUS算法开发与合成数据集验证
实验目的:开发针对稀有细胞精准鉴定的CellSIUS算法,并在合成数据集中验证其灵敏度与特异性。
方法细节:CellSIUS算法采用五步分析流程:1)在初始粗聚类簇内通过一维k-means聚类识别具有双峰表达模式的候选标记基因,筛选标准为高低表达组的平均表达差异≥2倍(log2尺度)、高表达组占比<50%、两组表达差异显著(t检验校正P<0.1);2)验证候选基因的簇特异性,要求簇内高表达组与簇外非零表达组的平均表达差异≥2倍(log2尺度)且差异显著(t检验校正P<0.1);3)通过MCL算法构建基因共表达网络,识别共表达基因集;4)基于基因集的平均表达水平,通过一维k-means聚类将细胞分配至亚群;5)合并细胞亚群并保留包含≥3个特征基因的稀有亚群。合成数据集基于K562细胞的转录组参数生成,包含2个均一细胞群及占比0.2%-10%的稀有细胞群,对比CellSIUS与RaceID3、GiniClust2的召回率、精确率、真阴性率。
结果解读:在合成数据集中,CellSIUS对占比≥0.2%的稀有细胞召回率达100%,精确率与真阴性率均为100%;而RaceID3的召回率仅约50%,真阴性率为95%,精确率低至10%;GiniClust2无法检测到任何稀有细胞群。同时,CellSIUS的性能在较宽的参数范围内保持稳定,显示出良好的鲁棒性。
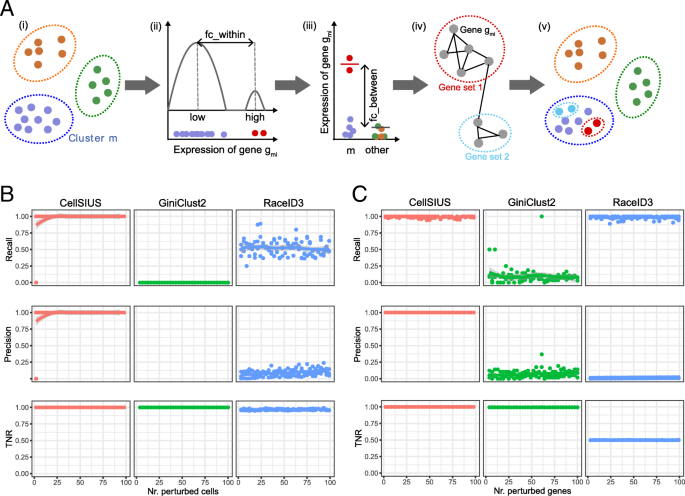
产品关联:文献未提及具体实验产品,领域常规使用R语言自定义算法包、MCL聚类工具。
3.3 细胞系数据集的CellSIUS性能验证
实验目的:在真实细胞系数据集中验证CellSIUS对不同稀有程度、转录组差异程度的稀有细胞的鉴定能力。
方法细节:从基准数据集中选取HEK293(100个细胞)、Ramos(100个细胞)作为丰度细胞群,Jurkat细胞(2、5、10个细胞)作为稀有细胞群,通过替换Jurkat细胞的部分基因表达值模拟其与Ramos细胞的转录组差异程度(替换率0-99.5%),生成包含不同稀有程度与转录组差异的数据集;采用固定初始聚类的策略,对比CellSIUS、RaceID3、GiniClust2的召回率与精确率。
结果解读:当稀有细胞占比低至0.08%(2个细胞)且转录组差异极小时(99.5%基因替换),CellSIUS仍能保持88.4%的平均精确率,显著高于GiniClust2的51.6%与RaceID3的15.6%;同时CellSIUS能输出具有明确功能关联的稀有细胞特征基因集,如Jurkat细胞的CD3G、CD3D(T细胞标记),H1437细胞的TFF1、BPIFA2(呼吸道上皮细胞标记),特征基因的表达模式与已知细胞类型功能完全一致。
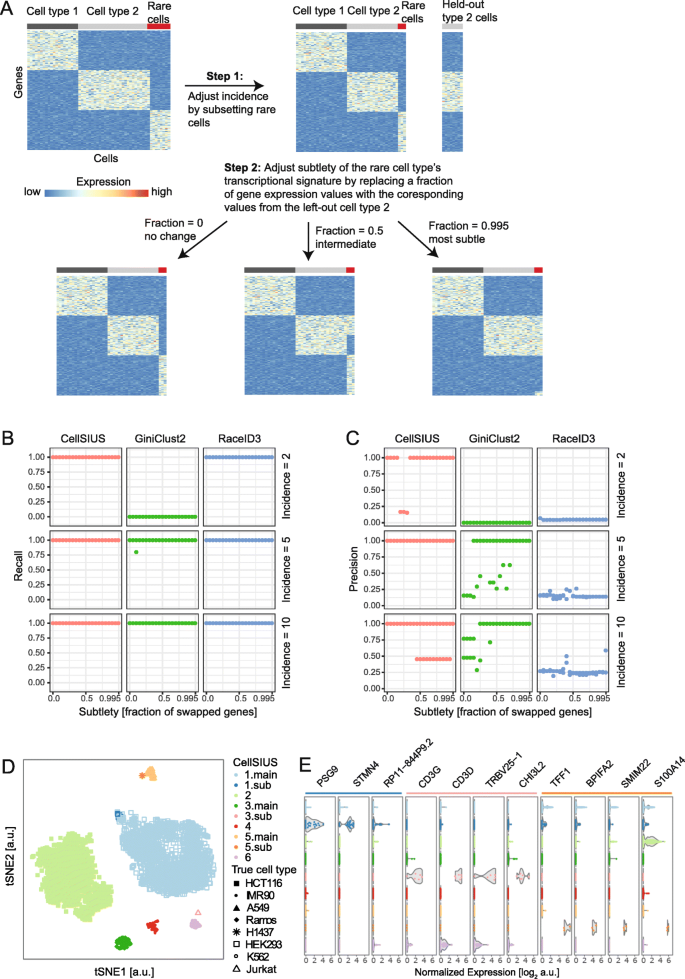
产品关联:实验所用关键产品:R语言CellSIUS、RaceID3、GiniClust2算法包。
3.4 人多能干细胞来源皮质神经元模型的CellSIUS应用
实验目的:在复杂神经发育体外模型中验证CellSIUS鉴定稀有细胞类型并解析其功能的能力。
方法细节:采用3D球体分化方案将H9人胚胎干细胞分化为皮质神经元,通过10X Genomics Chromium平台获取4857个单细胞转录组数据;先通过MCL算法进行初始粗聚类,再应用CellSIUS鉴定稀有细胞亚群;通过人类产前脑组织数据库(Harmonizome)的富集分析验证稀有脉络丛(CP)细胞特征基因的特异性,通过共聚焦显微镜检测TTR与PTGDS蛋白的共定位验证CP细胞的存在;采用Monocle算法进行发育轨迹分析,解析细胞分化路径。
结果解读:初始粗聚类识别出神经上皮祖细胞、神经元、胶质细胞、Cajal-Retzius细胞4类主要细胞群;CellSIUS进一步鉴定出7个稀有亚群,其中占比1.1%的CP细胞群包含10个特征基因,9个基因在人类产前CP组织中显著富集(标准化值≥1.3,校正P<0.05),共聚焦显微镜证实TTR与PTGDS蛋白在神经球外周细胞共定位;此外还鉴定出迁移状态Cajal-Retzius细胞群、周期活跃祖细胞群等稀有亚群;发育轨迹分析揭示了Cajal-Retzius细胞与V/VI层皮质神经元的分化分支点,为体外皮质发育模型的细胞异质性解析提供了新视角。
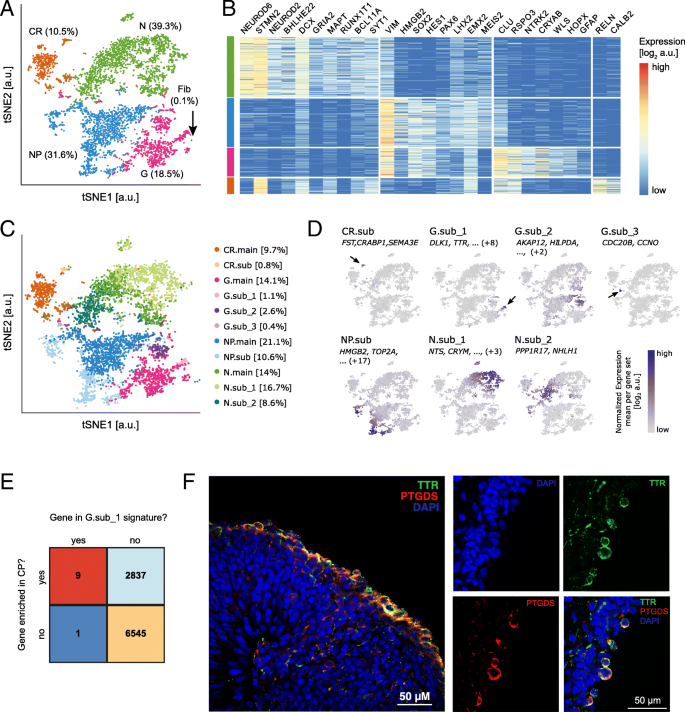
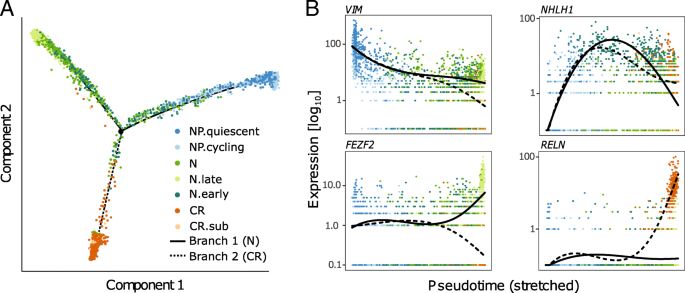
产品关联:实验所用关键产品:H9人胚胎干细胞系(WiCell)、10X Genomics Chromium平台、Olympus SD-OSR共聚焦显微镜、Transthyretin(TTR)抗体(Novus Biologicals, NBP2–52575)、Prostaglandin D2 synthase(PTGDS)抗体(Abcam, ab182141)、R语言Monocle分析包。
4. Biomarker研究及发现成果解析
本研究通过CellSIUS算法鉴定了多种稀有细胞类型的特征基因集,这些Biomarker具有明确的功能关联与细胞类型特异性,为稀有细胞的分离、功能研究及临床转化应用提供了核心靶点。
Biomarker定位
本研究中涉及的Biomarker为稀有细胞类型的特征基因集,涵盖T细胞、呼吸道上皮细胞、脉络丛细胞、迁移状态神经元、周期活跃祖细胞等多种稀有细胞类型;筛选与验证逻辑为“初始粗聚类→簇内双峰基因识别→簇特异性筛选→共表达基因集分析→细胞亚群分配→多数据集验证”,通过合成数据集、细胞系数据集、神经发育模型数据集的多轮验证,确保特征基因的特异性与灵敏度。
研究过程详述
这些Biomarker来源于人类细胞系单细胞转录组、人多能干细胞来源皮质神经元单细胞转录组;验证方法包括:1)合成数据集中通过模拟稀有细胞的特征基因高表达,验证CellSIUS的识别准确性;2)细胞系数据集中通过bulk RNA测序金标准验证特征基因的细胞类型特异性,差异表达倍数均≥2倍(校正P<0.1);3)神经发育模型中,CP细胞的9个特征基因在人类产前CP组织中显著富集(标准化值≥1.3,Benjamini-Hochberg校正P<0.05),共聚焦显微镜验证TTR与PTGDS蛋白在神经球外周细胞共定位,灵敏度达100%(所有CP细胞均被CellSIUS鉴定)。
核心成果提炼
本研究鉴定的稀有细胞特征基因集具有明确的功能关联:CP细胞特征基因与脑脊液分泌功能相关,迁移状态Cajal-Retzius细胞特征基因与神经元迁移调控相关,周期活跃祖细胞特征基因与细胞增殖调控相关;创新性在于首次在体外人多能干细胞皮质发育模型中发现并验证CP细胞群,且CellSIUS输出的特征基因集可直接用于稀有细胞的流式分选与功能研究;统计学结果显示,CP细胞群占比1.1%(n=4857,P<0.05,与其他细胞群的差异表达分析),所有特征基因的簇特异性表达差异均达2倍以上(校正P<0.1)。
