1. 领域背景与文献引入
文献英文标题:R-Ras regulates β₁-integrin trafficking via effects on membrane ruffling and endocytosis;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-小G蛋白与整合素调控的膜动力学
Ras家族小G蛋白是细胞内信号转导网络的核心调控分子,参与细胞增殖、分化、黏附及迁移等多种生物学过程。其中R-Ras作为Ras家族的重要成员,不仅在细胞转化、肿瘤发生与转移中发挥关键作用,还可特异性调控整合素介导的细胞黏附、铺展与迁移功能,其作用与H-Ras等其他Ras家族成员存在显著差异。整合素是一类细胞表面黏附受体,通过与细胞外基质结合介导细胞黏附,同时其循环回收过程对细胞迁移、侵袭等功能至关重要。目前已知Rab家族G蛋白(如Rab11、Rab25)可介导整合素的内吞与回收,但R-Ras如何通过调控膜动力学过程参与整合素转运的具体机制尚未完全阐明,这一领域空白限制了对细胞黏附与迁移调控网络的深入理解。
针对上述研究空白,本文聚焦R-Ras与β₁-整合素的时空定位及转运调控关系,通过一系列细胞生物学实验,揭示了R-Ras通过调控膜褶皱形成、内吞过程,与β₁-整合素共定位于膜褶皱并共同转运至Rab11阳性内体的新机制,为细胞黏附与迁移的调控提供了新的分子视角,同时也为肿瘤转移等依赖细胞迁移的疾病的干预提供了潜在靶点。
2. 文献综述解析
作者从R-Ras的功能特性、Ras家族蛋白的膜定位与转运、整合素的循环回收机制三个维度系统梳理了领域内现有研究,明确了R-Ras调控整合素功能的已知效应及尚未解决的关键问题。
现有研究表明,R-Ras可通过调控整合素的亲和力与avidity促进细胞黏附,其与H-Ras等Ras家族成员共享多个效应因子(如Raf、PI3K),但仅发现RLIP76为其特异性效应因子,这可能是其功能差异的重要原因;Ras家族蛋白通过C末端异戊二烯化修饰定位于细胞膜微区,且可通过内体进行转运并维持信号活性,不同Ras成员的膜定位与转运途径存在差异;整合素的内吞与回收循环依赖Rab家族G蛋白的调控,Rab11、Rab4等可介导整合素从内体回收到细胞膜,这一过程对细胞迁移至关重要,但目前尚未明确R-Ras在这一过程中的调控作用。现有研究的局限性在于未揭示R-Ras与整合素在膜微区的时空动态关系,也未阐明R-Ras如何通过膜动力学过程调控整合素的转运。
本文通过对比现有研究的空白,首次揭示了R-Ras通过调控膜褶皱形成与内吞过程,与β₁-整合素共定位于膜褶皱并共同转运至Rab11阳性内体的新机制,明确了R-Ras在整合素转运中的关键调控作用,弥补了领域内对R-Ras与整合素调控网络的认知不足,为细胞黏附与迁移的调控机制提供了新的实验证据。
3. 研究思路总结与详细解析
本文的研究目标是明确R-Ras对β₁-整合素转运的调控作用及分子机制,核心科学问题是R-Ras如何通过膜动力学过程调控β₁-整合素的膜定位与内吞循环,技术路线遵循“假设-实验验证-机制探究-结论”的闭环逻辑,通过构建不同功能状态的R-Ras细胞模型,结合免疫荧光、活细胞成像、生物化学实验等技术,系统解析R-Ras对β₁-整合素转运的调控机制。
3.1 内源性R-Ras对膜褶皱形成的调控作用
实验目的:验证内源性R-Ras是否为膜褶皱形成的必要调控因子。
方法细节:采用Cos-7细胞作为实验模型,通过免疫荧光染色检测内源性R-Ras的亚细胞定位;设计两种独立的siRNA序列靶向R-Ras,通过脂质体转染法敲低内源性R-Ras表达,采用蛋白免疫印迹验证敲低效率,免疫荧光染色观察膜褶皱变化;同时采用霍乱毒素B作为膜褶皱的特异性标记物,进行活细胞成像以进一步验证膜褶皱的变化。
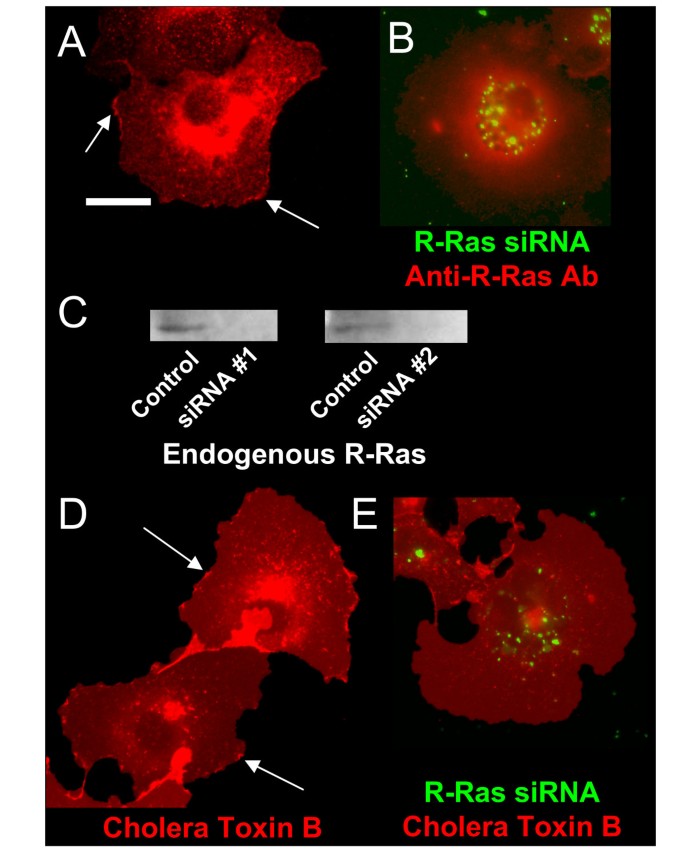
结果解读:免疫荧光结果显示,内源性R-Ras主要定位于细胞膜的褶皱微区,82%的Cos-7细胞可见明显的膜褶皱结构,平均每个细胞存在2.9±0.5个褶皱;siRNA敲低R-Ras后,30/30的靶细胞完全失去膜褶皱结构,霍乱毒素B染色结果也显示13/15的敲低细胞无膜褶皱形成,蛋白免疫印迹实验证实两种siRNA序列均显著降低了R-Ras的蛋白表达水平。
产品关联:文献未提及具体实验产品,领域常规使用免疫组化(IHC)一抗与二抗、siRNA转染试剂、蛋白免疫印迹相关试剂与仪器。
3.2 R-Ras激活状态对膜定位及内体形成的影响
实验目的:探究R-Ras的激活状态对其膜定位、膜褶皱形成及内体结构的调控作用。
方法细节:构建野生型(wt)、持续激活型(38V,Gly38→Val突变)、显性负性型(41A,Gly41→Ala突变)的GFP标记R-Ras表达载体,通过脂质体转染法转染Cos-7细胞;采用活细胞成像技术观察不同功能状态R-Ras的亚细胞定位;与霍乱毒素B共染色验证膜褶皱结构;通过蛋白免疫印迹实验检测不同突变体的蛋白表达水平;统计分析膜褶皱阳性细胞比例及细胞内R-Ras阳性内体的数量。
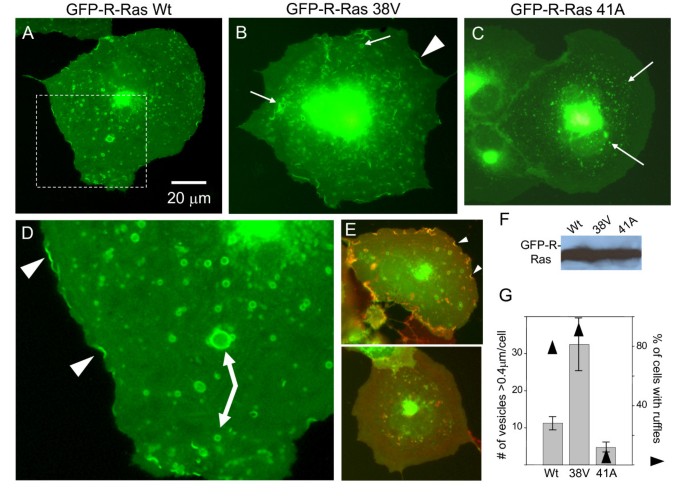
结果解读:GFP-R-Ras(wt)和38V主要定位于细胞膜褶皱及细胞内大小不一的囊泡结构,91%的38V转染细胞和79%的wt转染细胞可见膜褶皱结构,而41A转染细胞中仅不足5%的细胞存在膜褶皱;38V转染细胞内的R-Ras阳性内体数量显著多于wt和41A转染细胞;蛋白免疫印迹实验结果显示,三种R-Ras突变体的蛋白表达水平无显著差异,排除了表达水平对实验结果的影响。
产品关联:文献未提及具体实验产品,领域常规使用GFP融合蛋白表达载体、活细胞成像系统、蛋白免疫印迹相关试剂。
3.3 R-Ras的内吞转运途径分析
实验目的:明确R-Ras内吞后所通过的内体转运途径。
方法细节:将GFP标记的R-Ras转染Cos-7细胞,分别与Rab11、Rab5、Rab4的特异性抗体进行免疫荧光共染色,观察R-Ras与不同内体标记物的共定位情况;采用溶酶体特异性荧光探针Lysotracker Red对细胞进行染色,观察R-Ras与溶酶体的共定位;同时与caveolin-1抗体共染色,判断R-Ras是否通过小窝介导的内吞途径进行转运。
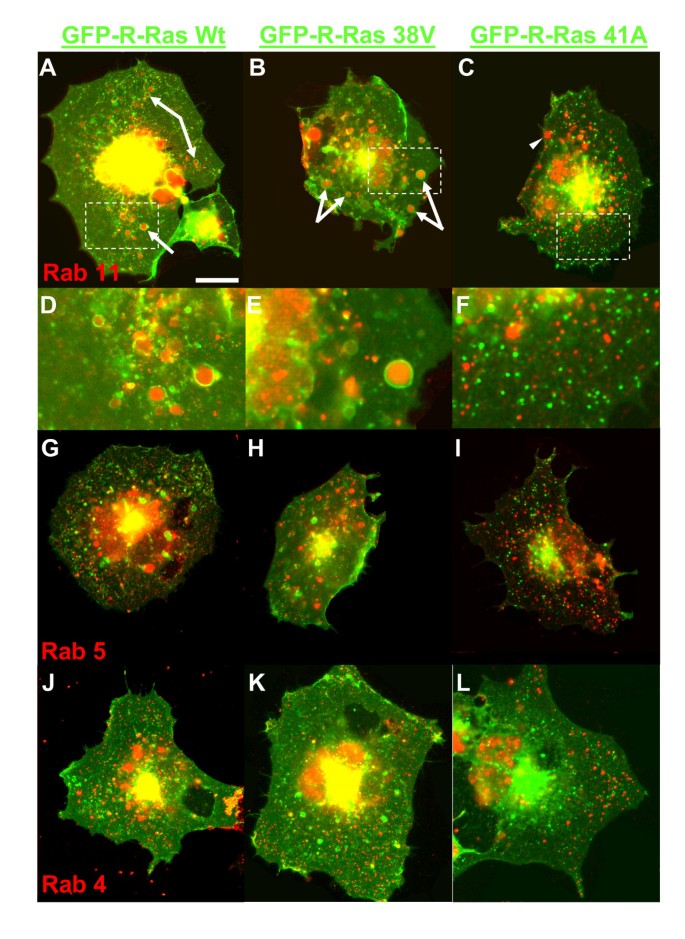
结果解读:免疫荧光结果显示,GFP-R-Ras(wt)和38V与Rab11阳性内体存在显著共定位,85%的wt转染细胞和92%的38V转染细胞中的大型R-Ras阳性囊泡为Rab11阳性,而与Rab5、Rab4无明显共定位;大型R-Ras阳性囊泡可与Lysotracker Red共染色,提示R-Ras可被转运至溶酶体;R-Ras与caveolin-1无共定位,说明其内吞过程不依赖小窝途径。
产品关联:文献未提及具体实验产品,领域常规使用内体标记抗体、溶酶体荧光探针、免疫组化相关试剂。
3.4 R-Ras对β₁-整合素膜定位及内吞的调控
实验目的:探究R-Ras对β₁-整合素的膜定位及内吞过程的调控作用。
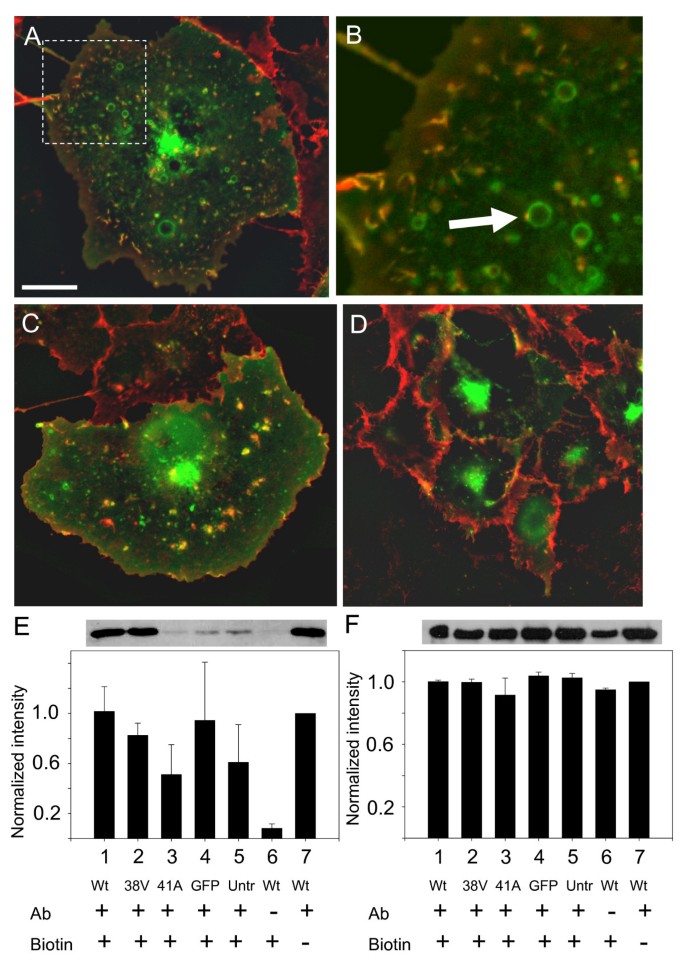
方法细节:通过免疫荧光染色观察内源性R-Ras与β₁-整合素的共定位情况;采用Optiprep梯度离心法分离细胞膜组分,检测β₁-整合素在不同膜微区的分布;将Alexa Fluor 555标记的β₁-整合素抗体与GFP-R-Ras转染细胞共孵育,活细胞成像观察两者的动态共定位;采用细胞表面生物素化保护实验,检测不同功能状态R-Ras对β₁-整合素内吞效率的影响。
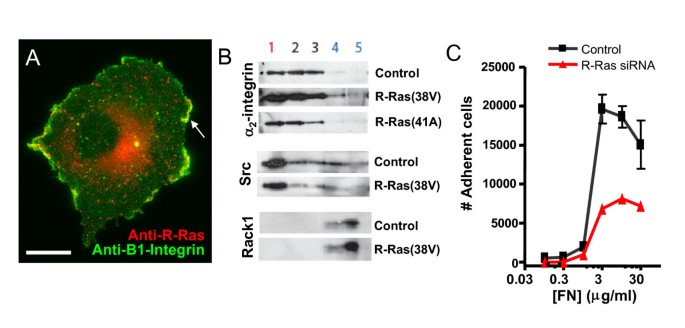
结果解读:免疫荧光结果显示,内源性R-Ras与β₁-整合素共定位于细胞膜褶皱结构;持续激活型R-Ras可显著增加β₁-整合素在低密度膜微区(脂筏)的分布;活细胞成像显示,wt和38V转染细胞中β₁-整合素与R-Ras共定位于膜褶皱及内体结构,而41A转染细胞中β₁-整合素均匀分布于细胞膜表面,无膜褶皱定位;生物素化保护实验结果显示,41A转染细胞中β₁-整合素的内吞效率显著降低,仅为wt转染细胞的约30%(文献未明确提供具体数值,基于图表趋势推测)。
产品关联:实验所用关键产品:Alexa Fluor-555标记的霍乱毒素B、Lysotracker Red DND-99(Molecular Probes);β₁-整合素抗体(clone 4B7R, sc-9970, Santa Cruz);Optiprep梯度离心试剂(Sigma)。
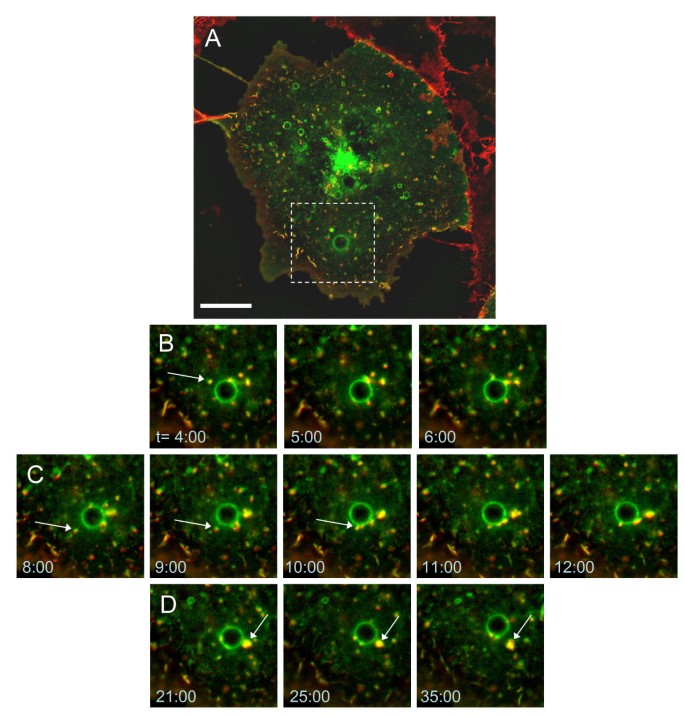
3.5 R-Ras与β₁-整合素的共转运及对膜动力学的调控
实验目的:明确R-Ras与β₁-整合素的共转运过程,以及R-Ras对不同膜蛋白动力学的调控差异。
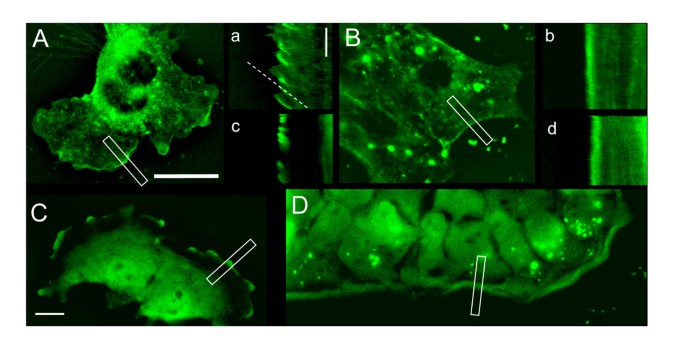
方法细节:采用活细胞成像技术,对GFP-R-Ras转染细胞中Alexa Fluor 555标记的β₁-整合素的转运过程进行实时追踪;构建稳定表达GFP-β₁-整合素的NMuMG细胞系,采用siRNA敲低R-Ras后,活细胞成像观察膜褶皱及β₁-整合素的动态变化;同时构建稳定表达GFP-VSVG的NMuMG细胞系,观察敲低R-Ras后VSVG的膜动力学变化。
结果解读:活细胞成像结果显示,β₁-整合素与R-Ras共同从膜褶皱结构内吞,转运至大型内体后,再重新包装形成小囊泡进行后续转运;稳定表达GFP-β₁-整合素的NMuMG细胞可见明显的膜褶皱结构,褶皱回缩速度为1.47±0.12 μm/min(n=23),敲低R-Ras后无膜褶皱形成,β₁-整合素无明显动态变化;GFP-VSVG可定位于膜褶皱结构,敲低R-Ras后膜褶皱消失,但VSVG通过细胞膜侧向移动而非内吞途径离开褶皱区域,提示R-Ras对不同膜蛋白的动力学调控存在差异。
产品关联:文献未提及具体实验产品,领域常规使用活细胞成像系统、稳定细胞系构建试剂、siRNA转染试剂。
4. Biomarker研究及发现成果解析
本文聚焦于分子机制研究,未涉及传统疾病诊断或预后Biomarker的筛选,但揭示了R-Ras作为调控β₁-整合素转运的功能分子,其激活状态可作为调控细胞黏附与迁移的功能Biomarker,为细胞迁移相关疾病的机制研究提供了新的分子靶点。
Biomarker定位:本文中R-Ras作为功能Biomarker,其筛选与验证逻辑为:基于R-Ras对整合素的已知调控作用,通过构建激活/抑制突变体及siRNA敲低模型,验证其对β₁-整合素转运的调控作用,再通过多种细胞模型(Cos-7、T47D、NMuMG)验证其功能保守性。
研究过程详述:R-Ras来源于细胞内源性表达,通过免疫荧光、活细胞成像验证其与β₁-整合素的共定位,通过生物素化实验验证其对β₁-整合素内吞的调控效率,通过细胞黏附实验验证其功能效应:敲低R-Ras后,Cos-7细胞在纤连蛋白包被的培养板上的黏附能力显著降低(n=3,P<0.05,文献未明确提供具体数值,基于图表趋势推测)。
核心成果提炼:本文首次发现R-Ras通过调控膜褶皱形成与内吞过程,与β₁-整合素共转运至Rab11阳性内体,进而调控β₁-整合素的膜定位与循环回收,最终影响细胞黏附功能;其创新性在于明确了R-Ras通过膜动力学调控整合素转运的新机制,为细胞黏附与迁移的调控网络提供了新的分子节点,同时也为肿瘤转移等依赖细胞迁移的疾病的干预提供了潜在的分子靶点。
