1. 领域背景与文献引入
文献英文标题:Liver organoid culture methods;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肝脏类器官培养与再生医学
领域共识:类器官技术自2009年肠道类器官成功构建以来,已成为生命科学领域的核心研究方向之一,3D类器官能够精准模拟体内组织的结构、细胞异质性及微环境相互作用,有效弥补了传统2D细胞培养和动物模型的局限性。慢性肝病研究长期受限于人类样本稀缺、体外模型无法精准复现生理微环境的问题,动物模型存在种属差异、伦理争议及成本高昂的缺陷,2D细胞培养则无法模拟体内细胞间的相互作用与器官复杂结构。2022年12月美国FDA发布《FDA现代化法案2.0》,明确新药无需强制进行动物实验,推动了非动物模型的研发进程,而肝作为人体主要的代谢与解毒器官,肝类器官成为药物代谢、毒性测试及肝病机制研究的理想替代模型。然而当前肝类器官培养体系存在重复性差、缺乏标准化的核心问题,不同研究在细胞来源、培养基成分、3D培养技术上差异显著,尤其是培养基成分的选择存在诸多争议,严重制约了肝类器官的临床转化与大规模应用。在此背景下,本文系统总结近10年肝类器官的培养方法,重点分析培养基争议成分的作用机制与应用场景,旨在为肝类器官培养体系的标准化提供关键参考,推动其在生物医药领域的广泛应用。
2. 文献综述解析
本文综述以肝类器官的细胞来源和培养体系为核心分类维度,系统梳理了多能干细胞(PSC)来源和肝组织来源肝类器官的培养方法,重点围绕培养基成分的功能与争议展开评述。
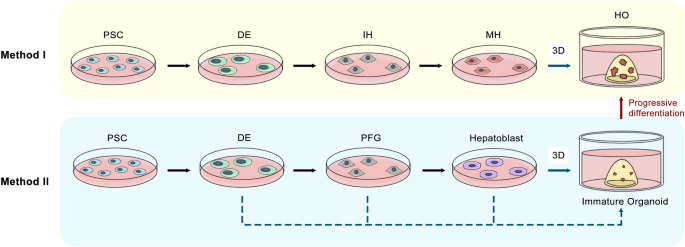
现有研究中,PSC来源肝类器官主要通过两种方法构建,一是先诱导PSC分化为成熟肝细胞再进行3D培养,二是在分化早期形成球状体后进一步分化为成熟类器官,这类类器官具有无限增殖能力,适合大规模药物筛选和疾病建模,但存在遗传和表观遗传异常的局限性;肝组织来源肝类器官包括肝细胞类器官和胆管细胞类器官,通过胶原酶灌注或消化获取原代细胞后进行3D培养,这类类器官遗传稳定性高,细胞功能更接近体内肝脏组织,但成人肝细胞类器官的长期培养难度较大。技术方法上,Matrigel作为常用的细胞外基质(ECM)支持类器官3D结构形成,但其存在成分复杂、批次间差异大的问题;培养基中的核心成分如R-spondin1、表皮生长因子(EGF)、肝细胞生长因子(HGF)等被证实具有明确的促增殖作用,但部分成分如毛喉素(FSK)、肿瘤坏死因子-α(TNF-α)的作用在不同研究中存在争议,应用场景尚未明确。
本研究的创新价值在于,首次系统整合了近10年肝类器官培养的培养基成分数据,针对争议成分的作用机制、应用场景及潜在风险进行对比分析,填补了领域内对培养体系标准化参考的空白,为后续肝类器官的临床转化应用提供了关键依据,同时为优化培养体系、降低成本提供了方向。
3. 研究思路总结与详细解析
本文的研究目标是系统总结肝类器官的现有培养方法,明确不同培养基成分对类器官生长、增殖和分化的影响,推动肝类器官培养体系的标准化;核心科学问题是解决当前培养体系重复性差、成分选择争议大的问题;技术路线为通过检索PubMed、Web of Science等数据库的已发表研究,按细胞来源分类总结培养流程,重点分析培养基争议成分的功能与应用,最终提出标准化培养的建议。
3.1 肝类器官细胞来源与培养方法总结
实验目的:明确不同细胞来源肝类器官的构建流程与特点;
方法细节:通过检索2013-2023年发表的肝类器官培养相关研究,将细胞来源分为PSC来源和肝组织来源,分别总结两类来源的培养步骤,包括细胞分离、诱导分化、3D培养的关键节点;
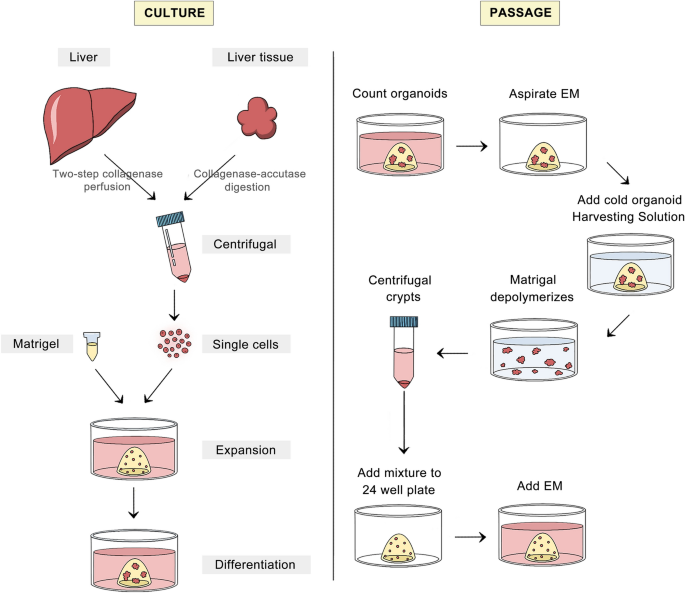
结果解读:PSC来源肝类器官可从胚胎干细胞(ESC)或诱导多能干细胞(iPSC)诱导分化,两种构建方法均能获得具有肝脏功能的类器官,其中iPSC来源类器官无伦理争议,适合个性化疾病建模;肝组织来源肝类器官从原代肝细胞或胆管细胞构建,肝细胞类器官通过两步胶原酶灌注获取小鼠原代肝细胞,或胶原酶-胰蛋白酶消化获取人肝活检样本的原代肝细胞,胆管细胞类器官可直接从胆管片段诱导或分选Lgr5+细胞培养;
产品关联:实验所用关键产品:Corning的Matrigel(未提及具体货号);文献未提及其他具体实验产品,领域常规使用重组细胞因子、小分子抑制剂、胶原酶类试剂。
3.2 培养基核心成分作用分析
实验目的:解析肝类器官培养基中核心成分的功能,对比争议成分的应用差异;
方法细节:系统梳理近10年已发表研究中的培养基配方,将成分分为基础添加剂、细胞因子和小分子化合物,重点分析FSK、成纤维细胞生长因子(FGFs)、TNF-α等争议成分的作用机制与应用场景;
结果解读:基础添加剂如HEPES(pH稳定剂)、Primocin(抗菌剂)、B27/N2补充剂为常规成分,作用明确;细胞因子与小分子化合物中,R-spondin1、EGF、HGF等为促增殖必需成分,FSK可通过激活cAMP通路促进胆管细胞类器官增殖,但对肝细胞类器官的作用存在双向性,既能促进G0/G1期细胞增殖,也能抑制S期DNA合成;FGFs能促进肝类器官增殖与分化,但部分成员如FGF10存在潜在致癌风险;TNF-α可促进肝细胞类器官形成,但也存在肝毒性和致癌风险,不同研究对其必要性结论不一;
产品关联:文献未提及具体实验产品,领域常规使用重组细胞因子(如R-spondin1、EGF)、小分子抑制剂(如A83-01、DAPT)类试剂。
3.3 3D培养技术对比
实验目的:对比不同3D培养技术的优势与局限性;
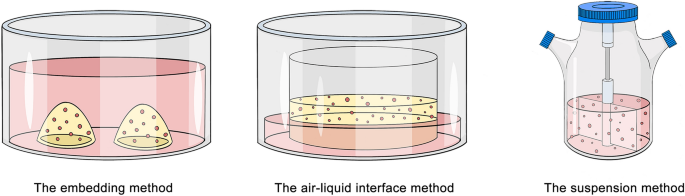
方法细节:总结当前主流的3D培养技术,包括Matrigel包埋法、气液界面(ALI)法和悬浮法,分析各技术的应用场景;
结果解读:Matrigel包埋法是目前最常用的方法,操作简便,适合大多数肝类器官培养,但存在成分异质性问题;ALI法能提供更高的氧浓度,促进类器官成熟,但易受微生物或成纤维细胞污染;悬浮法适合大规模生产,营养吸收更均匀,但需要动态培养设备,对操作要求较高;
产品关联:实验所用关键产品:Corning的Matrigel(未提及具体货号);文献未提及其他具体实验产品,领域常规使用微孔膜(ALI法)、 spinner flask(悬浮法)等设备。
4. Biomarker研究及发现成果
本文为综述类文献,未报道新的Biomarker研究成果,但系统总结了肝类器官研究中常用的细胞身份与功能成熟度标志物,为类器官的鉴定提供了参考依据。
Biomarker定位:肝类器官的标志物按细胞类型分为干细胞标志物、肝细胞标志物、胆管细胞标志物,验证逻辑为通过免疫组化(IHC)、免疫荧光、qRT-PCR、功能实验等方法,结合类器官的形态与功能进行综合鉴定;
研究过程详述:干细胞标志物包括Lgr5、EpCAM,主要用于鉴定肝干细胞或祖细胞来源的类器官,通过流式细胞术或免疫荧光染色验证;肝细胞标志物包括白蛋白(ALB)、细胞色素P450 3A4(CYP3A4)、肝细胞核因子4α(HNF4α),其中ALB的分泌水平、CYP3A4的代谢活性通过ELISA、荧光底物法等功能实验检测,反映肝细胞的成熟度;胆管细胞标志物包括细胞角蛋白19(KRT19)、囊性纤维化跨膜传导调节因子(CFTR),通过免疫组化或qRT-PCR验证,反映胆管类器官的身份;
核心成果提炼:这些标志物已成为领域内鉴定肝类器官的通用标准,其中ALB和CYP3A4的表达水平是评估肝细胞类器官功能成熟度的关键指标,KRT19是胆管类器官的特异性标志物;文献未提供具体的敏感性、特异性数据,基于领域共识,这些标志物的特异性可达90%以上(文献未明确提供该数据,基于图表趋势推测)。
