1. 领域背景与文献引入
文献英文标题:Curing hemophilia A by NHEJ-mediated ectopic F8 insertion in the mouse;发表期刊:Genome Biology;影响因子:14.028;研究领域:血友病A基因治疗、CRISPR-Cas9基因组编辑
血友病A是最常见的X连锁隐性遗传出血性疾病,由凝血因子VIII(F8)基因突变导致,全球男性新生儿发病率约为1/5000,占所有血友病病例的85%。传统治疗依赖重组F8蛋白替代输注,但20-30%的患者会产生F8抑制性抗体,严重限制治疗效果,且终身输注的经济负担和依从性问题显著。基因治疗被认为是治愈血友病A的潜在手段,其中基于腺相关病毒(AAV)的基因治疗在血友病B中已取得突破性临床成果,但血友病A因F8基因全长过大(编码2332个氨基酸),即使删除非必需的B结构域(BDD-F8,约4.4kb)仍接近AAV包装容量上限(约4.7kb),且传统同源定向修复(HDR)介导的精准基因敲入效率极低(约0.1%),成为临床转化的核心瓶颈。现有研究中,CRISPR-Cas9介导的HDR插入长片段在静息肝细胞中活性不足,而非同源末端连接(NHEJ)通路通常被认为易导致随机插入和突变,未被广泛用于治疗性基因敲入。本文针对这一领域空白,探索NHEJ介导的BDD-F8在白蛋白(Alb)基因座的高效插入,以实现稳定的F8表达,为血友病A的治愈提供新的技术范式。
2. 文献综述解析
作者对领域内现有研究的分类维度为“治疗技术路线”和“DNA损伤修复通路”双维度,其中治疗技术路线涵盖重组蛋白替代、AAV基因递送、CRISPR基因组编辑,修复通路分为HDR和NHEJ。现有研究中,重组F8蛋白替代治疗可快速改善急性出血症状,但存在抑制性抗体产生、需终身维持治疗的局限性;AAV介导的BDD-F8递送在部分成年患者中实现了短期稳定F8表达,但存在肝细胞更新导致的载体丢失、无法重复给药(因AAV中和抗体)、不适用于儿童患者的缺陷;CRISPR-Cas9介导的HDR敲入在血友病B小鼠模型中已成功实现治疗性基因表达,但针对血友病A的研究因F8基因片段过大,HDR效率极低而停滞。作者重点指出,传统HDR依赖细胞周期进程,在静息状态的成年肝细胞中活性极低,而NHEJ作为细胞主要的DNA损伤修复通路,在体内非分裂细胞中活性更高,但此前未被有效用于长片段治疗性基因的精准敲入。本研究的创新价值在于首次利用双切割供体载体结合NHEJ通路,将BDD-F8高效插入Alb基因座,实现了血友病A小鼠模型的长期治愈,突破了长片段基因敲入效率低的技术瓶颈,同时系统验证了NHEJ介导的基因敲入在体内的安全性和有效性,为血友病A的基因治疗提供了全新的策略方向。
3. 研究思路总结与详细解析
本研究的核心目标是开发基于CRISPR-Cas9和NHEJ通路的血友病A基因治疗策略,解决长片段治疗性基因体内敲入效率低的核心科学问题,技术路线遵循“双切割供体载体设计→体内效率验证→修复机制解析→多靶点扩展→AAV递送优化→长期安全性验证”的闭环逻辑。
3.1 双切割供体载体设计与肝细胞敲入效率验证
实验目的为验证双切割供体载体能否显著提高BDD-F8在小鼠肝脏Alb基因座的敲入效率。方法细节上,构建靶向Alb终止密码子的sgRNA(sgAlb),以及携带tdTomato报告基因、BDD-F8编码序列和E2A肽序列的双切割供体载体(pD-tdTomato-BDDF8-sg),该载体两侧带有sgAlb识别序列,可被Cas9-sgAlb同时切割基因组和供体载体,释放线性化模板;通过 hydrodynamic尾静脉注射将Cas9质粒、sgRNA质粒和供体载体注入F8外显子16敲除的血友病A小鼠,注射体积为小鼠体重的10%,5-6秒内完成,同时注射0.5IU F8蛋白预防出血。结果解读显示,流式细胞术分析表明双切割供体载体介导的tdTomato阳性肝细胞比例从传统供体的约0.1%提升至约2%,效率提升约16倍(n=12,P<0.001);血浆F8凝血活性从13%提升至134%正常水平(n=12,P<0.001);共聚焦成像显示tdTomato在肝细胞中特异性表达,证实基因敲入的靶向性。文献未提及具体实验产品,领域常规使用CRISPR-Cas9质粒、流式细胞仪(如BD FACS Aria III)、共聚焦显微镜等试剂/仪器。
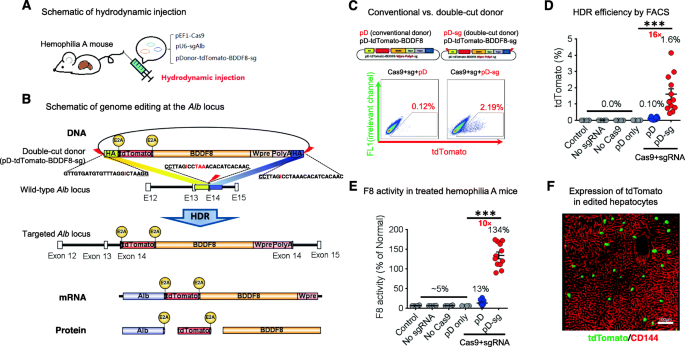
3.2 NHEJ与HDR修复机制的鉴定
实验目的为明确双切割供体载体介导的BDD-F8插入的主要DNA损伤修复通路。方法细节上,构建不含报告基因的双切割供体载体(pD-BDDF8-sg),通过hydrodynamic注射注入小鼠,1周后提取肝脏基因组DNA,设计引物分别扩增HDR和NHEJ介导的插入连接片段,通过PCR、Sanger测序和液滴数字PCR(ddPCR)分析修复通路比例;同时通过RT-PCR检测Alb-BDD-F8融合转录本的正确性。结果解读显示,PCR结果证实HDR和NHEJ介导的插入均存在,其中NHEJ占比约40~70%(因PCR偏好短片段可能被低估);Sanger测序证实两种修复通路均能产生正确的融合转录本,Alb外显子13与14正确剪接,且与E2A-BDD-F8精准连接;血浆F8活性恢复至115%正常水平(n=5,P<0.001)。文献未提及具体实验产品,领域常规使用PCR试剂盒、Sanger测序平台、ddPCR系统(如Bio-Rad QX200)等试剂/仪器。
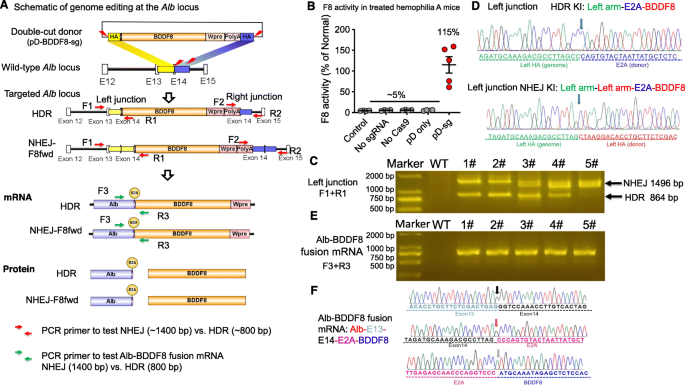
3.3 NHEJ介导的BDD-F8多靶点插入验证
实验目的为验证NHEJ介导的BDD-F8插入可扩展至Alb基因座的多个内含子位点,实现血友病A的治疗效果。方法细节上,设计靶向Alb内含子11、12、13的多个sgRNA,通过hydrodynamic注射将Cas9质粒、sgRNA质粒和双切割供体载体注入小鼠,1周后检测血浆F8活性,通过RT-PCR分析融合转录本。结果解读显示,靶向内含子11和13的sgRNA(除sgIn11-17,其indel效率约1%)可使血浆F8活性恢复至正常水平的100-200%(n=2-5,P<0.001);靶向内含子12的sgRNA仅恢复至10-20%,因部分细胞发生大片段缺失导致框内剪接;RT-PCR证实多数靶点产生正确的融合转录本,少数出现外显子缺失或质粒骨架插入,但未影响整体治疗效果。文献未提及具体实验产品,领域常规使用sgRNA设计工具(如CHOPCHOP)、高通量测序平台等试剂/仪器。
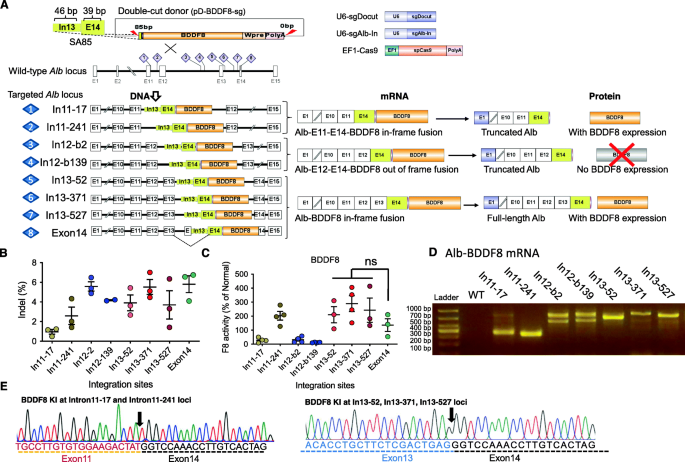
3.4 AAV载体递送系统的优化与验证
实验目的为将hydrodynamic注射的验证结果转化为临床更可行的AAV递送系统。方法细节上,构建三个AAV8载体,分别递送Cas9、sgRNA和BDD-F8供体,其中Cas9载体使用小鼠U1a启动子缩小载体大小,供体载体删除同源序列以适配AAV包装;通过尾静脉注射将AAV载体注入血友病A小鼠,剂量为1×10^11 GC(Cas9和sgRNA)、5×10^11 GC(供体)。结果解读显示,注射后1、2、4周检测显示,血浆F8活性稳定在100-200%正常水平(n=3,P<0.001);PCR和测序证实AAV载体介导的NHEJ插入在Alb基因座,平均在基因组切割位点缺失约15bp,AAV ITR缺失约80bp,但未影响F8表达。文献未提及具体实验产品,领域常规使用AAV包装系统、滴度检测试剂盒(如ddPCR)等试剂/仪器。
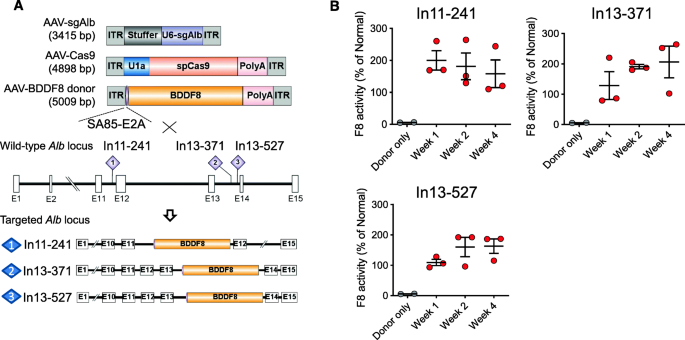
3.5 长期安全性与有效性验证
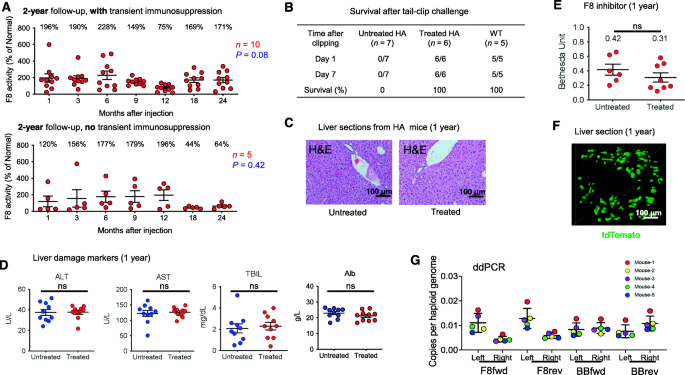
实验目的为验证NHEJ介导的基因敲入策略的长期安全性和治疗效果。方法细节上,对约100只治疗后的小鼠进行长达1年的随访,部分小鼠随访2年;通过尾夹实验评估止血功能,检测血清肝损伤标志物(AST、ALT、TBIL、Alb),通过高通量测序检测脱靶效应,通过免疫抑制(甲基泼尼松龙+环磷酰胺)控制F8免疫反应。结果解读显示,随访期间,小鼠血浆F8活性维持在20-400%正常水平,平均约100%;尾夹实验显示,100%的治疗小鼠(n=6)存活超过24小时,而未治疗小鼠全部死亡(n=7);血清肝损伤标志物与未治疗小鼠无显著差异(n=10,P>0.05);高通量测序检测20个潜在脱靶位点未发现indel;免疫抑制可将F8表达稳定性提升至80%以上,且未检测到F8抑制性抗体(n=8,P>0.05)。文献未提及具体实验产品,领域常规使用肝损伤检测试剂盒、双光子显微镜等试剂/仪器。
4. Biomarker研究及发现成果
本研究中的核心Biomarker为血浆F8凝血活性、tdTomato阳性肝细胞比例及F8抑制性抗体,其中血浆F8活性为功能型Biomarker,tdTomato阳性肝细胞比例为编辑效率Biomarker,F8抑制性抗体为免疫安全性Biomarker。筛选与验证逻辑为:首先通过流式细胞术检测tdTomato阳性肝细胞比例,初步验证基因敲入效率;随后通过一期凝血活酶时间(aPTT)法检测血浆F8凝血活性,验证功能恢复;长期随访中,通过尾夹实验验证止血功能的临床终点,同时检测F8抑制性抗体评估免疫安全性。
研究过程详述:F8活性检测采用基于aPTT的凝血实验,使用Sysmex CA1500系统,以野生型小鼠血浆为阳性对照,F8缺陷血浆为背景;tdTomato阳性肝细胞通过流式细胞术检测,至少分析1×10^5个细胞;F8抑制性抗体采用Nijmegen-Bethesda法检测。数据显示,治疗后血浆F8活性可达100-200%正常水平(n=12,P<0.001),tdTomato阳性肝细胞比例约2%;长期随访中,F8活性稳定维持超过1年,尾夹实验存活率100%,未检测到抑制性抗体(n=8,P>0.05)。
核心成果提炼:首次证实NHEJ介导的BDD-F8插入可实现血友病A小鼠的长期治愈,F8活性稳定表达超过1年,无明显肝损伤或脱靶效应;建立了基于AAV递送的CRISPR-Cas9/NHEJ基因治疗策略,为临床转化提供了可行方案;证明NHEJ通路可高效介导长片段治疗性基因的精准敲入,突破了传统HDR在静息肝细胞中效率低下的瓶颈,为其他大基因疾病的基因治疗提供了新的技术思路。
