1. 领域背景与文献引入
文献英文标题:Interleukin-17 promotes nitric oxide-dependent expression of PD-L1 in mesenchymal stem cells;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肿瘤免疫微环境与间充质干细胞调控
肿瘤免疫治疗是当前生命科学领域的研究前沿,以程序性死亡受体1(PD-1)/程序性死亡配体1(PD-L1)通路为靶点的免疫检查点抑制剂已在多种实体瘤治疗中取得突破性进展,其核心机制是阻断肿瘤细胞或基质细胞表面的PD-L1与T细胞表面PD-1的结合,恢复细胞毒性T细胞的抗肿瘤活性。领域共识:白细胞介素-17(IL-17)是一类具有双重生物学功能的细胞因子,在感染性疾病、自身免疫病中主要发挥促炎作用,但在肿瘤微环境中,IL-17常与患者不良预后相关,其促肿瘤进展的具体细胞与分子机制尚未完全阐明。间充质干细胞(MSCs)是肿瘤微环境的重要组成部分,可被肿瘤微环境中的细胞因子激活为肿瘤相关MSCs,通过分泌免疫抑制分子、招募免疫抑制细胞等方式促进肿瘤免疫逃逸。已有研究证实干扰素γ(IFNγ)和肿瘤坏死因子α(TNFα)可诱导MSCs表达PD-L1,但IL-17是否参与调控这一过程,以及相关的分子机制仍属研究空白,这一缺口限制了对IL-17促肿瘤效应的全面理解,也为肿瘤免疫治疗的新靶点开发留下了空间。本文正是针对这一空白,系统研究了IL-17对MSCs中PD-L1表达的调控作用及分子机制。
2. 文献综述解析
作者围绕IL-17的生物学功能、MSCs在肿瘤微环境中的作用、PD-L1的表达调控三个核心维度对现有研究进行系统评述,明确了领域内的研究现状与未解决问题。现有研究表明,IL-17主要由Th17细胞分泌,在感染和自身免疫病中通过招募中性粒细胞、诱导促炎细胞因子表达发挥促炎作用,但在肿瘤微环境中,IL-17可通过促进血管生成、诱导免疫抑制等途径促进肿瘤进展,这种双重效应的细胞与分子基础仍存在争议。关于MSCs的研究显示,MSCs可被肿瘤微环境中的细胞因子激活,转化为肿瘤相关MSCs,通过分泌趋化因子招募M2型巨噬细胞、调节性T细胞等免疫抑制细胞,或直接表达PD-L1、吲哚胺2,3-双加氧酶(IDO)等抑制分子,抑制细胞毒性T细胞的功能,从而促进肿瘤免疫逃逸。在PD-L1的调控方面,已有研究证实IFNγ和TNFα可协同诱导MSCs表达PD-L1,但IL-17与这两种细胞因子的协同作用尚未被报道,且IL-17调控MSCs中PD-L1表达的具体分子机制仍属未知。现有研究的局限性在于,缺乏对IL-17与MSCs上PD-L1表达关联的直接研究,尤其是中间介导分子的鉴定,无法解释IL-17在肿瘤微环境中促免疫抑制的具体通路。本文的创新价值在于,首次发现IL-17可与IFNγ、TNFα协同,通过一氧化氮(NO)介导的信号通路促进MSCs表达PD-L1,揭示了IL-17促肿瘤效应的新机制,填补了领域内关于IL-17调控MSCs免疫抑制功能的研究空白。
3. 研究思路总结与详细解析
本文的研究目标是明确IL-17对MSCs中PD-L1表达的调控作用及分子机制,核心科学问题是IL-17如何通过MSCs介导肿瘤免疫抑制,技术路线遵循“临床观察提出假设→细胞实验验证调控作用→分子机制解析中间介质与信号通路→动物实验验证体内功能”的闭环逻辑,系统阐明了IL-17-NO-STAT3-PD-L1轴在肿瘤微环境中的作用。
3.1 IL-17对MSCs中PD-L1表达的协同诱导作用
本环节的实验目的是验证IL-17是否能够调控MSCs表面PD-L1的表达,尤其是与IFNγ、TNFα的协同效应。实验方法为分离培养C57BL/6小鼠骨髓来源的MSCs,分别采用IL-17单独处理、IL-17联合IFNγ和TNFα处理的方式,设置不同时间梯度(12h、24h、48h),通过实时荧光定量PCR检测PD-L1的mRNA水平,流式细胞术检测细胞表面PD-L1的蛋白表达水平。实验结果显示,IL-17单独处理无法诱导MSCs表达PD-L1,但与IFNγ、TNFα联合处理后,24h时PD-L1的mRNA水平显著上调,48h时蛋白水平的平均荧光强度较单独IFNγ+TNFα处理组升高约2.5倍(n=3,P<0.05),且12h内未观察到协同效应,提示该调控作用为IL-17的次级效应。
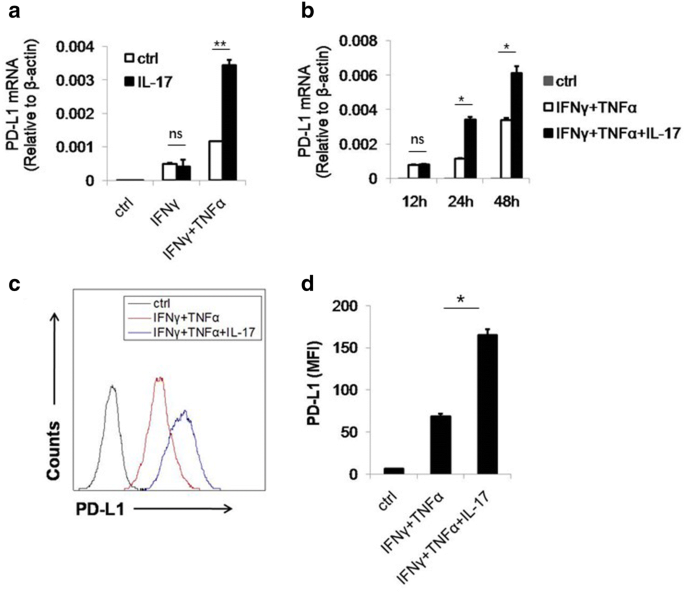
实验所用关键产品:重组小鼠IFNγ、TNFα、IL-17A及抗小鼠CD274(PD-L1)-APC抗体购自eBiosciences,流式细胞仪为BD FACS Calibur。
3.2 NO在IL-17协同诱导PD-L1中的介导作用
本环节的实验目的是鉴定IL-17协同诱导PD-L1表达的中间介导分子。实验方法包括采用Griess试剂检测MSCs培养上清中的NO浓度,使用诱导型一氧化氮合酶(iNOS)特异性抑制剂S-甲基异硫脲(SMT)处理MSCs,或采用iNOS基因敲除的MSCs进行实验,同时使用NO供体S-亚硝基-N-乙酰-DL-青霉胺(SNAP)模拟IL-17的作用,检测不同处理下PD-L1的mRNA和蛋白表达水平。实验结果显示,IL-17联合IFNγ、TNFα处理后,MSCs分泌的NO水平在12h后开始升高,24h达到峰值;SMT处理或iNOS基因敲除后,IL-17对PD-L1表达的协同诱导效应完全消失;SNAP可替代IL-17,在IFNγ和TNFα存在的情况下显著促进PD-L1的表达,但单独使用SNAP无法诱导PD-L1表达(n=3,P<0.01),表明NO是IL-17协同诱导PD-L1表达的必需分子。
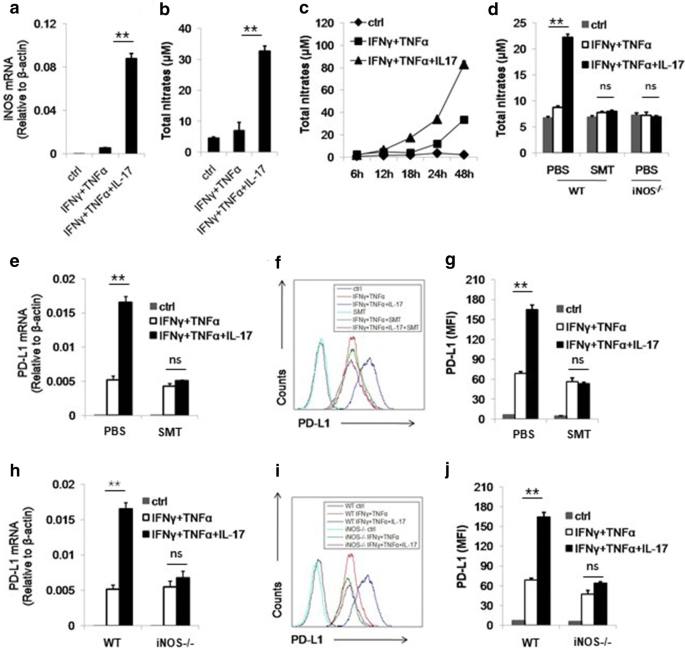

实验所用关键产品:SNAP、Griess试剂购自Sigma-Aldrich,iNOS抑制剂SMT购自碧云天生物技术。
3.3 STAT3通路在NO介导PD-L1表达中的作用
本环节的实验目的是解析NO调控PD-L1表达的下游信号通路。实验方法为采用蛋白质免疫印迹(Western blotting)技术检测MSCs中信号转导与转录激活因子3(STAT3)和核因子κB(NF-κB)p65的磷酸化水平,使用STAT3特异性抑制剂WP1066处理MSCs,检测PD-L1的mRNA表达水平。实验结果显示,IL-17联合IFNγ、TNFα处理可显著增强STAT3的磷酸化水平,但对NF-κB p65的磷酸化无进一步促进作用;NO供体SNAP同样可增强STAT3的磷酸化,而WP1066抑制STAT3磷酸化后,PD-L1的mRNA水平显著降低(n=3,P<0.05),表明STAT3是NO介导PD-L1表达的关键下游信号分子。此外,研究还发现SMT可诱导STAT3磷酸化但无法促进PD-L1表达,提示STAT3磷酸化是PD-L1表达的必要非充分条件,NO可能还通过其他通路协同调控PD-L1的表达。
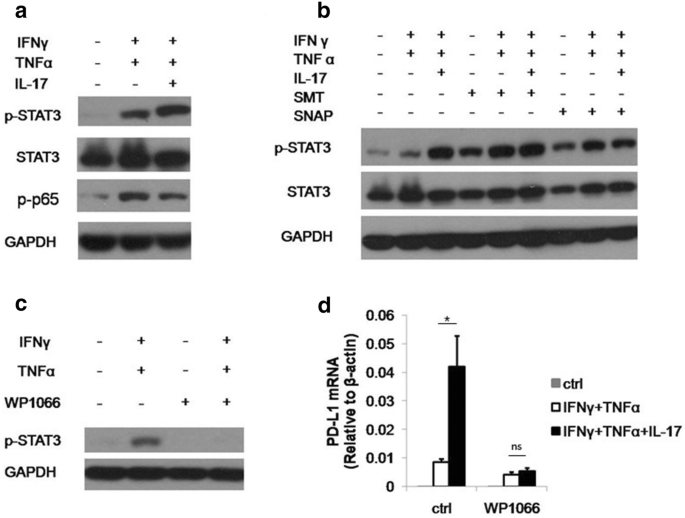
实验所用关键产品:抗p-STAT3、STAT3、p-p65、GAPDH抗体购自Cell Signaling Technology,STAT3抑制剂WP1066购自Santa Cruz Biotechnology。
3.4 IL-17预处理MSCs促肿瘤生长的体内验证
本环节的实验目的是验证IL-17诱导MSCs高表达PD-L1的体内生物学功能。实验方法为将经IFNγ+TNFα单独处理、IFNγ+TNFα+IL-17联合处理的MSCs,与B16F0黑色素瘤细胞共同注射到C57BL/6小鼠皮下,部分实验组在注射前用PD-L1中和抗体处理MSCs,或在肿瘤生长过程中腹腔注射PD-L1中和抗体,16天后处死小鼠并检测肿瘤重量。实验结果显示,IL-17预处理的MSCs可显著促进黑色素瘤的生长,肿瘤重量较对照组增加约40%(n=9,P<0.05);而PD-L1中和抗体可完全阻断IL-17预处理MSCs的促肿瘤效应,肿瘤重量降低至与对照组相当的水平(n=5/6,P<0.05),表明MSCs表面的PD-L1是IL-17促肿瘤效应的关键介导分子。
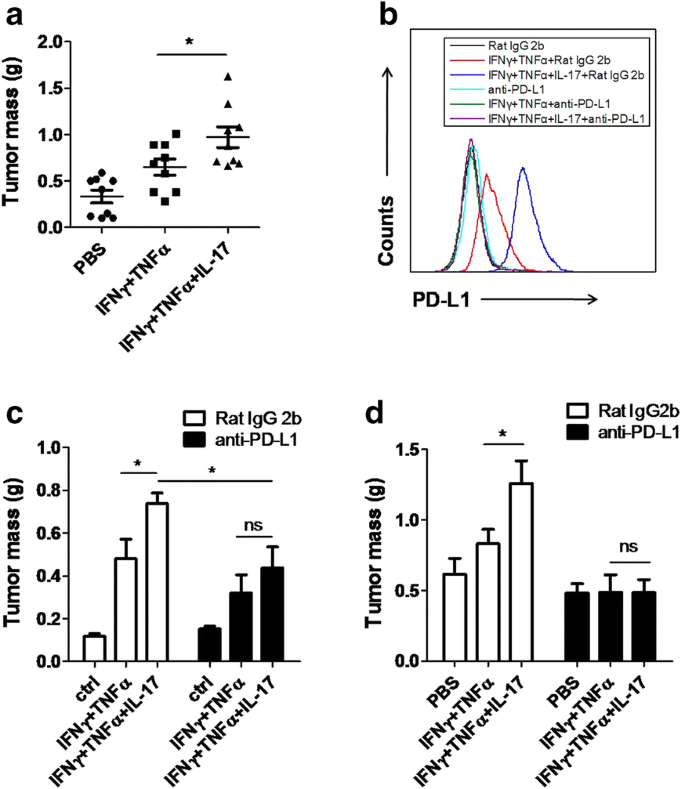
实验所用关键产品:PD-L1中和抗体购自eBiosciences。
4. Biomarker研究及发现成果
本文的核心Biomarker为间充质干细胞表面的程序性死亡配体1(PD-L1),同时鉴定了一氧化氮(NO)和信号转导与转录激活因子3(STAT3)为该Biomarker表达调控的关键分子,筛选与验证逻辑基于临床观察的相关性假设,通过细胞实验、分子机制实验和动物实验的多维度验证,明确了其在肿瘤免疫抑制中的功能与调控通路。
该Biomarker的来源为小鼠骨髓来源的MSCs,对应临床场景中肿瘤微环境内的肿瘤相关MSCs。验证方法包括实时荧光定量PCR检测PD-L1的mRNA表达水平,流式细胞术检测细胞表面PD-L1的蛋白表达,Griess试剂检测NO的分泌水平,蛋白质免疫印迹检测STAT3的磷酸化状态,以及体内肿瘤模型验证其功能。特异性方面,IL-17仅在IFNγ和TNFα存在的条件下,才能协同促进MSCs表达PD-L1,单独IL-17或NO供体均无法诱导PD-L1表达;iNOS基因敲除或抑制剂处理可完全阻断IL-17的协同效应,表明该调控具有严格的信号依赖性。敏感性数据显示,IL-17联合IFNγ、TNFα处理后,MSCs中PD-L1的mRNA水平较单独IFNγ+TNFα处理组上调约3倍(n=3,P<0.01),细胞表面蛋白的平均荧光强度升高约2.5倍(n=3,P<0.05)。核心成果方面,明确了PD-L1作为MSCs介导肿瘤免疫抑制的关键功能分子,IL-17-NO-STAT3-PD-L1轴是IL-17促肿瘤进展的新机制;该Biomarker的表达水平与肿瘤生长显著相关,体内实验中IL-17预处理组的肿瘤重量较对照组增加约40%(n=9,P<0.05),PD-L1中和抗体可完全逆转该效应;该研究首次揭示了IL-17通过MSCs调控PD-L1的分子通路,为肿瘤免疫治疗提供了潜在的新靶点,即通过阻断IL-17-NO-PD-L1轴增强抗肿瘤免疫应答。
