1. 领域背景与文献引入
文献英文标题:Myometrial oxidative stress drives MED12 mutations in leiomyoma;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:妇科肿瘤(子宫平滑肌瘤发病机制)
子宫平滑肌瘤(LM)是育龄女性最常见的良性肿瘤,全球发病率高达77%,每年导致美国约60万例子宫切除或肌瘤剔除术,经济负担达59-344亿美元。2011年《Science》首次报道超70%的LM携带中介体复合物亚基12(MED12)突变,主要集中在第2外显子c.130-131位点,该突变被认为是驱动LM发生的关键遗传事件。后续研究发现LM存在氧化应激代谢缺陷,如锰超氧化物歧化酶(MnSOD)活性降低、NADPH氧化酶4(NOX4)功能异常,导致活性氧(ROS)水平升高,但氧化应激与MED12突变的直接因果关系尚未明确。当前领域的核心未解决问题是MED12高频突变的分子起源,以及肌层微环境对突变的调控机制。本研究针对这一空白,通过体内外实验结合CRISPR/Cas9技术,验证肌层氧化应激通过8-羟基-2"-脱氧鸟苷(8-OHdG)介导的DNA错修复驱动MED12突变,为LM的发病机制提供了新的分子解释,也为LM的预防和早期干预提供了潜在靶点。
2. 文献综述解析
作者对现有研究的分类维度主要分为两大方向,一是LM的遗传突变研究,聚焦MED12突变的频率、位点及临床相关性;二是氧化应激与LM的关联研究,围绕ROS代谢缺陷、氧化应激对LM细胞功能的影响展开。现有研究的关键结论包括,MED12突变在LM中的占比超70%,是独立于HMGA2突变的另一类驱动事件,且突变率与LM的肿瘤负荷呈正相关;LM细胞存在先天的ROS代谢缺陷,解毒机制不足导致氧化应激水平持续升高,促进细胞增殖和存活。技术方法优势方面,全基因组测序和Sanger测序技术明确了MED12突变的高频位点和突变类型,免疫组化、RNA-seq等技术系统揭示了LM的氧化应激状态和转录组特征。局限性在于,现有研究仅建立了MED12突变与LM负荷的相关性,未阐明因果关系;氧化应激与MED12突变的直接分子机制缺乏实验验证,仅停留在理论推测层面;此外,现有研究未明确氧化应激诱导MED12突变的具体位点和错修复机制。本研究的创新价值在于,首次通过CRISPR/Cas9定点突变实验直接证明8-OHdG在MED12 c.130位点的错修复可诱导突变,结合临床样本和体外模型,明确了肌层氧化应激与MED12突变的因果关联,填补了LM发病机制中遗传突变诱因的空白,为氧化应激在肿瘤发生中的作用提供了新的证据。
3. 研究思路总结与详细解析
本研究的核心目标是验证“肌层氧化应激通过8-OHdG介导的DNA错修复驱动MED12突变”的科学假设,核心科学问题是氧化应激如何特异性诱导MED12 c.130-131位点的突变,技术路线遵循“临床样本关联分析→体内外模型验证→分子机制解析→高深度测序确认”的闭环逻辑,从临床现象到分子机制逐层验证假设。
3.1 临床样本MED12突变与LM负荷的关联分析
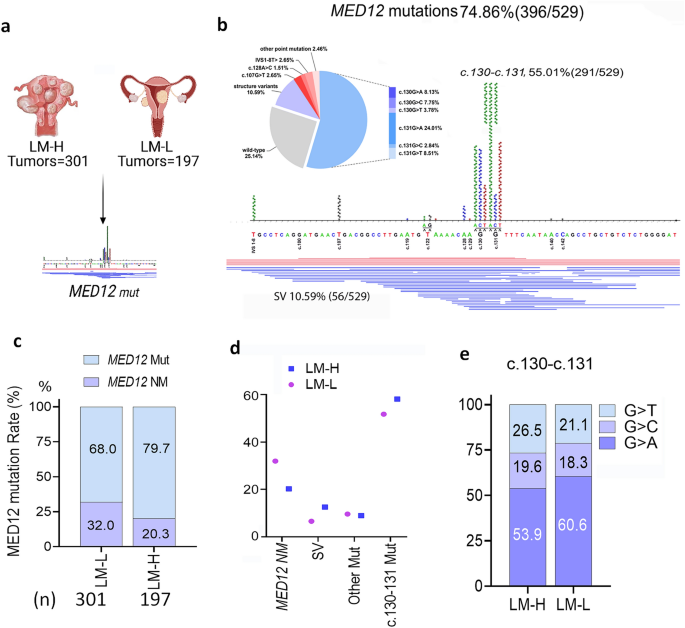
实验目的是明确MED12突变率与LM肿瘤负荷的相关性,为后续机制研究提供临床依据。方法细节为收集2010-2021年西北大学Prentice Women’s Hospital的309例预绝经患者的子宫组织,其中包含529个LM样本,按子宫内LM数量分为高负荷组(≥5个,n=301)、低负荷组(1-4个,n=197)及数量未知组(n=31),采用Sanger测序检测MED12第2外显子的突变情况。结果解读显示,高负荷组的MED12突变率为79.7%,显著高于低负荷组的68.0%(n=529,P<0.01);突变类型中c.130-131位点的点突变占比最高(55.0%),其次为缺失突变(10.6%),且高负荷组的c.130-131点突变和插入/缺失突变率均显著高于低负荷组(P<0.01),提示LM肿瘤负荷越高,MED12突变的概率越高,且突变位点集中在c.130-131区域。产品关联:文献未提及具体实验产品,领域常规使用DNA提取试剂盒、Sanger测序引物及测序仪等。
3.2 肌层组织氧化应激与DNA损伤的检测
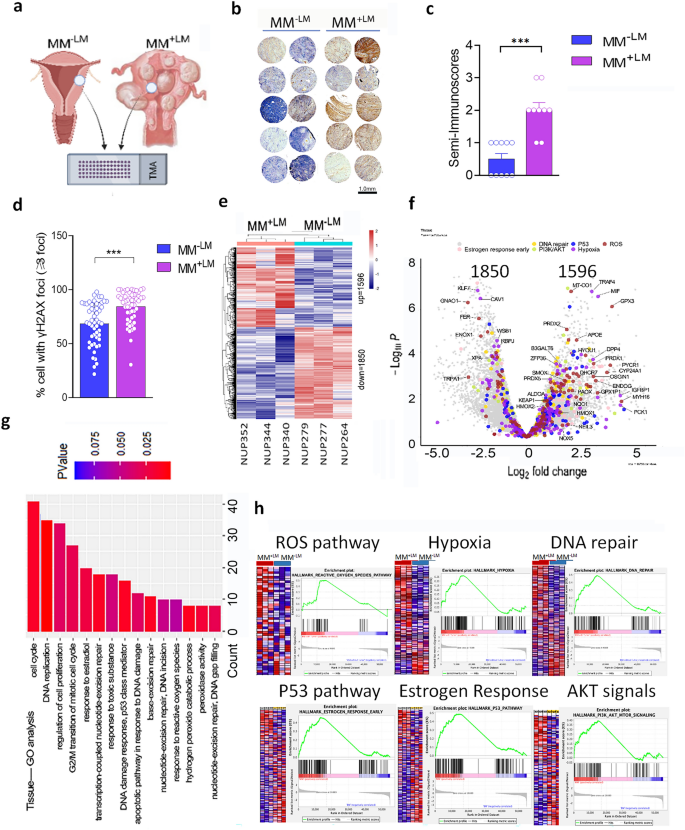
实验目的是比较伴LM和不伴LM的肌层组织的氧化应激状态,明确肌层微环境的氧化应激是否与MED12突变相关。方法细节为构建包含年龄匹配的伴LM肌层(MM+LM)和不伴LM肌层(MM-LM)样本的组织芯片,采用免疫组化(IHC)检测8-OHdG(氧化应激的经典标志物)的表达,免疫荧光检测γH2AX(DNA损伤标志物)的水平,同时对两组样本进行RNA-seq分析转录组差异。结果解读显示,MM+LM样本的8-OHdG免疫反应性显著高于MM-LM(n=10,P<0.001),γH2AX阳性细胞比例也显著升高(n=10,P<0.05);RNA-seq分析共鉴定出3446个差异表达基因,其中1596个基因上调、1850个基因下调,基因本体(GO)和京都基因与基因组百科全书(KEGG)富集分析显示,差异基因主要富集于ROS通路、DNA修复通路、p53通路等,提示伴LM的肌层组织存在更高的氧化应激水平和DNA损伤应答。产品关联:实验所用关键产品:8-OHdG抗体、γH2AX抗体(文献未明确品牌)、RNA-seq文库构建试剂盒等。
3.3 体外氧化应激模型验证肌层细胞的氧化损伤与基因表达变化
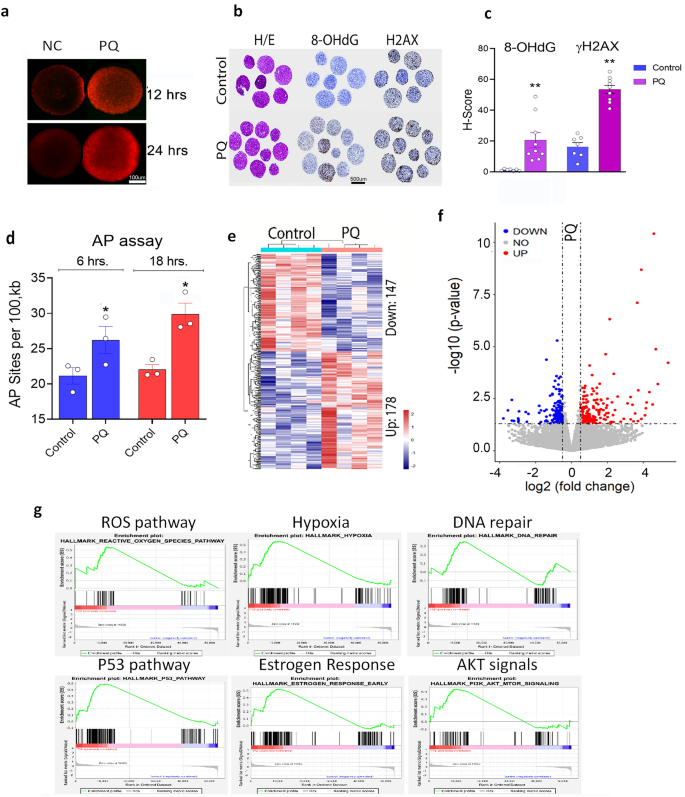
实验目的是验证ROS直接诱导肌层细胞的DNA氧化损伤和转录组变化,模拟临床肌层的氧化应激状态。方法细节为选取原代肌层细胞和肌层细胞系(myo-hTERT),采用ROS诱导剂百草枯(PQ)处理细胞,通过剂量预实验确定100 μM PQ处理24小时为最优条件(氧化应激水平最高且细胞死亡最少),采用二氢乙锭(DHE)染色检测ROS水平,免疫组化检测8-OHdG和γH2AX的表达,AP位点定量检测试剂盒检测基因组DNA中的无嘌呤/无嘧啶位点,同时对处理后的细胞进行RNA-seq分析。结果解读显示,PQ处理后肌层细胞的ROS水平显著升高,8-OHdG和γH2AX的免疫反应性增强,AP位点数量较对照组显著增加(n=3,P<0.05);RNA-seq分析鉴定出325个差异表达基因,其中178个上调、147个下调,基因集富集分析(GSEA)显示差异基因富集于ROS通路、DNA修复通路、p53通路等,与临床样本的转录组特征一致,证明ROS可直接诱导肌层细胞的DNA氧化损伤和转录组变化。产品关联:实验所用关键产品:百草枯(Sigma Aldrich, 36541)、AP Sites Quantitation Kit(Cell Biolabs)、DHE染色试剂等。
3.4 CRISPR/Cas9定点引入8-oxodG验证MED12的DNA错修复
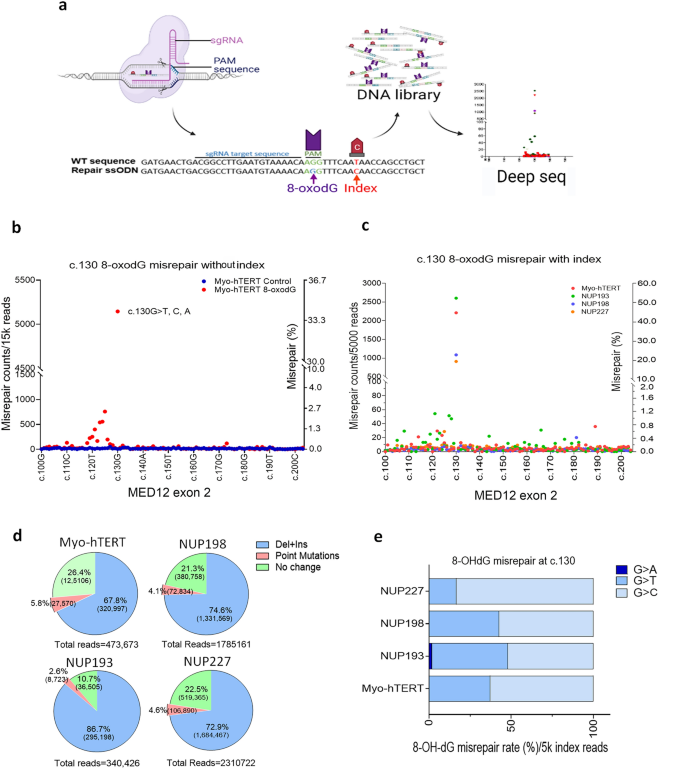
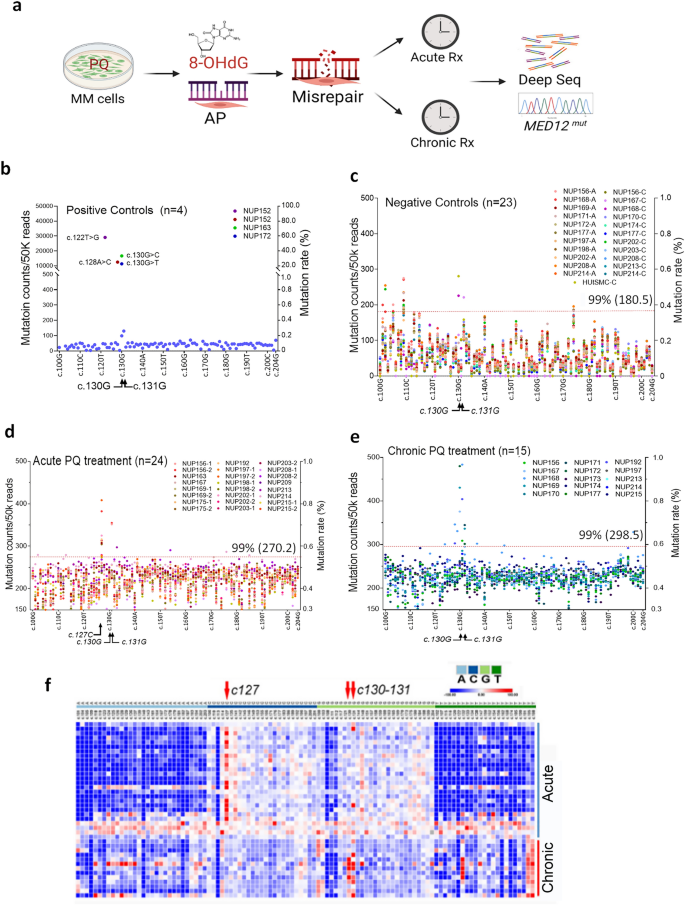
实验目的是直接证明8-OHdG可诱导MED12 c.130位点的DNA错修复,明确氧化应激诱导MED12突变的分子机制。方法细节为采用CRISPR/Cas9技术,将MED12 c.130位点的鸟嘌呤替换为8-oxodG(氧化型鸟嘌呤),同时引入c.138T>C作为标记位点,通过深度测序检测处理后细胞的MED12突变情况。结果解读显示,定点引入8-oxodG后,myo-hTERT细胞中c.130位点的错修复率达34.3%,原代肌层细胞的错修复率为16%-46%,其中G>T突变占比最高(96.0%-99.4%),证明8-OHdG在MED12 c.130位点的存在可显著诱导DNA错修复,进而导致突变。产品关联:实验所用关键产品:Alt-R CRISPR/Cas9 crRNA、Cas9酶、ssDNA供体模板(Integrated DNA Technologies)、深度测序文库构建试剂盒等。
3.5 体外PQ处理诱导肌层细胞MED12外显子2的错修复
实验目的是验证氧化应激可直接诱导肌层细胞的MED12突变,模拟体内肌层的氧化应激对MED12的影响。方法细节为将原代肌层细胞分为急性处理组(单次100 μM PQ处理24小时)和慢性处理组(100 μM PQ处理48小时后恢复24小时,重复5次),采用深度测序检测MED12第2外显子的突变情况,以已知MED12突变的LM样本作为阳性对照。结果解读显示,急性处理组的MED12外显子2核苷酸改变率平均为0.42%,其中c.127、c.130、c.131位点的突变率较高;慢性处理组的整体突变率与急性组无显著差异,但c.130-131位点的突变率显著升高,6/15样本的突变率超过阈值,提示慢性氧化应激更易诱导MED12的热点突变,与临床样本的突变位点高度一致。产品关联:文献未提及具体实验产品,领域常规使用深度测序相关试剂和细胞培养试剂等。
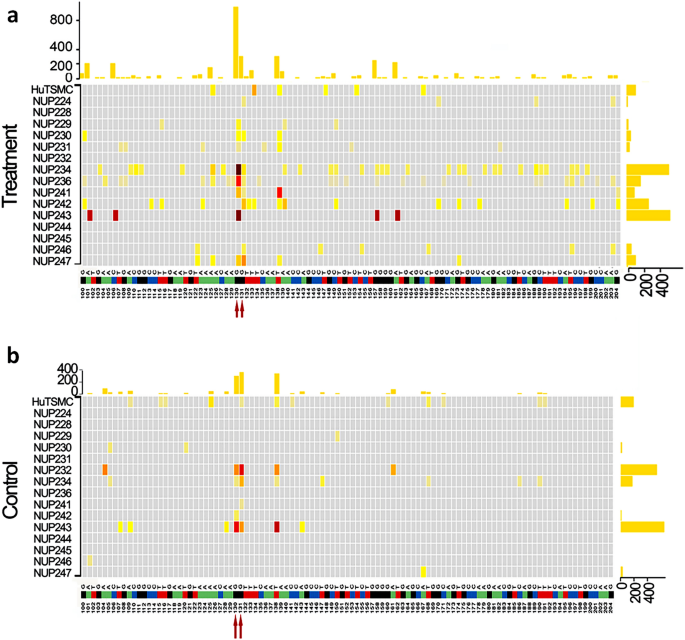
3.6 双链测序验证氧化应激诱导的MED12突变
实验目的是排除常规深度测序的误差,准确检测氧化应激诱导的低频率MED12突变。方法细节为选取16例慢性PQ处理的原代肌层细胞样本,采用双链测序技术检测MED12第2外显子的突变情况,该技术可通过单链核苷酸变化的一致性排除PCR误差,实现超高灵敏度的突变检测。结果解读显示,双链测序结果证实PQ处理组的c.130-131位点突变率显著高于对照组,与常规深度测序结果一致,进一步证明氧化应激可特异性诱导MED12的热点突变,排除了测序误差的干扰。产品关联:实验所用关键产品:KAPA HyperPrep library kit(Roche Sequencing)、xGen Lockdown Reagents(Integrated DNA Technologies)、Illumina NovaSeq 6000测序平台等。
4. Biomarker研究及发现成果解析
本研究涉及两类Biomarker,一是氧化应激的Biomarker 8-OHdG,二是LM的遗传Biomarker MED12 c.130-131突变。8-OHdG的筛选逻辑基于氧化应激诱导DNA损伤的经典理论,通过临床样本检测发现其在伴LM肌层中的高表达,再通过体外模型验证其与MED12突变的关联,最后通过CRISPR/Cas9实验明确其介导错修复的作用;MED12 c.130-131突变的筛选逻辑是先通过临床样本关联分析发现其与LM负荷的相关性,再通过体外模型验证其可由氧化应激诱导,最后通过高深度测序确认其突变特征。
研究过程详述方面,8-OHdG的来源为临床肌层组织和体外培养肌层细胞的基因组DNA,验证方法包括免疫组化、免疫荧光、AP位点定量检测,其特异性表现为伴LM肌层中的表达水平显著高于不伴LM肌层(n=10,P<0.001),可有效区分两类肌层组织的氧化应激状态;MED12 c.130-131突变的来源为LM临床样本和体外氧化应激处理的肌层细胞,验证方法包括Sanger测序、深度测序、双链测序,其在高负荷LM组中的突变率为55.0%,体外慢性PQ处理后部分样本的突变率达0.52%-0.57%,与临床样本的突变位点高度一致。
核心成果提炼包括,8-OHdG可作为肌层氧化应激的特异性Biomarker,其水平与MED12突变率正相关,可用于评估LM的发生风险;MED12 c.130-131突变是氧化应激诱导的热点突变,可作为LM发生的早期遗传Biomarker,提示肌层氧化应激的累积效应;本研究首次明确了氧化应激通过8-OHdG介导的DNA错修复驱动MED12突变的分子机制,为LM的发病机制提供了新的解释,也为氧化应激在肿瘤发生中的作用提供了直接的实验证据;统计学结果显示,高负荷组MED12突变率显著高于低负荷组(n=529,P<0.01),伴LM肌层的8-OHdG水平显著高于不伴LM肌层(n=10,P<0.001),CRISPR/Cas9实验中8-oxodG诱导的错修复率达16%-46%(n=4,P<0.05)。
