1. 领域背景与文献引入
文献英文标题:c-Jun N-terminal kinase (JNK) cooperates with Gsk3β to regulate Dishevelled-mediated microtubule stability;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:神经科学(Wnt信号通路调控神经元微管动态)
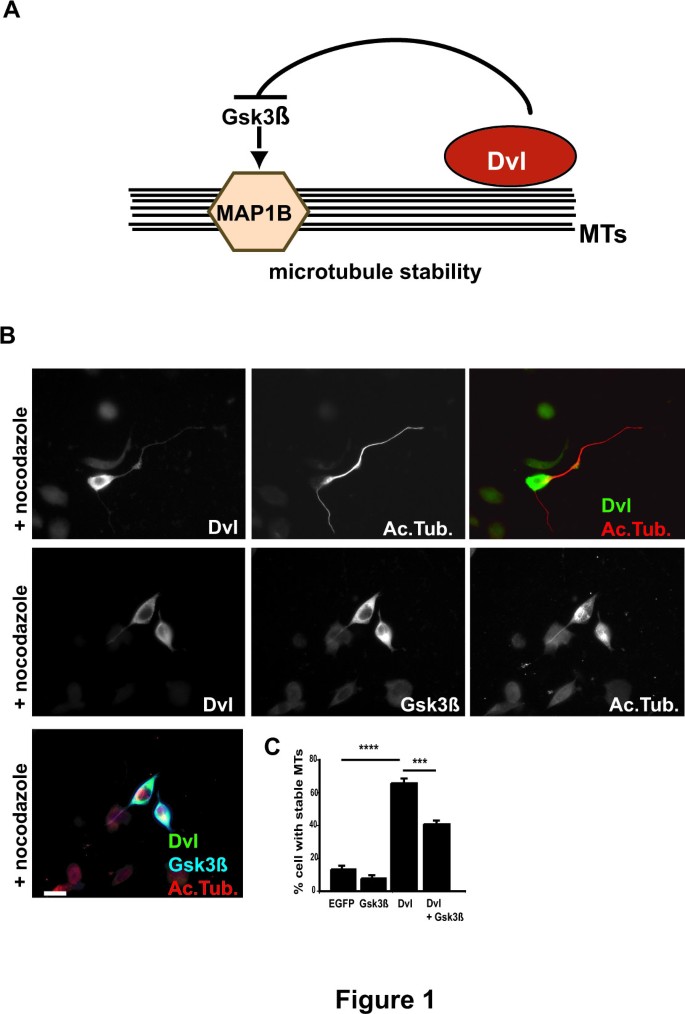
微管细胞骨架的动态调控是细胞分裂、极性维持、迁移等基本功能的核心机制,在神经系统中,微管的组装与解聚直接决定神经元轴突延伸、树突分支及突触连接形成,是神经环路构建的关键基础。目前已明确微管相关蛋白(MAPs)等细胞内分子可调控微管动态,但细胞外信号如何通过下游通路调控微管行为的机制仍不清晰。Wnt信号通路作为重要的细胞外信号家族,已被证实可直接调控微管的动态与组织,其中经典Wnt-Dvl通路通过抑制糖原合成激酶3β(Gsk3β)降低微管相关蛋白1B(MAP1B)的磷酸化,从而增强微管稳定性。然而,前期研究发现Gsk3β的药理学抑制仅能部分模拟散乱蛋白(Dvl)的微管稳定效应,提示Dvl可能通过额外通路调控微管动态,这一机制空白成为本研究的核心切入点。
2. 文献综述解析
作者对现有研究的分类维度分为两类:一是微管动态调控的分子机制,涵盖细胞内MAPs、激酶等对微管的调控,以及细胞外信号通路的调控作用;二是Wnt信号通路的分支功能,包括经典通路(调控β-catenin转录)、平面细胞极性(PCP)通路(调控Rho GTPases与JNK)及钙通路。现有研究的关键结论包括Gsk3β在Wnt-Dvl调控微管中的核心作用,以及Rho GTPases在PCP通路调控细胞骨架中的功能;技术方法优势在于通过细胞转染、药理学干预等明确了单通路的调控效应;局限性在于仅揭示了Wnt-Dvl调控微管的部分机制,Dvl的完整调控网络未被解析,且PCP通路相关分子是否参与微管调控尚未验证。本研究的创新价值在于首次证实JNK通路独立于Rho GTPases,与Gsk3β通路协同介导Wnt-Dvl的微管稳定效应,填补了Wnt信号通路调控细胞骨架的机制空白。
3. 研究思路总结与详细解析
本研究以“Dvl调控微管稳定性的额外通路鉴定”为核心目标,围绕“Wnt-Dvl是否通过JNK通路独立于Gsk3β调控微管动态”这一科学问题,采用“假设-验证-机制解析”的技术路线:首先验证Gsk3β抑制不能完全模拟Dvl的微管稳定效应,排除Rho GTPases的参与后,证实JNK激活是Dvl效应所必需的,最终通过结构域分析和 epistatic实验明确两条通路的独立协同关系。
3.1 Dvl调控微管稳定性的双通路验证
实验目的:确认Dvl除Gsk3β通路外存在额外的微管稳定调控通路;方法细节:采用分化的NB2a神经母细胞瘤细胞作为神经元模型,分别转染Dvl、Gsk3β及两者共转染,通过诺考达唑处理诱导微管解聚,以乙酰化微管免疫荧光染色检测稳定微管的保留情况;结果解读:单独转染Dvl的神经元在诺考达唑处理后仍保留大量稳定微管,而共转染Gsk3β仅能降低Dvl的微管稳定效应约30%(n=至少3次独立实验,P<0.0001),说明Gsk3β通路仅介导部分Dvl的功能,存在未被发现的调控通路;产品关联:文献未提及具体实验产品,领域常规使用脂质体转染试剂、诺考达唑、乙酰化微管抗体等。
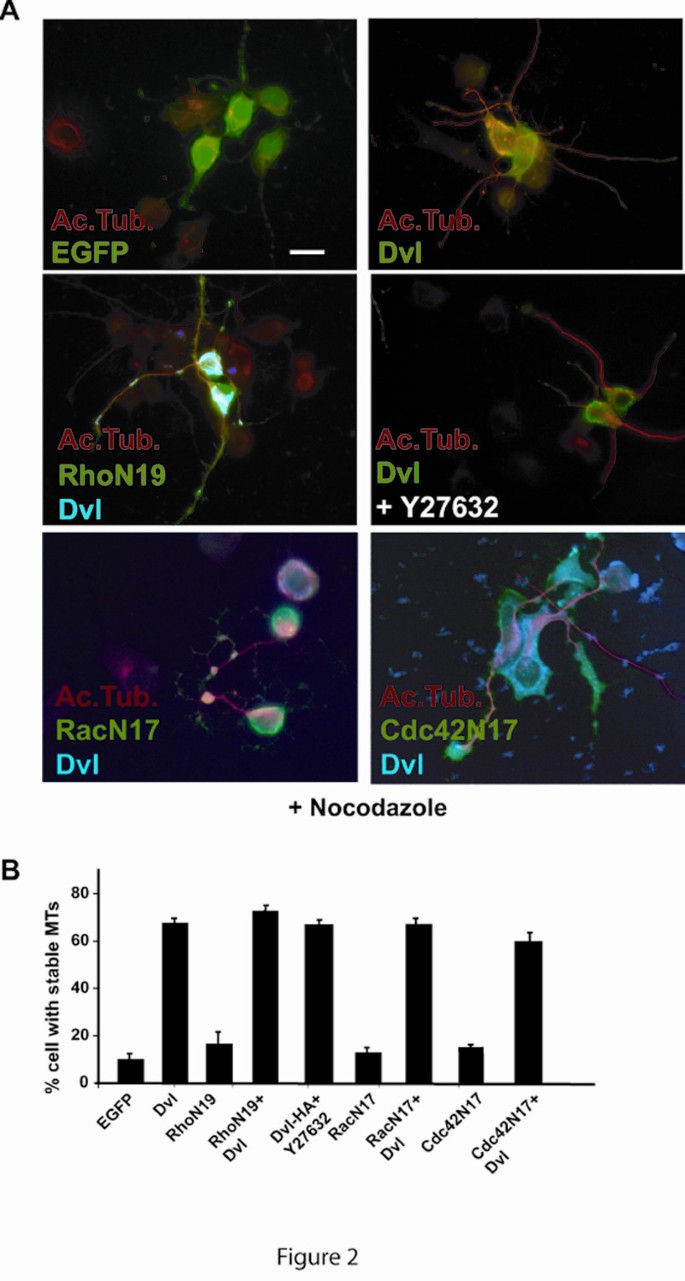
3.2 Rho GTPases在Dvl介导微管稳定性中的作用排除
实验目的:验证PCP通路核心分子Rho、Rac、Cdc42是否参与Dvl的微管稳定调控;方法细节:转染显性负性突变体RhoN19、RacN17、Cdc42N17与Dvl共表达,或采用ROCK抑制剂Y27632处理Dvl转染细胞,检测诺考达唑处理后的稳定微管比例;结果解读:共转染显性负性突变体或ROCK抑制剂处理后,仍有60%-70%的神经元保留稳定微管,与单独转染Dvl的神经元无显著差异,说明Rho GTPases及其下游ROCK通路不参与Dvl介导的微管稳定性调控;产品关联:Rho、Rac、Cdc42构建体由Dr C. Nobes提供,ROCK抑制剂Y27632购自Calbiochem。
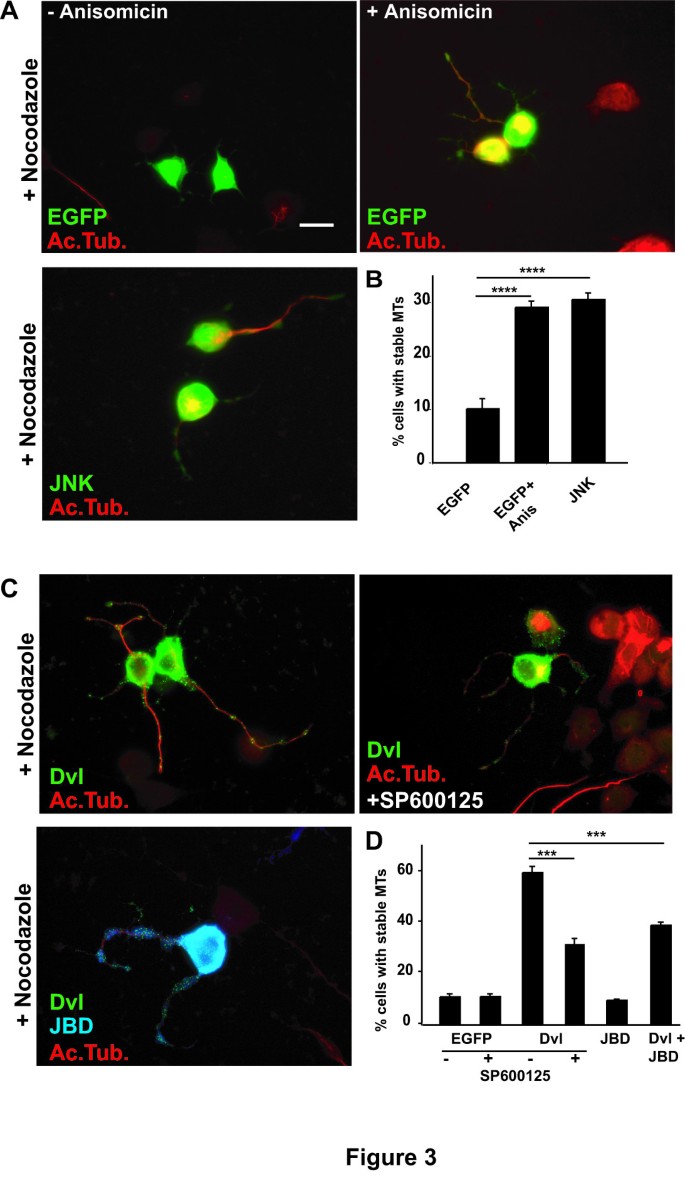
3.3 JNK通路激活对微管稳定性的调控作用
实验目的:验证JNK通路激活是否能诱导微管稳定,且是Dvl微管稳定效应的必需条件;方法细节:采用低浓度茴香霉素直接激活JNK,或转染全长JNK过表达载体,同时使用JNK特异性抑制剂SP600125或显性负性JBD抑制JNK活性,检测稳定微管比例;结果解读:茴香霉素处理或JNK过表达使约30%的神经元在诺考达唑处理后保留稳定微管(对照组仅8%,n=3,P<0.0001),而JNK抑制使Dvl的微管稳定效应降至38%-40%(单独Dvl为60%-65%,n=3,P<0.001),说明JNK激活是Dvl调控微管稳定性的关键环节;产品关联:茴香霉素购自Sigma,SP600125购自Tocris Co,JNK构建体由Roger Davis提供。
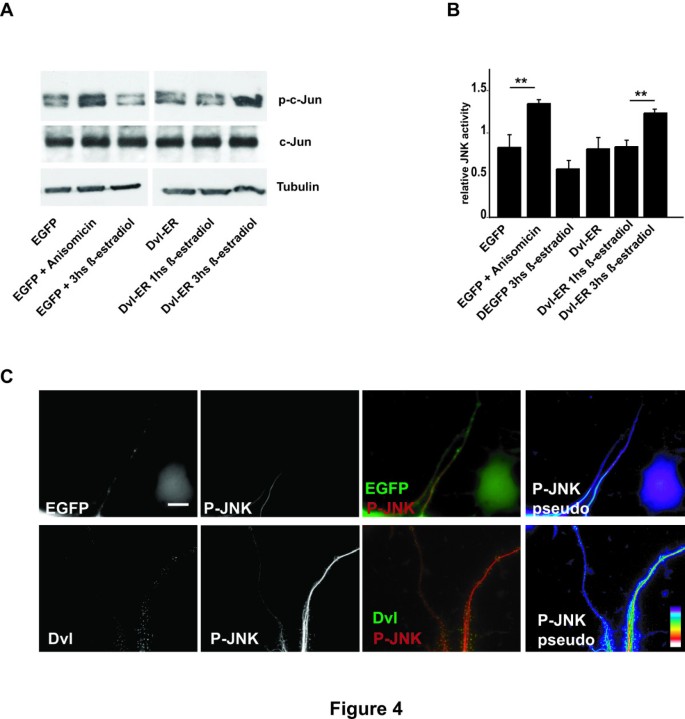
3.4 Dvl激活JNK的直接验证
实验目的:确认Dvl能直接激活神经元内的JNK通路;方法细节:采用Dvl-ER诱导系统(Dvl与雌激素受体融合),通过β-雌二醇处理时间依赖性激活Dvl,以Western blot检测磷酸化c-Jun(JNK活性特异性标志物)的水平,同时通过免疫荧光染色检测磷酸化JNK(p-JNK)与微管的结合情况;结果解读:β-雌二醇激活Dvl 3小时后,p-c-Jun水平较对照组升高40%(n=3,P<0.01),且Dvl表达显著增加了与微管结合的p-JNK水平,证实Dvl可直接激活神经元内的JNK通路;产品关联:p-c-Jun单克隆抗体购自Santa Cruz Biotechnology,免疫荧光二抗购自Molecular Probes。
3.5 Dvl结构域对JNK通路的调控作用
实验目的:明确Dvl中介导JNK通路激活的关键结构域;方法细节:构建缺失DIX、PDZ、DEP结构域的Dvl突变体,转染NB2a细胞后结合JNK抑制剂SP600125处理,检测微管稳定性;结果解读:缺失DEP结构域的ΔDEP-Dvl仍能维持与野生型Dvl相当的微管稳定效应,而缺失DIX或PDZ结构域的ΔDIX-Dvl、ΔPDZ-Dvl仅能维持48%和38%的微管稳定效应,且JNK抑制剂对这两种突变体的效应无额外影响,说明PDZ结构域(及部分DIX结构域)是Dvl激活JNK通路所必需的;产品关联:文献未提及具体标签抗体品牌,领域常规使用HA、Myc、Flag标签抗体进行转染蛋白检测。
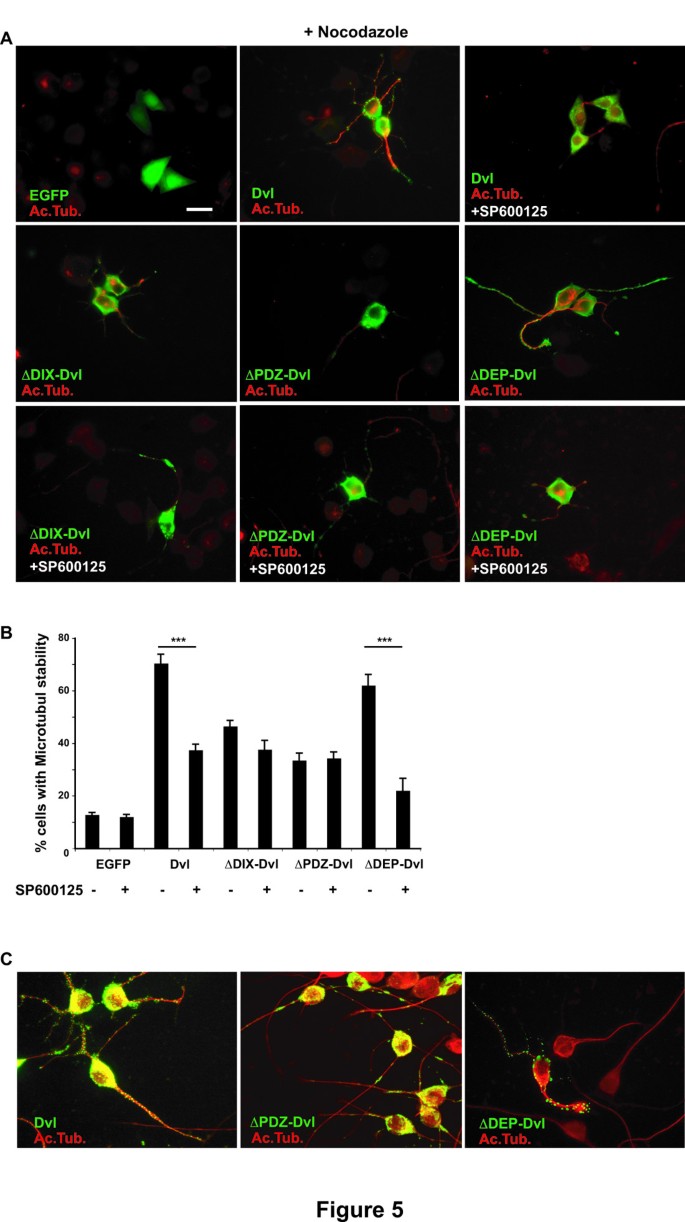
3.6 JNK与Gsk3β通路的独立性验证
实验目的:证明JNK通路与Gsk3β通路独立协同调控Dvl的微管稳定效应;方法细节:共转染Dvl与Gsk3β,同时用SP600125抑制JNK,或用茴香霉素激活JNK,检测微管稳定性及MAP1B的磷酸化水平(Gsk3β活性标志物);结果解读:同时抑制JNK和表达Gsk3β几乎完全阻断Dvl的微管稳定效应,而激活JNK不能逆转Gsk3β对Dvl的抑制作用,且JNK抑制不影响Dvl对MAP1B磷酸化的抑制(即不影响Gsk3β活性),说明两条通路独立发挥作用,共同介导Dvl的微管稳定效应;产品关联:磷酸化MAP1B抗体购自Affinity BioReagents, Inc。
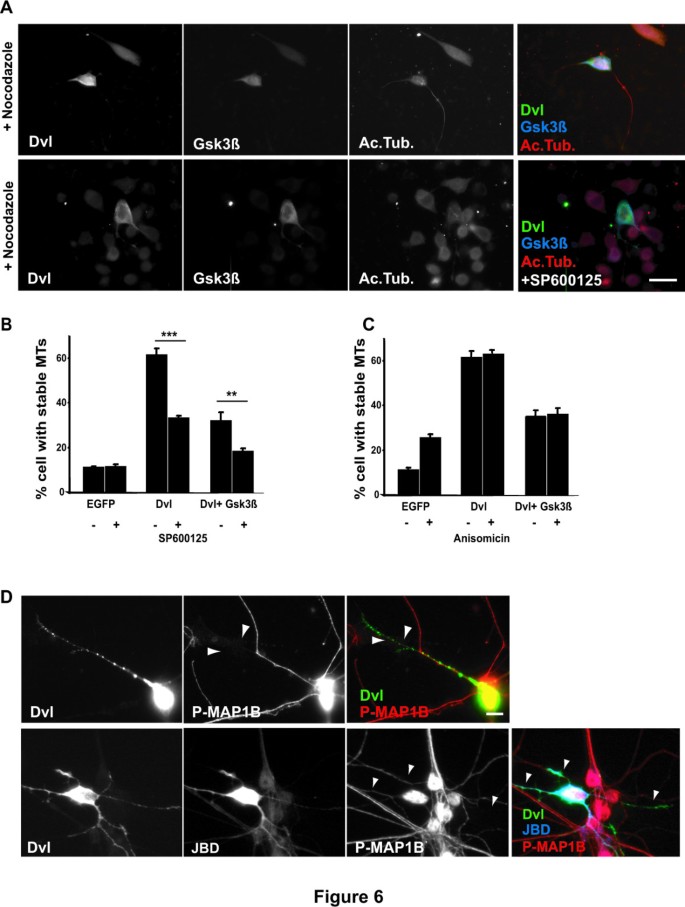
4. Biomarker研究及发现成果解析
Biomarker定位:本研究中鉴定的核心Biomarker为c-Jun N端激酶(JNK),属于Wnt-Dvl信号通路中调控微管稳定性的新型效应分子,筛选与验证逻辑为:首先排除PCP通路核心分子Rho GTPases的参与,基于JNK对细胞骨架的已知调控功能,通过药理学激活/抑制、过表达/显性负性突变等实验验证其在Dvl介导微管稳定性中的作用,最终通过epistatic实验明确其与Gsk3β通路的独立协同关系;研究过程详述:JNK为神经元内源性激酶,验证方法包括:①药理学激活(茴香霉素)与抑制(SP600125)实验,检测微管稳定性变化;②过表达与显性负性突变实验,确认JNK的功能必要性;③Western blot检测p-c-Jun水平,验证Dvl对JNK的激活作用;④免疫荧光染色,确认p-JNK与微管的结合定位;特异性与敏感性数据显示,JNK激活可使神经元稳定微管比例从8%提升至30%(n=3,P<0.0001),抑制JNK可阻断约40%的Dvl微管稳定效应;核心成果提炼:JNK作为Wnt-Dvl通路的新型效应分子,与Gsk3β通路独立协同调控微管稳定性,其功能无需转录参与,直接作用于微管骨架;创新性在于首次揭示Wnt信号通路可同时激活两条独立分支调控复杂细胞过程,为神经元轴突重塑、突触形成的机制研究提供新靶点;统计学结果包括:p-c-Jun水平升高40%(n=3,P<0.01),Gsk3β降低Dvl效应30%(P<0.0001),JNK抑制使Dvl效应降至38%-40%(P<0.001)。
