1. 领域背景与文献引入
文献英文标题:The Cpf1 CRISPR-Cas protein expands genome-editing tools;发表期刊:Genome Biology;影响因子:未公开;研究领域:基因组编辑与CRISPR-Cas系统研究
基因组编辑是生命科学领域的核心技术方向之一,成簇规律间隔短回文重复序列及相关蛋白(CRISPR-Cas)系统的发现与应用推动了该领域的革命性发展。领域共识:CRISPR序列于1987年首次被发现,2002年正式命名为CRISPR-Cas系统;2012年,Charpentier与Doudna团队证明Cas9蛋白可在RNA引导下实现可编程的DNA切割,奠定了其作为主流基因组编辑工具的基础;2013年,首个基于CRISPR-Cas9的真核生物基因组编辑实验成功完成。当前该领域的研究热点集中在拓展CRISPR工具的多样性、提高编辑的特异性与效率、拓展在疾病治疗、合成生物学等场景的应用。然而,现有以Cas9为核心的工具仍存在诸多未解决的核心问题,例如Cas9对富含G的原间隔相邻基序(PAM)的偏好限制了其靶向范围,切割产生的平末端易通过易错的非同源末端连接(NHEJ)修复破坏靶点,影响同源定向修复(HDR)的效率,同时工具的多样性不足也限制了复杂编辑需求的实现。在此背景下,本文聚焦于新型CRISPR-Cas蛋白Cpf1的功能验证与特性解析,旨在填补CRISPR工具库的空白,为基因组编辑提供新的技术选项。
2. 文献综述解析
本文综述部分以CRISPR-Cas系统的进化分类为核心维度,将已研究的系统分为Class1(Type I、III)与Class2(Type II)两大类,系统梳理了不同类型系统的功能机制与应用现状。现有研究已对Class1的Type I、III系统及Class2的Type II(Cas9)系统进行了详细解析,其中Cas9系统因仅需Cas9蛋白及向导RNA即可实现靶向切割,操作简便且可编程性强,已成为应用最广泛的基因组编辑工具,可实现基因敲除、激活、抑制及成像等多种功能。但现有研究也暴露了Cas9系统的局限性,例如其依赖反式激活CRISPR RNA(tracrRNA)与CRISPR RNA(crRNA)形成的双RNA结构(或人工合成的单向导RNA),原间隔相邻基序偏好(如化脓链球菌Cas9需5"-NGG-3")限制了靶向序列的选择范围,切割产生的平末端易引发非同源末端连接修复导致靶点破坏,降低同源定向修复介导的精准编辑效率,同时部分物种中Cas9的编辑效率仍有待提高。此外,已研究的CRISPR-Cas系统类型有限,Class2系统中仅Type II(Cas9)被广泛应用,工具的多样性不足限制了复杂编辑需求的满足。通过对比现有研究的未解决问题,本文的创新价值凸显:首次证明Class2 Type V系统的Cpf1是功能性CRISPR-Cas蛋白,其独特的单CRISPR RNA引导、不同的原间隔相邻基序偏好及切割特性,可弥补Cas9系统的不足,拓展基因组编辑的技术边界。
3. 研究思路总结与详细解析
本文的研究目标是验证Cpf1作为Class2 Type V CRISPR-Cas系统核心蛋白的功能,解析其作用机制与编辑特性,并探索其在人类细胞中的基因组编辑能力;核心科学问题包括Cpf1所属CRISPR-Cas系统的功能验证、Cpf1与Cas9在分子机制及编辑特性上的差异、Cpf1在真核细胞中的编辑效率;技术路线遵循“生物信息学分类验证→原核系统功能解析→真核细胞应用验证”的闭环逻辑,从系统分类到功能特性,逐步推进Cpf1的工具价值验证。
3.1 Cpf1所属CRISPR-Cas系统的功能验证
实验目的是确认Cpf1作为Type V CRISPR-Cas系统核心蛋白的功能性,并解析其原间隔相邻基序偏好。方法细节:研究人员将弗朗西斯菌(Francisella novicida)的cpf1基因、cas基因操纵子及CRISPR阵列克隆至大肠杆菌中,通过构建包含可变原间隔相邻基序序列的质粒文库,筛选Cpf1介导的干扰活性对应的原间隔相邻基序序列。结果解读:实验发现FnCpf1的原间隔相邻基序为5"-TTN-3"和5"-CTA-3"(位于置换链),首次证明Type V CRISPR-Cas系统是功能性的适应性免疫系统;进一步对15种其他Cpf1家族蛋白的分析显示,它们均具有类似的5"-TTN-3"或5"-TTTN-3"原间隔相邻基序偏好,与Cas9的G富集原间隔相邻基序形成互补,可拓展靶向A/T富集基因组的编辑范围。文献未提及具体实验产品,领域常规使用分子克隆试剂、质粒文库构建试剂盒、细菌培养试剂等。
3.2 Cpf1与Cas9的分子机制差异解析
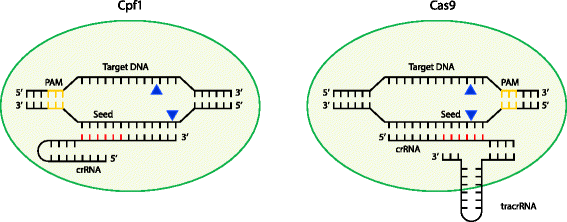
实验目的是对比Cpf1与Cas9在引导RNA需求、切割位点及产物特性上的差异,明确其独特的功能特性。方法细节:通过序列分析、体外核酸切割实验及结构对比,解析两者的RNA组成、切割位点及末端类型。结果解读:Cpf1仅需单一CRISPR RNA即可发挥功能,无需反式激活CRISPR RNA,其CRISPR RNA长度为42-44核苷酸(包含19nt重复序列和23-25nt间隔序列),相比Cas9所需的约100nt单向导RNA更短,降低了向导RNA的合成成本与复杂度;在切割特性上,Cas9通过RuvC和HNH样结构域在种子区内产生平末端双链断裂,而Cpf1仅通过RuvC样结构域在种子区外产生交错末端双链断裂,且原间隔相邻基序位于protospacer的5"端(与Cas9的3"端相反)。这些差异为Cpf1的编辑优势提供了分子基础,例如交错末端可能更有利于同源定向修复,且靶点不易被非同源末端连接修复破坏。对应实验结果如图1所示:
文献未提及具体实验产品,领域常规使用体外转录试剂、核酸电泳试剂、蛋白纯化试剂等。
3.3 Cpf1在人类细胞中的基因组编辑能力验证
实验目的是验证Cpf1在真核细胞中的基因组编辑活性,评估其作为编辑工具的应用潜力。方法细节:研究人员测试了8种不同来源的Cpf1蛋白的体外DNA切割活性,随后将其中活性较强的蛋白导入人类细胞,通过检测插入/缺失(indel)突变率评估体内编辑效率。结果解读:8种Cpf1蛋白均具有体外DNA切割活性,其中来自酸氨基球菌属(Acidaminococcus)和毛螺菌科(Lachnospiraceae)的Cpf1在人类细胞中产生的indel突变率与SpCas9相当;推测Cpf1的交错切割特性可减少非同源末端连接修复对靶点种子区的破坏,使其能够持续切割同一靶点直至同源定向修复完成,从而提高精准编辑效率,但该优势仍需后续实验验证。文献未提及具体实验产品,领域常规使用细胞转染试剂、基因编辑效率检测试剂盒(如T7E1酶切法)等。
4. Biomarker研究及发现成果
本文聚焦于新型CRISPR-Cas基因组编辑工具的开发与特性解析,未涉及疾病相关生物标志物(Biomarker)的筛选、验证或功能研究,核心成果集中在基因组编辑技术工具的拓展领域。
本文的核心技术成果为发现并验证了Cpf1作为Class2 Type V CRISPR-Cas系统的核心蛋白,具有独特的功能特性:仅需单CRISPR RNA引导、偏好A/T富集的原间隔相邻基序、产生交错末端双链断裂,这些特性弥补了现有Cas9工具的不足,拓展了基因组编辑的靶向范围与精准编辑潜力。该研究首次证明Type V CRISPR-Cas系统的功能性,为CRISPR-Cas系统的进化研究提供了新的视角,同时为基因组编辑领域提供了新的技术工具,推动了CRISPR工具库的多样性发展。
