1. 领域背景与文献引入
文献英文标题:Multi-omics approaches to disease;发表期刊:Genome Biology;影响因子:13.214(2017年);研究领域:系统生物学、复杂疾病多组学整合研究
生命科学领域中,组学技术的发展是推动疾病机制研究的核心动力。1990年代人类基因组计划启动,标志着基因组学成为首个成熟的组学领域,随后基因芯片技术的出现实现了转录组的高通量检测;2000年代,表达数量性状位点(eQTL)研究兴起,为基因组关联研究(GWAS)的功能解析提供了工具;下一代测序(NGS)技术的普及则推动了表观基因组学、转录组学、蛋白质组学、代谢组学及微生物组学等多个组学领域的快速发展。当前,复杂疾病(如心血管疾病、神经退行性疾病、代谢综合征等)的研究热点聚焦于多组学数据的整合分析,以解析疾病的多因素交互作用与因果机制。然而,单一组学研究仅能识别疾病相关的分子关联,无法区分因果关系与继发性改变;同时,复杂疾病的异质性、多组学数据的标准化与整合方法的局限性,仍是领域未解决的核心问题。
针对上述领域现状,本文系统综述了多组学技术的类型、多组学研究的实验设计考量、三类核心整合框架及未来发展方向,旨在为复杂疾病的多组学研究提供全面的方法论指导,填补了此前领域内缺乏系统性梳理多组学整合策略的空白,具有重要的学术参考价值。
2. 文献综述解析
本文综述部分以组学技术类型与整合策略为核心分类维度,系统梳理了现有多组学研究的进展、优势与局限性,并通过对比单一组学与多组学研究的差异,凸显多组学整合在疾病机制解析中的创新价值。
现有研究中,各类组学技术已广泛应用于疾病研究:基因组学通过GWAS识别了数千个与复杂疾病相关的遗传变异,但无法直接解析其功能机制;表观基因组学可检测DNA甲基化、组蛋白修饰等可逆调控,为环境与遗传的交互作用提供了研究视角,但存在组织特异性强、数据解读复杂的局限性;转录组学能全面分析RNA表达谱,发现非编码RNA等新型调控分子,但转录水平与蛋白水平的相关性有限;蛋白质组学可直接检测功能分子的表达与修饰,更贴近疾病的功能机制,但检测成本高、通量有限;代谢组学能反映细胞的功能状态,可作为基因型与表型的桥梁,但代谢物的动态变化受环境影响大;微生物组学则揭示了宿主与菌群的交互作用对疾病的影响,但菌群组成的异质性高。单一组学研究多聚焦于识别疾病相关的分子关联,而多组学整合研究则尝试解析分子间的因果关系与调控通路,但现有多组学研究存在实验设计不规范、数据分析方法不统一、样本异质性控制不足等问题。
与现有单一组学研究及零散的多组学研究相比,本文的创新之处在于首次系统提出了多组学整合的三类核心框架(基因组优先、表型优先、环境优先),并详细阐述了各类框架的应用场景与分析策略;同时,本文全面梳理了多组学研究的实验设计要点,包括样本量、数据标准化、动物模型与人类研究的互补性等,为领域内的多组学研究提供了标准化的方法论参考,解决了现有研究中缺乏系统性整合策略指导的问题。
3. 研究思路总结与详细解析
本文的研究目标是系统阐述多组学技术在疾病研究中的应用与整合策略,核心科学问题是如何通过多组学整合解析复杂疾病的分子机制与因果关系,技术路线遵循“组学技术介绍→实验设计考量→整合框架解析→整合方法与网络建模→未来方向展望”的逻辑闭环,全面覆盖多组学研究的核心环节。
3.1 组学技术类型与应用解析
实验目的:系统介绍各类组学技术的原理、应用场景与技术优势,为多组学研究的技术选择提供参考。
方法细节:按基因组学、表观基因组学、转录组学、蛋白质组学、代谢组学、微生物组学的分类,分别阐述各类组学的研究内容、核心技术(如GWAS、NGS、质谱等)及在疾病研究中的应用。
结果解读:明确了各类组学技术的优势与局限性,例如基因组学的遗传变异具有终身稳定性,可作为因果机制解析的锚点;转录组学能全面反映基因表达状态,但与蛋白水平相关性有限;微生物组学揭示了宿主-菌群交互作用的重要性,但数据异质性高。
产品关联:文献未提及具体实验产品,领域常规使用NGS测序平台(如Illumina系列)、质谱分析系统(如Thermo Fisher Orbitrap系列)、生物信息学分析工具(如QIIME、Cytoscape、DESeq2等)。
3.2 多组学研究实验设计考量
实验目的:阐述多组学研究实验设计的核心要素,指导研究者规范开展多组学研究。
方法细节:从疾病病因复杂性、样本量与统计效力、数据分析需求、人类研究与动物模型的互补性四个维度,分析多组学研究的实验设计要点,例如针对复杂疾病需考虑多时间点、多组织样本的采集,通过功率计算确定样本量,提前规划数据分析策略以避免技术偏差。
结果解读:明确了实验设计对多组学研究结果可靠性的关键作用,例如样本量不足会导致统计效力不足,无法检测到真实的关联信号;动物模型可弥补人类研究中环境控制差、组织样本难以获取的局限性,但存在物种差异的问题。
产品关联:文献未提及具体实验产品,领域常规使用生物样本库(如UK Biobank)、实验动物模型(如近交系小鼠)、样本处理标准化试剂盒等。
3.3 多组学数据整合框架解析
实验目的:系统解析三类多组学整合框架的应用场景与分析逻辑,为不同研究目标提供整合策略参考。
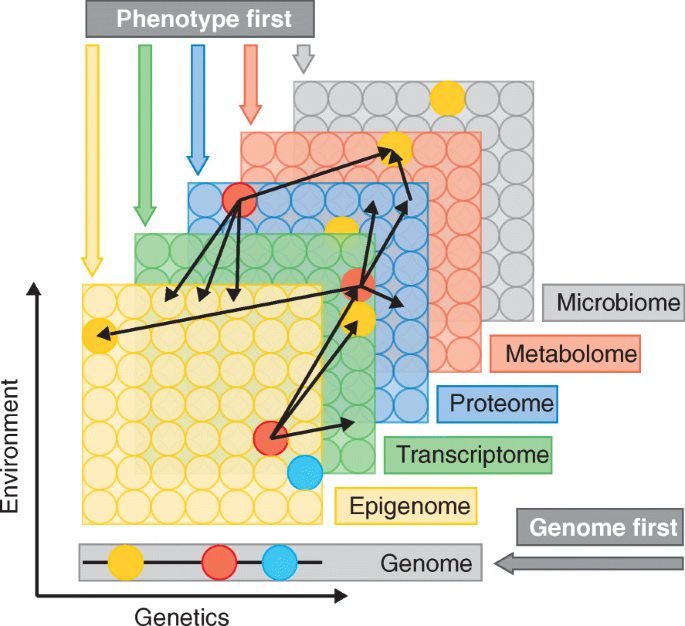
方法细节:将多组学整合框架分为基因组优先、表型优先、环境优先三类,分别通过具体研究案例阐述各类框架的分析流程,例如基因组优先框架以GWAS位点为锚点,结合转录组学、蛋白质组学解析其功能机制;表型优先框架从疾病表型出发,整合多组学数据解析调控通路;环境优先框架聚焦环境因素,分析其与组学数据的交互作用。
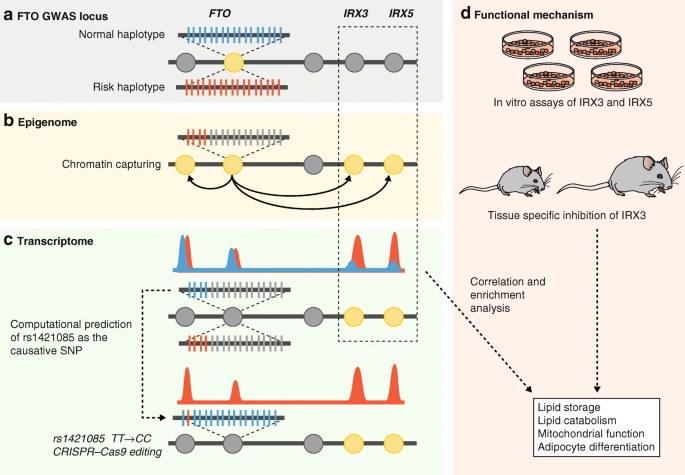
结果解读:通过FTO肥胖位点研究、阿尔茨海默病(AD)研究、饮食与代谢研究等案例,验证了三类整合框架的有效性,例如基因组优先框架成功解析了FTO位点通过调控IRX3/IRX5基因表达影响肥胖的机制;表型优先框架揭示了AD的遗传因素主要通过免疫功能调控,而表观变化主要由环境因素驱动。
3.4 多组学数据整合方法与网络建模
实验目的:阐述多组学数据整合的核心方法与网络建模策略,解析分子间的调控关系。
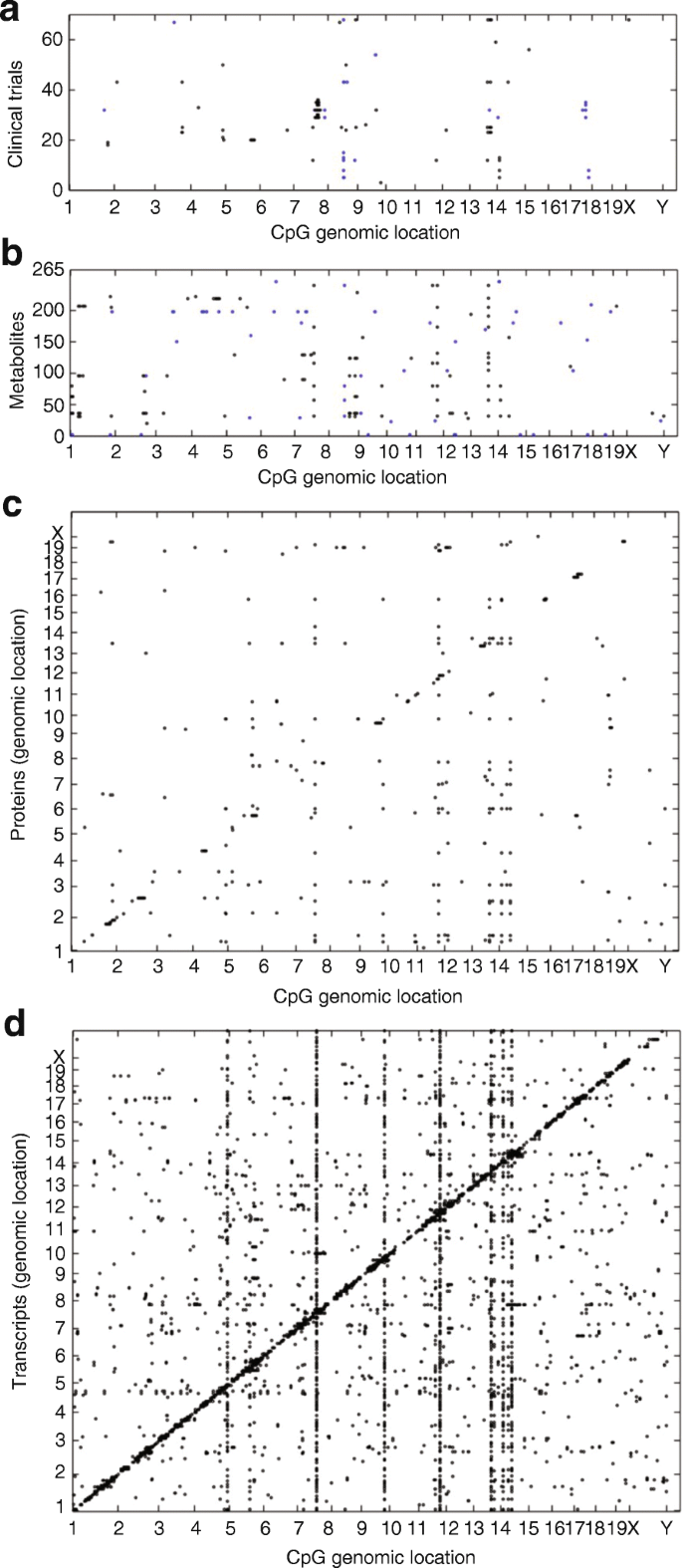
方法细节:介绍了相关性分析、中介分析、网络建模等整合方法,其中网络建模基于分子间的关联构建共表达网络、蛋白互作网络等,结合遗传数据推断因果关系。
结果解读:明确了多组学数据整合可解析分子间的因果关系与调控通路,例如通过网络建模可识别疾病相关的核心调控模块与关键驱动基因,缩小后续功能验证的范围。
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具(如WGCNA、Bayesian网络分析工具)、数据库(如KEGG、STRING)等。
4. Biomarker研究及发现成果解析
本文系统梳理了不同组学类型的Biomarker及其筛选、验证逻辑,强调多组学整合可提升Biomarker的特异性、敏感性与临床应用价值,为复杂疾病的诊断、预后与治疗提供新的分子靶点。
Biomarker定位
文中涉及的Biomarker类型涵盖基因组学(GWAS关联SNP)、表观基因组学(差异甲基化区域)、转录组学(差异表达非编码RNA)、蛋白质组学(差异表达蛋白及修饰)、代谢组学(差异代谢物)、微生物组学(菌群组成特征)。筛选与验证逻辑遵循“高通量组学筛选→多组学整合验证→临床样本验证”的链条,例如通过GWAS筛选疾病关联SNP,结合eQTL、表观组学数据验证其功能,再通过临床样本验证其与疾病表型的相关性。
研究过程详述
不同组学Biomarker的来源与验证方法不同:基因组学Biomarker来源于全基因组遗传变异检测,通过GWAS与连锁分析验证;表观基因组学Biomarker来源于组织或血液样本的DNA甲基化、组蛋白修饰检测,通过表观组关联研究(EWAS)验证;转录组学Biomarker来源于组织或血液样本的RNA-seq检测,通过实时荧光定量聚合酶链反应(qRT-PCR)验证表达水平;蛋白质组学Biomarker来源于组织或体液样本的质谱检测,通过免疫印迹(Western Blot)、酶联免疫吸附试验(ELISA)验证;代谢组学Biomarker来源于血液、尿液等样本的质谱或核磁共振检测,通过靶向代谢组学验证;微生物组学Biomarker来源于粪便、黏膜样本的16S rRNA测序或宏基因组测序,通过qPCR验证菌群丰度。文献未明确提供具体Biomarker的特异性、敏感性数据,但通过案例展示了多组学Biomarker的优势,例如AD研究中免疫相关的表观调控区域与GWAS位点的重叠,提示其作为预后Biomarker的潜力。
核心成果提炼
本文总结了多组学Biomarker的核心价值,相较于单一组学Biomarker,多组学Biomarker能更全面反映疾病的分子状态,提高诊断与预后的准确性;同时,多组学整合可解析Biomarker的功能机制,为治疗靶点的开发提供依据。例如FTO位点的多组学研究,不仅识别了其作为肥胖风险Biomarker的价值,还解析了其调控肥胖的分子机制,为肥胖的治疗提供了新的靶点(IRX3/IRX5基因)。文献未提供具体的统计学结果(如风险比HR值、ROC曲线AUC值),但强调了多组学Biomarker在复杂疾病研究中的创新性与应用前景。
