1. 领域背景与文献引入
文献英文标题:Fetal sex modulates placental microRNA expression, potential microRNA-mRNA interactions, and levels of amino acid transporter expression and substrates: INFAT study subpopulation analysis of n-3 LCPUFA intervention during pregnancy and associations with offspring body composition;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:胎儿发育营养与胎盘分子调控。
儿童肥胖已成为全球重大公共卫生与经济负担,胎儿编程理论指出孕期与哺乳期是预防儿童肥胖的关键窗口期,母体内环境可通过调控胎儿组织发育影响其长期代谢健康。n-3长链多不饱和脂肪酸(LCPUFA)被认为可通过调节基因表达改变脂肪组织发育,是潜在的儿童肥胖一级预防策略。胎盘作为母胎营养交换的核心界面,其营养转运功能直接调控胎儿生长,但目前关于胎盘分子调控的性别二态性,尤其是微小核糖核酸(miRNA)介导的基因表达网络,以及这些调控与后代长期体成分的关联尚未被系统揭示。前期INFAT研究已发现胎盘mRNA表达存在性别特异性的n-3长链多不饱和脂肪酸响应,但微小核糖核酸层面的调控机制仍不明确,本研究旨在填补这一空白,通过整合微小核糖核酸表达谱、靶标验证、氨基酸检测与临床数据,解析胎盘微小核糖核酸-mRNA互作网络的性别差异,及其与后代体成分的关联。
2. 文献综述解析
作者的综述逻辑围绕“儿童肥胖的公共卫生问题→胎儿编程的关键作用→n-3长链多不饱和脂肪酸的调控机制→胎盘的核心功能→微小核糖核酸的调控潜力→现有研究不足”展开,分类维度涵盖公共卫生、分子机制、临床研究三个层面。现有研究显示,n-3长链多不饱和脂肪酸可通过PPARγ等核受体通路调控胎盘营养转运相关基因表达,但其具体调控网络仍不清晰;胎盘微小核糖核酸具有高度组织特异性,且在胎盘发育中发挥关键作用,但微小核糖核酸与氨基酸转运体的直接调控关系尚未被证实;多数研究基于细胞或动物模型,缺乏人类孕期营养干预的临床样本数据,尤其是针对胎儿性别分层的分析,无法揭示性别特异性的调控机制。本研究的创新价值在于,首次在人类随机对照干预队列中,结合多组学技术与长期临床随访数据,系统解析了胎盘微小核糖核酸-99a(miR-99a)介导的性别特异性调控网络,明确了其与氨基酸转运及后代体成分的关联,为孕期营养干预的精准化提供了分子依据。
3. 研究思路总结与详细解析
本研究以探索n-3长链多不饱和脂肪酸干预下胎盘微小核糖核酸-mRNA互作的性别二态性及其与后代体成分的关联为核心目标,围绕“微小核糖核酸筛选→靶标预测→实验验证→关联分析”的闭环技术路线展开,核心科学问题聚焦于胎儿性别如何通过胎盘微小核糖核酸调控氨基酸转运通路,进而影响后代生长发育轨迹。
3.1 探索性胎盘微小核糖核酸表达谱分析
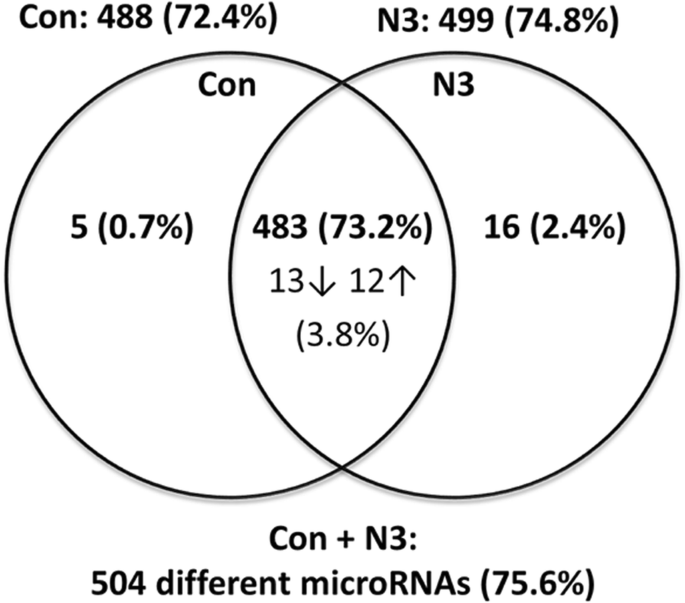
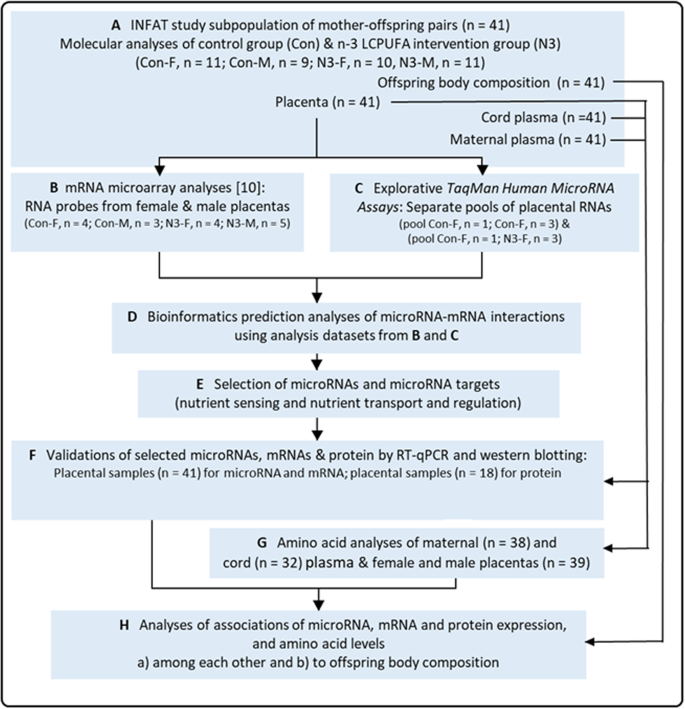
本环节的核心目标是筛选n-3长链多不饱和脂肪酸干预下女性胎盘组织中差异表达的微小核糖核酸。研究选取INFAT队列中对照组与n-3长链多不饱和脂肪酸干预组各3例女性后代的胎盘样本,提取含小RNA的总RNA并分别混合成组特异性样本池,采用384孔TaqMan低密度人类微小核糖核酸芯片对667种人类微小核糖核酸进行检测。结果显示,两组共检测到504种微小核糖核酸,其中46种呈现差异表达特征,包括25种在两组间表达水平显著差异的微小核糖核酸(12种上调、13种下调),以及21种仅在单组中检测到表达的微小核糖核酸;染色体19微小核糖核酸簇(C19MC)的43种微小核糖核酸在两组中均有表达,其中微小核糖核酸-517b与微小核糖核酸-522呈现显著的干预响应差异。
文献未提及具体实验产品,领域常规使用TaqMan微小核糖核酸芯片、TRIzol总RNA提取试剂等。
3.2 微小核糖核酸-mRNA互作预测与靶标筛选
本环节旨在预测差异微小核糖核酸的靶mRNA,并筛选与营养感知及氨基酸转运相关的调控对。研究利用DIANA mirExTra生物信息学工具,将前期筛选得到的46种差异微小核糖核酸与INFAT队列中n-3长链多不饱和脂肪酸调控的459种mRNA进行结合位点分析,结合已发表文献筛选参与营养转运通路的微小核糖核酸及其靶基因。结果显示,23种微小核糖核酸在差异mRNA上的结合位点显著富集,其中微小核糖核酸-99a、微小核糖核酸-30d、微小核糖核酸-100、微小核糖核酸-320被预测靶向mTOR、SLC7A5(编码L型氨基酸转运体1,LAT1)、SLC6A6(编码牛磺酸转运体,TauT)等营养感知与转运相关基因,最终微小核糖核酸-99a及其靶基因因在氨基酸转运调控中的核心作用被选为后续验证对象。
文献未提及具体实验产品,领域常规使用DIANA系列生物信息学分析工具、miRDB靶标预测数据库等。
3.3 分子表达的性别特异性与干预响应验证
本环节的核心目标是验证微小核糖核酸-99a及其靶基因在不同性别、不同干预组胎盘组织中的表达差异。研究选取INFAT队列中41例胎盘样本(对照组20例,干预组21例,涵盖男女后代),采用逆转录实时定量PCR(RT-qPCR)检测微小核糖核酸-99a、mTOR mRNA、SLC7A5 mRNA、SLC6A6 mRNA的表达水平,采用蛋白印迹法(Western blot)检测LAT1蛋白表达。结果显示,微小核糖核酸-99a在干预组胎盘的表达水平显著高于对照组(1.49倍,n=41,p=0.001),且仅女性后代的胎盘在干预后呈现显著的表达上调(1.86倍,n=21,p<0.001);对照组中男性后代胎盘的mTOR、SLC7A5 mRNA表达水平显著高于女性,而干预组中女性后代胎盘的这些靶基因表达显著上调,使得性别间的表达水平趋于平衡;LAT1蛋白在男性后代胎盘的表达水平显著低于女性,且干预组整体表达水平显著降低(1.35倍,n=41,p=0.010)。
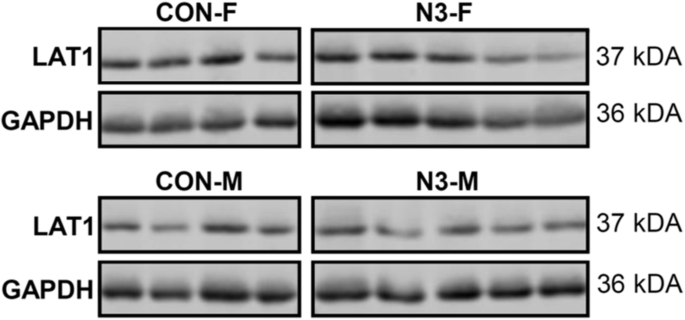
实验所用关键产品:Sigma Aldrich的LAT1抗体、Ambion的GAPDH内参抗体、LI-COR的红外荧光二抗。
3.4 母胎循环氨基酸水平检测与关联分析
本环节旨在检测母胎循环中氨基酸底物的水平,并分析其与分子表达的关联。研究采集孕32周母血、脐血及胎盘组织样本,采用液相色谱-串联质谱(LC-MS/MS)检测LAT1底物色氨酸与TauT底物牛磺酸的水平,并通过相关性分析探索其与微小核糖核酸-99a及靶基因表达的关联。结果显示,干预组孕32周母血中色氨酸水平显著升高、牛磺酸水平显著降低,且存在性别特异性差异:干预组中女性后代母亲的色氨酸水平显著高于对照组,男性后代母亲的牛磺酸水平显著低于对照组;脐血牛磺酸水平在干预组男性后代中显著高于女性;mTOR mRNA与胎盘组织中的牛磺酸、色氨酸水平呈显著正相关,LAT1蛋白与脐血牛磺酸水平呈显著正相关。
文献未提及具体实验产品,领域常规使用LC-MS/MS系统、aTRAQ氨基酸衍生试剂等。
3.5 分子表达与后代体成分的关联分析
本环节的核心目标是探索胎盘分子表达、氨基酸水平与后代出生至5岁体成分的关联。研究收集后代出生、1岁、3岁、5岁的体成分数据(包括体重、瘦体重、脂肪量等),采用线性回归分析探索各分子指标与后代体成分的关联。结果显示,mTOR mRNA与出生时体重/胎盘重量比呈显著正相关,微小核糖核酸-99a与该比值呈显著负相关;SLC7A5 mRNA与1岁时的体重、瘦体重及3岁时的脂肪量呈显著正相关;母血色氨酸水平与1岁、5岁时的体重,1岁、3岁时的瘦体重,3岁时的脂肪量呈显著正相关;母血牛磺酸水平与1岁、3岁时的体重呈显著负相关。
文献未提及具体实验产品,领域常规使用体成分测量设备(如皮褶厚度计、生物电阻抗分析仪)、SPSS统计分析软件等。
4. Biomarker研究及发现成果解析
本研究涉及的生物标志物(Biomarker)包括胎盘微小核糖核酸-99a、mTOR mRNA、SLC7A5 mRNA,以及母胎循环中的色氨酸与牛磺酸,筛选与验证逻辑为:基于女性胎盘微小核糖核酸表达谱筛选差异微小核糖核酸→生物信息学预测靶标mRNA→大样本临床验证分子表达的性别特异性与干预响应→检测氨基酸底物水平→关联分析与后代体成分的关系。
研究过程中,Biomarker的来源涵盖人类胎盘组织、孕32周母血及脐血样本;验证方法包括逆转录实时定量PCR检测微小核糖核酸与mRNA表达、蛋白印迹法检测蛋白表达、液相色谱-串联质谱检测氨基酸水平;特异性与敏感性数据显示,微小核糖核酸-99a在干预组女性胎盘的表达上调具有高度性别特异性(n=21,p<0.001),SLC7A5 mRNA在对照组男性胎盘的基础表达显著高于女性(n=20,p=0.001);母血色氨酸水平在干预组的受试者工作特征曲线(ROC)数据未明确提供,但与后代5岁体重的关联具有统计学意义(p<0.05)。
核心成果方面,该研究首次揭示胎盘微小核糖核酸-99a介导的性别特异性调控网络,微小核糖核酸-99a可通过调控mTOR、SLC7A5、SLC6A6等基因参与氨基酸转运,且这些分子与母胎循环中的氨基酸水平共同影响后代体成分;微小核糖核酸-99a与mTOR、SLC7A5 mRNA呈正相关,与SLC6A6 mRNA呈负相关,提示其可能通过转录后调控与转录激活的双重机制发挥作用;母血色氨酸、牛磺酸水平与后代长期体成分的关联,为孕期营养干预的精准化提供了潜在靶点。此外,研究还发现这些Biomarker可作为预测后代体成分的潜在指标,其中SLC7A5 mRNA与后代1岁瘦体重的关联风险比(HR)数据未明确提供,但相关性分析显示显著正相关(p=0.003)。
