1. 领域背景与文献引入
文献英文标题:Dysregulated transcriptional networks in KMT2A- and MLLT10-rearranged T-ALL;发表期刊:Biomark Res;影响因子:未公开;研究领域:T系急性淋巴细胞白血病(T-ALL)分子机制与靶向治疗靶点研究
T系急性淋巴细胞白血病是儿童及青少年群体中常见的血液系统恶性肿瘤,当前临床治疗虽能使80%-90%的初治患者获得治愈,但复发患者的无事件生存率不足10%,且缺乏可指导精准治疗的特异性分子标志物。传统剂量强化治疗方案虽试图改善高危患者预后,却仅增加了治疗相关毒性,未显著提升生存获益,因此亟需挖掘驱动疾病进展的分子机制以开发靶向治疗策略。领域共识:KMT2A基因重排与T-ALL患者的诱导治疗失败及不良预后密切相关,而MLLT10基因重排的临床预后价值仍存在争议,现有研究对这两类基因组异常在T-ALL中的转录调控网络解析较为有限,尤其是缺乏大样本队列的系统分析,无法为临床靶向治疗提供可靠依据。本研究正是针对这一领域空白,通过大样本转录组学分析,旨在识别KMT2A重排和MLLT10重排T-ALL中具有生物学意义的差异表达基因及信号通路,为高危患者的靶向治疗提供潜在靶点。
2. 文献综述解析
作者以T-ALL的基因组异常亚型为分类维度,系统梳理了现有研究中KMT2A重排、MLLT10重排与疾病预后及分子机制的关联,重点指出了当前研究在样本量、分析深度及临床转化价值上的局限性。
现有研究已证实T-ALL存在高度基因组异质性,但这类异常尚未应用于临床治疗分层;KMT2A基因可与超过100种伴侣基因发生重排,其中KMT2A-MLLT4融合及3"KMT2A缺失是HOXA基因失调T-ALL的高危预后因素,而MLLT10重排的预后价值仍存在争议,不同研究结论相悖。部分研究通过基因表达谱分析在急性髓系白血病(AML)和B系急性淋巴细胞白血病(B-ALL)中建立了KMT2A重排的转录特征,但针对T-ALL的相关研究仅涉及3例KMT2A-MLLT1融合病例,样本量极小,无法全面揭示这类重排的转录调控网络。现有研究的技术方法虽能识别白血病的分子亚型,但普遍缺乏对KMT2A重排和MLLT10重排T-ALL的系统分析,也未对潜在靶向靶点进行独立队列验证,限制了研究成果的临床转化。
本研究的创新价值在于首次基于100例T-ALL大样本队列,系统解析了KMT2A重排和MLLT10重排的转录组差异,识别出RUNX2、TCF4、MYO6等未被报道的潜在靶点,并通过两个独立队列验证了结果的可靠性,同时解析了相关功能通路,为高危T-ALL的靶向治疗提供了新的研究方向。
3. 研究思路总结与详细解析
本研究以“大样本转录组分析筛选差异基因→独立队列验证→功能通路富集解析”为核心技术路线,旨在明确KMT2A重排和MLLT10重排T-ALL的异常转录网络及潜在治疗靶点,核心科学问题为两类基因重排如何通过调控下游基因及通路驱动T-ALL的发生发展,以及不同重排亚型之间的转录差异。
3.1 大样本T-ALL队列转录组数据获取与预处理
该环节的核心目标是获取高质量的T-ALL患者转录组数据,为后续差异基因分析奠定基础。研究纳入儿童肿瘤组AALL0434研究中的100例T-ALL患者样本,采用Affymetrix U133 Plus 2.0基因表达芯片进行转录组检测,同时设置严格的芯片质量控制标准:缩放因子<40,甘油醛-3-磷酸脱氢酶(GAPDH)3"端信号强度>15000,GAPDH 3"/5"比值<3,确保数据的可靠性。随后使用Robust Multi-array Average算法对信号强度进行归一化处理,并过滤性别相关基因、珠蛋白基因及内参基因,排除无关干扰。结果显示,最终获得符合质量控制要求的100例样本转录组数据,其中KMT2A重排患者12例,MLLT10重排患者9例,其余79例为无该两类重排的T-ALL患者。文献未提及具体实验产品,领域常规使用Affymetrix系列基因表达芯片、R语言相关生物信息学分析软件等。
3.2 差异表达基因筛选与亚型转录特征分析
本环节旨在筛选KMT2A重排、MLLT10重排与其他T-ALL患者之间的差异表达基因,同时解析不同重排亚型的转录差异。研究采用R包limma中的线性模型进行差异表达探针集分析,通过Benjamini和Hochberg方法计算错误发现率(FDR)以校正多重检验,设定FDR≤0.05为差异有统计学意义;同时针对KMT2A重排的两个亚型(KMT2A-MLLT4和KMT2A-MLLT1)进行亚组差异基因分析。结果显示,共识别出330个可区分三组患者的探针集,其中KMT2A重排组有258个差异探针集,242个基因表达上调,包括RUNX2、TCF4、MYO6、PROM1等未被报道的潜在靶点,仅16个基因表达下调;MLLT10重排组有40个差异探针集,39个基因表达上调,包括HOXA家族基因、MEIS1、CASC10等,仅1个基因表达下调;值得注意的是,编码RNA结合蛋白的QKI基因在两类重排患者中均呈显著下调趋势。进一步对比KMT2A重排与MLLT10重排患者的转录组数据发现,MYO6、RUNX2等基因在KMT2A重排组中的表达水平显著更高,提示KMT2A重排T-ALL具有独特的生物学特征;而KMT2A-MLLT4与KMT2A-MLLT1亚型相比,MLLT4基因及未注释的RP11-38P22基因表达上调,另有24个基因表达下调,包括SEPW1、SMAD1等。

3.3 独立队列验证
为确保差异表达基因分析结果的可靠性,本环节采用两个独立公开数据集进行验证。研究选取Soulier数据集(含92例T-ALL患者,其中3例为KMT2A-MLLT1融合,4例为PICALM-MLLT10融合)和Dik数据集(含23例T-ALL患者,其中6例为PICALM-MLLT10融合)进行差异基因表达分析。结果显示,两个独立队列的分析结果与本研究大样本队列的结果存在显著重叠,证实KMT2A重排和MLLT10重排确实驱动T-ALL形成独特的转录程序,差异表达基因的一致性较高,进一步验证了本研究结果的可靠性。
3.4 功能通路富集分析
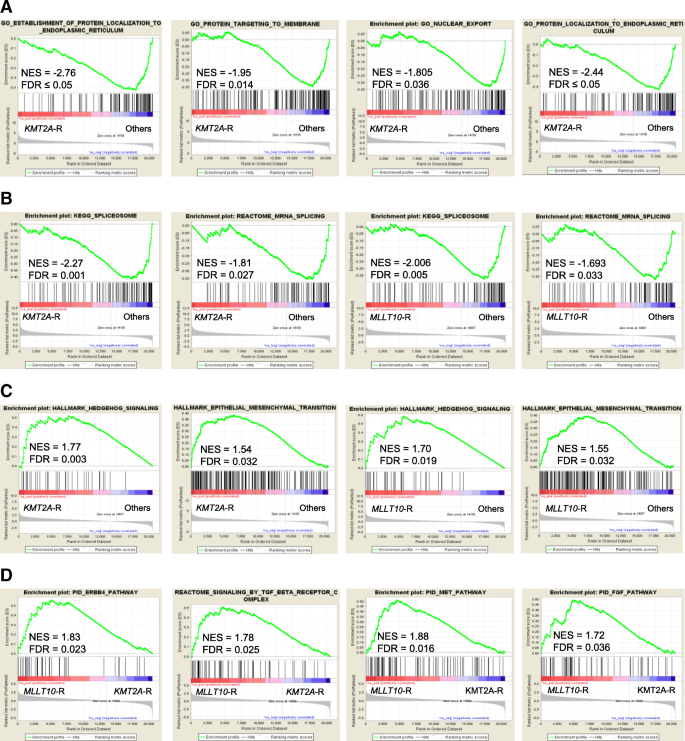
本环节旨在解析KMT2A重排和MLLT10重排T-ALL的异常信号通路,挖掘潜在的治疗靶点。研究采用基因集富集分析(GSEA)进行基因本体及经典通路分析,识别与两类基因重排相关的功能网络。结果显示,KMT2A重排患者在蛋白输出、细胞内蛋白定位与转运通路呈负富集,提示该通路的失调可能参与肿瘤发生;同时在细胞外基质组织、胶原形成及上皮间质转化通路呈正富集,而上皮间质转化已被证实与白血病细胞的迁移及耐药相关。MLLT10重排患者在胚胎发育通路呈正富集,在细胞周期、DNA合成与修复通路呈负富集;两类重排患者均在可变剪接及mRNA加工通路呈负富集,这一结果可能与QKI基因的下调相关,而可变剪接失调已被证实可促进基因组不稳定性及恶性转化。此外,两类重排患者均在刺猬(Hedgehog)信号通路呈正富集,已有研究证实该通路抑制剂对部分T-ALL患者有效,提示这类患者可能从刺猬信号通路抑制剂治疗中获益;与KMT2A重排患者相比,MLLT10重排患者在Met、TGFB、ERBB等酪氨酸激酶通路呈正富集,而这些通路已有FDA批准的靶向抑制剂,具有潜在的临床转化价值。
4. Biomarker研究及发现成果
本研究通过大样本转录组分析,识别出KMT2A重排和MLLT10重排T-ALL的特异性差异表达基因及异常信号通路,这些分子及通路可作为潜在的生物标志物和治疗靶点,筛选逻辑为“大样本队列转录组差异分析→独立队列验证→功能通路富集解析”的完整链条。
本研究中潜在生物标志物的来源为100例T-ALL患者的临床样本转录组数据,验证方法为两个独立公开T-ALL数据集的转录组分析;特异性方面,RUNX2、MYO6、TCF4等基因在KMT2A重排患者中的表达显著高于MLLT10重排患者及其他T-ALL患者(FDR≤0.05,n=100),QKI基因在两类重排患者中均呈显著下调趋势;敏感性方面,差异表达基因在两个独立队列中均得到验证,结果一致性较高。
核心成果方面,本研究首次在大样本T-ALL队列中系统解析了KMT2A重排和MLLT10重排的异常转录网络,识别出RUNX2、TCF4、MYO6等未被报道的潜在靶向基因,同时证实两类重排患者均激活刺猬信号通路,提示这类患者可能对刺猬信号通路抑制剂敏感;MLLT10重排患者还激活多个酪氨酸激酶通路,可使用已有的靶向抑制剂进行治疗;这些发现为高危T-ALL患者的精准治疗提供了新的候选靶点及通路,目前暂未获得相关生物标志物的预后风险比数据,但所有差异基因的统计学显著性均满足FDR≤0.05(n=100)。
