1. 领域背景与文献引入
文献英文标题:Molecular characterization of HIV-1 genome in fission yeast Schizosaccharomyces pombe;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:HIV-1病毒学与模式生物功能研究
人类免疫缺陷病毒1型(HIV-1)是获得性免疫缺陷综合征(艾滋病)的病原体,其约9.7 kb的RNA基因组编码多种结构蛋白(Gag、Pol、Env)、调节蛋白(Rev、Tat)和辅助蛋白(Vpu、Vif、Vpr、Nef),病毒的生命周期依赖这些蛋白与宿主细胞的精准相互作用。领域共识:HIV-1蛋白功能的传统研究主要依赖哺乳动物细胞模型,但该模型存在操作流程复杂、宿主背景干扰因素多、实验周期长等局限性。裂殖酵母(Schizosaccharomyces pombe)作为经典的模式真核生物,具有与高等真核生物相似的细胞周期调控机制、信号转导通路和RNA剪接系统,且遗传操作简便、生长周期短,已被用于部分HIV-1蛋白的初步功能研究。然而,目前尚未有研究在裂殖酵母中系统分析HIV-1全基因组编码蛋白的亚细胞定位和功能效应,这一研究空白限制了对HIV-1蛋白功能的全面理解以及酵母模型在HIV-1研究中的广泛应用。本研究旨在填补这一空白,通过在裂殖酵母中系统表达所有HIV-1编码蛋白,解析其亚细胞定位和对细胞增殖的影响,并深入探究关键蛋白Rev的作用机制,为利用裂殖酵母模型研究HIV-1蛋白功能提供全面的实验依据。
2. 文献综述解析
作者围绕HIV-1蛋白功能研究和模式生物应用两个核心维度,系统梳理了领域内的研究进展与现存空白。现有研究中,HIV-1各蛋白的功能在哺乳动物细胞中已被部分阐明:Gag蛋白参与病毒组装与成熟,Pol蛋白编码病毒复制所需的关键酶(蛋白酶、逆转录酶、整合酶),Env蛋白介导病毒进入宿主细胞,调节蛋白Rev和Tat分别调控病毒RNA的核输出和转录激活,辅助蛋白则参与病毒感染的多个环节。在模式生物应用方面,裂殖酵母和酿酒酵母已被用于研究部分HIV-1蛋白的细胞效应,比如Vpr对细胞周期的调控、Rev对RNA剪接的影响等,这些研究证明酵母模型具有操作简便、背景干扰少的优势,但局限性在于仅针对单个或少数蛋白进行分析,缺乏全基因组层面的系统对比,无法全面评估酵母模型与哺乳动物细胞模型的一致性。本研究的创新价值在于首次在裂殖酵母中系统表达并分析所有HIV-1编码蛋白的亚细胞定位和功能效应,通过与哺乳动物细胞中的研究结果对比,验证了裂殖酵母作为HIV-1蛋白功能研究模型的可行性,为后续利用酵母模型开展HIV-1蛋白的高通量功能筛选和机制研究奠定了基础。
3. 研究思路总结与详细解析
本研究的整体思路为“全基因组克隆与表达→亚细胞定位分析→功能效应筛选→关键蛋白机制解析→跨模型验证”,研究目标是系统解析HIV-1全基因组编码蛋白在裂殖酵母中的亚细胞定位和功能效应,验证裂殖酵母作为HIV-1蛋白研究模型的可行性;核心科学问题是HIV-1各蛋白在裂殖酵母中的亚细胞定位是否与哺乳动物细胞一致,哪些蛋白会影响裂殖酵母的细胞增殖,以及其作用机制是否在哺乳动物细胞中保守;技术路线遵循“基因克隆→表达载体构建→诱导表达→表型检测→机制验证→跨模型验证”的闭环逻辑。
3.1 HIV-1基因克隆与裂殖酵母诱导表达体系构建
实验目的是构建可在裂殖酵母中可控表达所有HIV-1编码蛋白的重组载体,为后续功能分析提供工具。方法细节:以携带完整HIV-1基因组的pNL4-3质粒为模板,通过PCR技术克隆除rev和tat外的所有HIV-1基因,其中rev基因来自PSV-Rev质粒,tat基因来自ptatC6H质粒;将克隆得到的基因分别插入裂殖酵母诱导表达载体pYZ1N(用于细胞增殖功能分析)和pYZ3N(N端融合绿色荧光蛋白GFP,用于亚细胞定位分析),两种载体均携带nmt1启动子,可通过培养基中硫胺素的存在(抑制表达)或缺失(诱导表达)实现基因表达的精准调控;通过电穿孔法将重组载体转化至野生型裂殖酵母SP223菌株,利用载体携带的营养缺陷型标记筛选阳性转化子,并通过Sanger测序验证插入基因的序列正确性。结果解读:成功构建了覆盖HIV-1全基因组的15个基因的裂殖酵母表达载体,所有插入基因的序列与预期一致,确保后续实验的可靠性。产品关联:文献未提及具体实验产品,领域常规使用PCR扩增试剂盒、限制性内切酶、T4 DNA连接酶等分子克隆试剂,以及电穿孔仪、DNA测序仪等仪器设备。
3.2 HIV-1蛋白亚细胞定位分析
实验目的是明确各HIV-1编码蛋白在裂殖酵母中的亚细胞分布模式,并与哺乳动物细胞中的定位结果进行对比,评估酵母模型的相关性。方法细节:将携带GFP融合HIV-1蛋白的pYZ3N重组载体转化裂殖酵母,先在含20μM硫胺素的EMM培养基中培养至对数生长期以抑制基因表达,随后收集细胞并洗涤去除硫胺素,转移至无硫胺素的EMM培养基中诱导表达24-30小时;收集诱导表达后的细胞,用4",6-二脒基-2-苯基吲哚(DAPI)染色细胞核,通过荧光显微镜分别观察GFP信号(蛋白定位)和DAPI信号(细胞核定位),并通过图像融合分析蛋白的亚细胞分布。结果解读:GFP单独表达时均匀分布于整个细胞内,作为定位参照;Gag前体蛋白在细胞质中形成未知聚集位点,与哺乳动物细胞中的定位模式一致;结构蛋白P17(MA)仅定位于细胞质,P24(CA)同时分布于细胞核和细胞膜,P7(NC)主要定位于细胞核,P6均匀分布于细胞;Pol家族蛋白中,P66(逆转录酶大亚基)主要定位于细胞核,P51(逆转录酶小亚基)仅分布于细胞质,IN(整合酶)主要定位于细胞核,PR(蛋白酶)均匀分布;Env家族蛋白Gp120和Gp41主要定位于细胞核;调节蛋白Rev、Tat和辅助蛋白Vpr、Vif主要定位于细胞核,Vpu仅分布于细胞质,Nef均匀分布于细胞。整体来看,HIV-1蛋白在裂殖酵母中的亚细胞定位与哺乳动物细胞中的已有报道存在普遍一致性,证明裂殖酵母模型可在一定程度上模拟HIV-1蛋白在高等真核细胞中的分布特征。
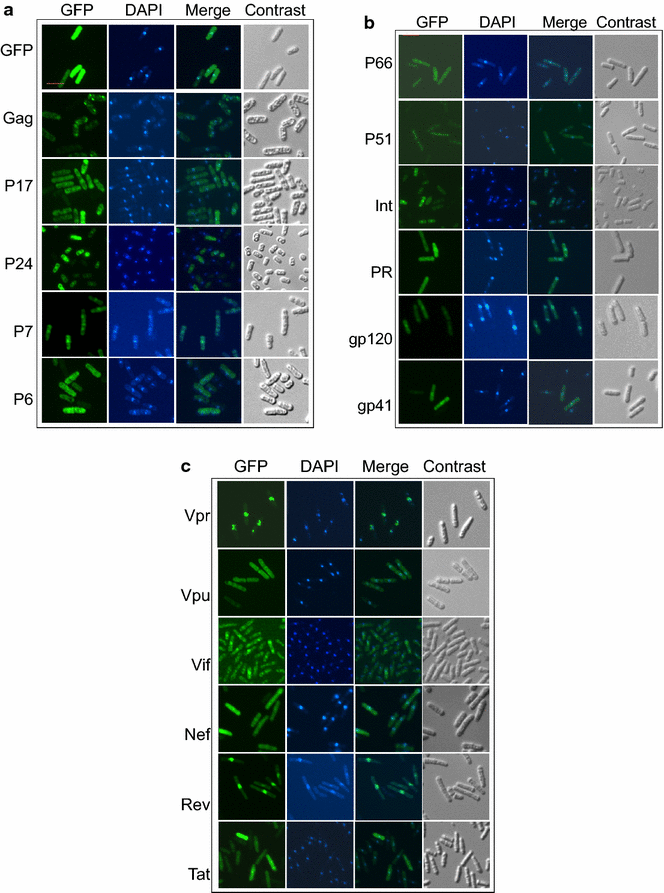
产品关联:文献未提及具体实验产品,领域常规使用荧光显微镜、DAPI染色剂、细胞培养耗材等。
3.3 HIV-1蛋白对裂殖酵母细胞增殖的影响筛选
实验目的是筛选出对裂殖酵母细胞增殖具有显著效应的HIV-1蛋白,为后续机制研究提供靶点。方法细节:将携带HIV-1基因的pYZ1N重组载体转化裂殖酵母,在含硫胺素的EMM液体培养基中培养至对数生长期,收集细胞并洗涤去除硫胺素,将细胞梯度稀释后分别接种至含硫胺素(基因抑制)和不含硫胺素(基因诱导)的EMM固体培养基,30℃培养6天后观察菌落形成情况;以表达HIV-1 Vpr的菌株为阳性对照(已知Vpr抑制裂殖酵母菌落形成),以空pYZ1N载体转化菌株为阴性对照。结果解读:在基因抑制条件下,所有转化菌株均形成大小一致的正常菌落;在基因诱导条件下,空载体对照菌株和多数HIV-1基因表达菌株形成与对照大小相近的菌落,但表达Vpr、PR和Rev的菌株菌落显著减小或无法形成,表明这三种蛋白可显著抑制裂殖酵母的细胞增殖。
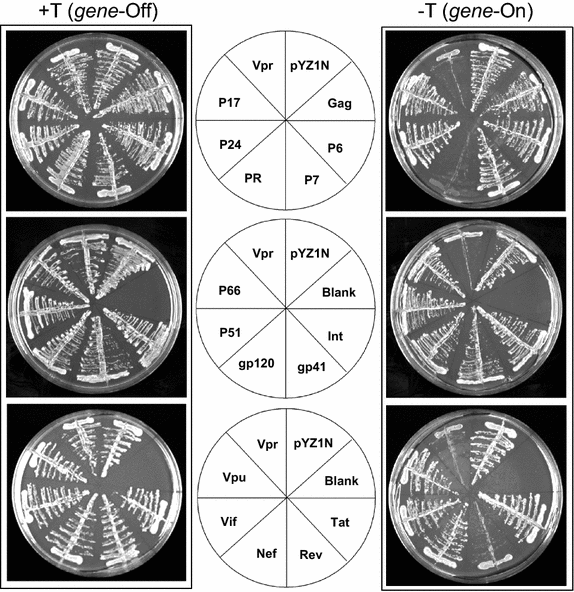
产品关联:文献未提及具体实验产品,领域常规使用微生物培养箱、无菌操作台、细胞计数仪等设备。
3.4 Rev蛋白抑制裂殖酵母细胞增殖的机制解析
实验目的是阐明Rev蛋白抑制裂殖酵母细胞增殖的具体分子机制,明确其是否导致细胞死亡、影响细胞周期或诱导细胞应激反应。方法细节:首先通过生长动力学实验检测Rev对细胞生长的动态影响,将携带pYZ1N-rev的菌株分别在含硫胺素和不含硫胺素的EMM液体培养基中培养,每隔一定时间取样并通过光密度法检测细胞密度,绘制生长曲线;通过半定量菌落稀释实验验证Rev是否诱导细胞死亡,将诱导表达Rev的菌株进行3倍梯度稀释(从1000个细胞至3个细胞),接种至固体培养基,观察菌落形成数量和大小;通过流式细胞术分析Rev对细胞周期的影响,收集诱导表达Rev 24小时和67小时的细胞,用碘化丙啶染色后检测细胞周期各阶段(G1、S、G2)的比例;通过活性氧(ROS)检测实验验证Rev是否诱导氧化应激,将诱导表达Rev的细胞用二氢乙啶(DHE)染色,通过荧光显微镜观察DHE阳性细胞比例,同时加入ROS清除剂3,3,5,5-四甲基吡咯啉N-氧化物(TMPO)作为特异性对照。结果解读:生长动力学实验显示,Rev诱导表达24小时后,细胞生长速度显著减慢,与对照组的生长差异在48小时达到最大;半定量菌落稀释实验显示,所有Rev表达菌株均能形成与稀释比例对应的菌落数量,仅菌落大小显著小于对照组,表明Rev导致细胞生长延迟而非细胞死亡;流式细胞术结果显示,Rev表达后细胞周期各阶段的比例与对照组无显著差异,表明Rev不影响裂殖酵母的细胞周期分布;ROS检测实验显示,Rev诱导表达21小时后,约50%的细胞呈DHE阳性,加入TMPO后阳性细胞比例显著降低,且随着培养时间延长,阳性细胞比例逐渐下降(24小时约30%,30小时约10%),表明Rev诱导短暂的细胞氧化应激反应。
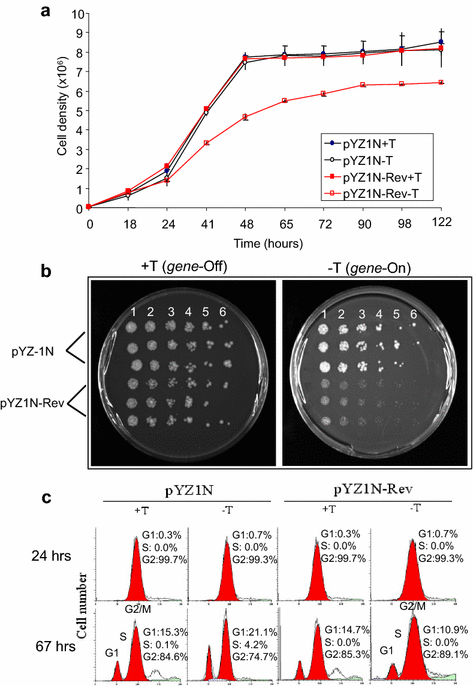
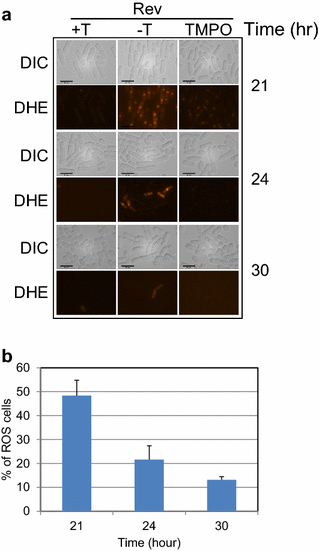
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、ROS检测试剂盒、酶标仪等设备。
3.5 Rev蛋白功能的哺乳动物细胞验证
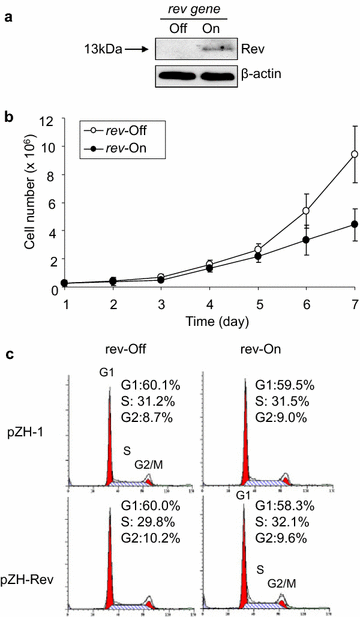
实验目的是验证Rev蛋白的功能效应在哺乳动物细胞中是否保守,进一步证明裂殖酵母模型的可靠性。方法细节:将HIV-1 rev基因克隆至蜕皮激素诱导表达载体pZH-1,转染至293VE632细胞(稳定表达修饰型蜕皮激素受体的细胞系),通过潮霉素筛选获得稳定转染细胞株;加入蜕皮激素类似物莫西酮A(muristerone A)诱导Rev表达,通过蛋白质免疫印迹(Western blot)验证Rev蛋白的表达;通过生长动力学实验检测Rev对哺乳动物细胞增殖的影响,将诱导表达Rev的细胞连续培养7天,每天用台盼蓝染色计数活细胞数量,绘制生长曲线;通过流式细胞术检测Rev对哺乳动物细胞周期的影响,收集诱导表达5天的细胞,用碘化丙啶染色后分析细胞周期各阶段比例。结果解读:蛋白质免疫印迹(Western blot)检测到约13 kDa的Rev蛋白特异性条带,表明Rev在293VE632细胞中成功诱导表达;生长动力学实验显示,Rev诱导表达5天后,活细胞数量显著少于对照组,生长抑制效应与裂殖酵母中的结果一致;流式细胞术结果显示,Rev表达后哺乳动物细胞周期各阶段比例与对照组无显著差异,表明Rev在哺乳动物细胞中同样不影响细胞周期分布。
产品关联:文献未提及具体实验产品,领域常规使用蛋白质免疫印迹(Western blot)试剂盒、细胞培养试剂、流式细胞仪等设备。
4. Biomarker研究及发现成果解析
本研究聚焦于HIV-1蛋白在模式生物中的功能机制解析,未涉及疾病诊断、预后或治疗相关生物标志物(Biomarker)的筛选与验证研究。本研究的核心成果为:1. 系统解析了HIV-1全基因组编码15个蛋白在裂殖酵母中的亚细胞定位,发现其中11个蛋白(P24、P7、P66、IN、Gp120、Gp41、Vpr、Vif、Rev、Tat)主要定位于细胞核,2个蛋白(P17、Vpu)定位于细胞质,2个蛋白(PR、Nef)均匀分布于细胞,且该定位模式与哺乳动物细胞中的研究结果普遍一致;2. 筛选出3个可抑制裂殖酵母细胞增殖的HIV-1蛋白(Vpr、PR、Rev),并深入阐明Rev蛋白通过诱导短暂的细胞氧化应激反应抑制细胞增殖,但不导致细胞死亡或影响细胞周期分布;3. 验证了Rev蛋白的功能效应在裂殖酵母和哺乳动物细胞中高度保守,证明裂殖酵母可作为研究HIV-1蛋白功能的简便、有效的模式生物系统,为后续HIV-1蛋白的高通量功能筛选和机制研究提供了新的模型选择。
