1. 领域背景与文献引入
文献英文标题:HAC stability in murine cells is influenced by nuclear localization and chromatin organization;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:染色体生物学(人工染色体方向)。
人类人工染色体(HAC)是一类可自主复制、分离的人工染色体,自诞生以来成为研究着丝粒染色质组织、动粒结构的重要工具,同时也是理想的基因表达载体,在人类细胞中通常可稳定维持(无选择压力下长期培养丢失率低)。领域共识:HAC的稳定性与着丝粒功能、染色质修饰密切相关,但其转移至啮齿类细胞后稳定性存在显著克隆间差异,现有研究多将差异归因于HAC的结构(环形/线性)、组成或着丝粒蛋白缺失,但部分情况下HAC结合关键着丝粒蛋白(如CENP-A)仍表现出高不稳定性,提示存在未被阐明的调控机制。当前研究空白在于核架构对HAC稳定性的调控作用尚未明确,因此本研究旨在探究小鼠细胞中HAC的核定位、染色质组织与稳定性的关联,为构建稳定的HAC小鼠模型提供理论依据。
2. 文献综述解析
作者系统综述了HAC的研究现状,按研究背景(HAC的功能与应用)、跨物种转移的稳定性差异、现有机制解释三个维度分类评述。首先,作者总结了HAC在人类细胞中的研究进展:HAC可用于解析人类着丝粒的表观遗传调控、动粒组装,且作为基因载体具有容量大、无整合风险的优势,在人类细胞中稳定性良好,仅存在轻微的分离错误。其次,针对HAC跨物种转移至啮齿类细胞的研究,作者指出不同克隆的HAC稳定性差异显著,从完全稳定到高度不稳定不等,现有解释包括HAC的结构差异(如环形与线性HAC的稳定性不同)、组成差异,或着丝粒关键蛋白(如CENP-C)缺失导致着丝粒功能异常,但多数情况下HAC的CENP-A结合水平与内源性染色体相当,仍存在高不稳定性,说明这些机制无法完全解释稳定性差异。最后,作者提出核架构可能是调控HAC稳定性的关键因素,因为小鼠细胞核具有高度区室化的结构,染色中心(多个染色体的着丝粒旁区聚集形成)参与调控DNA复制时间与染色体分离,而HAC的核定位尚未被作为稳定性的影响因素进行系统研究。本研究的创新价值在于首次将HAC的核定位与稳定性直接关联,填补了核架构对人工染色体稳定性调控的研究空白,为HAC在小鼠细胞中的应用提供了新的理论基础。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确小鼠细胞中HAC稳定性的调控因素,核心科学问题是核定位与染色质组织如何影响HAC的有丝分裂稳定性,技术路线为:构建不同HAC的小鼠细胞系→分析HAC的着丝粒功能与染色质组成→检测HAC的有丝分裂稳定性→关联核定位、组蛋白修饰、复制时间与稳定性→解析稳定性差异的机制。
3.1 HAC细胞系构建与结构分析
实验目的是获得来源于不同人类HAC的小鼠细胞系,排除细胞系背景差异,并分析HAC的结构变化是否影响稳定性。方法细节:将人类HT1080细胞中构建的LJ2-1(含17α卫星DNA)和AG6-1(含17α卫星DNA与HPRT基因座)HAC,通过微细胞介导染色体转移(MMCT)技术转移至STO小鼠胚胎成纤维细胞,经嘌呤霉素与G418筛选获得阳性克隆,分别命名为SM1-1(C6)(LJ2-1衍生物)、Sag1.1、Sag1.2、Sag2.2、Sag2.3(AG6-1衍生物);采用脉冲场凝胶电泳(PFGE)结合17α卫星DNA探针杂交分析HAC的结构,通过荧光原位杂交(FISH)检测克隆中是否存在小鼠DNA插入或人类其他染色体污染。结果解读:成功获得5株HAC阳性小鼠细胞系,FISH结果显示所有克隆均不含小鼠DNA插入或人类其他染色体污染;PFGE分析显示LJ2-1的衍生物SM1-1(C6)存在明显结构重排,而AG6-1的衍生物结构与亲本HAC无显著差异,说明结构重排可能是部分HAC不稳定的原因,但AG6-1衍生物的稳定性差异无法用结构解释。
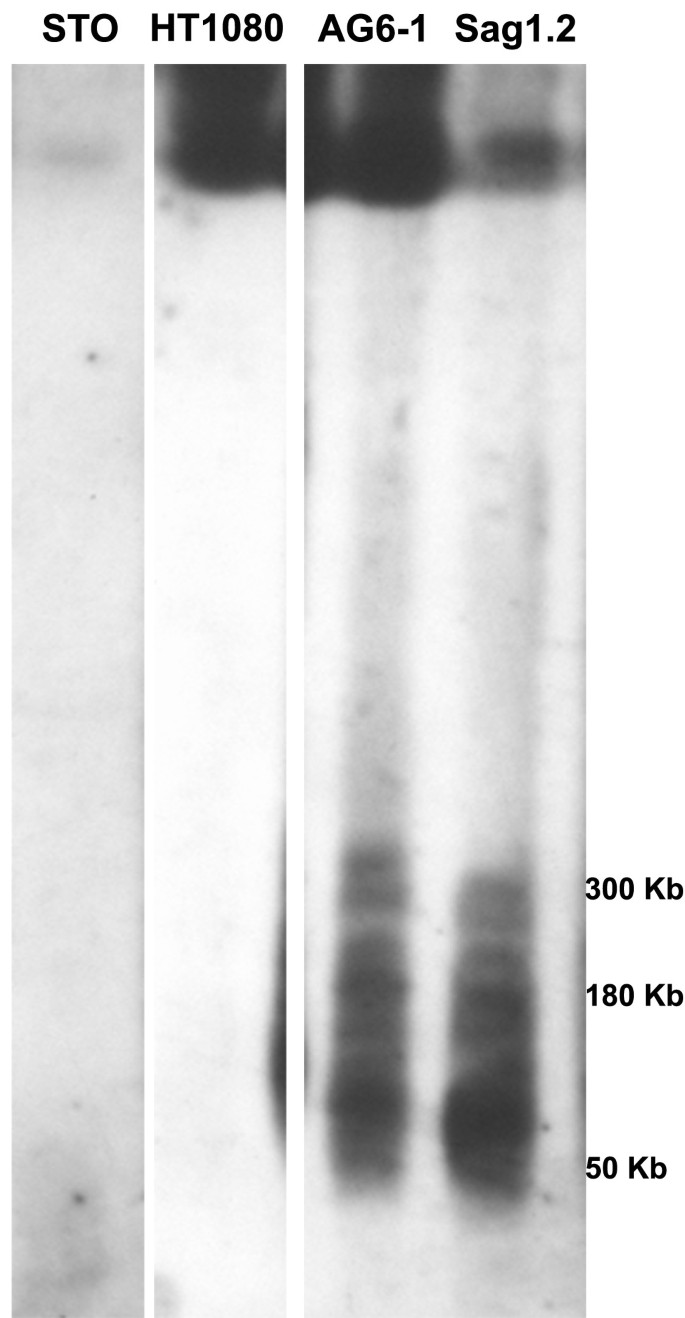
实验所用关键产品:抗CENP-A抗体(Abcam)、抗组蛋白H3赖氨酸9三甲基化(H3K9me3)抗体(Abcam)、细胞松弛素B、Aphidicolin、BrdU(Sigma)。
3.2 着丝粒蛋白与组蛋白修饰分析
实验目的是确认HAC的着丝粒功能完整性与染色质组成是否正常,排除着丝粒蛋白缺失或染色质组成异常导致的稳定性差异。方法细节:采用免疫荧光原位杂交(Immuno-FISH)技术,在中期染色体标本上同时检测HAC的17α卫星DNA信号与着丝粒蛋白CENP-A、组蛋白修饰标记(常染色质标记组蛋白H3赖氨酸4二甲基化H3K4me2、异染色质标记H3K9me3、有丝分裂相关修饰H3丝氨酸10/28磷酸化)的荧光信号;使用ImageJ软件定量25个中期染色体上HAC的H3K9me3荧光强度,以小鼠19号染色体为参照计算相对比值,分析组内荧光强度的变异程度。结果解读:所有HAC均能结合CENP-A,且结合水平与人类或小鼠内源性染色体相当,说明着丝粒功能基本正常;所有HAC同时含有H3K4me2标记的常染色质与H3K9me3标记的异染色质结构,H3丝氨酸10/28磷酸化修饰水平也与内源性染色体一致,提示HAC的染色质组成无明显异常。
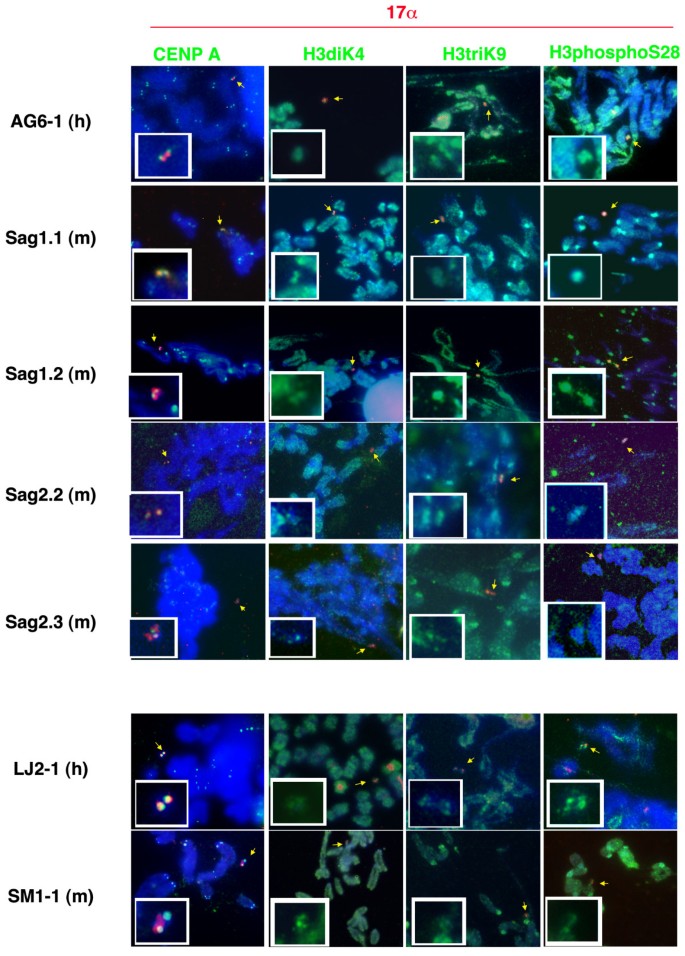
3.3 HAC有丝分裂稳定性检测
实验目的是评估不同HAC在小鼠细胞中的有丝分裂稳定性差异,为后续关联分析提供基础数据。方法细节:将各HAC细胞系在无选择压力下培养至少150天,定期收集中期染色体标本,通过荧光原位杂交(FISH)检测HAC的存在率,计算每日丢失率;其中SM1-1(C6)培养30天后即完全丢失,单独统计其丢失情况。结果解读:人类亲本HAC在HT1080细胞中稳定性良好,每日丢失率为0.04%-0.07%;而小鼠细胞中所有HAC的稳定性均显著降低,克隆间差异显著:Sag1.1最稳定,初始存在率80%,培养150天后仍有20%的细胞含有HAC(每日丢失率0.92%,n=至少150天培养);SM1-1(C6)最不稳定,初始存在率100%,培养30天后完全丢失(每日丢失率5.2%,n=30天培养)。
3.4 核定位与HAC稳定性的关联分析
实验目的是探究HAC在小鼠细胞核内的定位是否影响其稳定性。方法细节:采用荧光原位杂交(FISH)技术,在间期细胞标本上同时检测HAC的17α卫星DNA信号、小鼠染色中心的主要卫星DNA信号、着丝粒的次要卫星DNA信号;对每个克隆统计150个间期细胞中HAC与染色中心、着丝粒的共定位比例,采用Pearson相关性分析共定位比例与HAC每日丢失率的关联。结果解读:HAC与染色中心的共定位比例与每日丢失率呈显著负相关(r=-0.9282,P=0.0114,n=150),即与染色中心关联越紧密的HAC稳定性越高:Sag1.1与染色中心的共定位比例最高(30.5%),稳定性最好;SM1-1(C6)与染色中心无共定位(0%),稳定性最差。而HAC与着丝粒的共定位比例与丢失率无显著相关性(P=0.0878,n=150)。
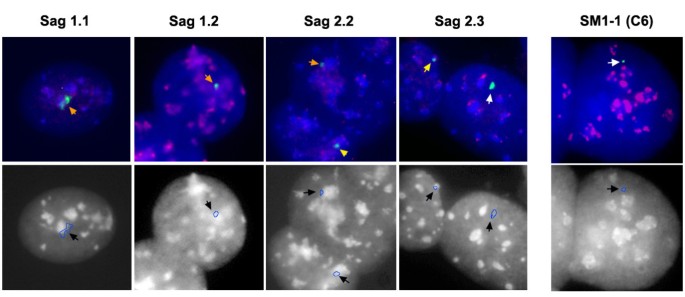
3.5 H3K9me3修饰异质性与稳定性的关联分析
实验目的是解析染色质修饰对HAC稳定性的调控机制,重点关注异染色质标记H3K9me3的作用。方法细节:基于ImageJ定量的25个中期染色体H3K9me3荧光强度数据,计算每个克隆中HAC的H3K9me3相对比值的组内标准差,分析组内变异程度与HAC每日丢失率、分离错误比例的相关性。结果解读:所有HAC的平均H3K9me3水平与小鼠内源性染色体相当(比值1.157-1.3922),但组内变异程度与每日丢失率呈显著正相关(r=0.9502,P=0.0066,n=25),与不分离事件比例也呈显著正相关(r=0.877,P=0.0255,n=25);SM1-1(C6)的H3K9me3组内变异最大(比值范围0.535-2.5),对应最高的丢失率与分离错误比例,提示H3K9me3修饰的异质性可能导致着丝粒功能不稳定,进而增加分离错误。
3.6 分离错误与复制时间的机制解析
实验目的是明确HAC丢失的直接机制,即是否由有丝分裂分离错误或DNA复制时间异常导致。方法细节:采用胞质分裂阻滞微核实验(CBMN),用细胞松弛素B处理细胞阻断胞质分裂,获得双核细胞,统计至少60个双核细胞中HAC不分离事件的比例(即两个子细胞中HAC信号数量不平衡的情况);采用BrdU标记结合荧光原位杂交(FISH)技术,将细胞同步化后在S期不同阶段(早S、中S、晚S)加入BrdU,检测HAC的复制时间分布,分析复制时间与丢失率的相关性。结果解读:HAC的不分离事件比例与每日丢失率呈显著正相关(r=0.875,P=0.0261,n=60),SM1-1(C6)的不分离事件比例最高(23.4%),提示分离错误是HAC丢失的主要原因;复制时间分析显示,人类亲本HAC主要在中S期复制,而小鼠细胞中稳定性差的HAC(如SM1-1(C6))主要在晚S期复制(60%),晚S期复制比例与每日丢失率呈显著正相关(r=0.849,P=0.0343),提示复制时间延迟可能加剧HAC的不稳定性。
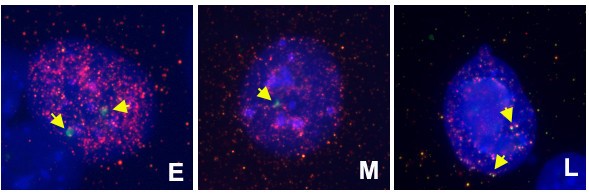
4. Biomarker研究及发现成果解析
本研究未聚焦传统疾病生物标志物,而是鉴定了与HAC在小鼠细胞中稳定性相关的功能性生物标志物,包括HAC与小鼠染色中心的共定位比例、H3K9me3修饰的组内变异程度、S期晚期复制比例,这些标志物可用于预测HAC在小鼠细胞中的稳定性。
Biomarker定位:将HAC与染色中心的共定位比例、H3K9me3修饰的组内变异、S期晚期复制比例作为预测HAC稳定性的功能性标志物,筛选逻辑为通过相关性分析从多个细胞生物学指标中筛选出与HAC丢失率显著相关的因子,验证逻辑为在多个独立HAC克隆中重复验证相关性的统计学显著性。
研究过程详述:HAC与染色中心的共定位比例来源于150个间期细胞的荧光原位杂交(FISH)检测结果,通过人工计数共定位细胞的比例获得;H3K9me3修饰的组内变异通过ImageJ定量25个中期染色体的荧光强度,计算相对比值的标准差获得;S期晚期复制比例来源于S期不同阶段BrdU标记后的荧光原位杂交(FISH)检测结果,统计晚S期阶段HAC已复制的细胞比例。特异性与敏感性方面,共定位比例与丢失率的相关性具有统计学显著性(P=0.0114),可有效区分稳定与不稳定的HAC克隆;H3K9me3组内变异与不分离事件的相关性显著(P=0.0255),可反映着丝粒功能的异质性;晚S期复制比例与丢失率的相关性显著(P=0.0343),可预测HAC的复制异常风险。
核心成果提炼:本研究首次发现HAC在小鼠细胞中的稳定性与核定位直接相关,与染色中心的紧密关联可显著提高HAC的稳定性;H3K9me3修饰的异质性和S期晚期复制是介导稳定性差异的关键机制,其中不分离事件是HAC丢失的主要直接原因。这些成果的创新性在于首次揭示了核架构对人工染色体稳定性的调控作用,为构建稳定的HAC小鼠模型提供了新的策略,例如通过调控HAC的核定位或染色质修饰来提高其稳定性,同时也为理解跨物种染色体稳定性的调控机制提供了新的视角。
