1. 领域背景与文献引入
文献英文标题:KITENIN promotes aerobic glycolysis through PKM2 induction by upregulating the c-Myc/hnRNPs axis in colorectal cancer;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:结直肠癌代谢重编程与肿瘤发生机制
结直肠癌是全球范围内发病率与死亡率均位居前列的恶性肿瘤,其发病机制涉及多基因、多步骤的遗传与表观遗传异常,包括癌基因激活、抑癌基因失活及信号通路紊乱等。代谢重编程是肿瘤细胞的核心特征之一,即Warburg效应(有氧糖酵解),指肿瘤细胞在有氧条件下优先通过糖酵解获取能量,同时为细胞快速增殖提供核苷酸、氨基酸等生物合成前体。目前已知多个关键分子参与调控肿瘤糖酵解过程,如转录因子c-Myc、缺氧诱导因子HIF-1α及糖酵解关键酶丙酮酸激酶M2(PKM2)等,但仍有大量调控通路未被阐明,限制了代谢靶向治疗策略的开发。
KITENIN作为一种癌蛋白,已被证实与肿瘤侵袭、转移、上皮间质转化(EMT)及干细胞特性密切相关,其高表达与多种肿瘤的不良预后相关,但此前其在肿瘤代谢重编程中的作用尚未被报道,这一研究空白导致对KITENIN致癌机制的理解不全面,也缺乏针对其代谢调控功能的治疗手段。因此,本研究旨在明确KITENIN对结直肠癌细胞有氧糖酵解的调控作用及分子机制,为结直肠癌的代谢靶向治疗提供新的靶点与理论依据。
2. 文献综述解析
作者首先系统梳理了KITENIN的已知致癌功能及肿瘤代谢重编程的核心调控通路,通过对比现有研究的未解决问题,凸显了本研究的创新价值。
作者首先对KITENIN的研究现状进行了综述,指出KITENIN已被证实参与调控肿瘤侵袭、转移、EMT及干细胞特性,且已有部分针对KITENIN的抑制剂研究,如DKC1125,但其作用机制主要聚焦于抑制肿瘤侵袭,未涉及代谢层面。接着,作者对肿瘤代谢重编程的核心机制进行了梳理,重点阐述了c-Myc通过上调异质核糖核蛋白(hnRNP)家族蛋白促进PKM2的选择性剪接,进而增强有氧糖酵解的通路,同时PKM2还可发生核转位,作为转录共激活因子调控下游癌基因的表达,形成正反馈调控网络。现有研究已明确c-Myc/hnRNPs/PKM2通路在肿瘤代谢中的关键作用,但尚未将KITENIN纳入这一调控网络中,也未探讨针对KITENIN的抑制剂对代谢通路的影响。
本研究的创新点在于首次揭示了KITENIN通过c-Myc/hnRNPs轴调控PKM2介导的有氧糖酵解,将KITENIN的致癌功能从侵袭转移拓展至代谢重编程领域,完善了KITENIN的致癌机制网络;同时证实了KITENIN抑制剂可通过抑制糖酵解通路发挥抗肿瘤作用,为KITENIN靶向治疗提供了新的作用靶点与临床应用方向,填补了现有研究的空白。
3. 研究思路总结与详细解析
本研究以“KITENIN是否调控结直肠癌细胞有氧糖酵解”为核心科学问题,采用细胞模型、动物实验及临床数据库分析相结合的方法,依次验证KITENIN对糖酵解的功能调控、解析其分子机制、明确反馈调控通路,并评估KITENIN抑制剂的代谢抑制效果,形成了“功能验证→机制解析→临床转化”的完整研究闭环。
3.1 KITENIN对结直肠癌细胞糖酵解的功能验证
本环节的核心目标是明确KITENIN过表达或敲低对结直肠癌细胞有氧糖酵解的直接影响。研究人员构建了KITENIN过表达的人结直肠癌细胞系CaCo2、小鼠结直肠癌细胞系CT26及KITENIN敲低的细胞系,采用Seahorse XF96细胞代谢分析仪检测细胞外酸化率(ECAR)与耗氧率(OCR),计算糖酵解质子外流率(glycoPER)以量化糖酵解水平;通过Transwell实验检测细胞侵袭能力;采用实时荧光定量PCR(qRT-PCR)与蛋白质免疫印迹(Western blot)检测糖酵解关键分子葡萄糖转运蛋白1(GLUT1)、己糖激酶2(HK2)、PKM2、乳酸脱氢酶A(LDHA)的表达水平。
结果显示,KITENIN过表达显著提高了细胞的glycoPER、基础糖酵解及代偿性糖酵解水平(n=3,P<0.01),但对线粒体呼吸(OCR)无显著影响,表明KITENIN特异性调控有氧糖酵解而非线粒体代谢;同时,KITENIN过表达显著增强了细胞的侵袭能力(n=3,P<0.001),并上调了GLUT1、HK2、PKM2、LDHA的mRNA与蛋白表达水平,且PKM2/PKM1的比值显著升高(n=3,P<0.01),提示KITENIN促进了丙酮酸激酶的M1向M2亚型转换。KITENIN敲低则显著抑制了糖酵解水平及上述糖酵解分子的表达,进一步验证了KITENIN的糖酵解调控功能。
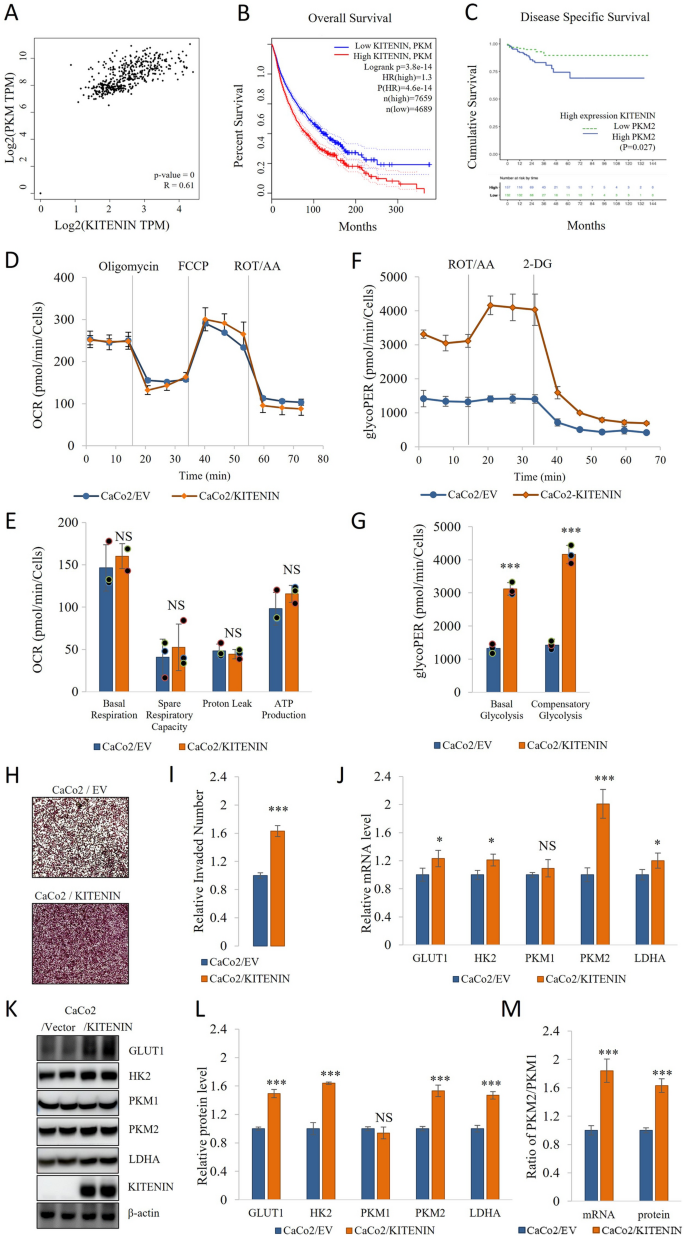
实验所用关键产品:Seahorse XF96细胞代谢分析仪(Agilent)、Transwell小室(Corning)、实时荧光定量PCR试剂(Enzynomics)、蛋白质免疫印迹抗体(信息见补充材料Table S2)。
3.2 MYO1D在KITENIN调控糖酵解中的作用验证
本环节旨在明确MYO1D对KITENIN介导的糖酵解调控的辅助作用。研究人员在KITENIN过表达及对照细胞系中转染MYO1D的小干扰RNA(siRNA),检测glycoPER、糖酵解分子表达及细胞周期分布;采用流式细胞术分析细胞周期各阶段的细胞比例。
结果显示,MYO1D敲低显著降低了KITENIN过表达细胞的glycoPER水平(n=3,P<0.01),并下调了GLUT1、HK2、PKM2、LDHA的表达;同时,MYO1D敲低导致细胞周期阻滞于G1/S期,提示MYO1D通过维持KITENIN/ErbB4复合物在细胞膜上的稳定性,促进KITENIN的信号传导,进而调控糖酵解与细胞周期进展。
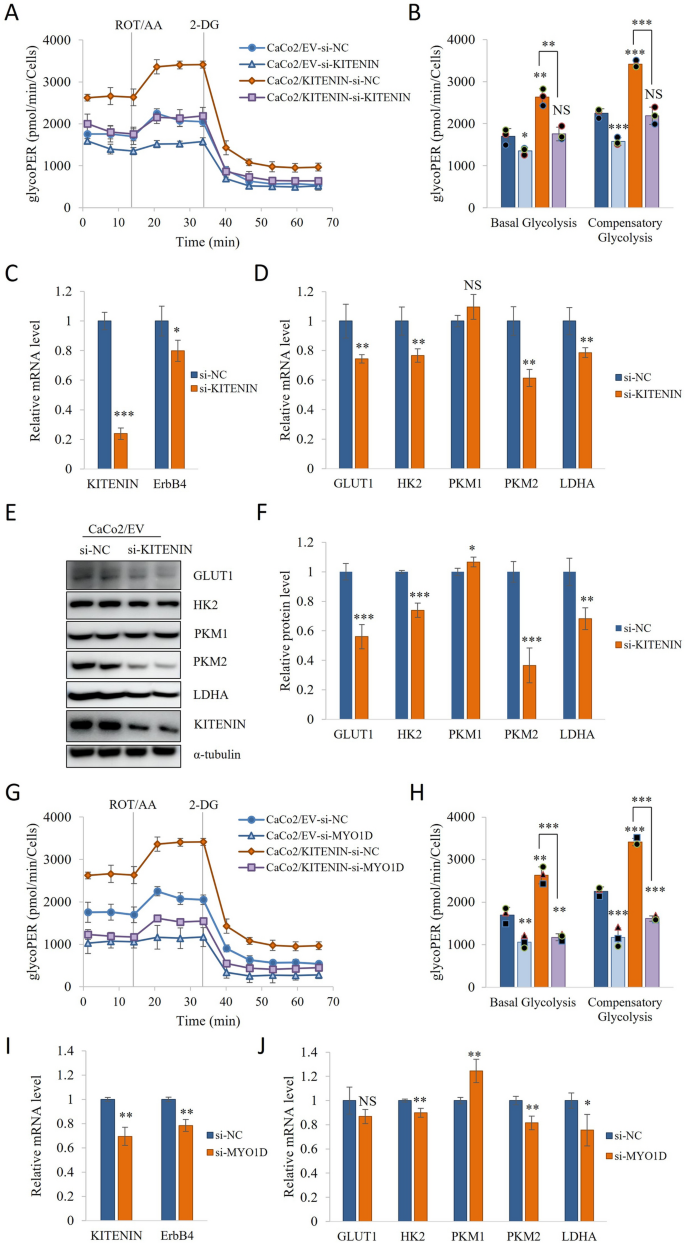
实验所用关键产品:MYO1D siRNA(Thermo Scientific/Invitrogen)、流式细胞仪(Beckman Coulter CytoFLEX)。
3.3 PKM2在KITENIN调控糖酵解中的介导作用验证
本环节的核心目标是明确PKM2是否为KITENIN调控糖酵解的关键效应分子。研究人员在KITENIN过表达细胞中转染PKM2的siRNA,检测glycoPER与细胞侵袭能力;在KITENIN敲低细胞中过表达PKM2,检测糖酵解分子表达与细胞侵袭能力的恢复情况。
结果显示,PKM2敲低显著抑制了KITENIN过表达细胞的glycoPER水平(n=3,P<0.001)与侵袭能力(n=3,P<0.01);而过表达PKM2可部分恢复KITENIN敲低细胞的糖酵解水平与侵袭能力,证实PKM2是KITENIN调控糖酵解与细胞侵袭的关键下游分子,KITENIN对糖酵解的调控依赖于PKM2的表达与功能。
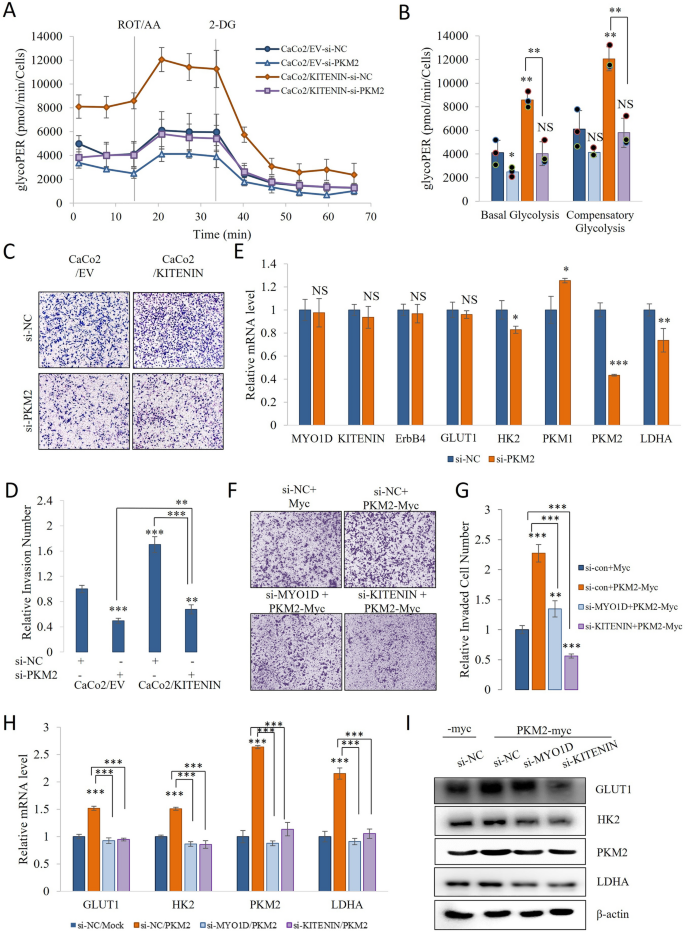
实验所用关键产品:PKM2 siRNA(Bioneer)、PKM2过表达质粒(Origene)。
3.4 KITENIN调控PKM2表达的分子通路解析
本环节旨在明确KITENIN调控PKM2表达的分子机制。研究人员采用亚细胞组分分离与蛋白质免疫印迹检测c-Myc的核定位;通过实时荧光定量PCR与蛋白质免疫印迹检测hnRNP家族蛋白(hnRNPI、hnRNPA1、hnRNPA2)的表达;采用免疫共沉淀(Co-IP)检测c-Myc与PKM2的相互作用;通过GEPIA数据库分析KITENIN与hnRNP家族蛋白在结直肠癌组织中的表达相关性及预后价值。
结果显示,KITENIN过表达显著促进c-Myc的核转位(n=3,P<0.01),并上调了hnRNPI、hnRNPA1、hnRNPA2的mRNA与蛋白表达水平(n=3,P<0.05);Co-IP结果显示KITENIN过表达增强了c-Myc与PKM2的相互作用;GEPIA数据库分析显示KITENIN与hnRNP家族蛋白在结直肠癌组织中呈正相关(Pearson相关系数>0.3,P<0.001),且高表达与患者的不良预后相关。这些结果证实KITENIN通过上调c-Myc的核定位与表达,进而促进hnRNP家族蛋白的表达,而hnRNP家族蛋白作为剪接因子,可促进PKM前体mRNA的选择性剪接,增加PKM2/PKM1的比值,最终增强有氧糖酵解。
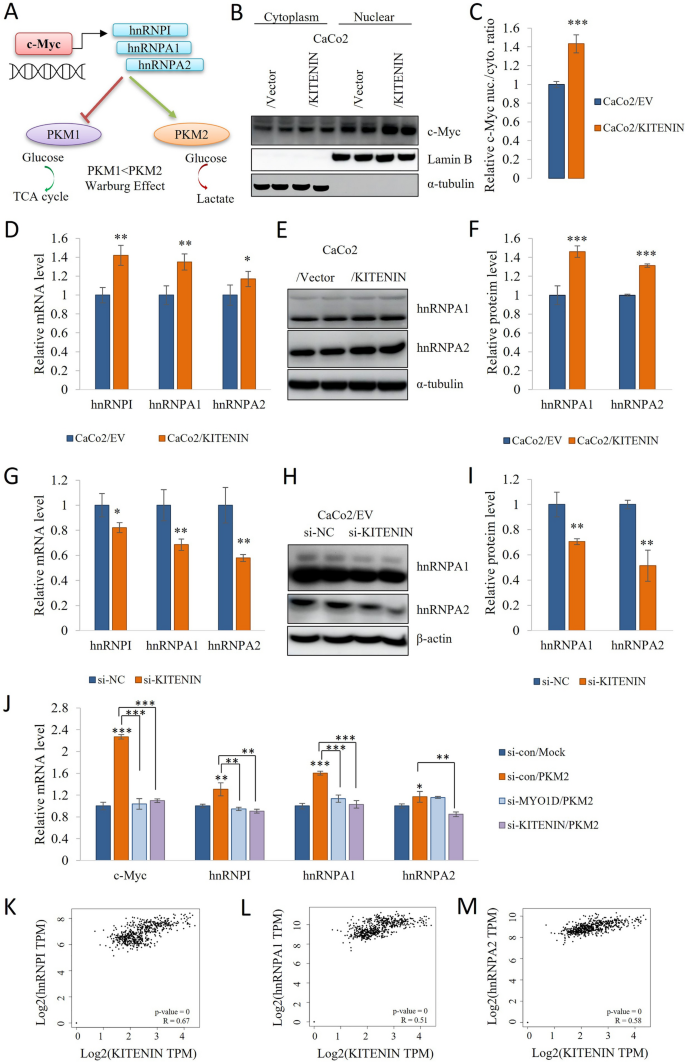
实验所用关键产品:亚细胞分离试剂盒(Thermo Scientific NE-PER)、免疫共沉淀试剂(Thermo Scientific Protein A/G Sepharose)。
3.5 KITENIN调控PKM2核转位的反馈机制验证
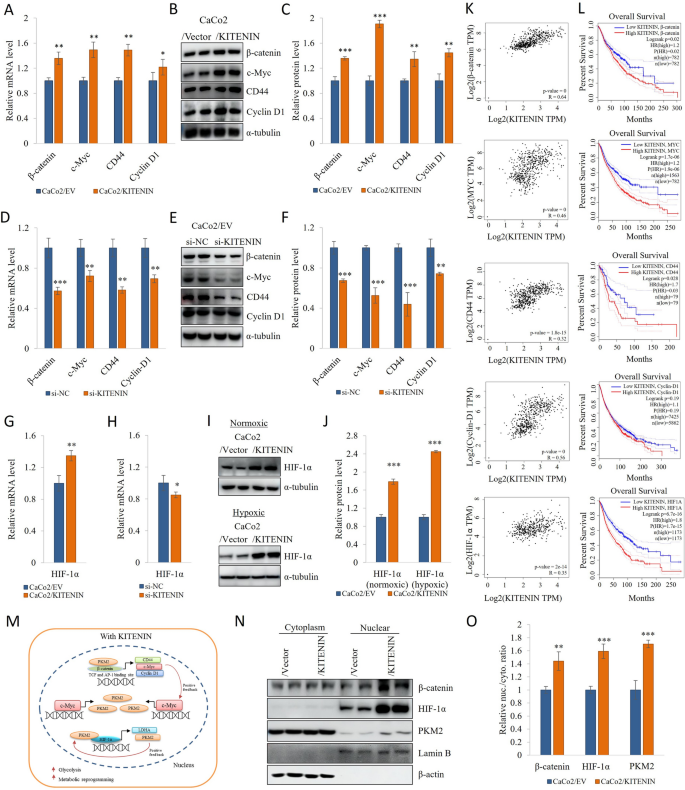
本环节旨在明确KITENIN通过PKM2核转位调控下游转录因子的作用及反馈机制。研究人员采用亚细胞组分分离与蛋白质免疫印迹检测β-连环蛋白(β-catenin)、HIF-1α的核定位;通过实时荧光定量PCR与蛋白质免疫印迹检测β-catenin、c-Myc、CyclinD1、CD44、HIF-1α的表达;通过GEPIA数据库分析KITENIN与这些转录因子的临床相关性。
结果显示,KITENIN过表达显著促进β-catenin、HIF-1α及PKM2的核转位(n=3,P<0.01),并上调了β-catenin、c-Myc、CyclinD1、CD44、HIF-1α的mRNA与蛋白表达水平;GEPIA数据库分析显示KITENIN与这些分子在结直肠癌组织中呈正相关(P<0.001),且高表达与不良预后相关。核转位的PKM2可作为转录共激活因子,与β-catenin、HIF-1α形成复合物,进一步上调c-Myc等转录因子的表达,形成KITENIN→c-Myc→hnRNPs→PKM2→β-catenin/HIF-1α→c-Myc的正反馈调控通路,持续增强有氧糖酵解与肿瘤细胞的恶性表型。
3.6 KITENIN抑制剂对糖酵解的抑制作用验证
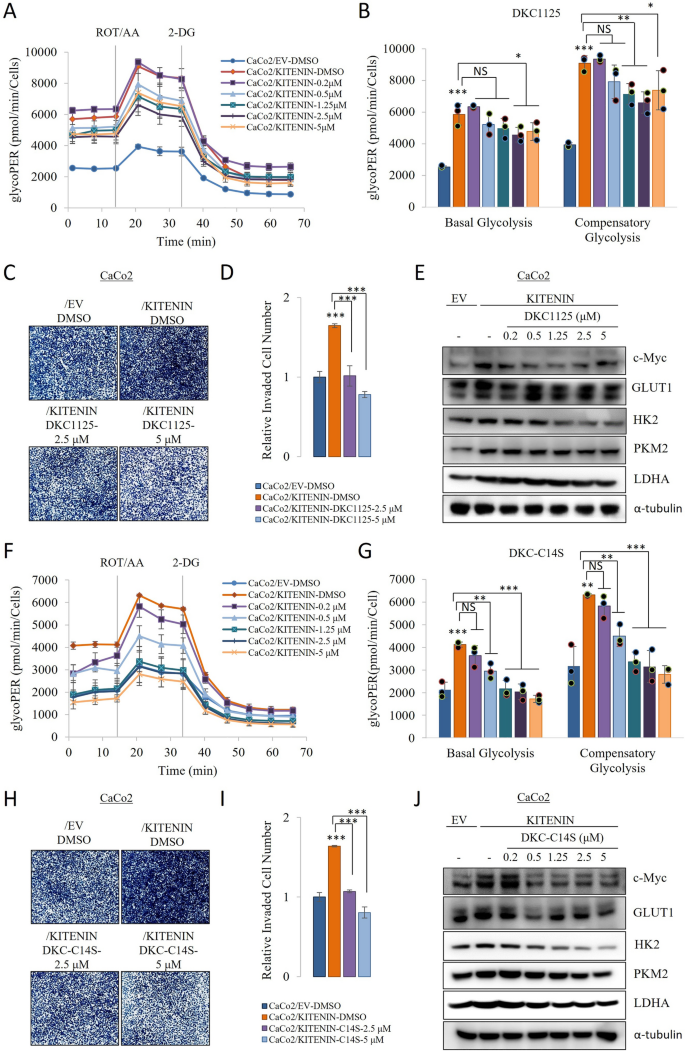
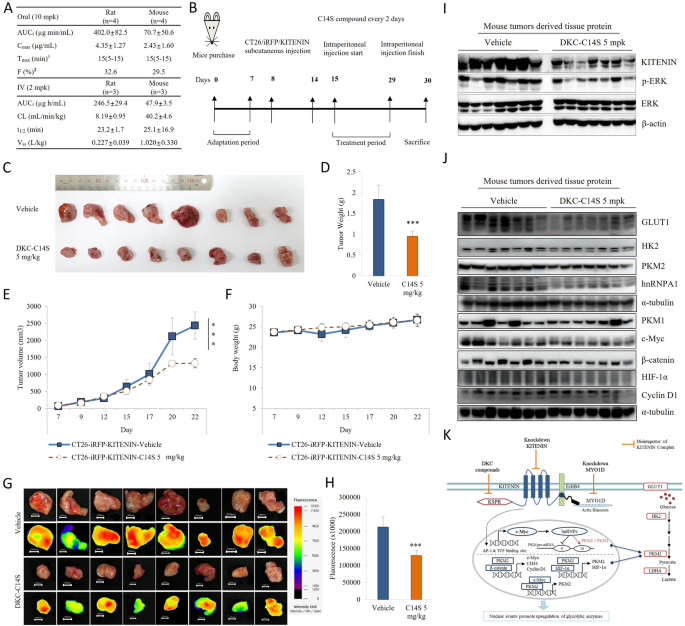
本环节的核心目标是明确KITENIN抑制剂对KITENIN介导的糖酵解的抑制效果及体内抗肿瘤活性。研究人员在KITENIN过表达细胞中处理不同浓度的DKC1125或其优化体DKC-C14S,检测glycoPER、糖酵解分子表达及细胞侵袭能力;构建结直肠癌异种移植模型,评估DKC-C14S对肿瘤生长及代谢相关分子表达的影响;采用液相色谱-串联质谱(LC-MS/MS)分析DKC-C14S的体内药代动力学特性。
结果显示,DKC1125与DKC-C14S均以剂量依赖的方式抑制KITENIN过表达细胞的glycoPER水平(n=3,P<0.01),下调GLUT1、HK2、PKM2、c-Myc等分子的表达,并抑制细胞侵袭能力;体内实验显示DKC-C14S显著抑制肿瘤生长,肿瘤重量降低50%-55%(n=8,P<0.001),并下调肿瘤组织中KITENIN、磷酸化ERK(p-ERK)、GLUT1、HK2、PKM2等分子的表达;药代动力学分析显示DKC-C14S具有良好的生物利用度与代谢稳定性,适合体内给药。这些结果证实KITENIN抑制剂可通过抑制KITENIN介导的糖酵解通路发挥抗肿瘤作用,具有潜在的临床转化价值。
实验所用关键产品:DKC1125、DKC-C14S(本研究合成)、小动物活体成像系统(FOBI)、LC-MS/MS系统(AB SCIEX API 3200)。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker包括KITENIN、PKM2、c-Myc及hnRNP家族蛋白,采用“细胞功能验证→分子机制解析→临床数据库验证”的多维度筛选与验证逻辑,明确了其在结直肠癌代谢重编程中的临床价值。
研究人员首先通过细胞系实验验证了KITENIN对PKM2、c-Myc及hnRNP家族蛋白的调控作用,随后通过GEPIA数据库分析了这些分子在结直肠癌组织中的表达相关性及预后价值,最后通过动物实验验证了针对KITENIN的抑制剂对这些分子表达及糖酵解的抑制效果。具体而言,KITENIN、PKM2、c-Myc及hnRNP家族蛋白的表达水平通过实时荧光定量PCR、蛋白质免疫印迹进行检测,其与糖酵解功能的关联通过Seahorse代谢分析仪进行验证;临床相关性分析显示KITENIN与PKM2在结直肠癌组织中呈显著正相关(Pearson相关系数>0.3,P<0.001),且KITENIN高表达合并PKM2高表达的患者疾病特异性生存率显著低于KITENIN高表达但PKM2低表达的患者(n=157 vs n=132,P<0.05)。
本研究的核心成果在于,KITENIN可作为结直肠癌代谢重编程的新型Biomarker,其与PKM2的联合表达可用于预测患者的不良预后;同时,KITENIN调控的c-Myc/hnRNPs/PKM2通路可作为结直肠癌代谢靶向治疗的新靶点,为开发新型代谢抑制剂提供了方向;此外,KITENIN抑制剂DKC-C14S可通过抑制该通路发挥抗肿瘤作用,具有良好的体内活性与药代动力学特性,具有潜在的临床转化价值。目前尚未有针对该通路的临床药物,本研究为后续的临床前研究与临床试验奠定了基础。
