1. 领域背景与文献引入
文献英文标题:Knock-down of methyl CpG-binding protein 2 (MeCP2) causes alterations in cell proliferation and nuclear lamins expression in mammalian cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(核纤层调控与细胞增殖)
MeCP2(甲基CpG结合蛋白2)是一种多功能核蛋白,最初因与雷特综合征(一种严重神经发育障碍)的关联成为神经科学领域核心研究靶点,其编码基因的突变会导致神经元染色质重塑异常与功能紊乱。近年来,MeCP2的非神经元功能逐渐被揭示,包括参与细胞生长、增殖、纤维化及染色质高级结构调控等过程。核纤层是核膜的核心组成结构,主要由核纤层蛋白(lamin A/C、lamin B1等)构成,在维持核膜完整性、调控有丝分裂进程、DNA复制与转录等关键细胞活动中发挥不可替代的作用,核纤层蛋白的突变或表达异常会引发核膜形态异常、细胞周期紊乱甚至早衰综合征等疾病。领域共识:核膜结构的稳定性与细胞增殖能力密切相关,核纤层蛋白的表达调控是维持核膜功能的核心环节。当前研究中,MeCP2与核纤层的直接关联机制尚未明确,MeCP2缺失是否通过调控核纤层蛋白表达影响核膜结构及细胞增殖的具体通路仍属空白。针对这一研究空白,本研究假设MeCP2可能参与核膜稳定性调控,进而影响高增殖系统的增殖模式,通过在多种哺乳动物细胞系中进行MeCP2功能缺失实验,验证该假设并揭示其潜在机制,为MeCP2的非神经元功能研究提供新的方向。
2. 文献综述解析
作者围绕MeCP2的功能拓展与核膜调控的关联构建综述逻辑,先从MeCP2的经典神经元功能切入,逐步延伸至非神经元领域的研究进展,再结合核纤层蛋白的功能特性,提出MeCP2作为连接异染色质与核膜的桥梁的科学假设。
现有研究表明,MeCP2突变会导致培养淋巴细胞的生长劣势,其功能缺失可抑制胶质细胞、间充质干细胞及前列腺癌细胞的增殖;MeCP2可与核膜蛋白LBR(lamin B受体)及异染色质蛋白HP1相互作用,参与染色质重塑与基因沉默过程。核纤层蛋白作为核膜的核心组分,不仅维持核膜结构完整性,还参与细胞周期调控、DNA复制等关键过程,核纤层蛋白的表达异常会引发核膜形态改变和细胞功能紊乱。但现有研究多聚焦于MeCP2的染色质调控功能或核纤层蛋白的独立作用,缺乏对两者相互调控机制的直接验证,且未明确MeCP2缺失通过核纤层影响细胞增殖的具体路径。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在多种细胞系中验证MeCP2敲低可导致核纤层蛋白(lamin A/C、lamin B1、LBR)表达显著下调,并伴随核膜形态异常,同时明确这一核膜结构变化与细胞增殖抑制的直接关联,填补了MeCP2非神经元功能中核膜调控机制的空白,为理解MeCP2在细胞增殖中的作用提供了新的实验依据。
3. 研究思路总结与详细解析
本研究以“MeCP2调控核膜稳定性进而影响细胞增殖”为核心科学问题,采用“功能缺失表型分析→机制验证→形态学观察”的闭环技术路线,在正常小鼠成纤维细胞(NIH-3T3)及人前列腺癌细胞系(PC-3、LNCaP)中开展实验,明确MeCP2对细胞增殖、细胞周期及核膜结构的调控作用。
3.1 细胞增殖与细胞周期变化检测
实验目的:验证MeCP2功能缺失对哺乳动物细胞增殖能力及细胞周期进程的影响。
方法细节:在NIH-3T3、PC-3、LNCaP细胞中,采用Dharmacon的MeCP2 siRNA SMARTpool进行转染,设置非靶向siRNA作为对照组,分别在转染后3、5、7天进行细胞计数检测增殖;同时采用流式细胞术(FACS)分析细胞周期分布,通过BrdU/PI双参数染色检测S/G2M期细胞比例,所有实验独立重复3次。
结果解读:如图1所示,MeCP2敲低后细胞增殖能力显著下降,PC-3细胞在转染7天后细胞数量仅为对照组的13%左右(n=3,P<0.005),LNCaP和NIH-3T3细胞增殖下降约60%;细胞周期分析显示,MeCP2缺失细胞的G1期细胞比例减少,亚G0/G1期(非循环细胞)增加约10-15%,S/G2M期细胞比例增加约20%,表明细胞周期进程受阻于S/G2M阶段,且出现部分细胞死亡或周期停滞。
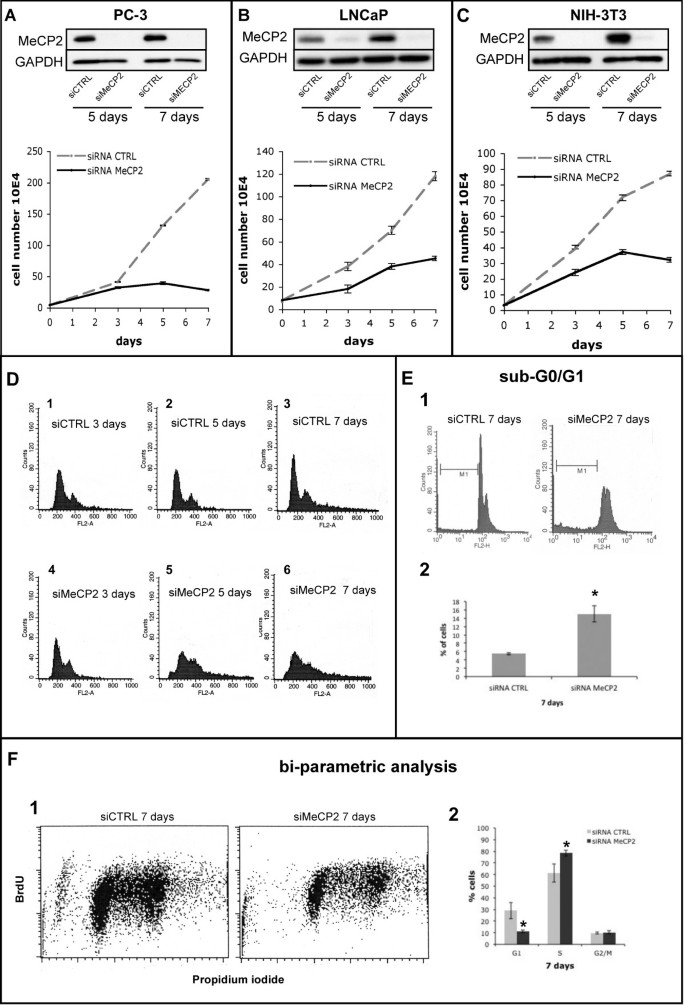
产品关联:实验所用关键产品:Dharmacon的MeCP2 siRNA SMARTpool及非靶向siRNA、BD的FACSCalibur流式细胞仪、Sigma的碘化丙啶(PI)、Becton Dickinson的BrdU抗体及Annexin V-FITC凋亡检测试剂盒。
3.2 凋亡与衰老表型评估
实验目的:排除凋亡与衰老作为MeCP2缺失导致细胞增殖抑制的主要原因,明确核膜变化的核心作用。
方法细节:在PC-3细胞中,MeCP2敲低后5、7天采用Annexin V-FITC/PI双染色法检测凋亡细胞比例,通过Western blot检测Cleaved-PARP(凋亡标志物)的表达;转染7天后采用SA-β-半乳糖苷酶染色检测衰老细胞比例,同时通过免疫荧光检测衰老相关异染色质灶(SAHFs)的形成,实验独立重复3次。
结果解读:如图2所示,MeCP2敲低后凋亡细胞比例虽略有升高,但最高仅约12%(n=3,P<0.001),Cleaved-PARP表达水平无显著升高;SA-β-半乳糖苷酶阳性细胞比例约为4.4%,SAHFs阳性细胞比例约为4%,远低于增殖抑制的幅度,表明凋亡与衰老并非细胞增殖下降的主要原因,核膜结构异常可能是核心调控因素。
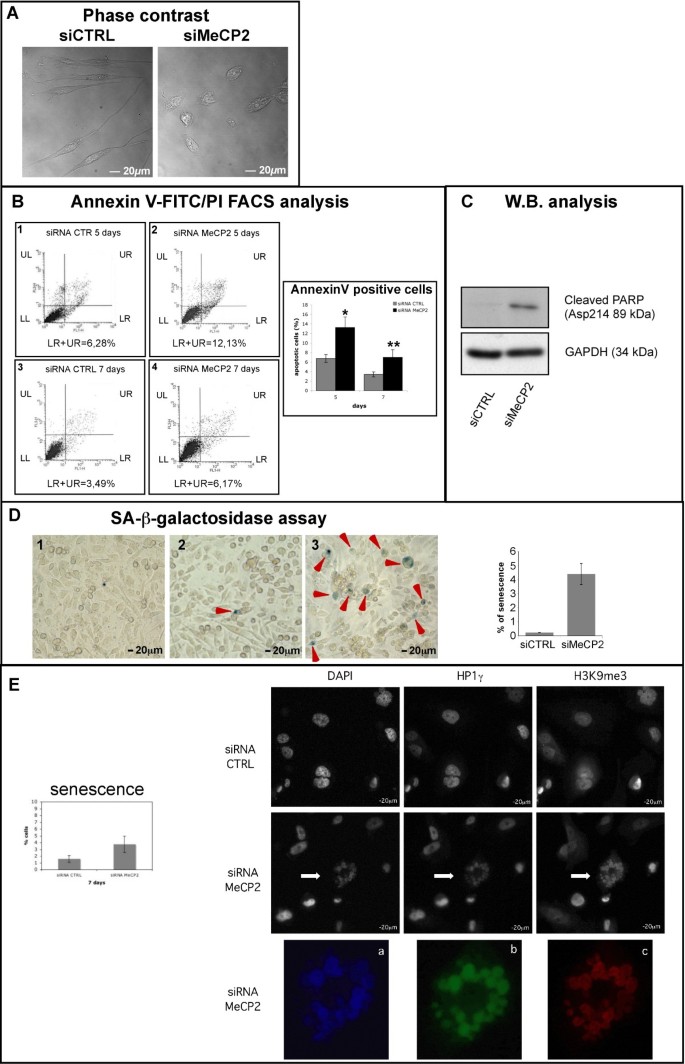
产品关联:实验所用关键产品:BD Pharmingen的Annexin V-FITC凋亡检测试剂盒、Cell Signaling Technology的Cleaved-PARP抗体、Millipore的SA-β-半乳糖苷酶检测试剂盒、Abcam的HP1γ及H3K9me3抗体。
3.3 核纤层蛋白表达与核膜形态分析
实验目的:验证MeCP2缺失对核纤层蛋白表达及核膜形态的调控作用。
方法细节:在PC-3、LNCaP、NIH-3T3细胞中,MeCP2敲低后5、7天采用Western blot检测lamin A/C、lamin B1、LBR的蛋白表达水平,通过RT-qPCR检测其mRNA水平;转染7天后采用免疫荧光结合共聚焦显微镜观察lamin A的定位及核膜形态,分析蛋白表达的荧光强度分布,实验独立重复3次。
结果解读:如图3所示,MeCP2敲低后,lamin A蛋白表达下降约50%,lamin C、lamin B1、LBR蛋白表达下降约30-40%(n=3,P<0.001),其mRNA水平也呈相应下调趋势;共聚焦显微镜观察显示,lamin A的核膜定位未发生明显改变,但核膜形态出现异常,表现为核边缘不规则,部分细胞呈现类似早衰综合征的核形态特征,荧光强度分析证实MeCP2缺失与lamin A表达水平呈正相关。
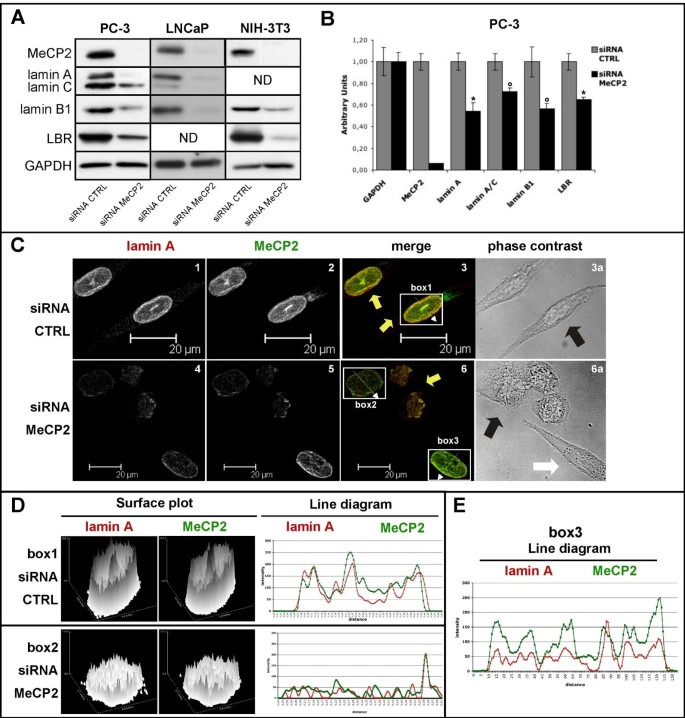
产品关联:实验所用关键产品:Santa Cruz的lamin A/C、lamin B1抗体、Covance的LBR抗体、Sigma的MeCP2抗体、Zeiss LSM410激光扫描共聚焦显微镜、Bio-Rad的iQ™SYBR Green Supermix用于RT-qPCR。
4. Biomarker研究及发现成果
本研究将MeCP2定位为调控核膜稳定性与细胞增殖的关键分子,通过功能缺失实验验证其对核纤层蛋白的调控作用,明确MeCP2作为连接异染色质与核膜的“桥梁”分子的核心功能。
MeCP2作为细胞增殖与核膜结构的调控型Biomarker,筛选逻辑基于已知的MeCP2与核膜蛋白LBR的相互作用,通过在多种细胞系中进行功能缺失实验,验证其对核纤层蛋白表达及核膜形态的调控效应,形成“分子相互作用→功能验证→形态学观察”的完整验证链条。
MeCP2的研究样本为正常小鼠成纤维细胞(NIH-3T3)及人前列腺癌细胞系(PC-3、LNCaP),验证方法包括Western blot及RT-qPCR检测核纤层蛋白的表达水平,免疫荧光结合共聚焦显微镜检测核膜形态变化;特异性方面,MeCP2敲低可特异性下调多种核纤层蛋白的表达,其中lamin A的下调幅度最大(约50%,n=3,P<0.001);敏感性方面,MeCP2表达水平的降低与核膜形态异常率呈正相关,部分细胞在MeCP2部分敲低时即出现核膜早期损伤迹象。
核心成果提炼:MeCP2作为连接异染色质与核膜的关键“桥梁”分子,其缺失会导致核纤层蛋白表达下调及核膜结构异常,进而抑制细胞增殖并阻碍细胞周期进程;本研究首次揭示MeCP2对核纤层蛋白的转录调控作用,创新性地将MeCP2的功能拓展至核膜稳定性调控领域,为理解MeCP2的非神经元功能及核膜相关疾病的机制提供了新的实验依据;研究未提供临床样本数据,其在体内的调控效应及作为疾病Biomarker的临床价值需进一步验证。
