1. 领域背景与文献引入
文献英文标题:Full Length Bid is sufficient to induce apoptosis of cultured rat hippocampal neurons;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:神经科学(兴奋性毒性神经元死亡机制)
兴奋性毒性神经元死亡是缺血性、创伤性及癫痫诱导脑损伤的核心病理机制之一,领域共识:谷氨酸受体过度激活可引发两种截然不同的细胞死亡类型——高强度激活会直接导致坏死,伴随离子稳态失衡、线粒体膜电位去极化、ATP耗竭及早期细胞膜渗漏;低强度激活则会引发延迟性凋亡,伴随线粒体释放细胞色素C(cyt-C)和凋亡诱导因子(AIF)等促凋亡因子。目前,兴奋性毒性中促凋亡因子从线粒体释放的具体机制尚未完全明确,尤其是BH3-only蛋白家族的调控作用存在研究空白。现有研究显示,Bid作为BH3-only蛋白家族成员,在死亡受体介导的凋亡中需经caspase-8切割为截短型Bid(tBid),才能转位至线粒体诱导cyt-C释放,但兴奋性毒性中caspase级联反应激活较弱,甚至被钙蛋白酶抑制,因此Bid在该途径中的激活方式及功能仍不明确。本文旨在探究全长Bid(FL-Bid)在谷氨酸受体过度激活诱导的海马神经元凋亡中的作用,明确其是否无需caspase-8切割即可介导线粒体死亡途径,为兴奋性毒性脑损伤的干预提供新的分子靶点。
2. 文献综述解析
作者按细胞死亡信号通路类型(死亡受体介导通路vs谷氨酸受体过度激活通路)对现有研究进行分类评述,系统梳理了Bid在不同通路中的作用机制及兴奋性毒性神经元死亡的未解问题。现有研究显示,死亡受体介导的凋亡中,Bid经caspase-8切割为tBid,随后发生肉豆蔻酰化并转位至线粒体,激活Bax/Bak形成通道,诱导cyt-C释放,该机制已在多种细胞模型中得到验证;兴奋性毒性神经元死亡领域,已有研究证实BH3-only蛋白Bad参与谷氨酸及钙诱导的神经元凋亡,Bid敲除小鼠对缺血性损伤的抗性增强,但Bid在该途径中的激活方式及具体作用仍不明确,且现有研究未关注FL-Bid是否具备独立的促凋亡功能。现有研究的局限性在于,未明确兴奋性毒性中Bid的激活是否依赖caspase切割,以及FL-Bid是否可直接介导凋亡。本文的创新价值在于,首次通过细胞实验证明FL-Bid转位线粒体足以诱导海马神经元凋亡,无需caspase-8的切割激活,填补了兴奋性毒性中Bid非依赖切割激活机制的研究空白。
3. 研究思路总结与详细解析
本文的研究目标是明确FL-Bid在谷氨酸受体过度激活诱导的海马神经元凋亡中的作用及激活机制,核心科学问题为FL-Bid是否无需caspase-8切割即可转位线粒体并介导凋亡,技术路线遵循“假设验证-机制解析-功能确认”的闭环逻辑:首先验证NMDA处理后FL-Bid的切割情况,其次检测其向线粒体的转位及伴随的cyt-C释放,最后通过过表达FL-Bid及非切割突变体验证其促凋亡功能。
3.1 NMDA处理后FL-Bid切割情况验证
实验目的:确认谷氨酸受体过度激活诱导的兴奋性毒性中,Bid是否经caspase-8切割激活。方法细节:以HeLa D98细胞和原代培养大鼠海马神经元为模型,分别用肿瘤坏死因子-α/环己酰亚胺(TNF-α/CHX)、星形孢菌素(STS)作为阳性对照,用300μM NMDA处理海马神经元5分钟,在处理后4h、8h提取细胞总蛋白,采用免疫印迹法检测Bid的切割产物,同时检测钙蛋白酶底物α-spectrin的切割情况以验证NMDA处理的有效性。结果解读:免疫印迹结果显示,阳性对照处理组可检测到FL-Bid的切割产物,而NMDA处理组未检测到FL-Bid含量减少或切割产物生成,但α-spectrin被切割为150kDa和145kDa的钙蛋白酶特异性产物,说明NMDA处理后钙蛋白酶激活,但Bid未发生显著切割(n=4,重复实验结果一致)。
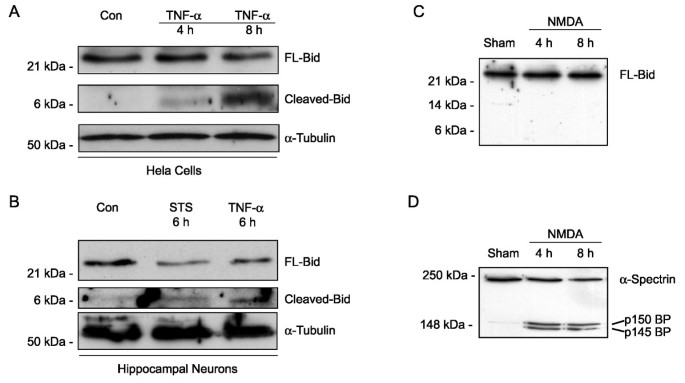
实验所用关键产品:Sigma的N-甲基-D-天冬氨酸(NMDA)、肿瘤坏死因子-α(TNF-α)、环己酰亚胺(CHX),Alexis的星形孢菌素(STS),Chemicon的α-spectrin单克隆抗体,针对Bid的兔多克隆抗体(AR-53)。
3.2 FL-Bid向线粒体转位的验证
实验目的:确认NMDA处理后FL-Bid是否从胞质转位至线粒体,并伴随cyt-C的释放。方法细节:对NMDA处理后的海马神经元进行选择性细胞膜通透,分离胞质组分和线粒体沉淀组分,采用免疫印迹法检测Bid和cyt-C在两组分中的分布,同时采用免疫荧光染色法观察Bid和cyt-C的细胞定位,并用Hoechst33258染色观察核染色质浓缩情况。结果解读:免疫印迹结果显示,NMDA处理后4h和8h,FL-Bid从胞质组分转位至线粒体沉淀组分,且伴随cyt-C从线粒体向胞质的释放,8h时线粒体中cyt-C含量显著降低,但胞质中cyt-C未相应增加,推测其释放后被降解;免疫荧光结果显示,对照组Bid呈弥漫性分布,cyt-C呈线粒体特异性点状分布,NMDA处理后Bid聚集在核周,cyt-C释放,且细胞核染色质浓缩(n=2,重复实验结果一致)。
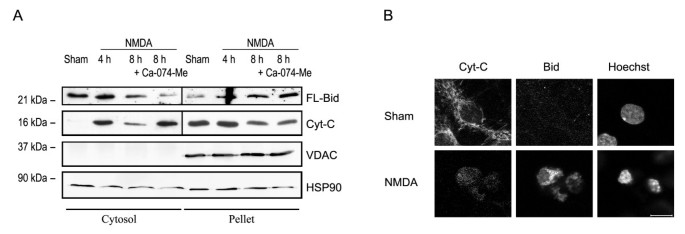
实验所用关键产品:Calbiochem的电压依赖性阴离子通道(VDAC)单克隆抗体,San Diego的抗细胞色素C单克隆抗体(6H2.B4),Sigma的Hoechst33258染料。
3.3 FL-Bid及非切割突变体过表达诱导凋亡的验证
实验目的:验证FL-Bid是否无需caspase-8切割即可诱导海马神经元凋亡。方法细节:构建四环素诱导的腺病毒载体,分别表达野生型FL-Bid和caspase-8非切割突变体Bid(D59A),以50感染复数(MOI)感染原代海马神经元,24h后加入1μg/ml强力霉素诱导表达,24h后采用免疫印迹法检测Bid的过表达水平,Hoechst染色检测核损伤率,免疫荧光法检测AIF的释放情况。结果解读:免疫印迹结果显示,强力霉素诱导后FL-Bid和Bid(D59A)均实现轻度过表达;Hoechst染色结果显示,FL-Bid过表达组神经元核损伤率达80.1±2.7%(n=3,P<0.01),Bid(D59A)过表达组核损伤率为73.5±3.1%,与FL-Bid组无显著统计学差异(P>0.1);免疫荧光结果显示,过表达组伴随AIF从线粒体向细胞核的释放,而未诱导组神经元保持存活。
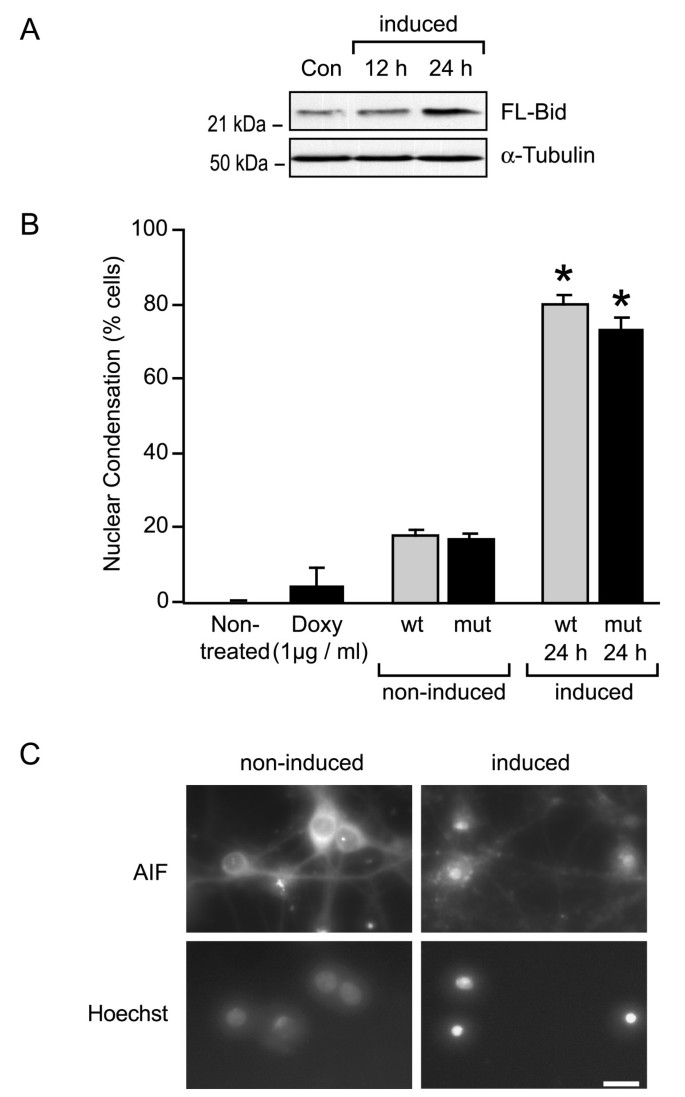
实验所用关键产品:Sigma的强力霉素,腺病毒载体由作者基于已有方法构建(引用文献[32]),针对AIF的兔多克隆抗体。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker为全长Bid(FL-Bid),属于蛋白质类生物标志物,其筛选与验证逻辑为:先通过细胞模型验证NMDA处理后FL-Bid的转位及未切割状态,再通过过表达实验确认其独立的促凋亡功能,形成完整的“状态观察-功能验证”链条。研究过程详述:该Biomarker来源于原代培养大鼠海马神经元的内源性蛋白,验证方法包括免疫印迹法、免疫荧光法及过表达功能实验;特异性方面,NMDA处理后仅FL-Bid发生转位,未检测到caspase-8切割产物,说明其激活不依赖切割;敏感性方面,轻度过表达FL-Bid即可诱导80%以上的海马神经元凋亡。核心成果提炼:FL-Bid可作为兴奋性毒性神经元凋亡的介导因子,其无需caspase-8切割即可转位至线粒体,诱导cyt-C和AIF释放,进而介导凋亡;创新性在于首次在海马神经元中证明FL-Bid具备独立的促凋亡功能,揭示了Bid在兴奋性毒性中的非经典激活机制;统计学结果显示,FL-Bid过表达诱导的神经元核损伤率为80.1±2.7%(n=3,P<0.01),Bid(D59A)过表达组为73.5±3.1%(P>0.1 vs FL-Bid组)。
