1. 领域背景与文献引入
文献英文标题:The architecture of chicken chromosome territories changes during differentiation;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学(染色体核架构与细胞分化)
染色体领地是间期细胞核中每条染色体占据的特定空间区域,1985年通过荧光原位杂交(FISH)技术首次被明确证实,为核架构研究奠定了基础。此后数十年,领域内的研究聚焦于染色体领地的内部组织规律,尤其是基因转录活性与基因在领地内位置的关联。部分研究发现活跃基因偏好位于染色体领地的表面或外部区域,如主要组织相容性复合体(MHC)、表皮分化复合体(EDC)等基因簇在激活后会环出染色体领地;但也有研究显示转录信号可分布于整个染色体领地,活跃基因也可位于领地内部,这一矛盾表明基因位置与转录活性的关系尚未明确。当前未解决的核心问题包括:不同分化阶段细胞的染色体领地内部结构是否存在特异性变化?分化过程中基因位置的改变是转录调控的直接结果,还是染色体架构全局重构的伴随现象?这些问题的解决将有助于深入理解细胞分化的核调控机制。
针对上述研究空白,本研究以鸡造血细胞的多阶段分化模型为研究对象,结合3D荧光原位杂交技术和定量图像分析,系统解析了染色体领地形态、基因座及着丝粒位置的动态变化,揭示了细胞分化过程中染色体核架构的全局重构规律,为核架构与细胞分化的关系提供了新的实验证据。
2. 文献综述解析
作者在综述中按研究结论的差异(活跃基因位置的不同观点)和技术应用方向(不同基因座的荧光原位杂交研究)对现有文献进行分类,梳理了染色体领地研究的核心争议与进展。
现有研究的关键结论存在明显分歧,一类研究通过荧光原位杂交技术观察到MHC、EDC等基因簇在激活后会环出染色体领地,认为活跃基因偏好位于领地表面或外部;另一类研究则发现转录信号可分布于整个染色体领地,部分活跃基因也可位于领地内部,如ANT2、ANT3基因的活性与领地内位置无严格对应关系。技术方法上,荧光原位杂交尤其是3D荧光原位杂交技术为染色体和基因的空间定位提供了直观手段,能精准捕捉核架构的细节特征;但现有研究的局限性在于多针对特定基因簇,单个基因的情况缺乏系统研究,且未关注细胞分化过程中染色体领地的全局变化,导致对基因位置与转录活性关系的理解存在片面性。
与现有研究相比,本研究的创新点在于首次以细胞分化的完整阶段为模型,同时分析染色体领地的形态变化、单个基因座和着丝粒的位置动态,而非仅关注基因转录相关的局部变化。现有研究多聚焦于基因活性与位置的直接关联,而本研究发现分化过程中染色体领地的全局重构是基因位置变化的背景,着丝粒位置与基因座同步变化,提示基因位置变化可能是染色体架构全局变化的伴随结果,而非转录调控的直接原因,这一发现为核架构与细胞分化的关系提供了全新视角。
3. 研究思路总结与详细解析
本研究的整体框架为:以代表鸡造血细胞不同分化阶段的5种细胞系为模型,通过3D荧光原位杂交技术标记染色体领地、溶菌酶基因座和着丝粒,结合共聚焦显微镜成像和定量图像分析,系统研究染色体领地的形态变化、基因及着丝粒的位置动态、染色体的核径向分布及核体积变化,最终揭示细胞分化过程中染色体核架构的重构规律。研究目标是阐明分化过程中染色体领地架构的动态变化特征,核心科学问题是分化阶段与染色体领地形态、基因位置的关联机制,技术路线遵循“模型建立→标记成像→定量分析→结论推导”的闭环逻辑。
3.1 分化阶段细胞模型的建立与样本制备
实验目的:获取覆盖造血细胞从多能前体到终末分化的完整阶段细胞模型,制备适用于3D荧光原位杂交的细胞核样本,为核架构分析提供基础。
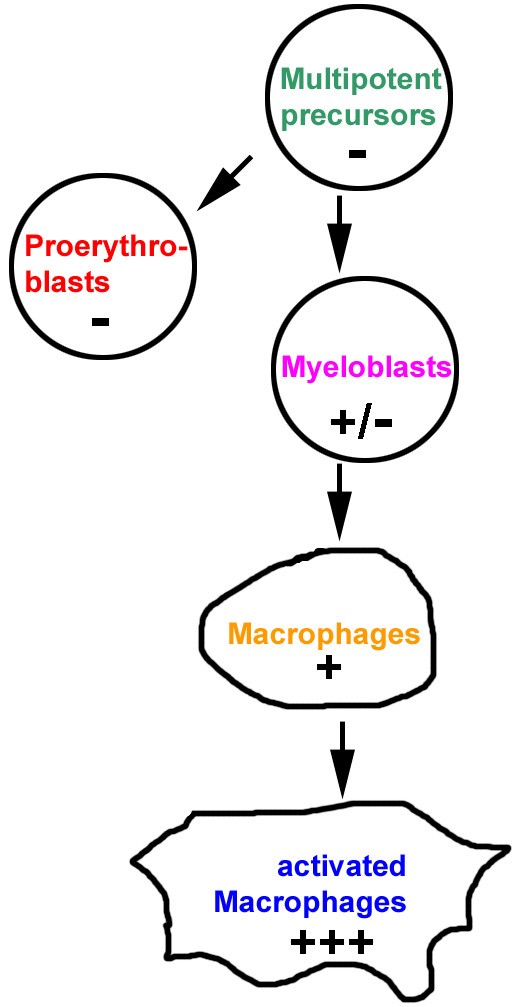
方法细节:选取5种鸡造血细胞系,包括多能髓系前体细胞(不表达溶菌酶)、成髓细胞(低表达溶菌酶)、未刺激巨噬细胞(中表达溶菌酶)、LPS刺激巨噬细胞(高表达溶菌酶)、成红细胞(不表达溶菌酶);细胞培养于添加2%鸡血清、8%胎牛血清和2mmol/L谷氨酰胺的IMDM培养基,置于37℃、5%CO₂培养箱中培养;巨噬细胞通过添加5μg/mL LPS刺激过夜以激活并诱导溶菌酶高表达;细胞固定于经多聚-L-赖氨酸预处理的盖玻片,依次经1.2%甲醛固定、0.5%Triton X-100透化、20%甘油处理、液氮冻融5次、0.1M HCl处理等步骤,制备结构完整的间期细胞核样本。
结果解读:不同细胞系代表了造血细胞分化的不同阶段,溶菌酶基因表达水平随分化阶段呈现梯度变化,成功建立了覆盖多能前体到终末分化的细胞模型;样本制备过程保留了细胞核的三维结构,为3D荧光原位杂交分析提供了可靠基础。
产品关联:文献提及实验所用关键产品:Sigma的多聚-L-赖氨酸(货号P5899)、Sigma的LPS(货号L-8275)。
3.2 3D荧光原位杂交探针制备与细胞核标记
实验目的:特异性标记染色体1、8领地、溶菌酶基因座及染色体1着丝粒,实现不同标记信号的空间分辨,为核架构分析提供可视化工具。
方法细节:染色体1和8的涂染探针通过流式分选染色体后经DOP-PCR扩增制备,混合早期扩增产物和多次扩增产物以同时标记整个染色体和着丝粒;溶菌酶基因座探针通过pPoly-III-i Lys质粒经缺口平移标记地高辛-dUTP;探针混合物与鸡Cot 1 DNA共沉淀,变性后与样本在37℃杂交24-72小时;采用抗地高辛抗体结合Alexa488、Avidin-Cy3分别检测溶菌酶基因座和染色体1信号,DAPI和TOPRO-3复染细胞核,使用Leica TCS SP共聚焦激光扫描显微镜获取3D图像栈。
结果解读:成功实现染色体领地、基因座和着丝粒的特异性标记,共聚焦图像可清晰分辨不同标记信号的空间位置;染色体1涂染探针可同时显示整个染色体领地和着丝粒的明亮信号,为后续位置分析提供了精准标记。
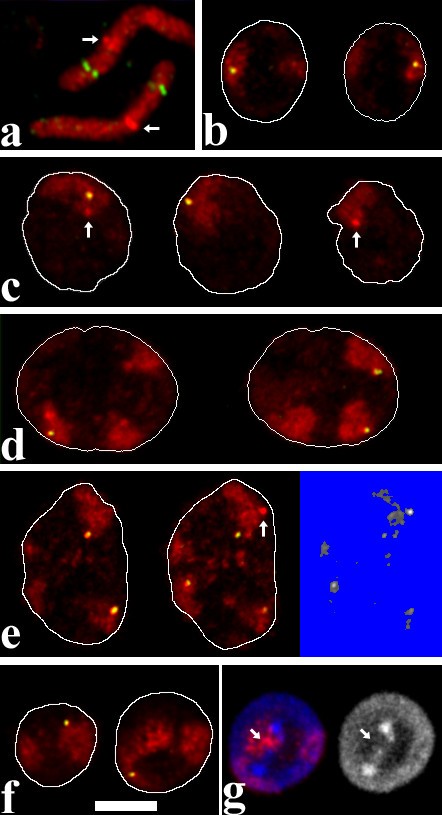
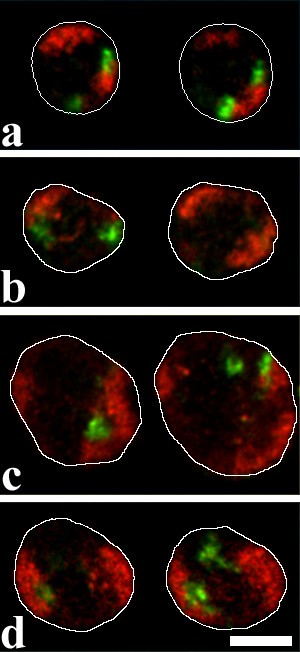
产品关联:文献提及实验所用关键产品:Roche Applied Science的生物素-16-dUTP和地高辛-16-dUTP、Sigma的抗地高辛抗体和Alexa488标记的羊抗兔抗体、Dianova的Avidin-Cy3、Molecular Probes的DAPI和TOPRO-3、Vector Laboratories的Vectashield封片液、Leica TCS SP共聚焦激光扫描显微镜。
3.3 染色体领地形态的定量分析
实验目的:量化不同分化阶段细胞中染色体领地的分散度差异,揭示分化过程中染色体领地形态的动态变化规律。
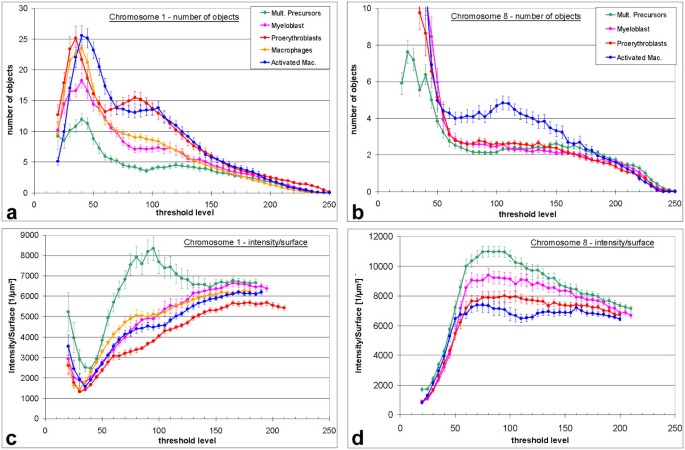
方法细节:使用自定义图像分析程序对共聚焦图像栈进行高斯滤波和归一化处理,从阈值20开始逐步提高阈值,统计每个阈值下染色体领地分解的物体数量(仅计数≥10个体素的结构);选取阈值80及以上的最大物体数量进行统计分析,采用单因素ANOVA和Sidak检验比较不同细胞系的差异;同时计算每个物体的染色质含量(信号强度)与表面积的比值,评估领地的紧凑程度。
结果解读:多能髓系前体细胞的染色体1领地最为紧凑,在阈值80及以上分解的物体数量最少;随着分化推进,成髓细胞、成红细胞、巨噬细胞的染色体1领地逐渐分散,分解的物体数量显著增加,单因素ANOVA分析显示组间差异具有高度统计学显著性(F(2,119)=58.5,P<0.001);LPS刺激的巨噬细胞领地分散度最高,物体数量显著高于其他细胞系。染色体8领地的变化趋势类似,但仅在刺激巨噬细胞中分散度显著高于其他细胞类型(P<0.001)。染色质含量/表面积比值显示前体细胞的领地更为紧凑,分化细胞的领地更为松散。
产品关联:文献未提及具体图像分析软件,领域常规使用ImageJ、SPSS等软件进行图像分割、计数和统计分析。
3.4 溶菌酶基因座与着丝粒的位置动态分析
实验目的:分析溶菌酶基因座和染色体1着丝粒在领地内的位置变化,探讨其与基因转录活性及细胞分化的关联。
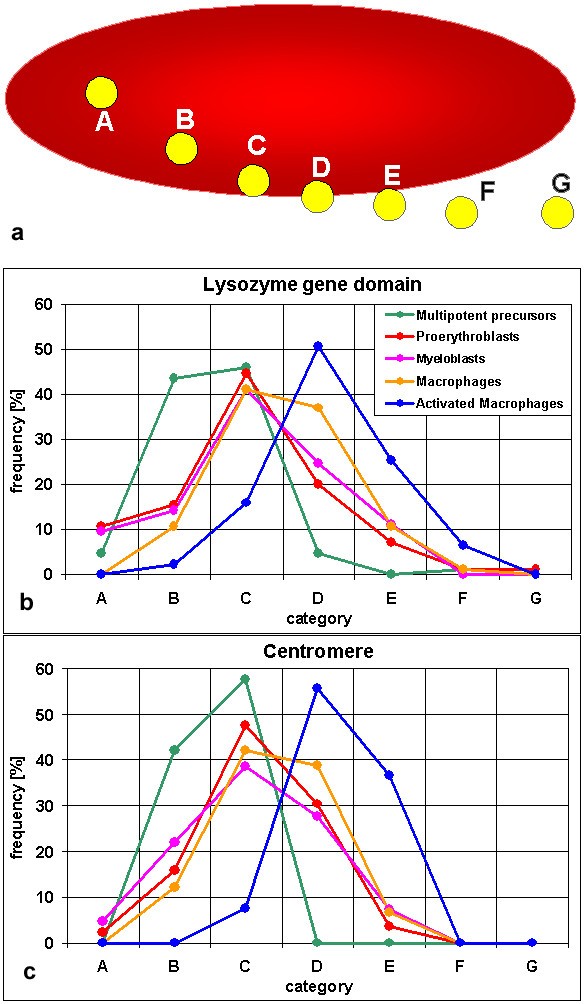
方法细节:采用预设分类标准,将基因/着丝粒信号分为7个类别:A(领地内部远离边缘)、B(领地内部靠近边缘)、C(接触领地边缘)、D(领地表面)、E(外部接触表面)、F(邻近领地无接触)、G(远离领地);统计不同细胞系中各类别的信号比例,采用Mann-Whitney U检验比较组间差异;同时使用Showpos程序测量溶菌酶基因座与着丝粒的3D距离,判断是否存在共定位。
结果解读:多能前体细胞中,48%的溶菌酶基因位于领地内部(A、B类),46%接触边缘(C类);分化后,基因逐渐向领地边缘移动,LPS刺激的巨噬细胞中82%的基因位于表面或外部(D-G类),与前体细胞的差异具有高度统计学显著性(P<0.001)。染色体1着丝粒的位置变化与基因座高度相似,前体细胞中全部位于领地内部,刺激巨噬细胞中93%位于表面或外部(P<0.001)。3D距离测量显示溶菌酶基因座与着丝粒的最小距离为0.5μm,排除了沉默基因与着丝粒异染色质共定位的可能。
产品关联:文献提及实验所用关键产品:自定义的Showpos程序用于3D距离测量,SPSS用于统计分析。
3.5 染色体领地的核径向分布与核体积测量
实验目的:分析染色体1和8在细胞核内的径向位置变化,以及核体积随分化的变化规律,全面揭示核架构的分化相关特征。
方法细节:使用专用程序分析染色体领地的径向分布,计算信号中位数对应的核半径比例,采用Kolmogorov-Smirnov检验比较组间差异;同时测量细胞核的体积,统计不同细胞系的核体积均值并进行组间比较。
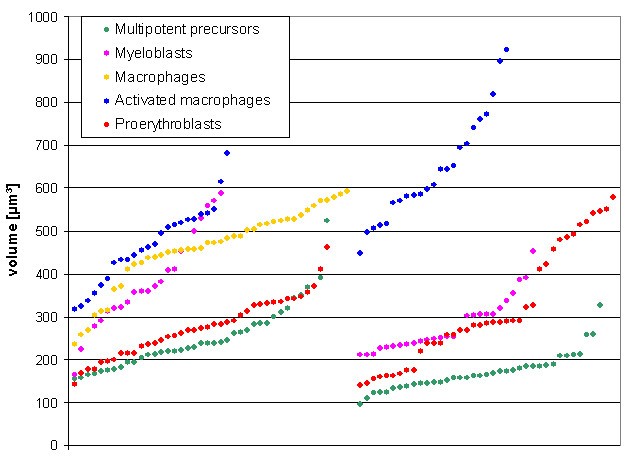
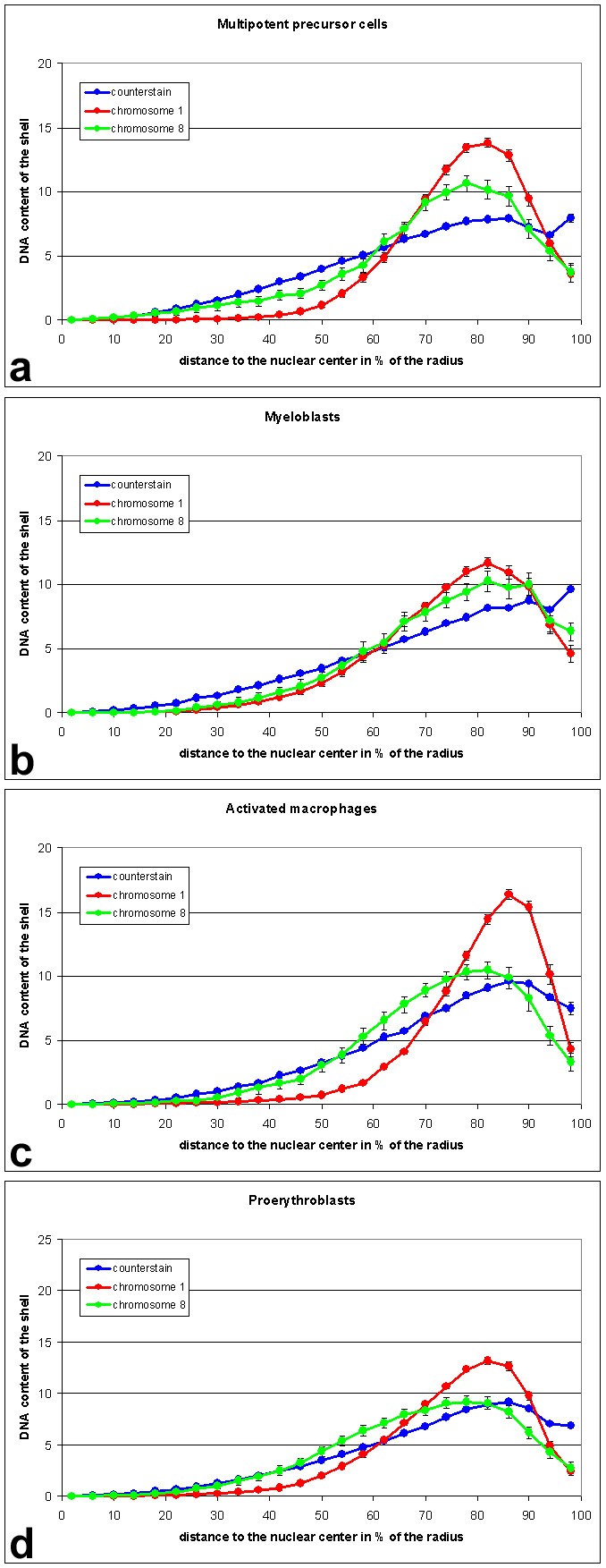
结果解读:多能前体细胞、成红细胞和LPS刺激巨噬细胞中,染色体1位于核外周,染色体8位于核内部,两者的径向分布差异具有统计学显著性(P<0.005);成髓细胞中两者的径向分布无显著差异。染色体1的径向分布在不同细胞系间存在显著差异,刺激巨噬细胞的染色体1最靠近核边缘(P<0.001)。核体积方面,多能前体细胞的平均体积为212μm³(n=76),成髓细胞为327μm³(n=50),组间差异具有高度统计学显著性(P<0.001);成红细胞平均体积为296μm³(n=78),与前体细胞无显著差异;刺激巨噬细胞平均体积为554μm³(n=78),显著大于未刺激巨噬细胞(P<0.05)。
产品关联:文献未提及具体核体积测量软件,领域常规使用基于共聚焦图像的3D分割软件(如Imaris)进行核体积测量。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为与细胞分化阶段相关的染色体核架构特征,包括染色体领地的分散度、溶菌酶基因座在染色体领地内的位置、染色体的核径向分布,这些特征可作为判断造血细胞分化状态的核架构标志物。
Biomarker定位
本研究中的Biomarker属于细胞分化状态的核架构标志物,筛选与验证逻辑为:基于已知的鸡造血细胞分化阶段模型,通过3D荧光原位杂交技术标记染色体领地、基因座和着丝粒,结合定量图像分析验证这些核架构特征与分化阶段的关联,形成“模型建立→标记验证→特征确认”的完整逻辑链条。
研究过程详述
Biomarker的来源为5种不同分化阶段的鸡造血细胞系的细胞核样本;验证方法包括3D荧光原位杂交特异性标记、共聚焦显微镜高分辨率成像、定量图像分析(领地分散度计数、位置分类统计、径向分布测量);特异性与敏感性数据显示,染色体1领地分散度在多能前体细胞与分化细胞间的差异具有高度统计学显著性(ANOVA分析F(2,119)=58.5,P<0.001),溶菌酶基因位置在LPS刺激巨噬细胞与其他细胞系间的差异具有高度统计学显著性(Mann-Whitney U检验P<0.001),染色体径向分布在特定细胞系间的差异具有统计学显著性(如前体细胞中染色体1与8的差异P<0.005)。
核心成果提炼
该Biomarker的功能关联在于可作为判断造血细胞分化状态的核架构特征,不同分化阶段的细胞具有特异性的染色体领地形态、基因位置和径向分布模式;创新性在于首次揭示细胞分化过程中染色体领地的全局重构规律,发现着丝粒位置与基因座同步变化,提示基因位置变化是染色体架构全局变化的伴随结果,而非基因转录调控的直接原因,这一发现突破了现有研究中基因位置与转录活性直接关联的认知;关键统计学结果包括染色体1领地分散度的ANOVA分析F(2,119)=58.5(P<0.001),溶菌酶基因位置的Mann-Whitney U检验P<0.001,染色体径向分布的Kolmogorov-Smirnov检验P<0.005等。
