1. 领域背景与文献
文献英文标题:Single-cell RNA sequencing unveils enhanced antitumor immunity in colorectal cancer with PD-1 blockade and LINC00673 deletion;发表期刊:Biomarker Research;影响因子:未公开;研究领域:结直肠癌肿瘤免疫治疗。
结直肠癌是全球范围内严重威胁人类健康的恶性肿瘤,领域共识显示其2024年全球新发病例达193万例,死亡病例93.5万例,发病率居所有恶性肿瘤第三位,死亡率居第二位,且约半数患者确诊时已处于晚期,现有治疗手段疗效有限,预后较差。免疫检查点抑制剂(ICIs)的问世彻底改变了多个恶性肿瘤的治疗格局,在黑色素瘤、非小细胞肺癌中已取得显著临床获益,但在结直肠癌中,其疗效仅局限于占比约15%的微卫星高度不稳定(MSI-H)/错配修复缺陷(dMMR)亚型,占比85%的微卫星稳定(MSS)/错配修复正常(pMMR)亚型患者因存在高度免疫抑制的肿瘤微环境(TME),对免疫检查点抑制剂治疗响应率极低,是目前结直肠癌免疫治疗领域亟待解决的核心难题。长链非编码RNA(lncRNA)是一类长度超过200个核苷酸的非编码转录本,既往研究已证实其可通过RNA-RNA、RNA-蛋白互作参与肿瘤发生发展的多个环节,部分长链非编码RNA还可编码功能性微肽发挥调控作用,其中LINC00673已被报道在胰腺癌、非小细胞肺癌、胃癌等多种实体瘤中高表达,通过调控Wnt/β-catenin、PI3K/AKT等致癌通路促进肿瘤增殖、转移,与患者不良预后密切相关,但该分子在结直肠癌肿瘤微环境中的调控作用尚未明确。近年来单细胞RNA测序(scRNA-seq)技术的快速发展为在单细胞分辨率解析肿瘤微环境的细胞异质性、转录组特征及细胞间互作提供了高分辨率工具,为揭示结直肠癌免疫耐药机制、挖掘新型免疫治疗靶点提供了技术支撑。本研究针对上述领域空白,系统解析LINC00673对结直肠癌抗肿瘤免疫的调控作用,验证其作为免疫治疗增敏靶点的潜力,为提升结直肠癌免疫治疗疗效提供新的理论依据和干预策略。
2. 文献综述解析
作者的文献综述按照研究方向分为三个核心维度展开,分别为结直肠癌免疫治疗的研究进展、长链非编码RNA的肿瘤调控功能研究、LINC00673的现有研究基础,系统梳理了领域内的关键进展与未解决问题,为本次研究的开展提供了充分的立论依据。
在结直肠癌免疫治疗领域,现有研究明确了免疫检查点抑制剂仅对微卫星高度不稳定/错配修复缺陷亚型有效的临床现状,证实免疫抑制性肿瘤微环境是微卫星稳定亚型患者免疫检查点抑制剂耐药的核心机制,目前已开展的免疫检查点抑制剂联合抗血管生成药物、局部治疗等策略虽取得一定进展,但整体有效率仍不足20%,尚未满足临床需求;该部分研究的技术优势在于已建立了完善的结直肠癌免疫分型体系与临床疗效评估体系,局限性在于缺乏可有效逆转微卫星稳定亚型免疫抑制微环境的精准干预靶点。在长链非编码RNA研究领域,现有研究已打破了长链非编码RNA仅为“转录噪音”的传统认知,证实部分长链非编码RNA可编码功能性微肽,通过多重调控机制参与肿瘤的增殖、转移、免疫逃逸等多个生物学过程;技术优势在于已建立了成熟的长链非编码RNA筛选、功能验证技术体系,局限性在于大部分长链非编码RNA在肿瘤免疫调控中的功能尚未被解析。在LINC00673研究领域,现有研究已证实其在多种实体瘤中作为促癌分子发挥作用,可通过调控多条致癌通路促进肿瘤进展,且与患者不良预后相关;技术优势在于已明确了其部分下游调控通路,局限性在于其在结直肠癌中对肿瘤免疫微环境的调控作用完全未知,也缺乏其作为免疫治疗靶点的功能验证。
通过对比现有研究的未解决问题,本研究的创新价值主要体现在三个方面:首次揭示LINC00673在结直肠癌中同时发挥肿瘤内在促癌作用与外在免疫抑制作用的双重功能;首次在单细胞分辨率系统解析了LINC00673敲除对结直肠癌肿瘤微环境的重塑机制;首次证实LINC00673敲除可显著增强程序性死亡受体1抑制剂的抗肿瘤疗效,为结直肠癌免疫治疗提供了新的潜在增敏靶点,填补了领域内的研究空白。
3. 研究思路总结与详细解析
本研究的总体研究目标为明确LINC00673对结直肠癌抗肿瘤免疫的调控作用,探索其作为免疫治疗增敏靶点的临床转化潜力;核心科学问题为LINC00673如何调控结直肠癌肿瘤微环境的免疫状态,以及其敲除联合程序性死亡受体1阻断发挥协同抗肿瘤作用的分子机制;整体技术路线遵循“生物信息学筛选→临床样本验证→动物模型功能验证→单细胞测序机制解析→体外细胞实验验证→临床队列相关性验证”的闭环逻辑,研究设计严谨,结果可靠性高。
3.1 LINC00673的临床相关性筛选与验证
本环节核心目标是筛选结直肠癌中与免疫调控相关的长链非编码RNA,验证LINC00673的表达特征及临床预后价值、免疫相关性。方法细节:首先采用ImmLnc算法分析癌症基因组图谱(TCGA)结直肠癌数据集的免疫相关长链非编码RNA,结合基因表达谱交互分析2(GEPIA2)数据库的表达差异数据(筛选标准为肿瘤vs癌旁|logFC|>1,P<0.05),最终筛选得到LINC00673作为研究对象;随后收集复旦大学附属肿瘤医院的20对结直肠癌及配对癌旁新鲜组织,分别通过免疫印迹(WB)、实时荧光定量PCR(qRT-PCR)检测LINC00673的蛋白和RNA表达水平;采用包含106例结直肠癌及配对癌旁组织的组织微阵列(TMA)进行免疫组化(IHC)染色,分析LINC00673的表达水平与患者总生存期的相关性;同时分析公共数据库中接受新辅助程序性死亡受体1阻断治疗的错配修复缺陷/微卫星高度不稳定结直肠癌患者的单细胞RNA测序数据,解析LINC00673表达与免疫细胞浸润、治疗响应的相关性。结果解读:生物信息学筛选流程如图1所示,
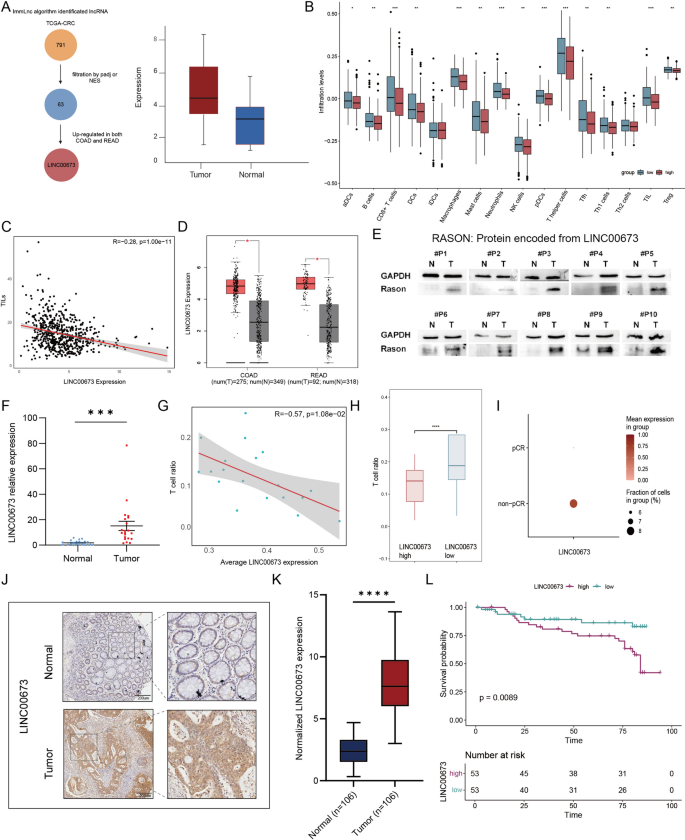
癌症基因组图谱数据集的单样本基因集富集分析(ssGSEA)显示,LINC00673高表达的结直肠癌样本中CD8+T细胞、肿瘤浸润淋巴细胞(TIL)的富集评分显著降低;相关性分析显示LINC00673表达水平与肿瘤浸润淋巴细胞浸润丰度呈显著负相关(R=-0.21,P<0.001);基因表达谱交互分析2数据库验证显示LINC00673在结肠癌和直肠癌组织中的表达均显著高于癌旁组织;临床样本验证结果显示,结直肠癌组织中LINC00673的蛋白和RNA水平均显著高于癌旁组织,其中RNA表达量为癌旁组织的2.7倍(n=20,P<0.001);公共单细胞测序数据分析显示,LINC00673表达与总T细胞浸润、CD8+T细胞数量呈显著负相关,且在未获得病理完全缓解(non-pCR)的患者中表达显著高于病理完全缓解患者(病理完全缓解组n=15,非病理完全缓解组n=4,P<0.05);免疫组化染色显示LINC00673主要表达于肿瘤细胞胞质中,肿瘤组织的免疫组化染色评分显著高于癌旁组织(n=53对,P<0.001);Kaplan-Meier生存分析显示,LINC00673高表达患者的总生存期显著短于低表达患者(log-rank P=0.0089)。产品关联:文献未提及该环节具体实验产品的品牌及货号,领域常规使用RNA提取试剂盒、实时荧光定量PCR试剂、免疫组化检测试剂盒、LINC00673特异性一抗及对应二抗等。
3.2 动物模型构建与体内功能验证
本环节核心目标是在体内验证Linc00673敲除单独及联合程序性死亡受体1阻断的抗肿瘤效果,以及其对肿瘤免疫微环境的调控作用。方法细节:采用CRISPR/Cas9基因编辑技术构建Linc00673全身敲除(KO)小鼠,通过基因型PCR验证敲除成功;采用AOM/DSS诱导构建结肠炎相关结直肠癌模型,6周龄雄性C57BL/6J小鼠随机分为4组:野生型(WT)对照组、野生型+程序性死亡受体1阻断组、Linc00673敲除组、Linc00673敲除+程序性死亡受体1阻断组,每组n=8;造模方案为腹腔注射10mg/kg的偶氮甲烷(AOM),7天后给予2.5%葡聚糖硫酸钠(DSS)饮水7天,随后给予普通饮水14天,上述葡聚糖硫酸钠处理循环重复3次;程序性死亡受体1阻断抗体给药方案为6mg/kg,每3天尾静脉注射一次;实验终点处死小鼠,收集结肠组织,统计肿瘤数量与体积,采用流式细胞术(FCM)检测肿瘤组织中浸润免疫细胞的比例与功能表型。结果解读:动物实验流程与结果如图2所示,
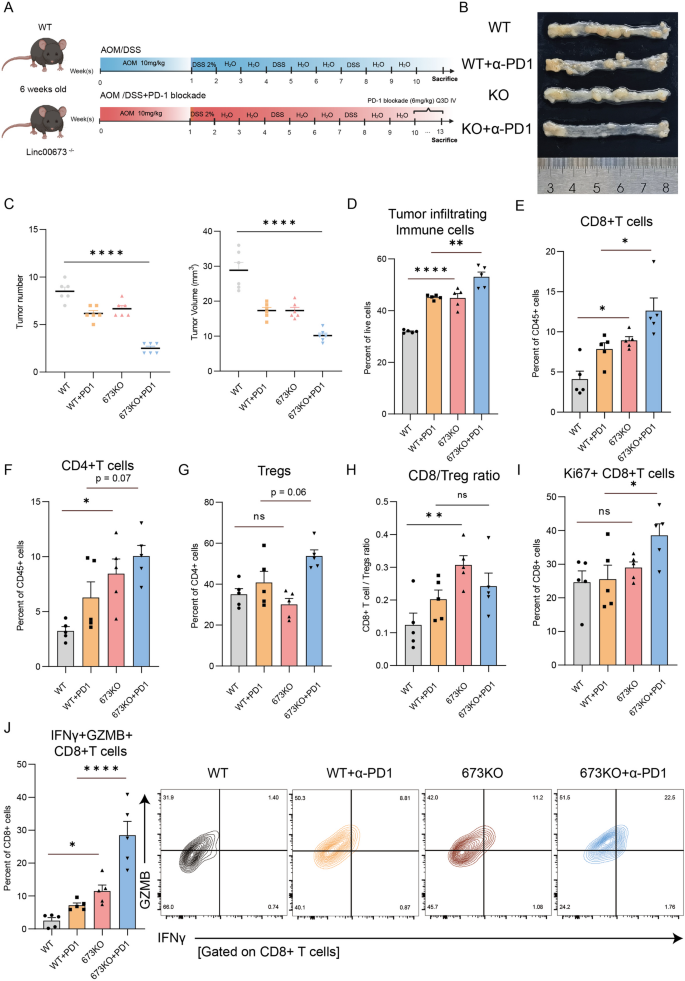
各组小鼠的体重、血清生化指标(谷草转氨酶AST、谷丙转氨酶ALT、肌酐CREA、尿酸UA、乳酸脱氢酶1 LDH1)均无显著差异,提示Linc00673敲除无明显系统毒性;与野生型组相比,Linc00673敲除组的肿瘤数量减少42%(n=6,P<0.01),肿瘤体积减少57%(n=6,P<0.001),联合程序性死亡受体1阻断后肿瘤负荷进一步降低,肿瘤数量减少68%(n=6,P<0.001),肿瘤体积减少79%(n=6,P<0.0001);流式细胞术检测显示,Linc00673敲除组肿瘤组织中CD45+免疫细胞浸润比例升高1.8倍(n=6,P<0.01),CD8+T细胞比例升高2.1倍(n=6,P<0.001),CD4+T细胞比例升高1.3倍(n=6,P<0.05);CD8+T细胞/调节性T细胞(Treg)比值升高2.7倍(n=6,P<0.001),Ki67+增殖型CD8+T细胞比例升高1.9倍(n=6,P<0.01),表达干扰素-γ(IFN-γ)和颗粒酶B(GZMB)的功能性CD8+T细胞比例升高2.3倍(n=6,P<0.001),联合程序性死亡受体1阻断后上述指标均进一步提升。产品关联:实验所用关键产品:BioLegend的程序性死亡受体1阻断抗体、流式细胞术相关抗体(货号文献未明确提及),Miltenyi Biotec的小鼠肿瘤解离试剂盒、死细胞去除试剂盒,BD公司的Accuri™ C6流式细胞仪。
3.3 单细胞转录组测序分析肿瘤微环境重塑机制
本环节核心目标是在单细胞分辨率解析Linc00673敲除联合程序性死亡受体1阻断对结直肠癌肿瘤微环境细胞组成、转录组特征的调控机制。方法细节:收集4组各2只小鼠的肿瘤组织,使用小鼠肿瘤解离试剂盒制备单细胞悬液,采用10x Genomics Chromium Next GEM Single Cell 3ʹ 试剂盒构建单细胞RNA测序文库,使用Illumina NovaSeq 6000平台进行测序;测序数据使用Cell Ranger软件比对到mm10参考基因组,采用Seurat R包进行质控,过滤基因数<200或>8000、线粒体基因表达占比>10%的低质量细胞,使用DoubletFinder去除双细胞,最终获得46603个高质量细胞用于后续分析;通过均匀流形逼近与投影(UMAP)降维、无监督聚类,根据细胞类型经典marker基因注释细胞类群;进一步对T细胞、B细胞、髓系细胞、恶性上皮细胞进行亚群注释,通过差异基因分析、基因本体(GO)富集分析、CellPhoneDB细胞间互作分析解析调控机制。结果解读:单细胞测序分析流程与结果如图3所示,
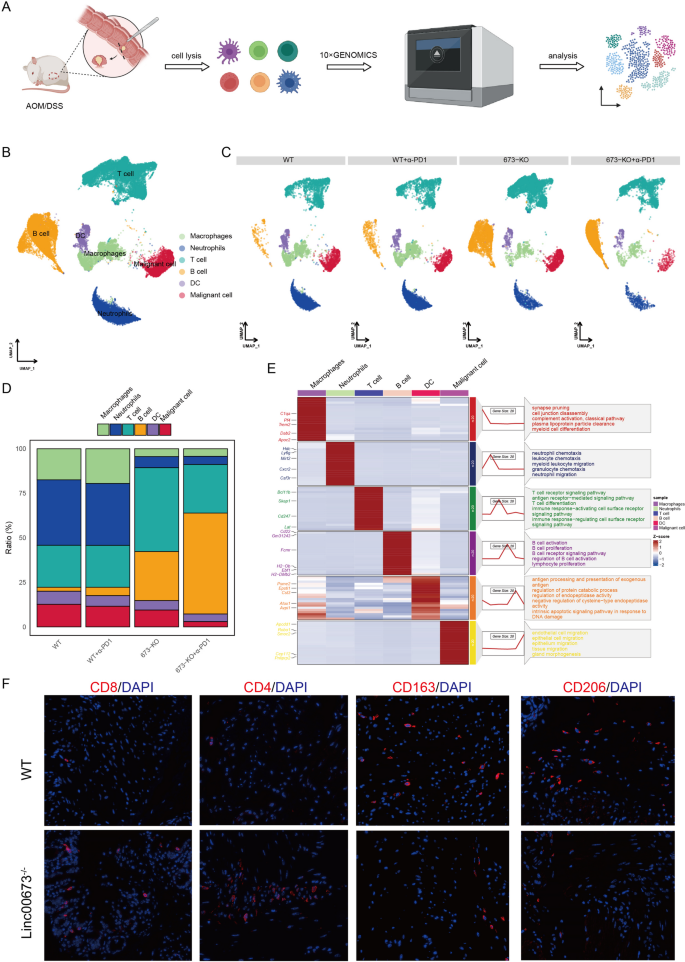
共注释得到6种主要细胞类群:上皮细胞、树突状细胞(DC)、T细胞、B细胞、中性粒细胞、巨噬细胞;与野生型组相比,Linc00673敲除联合程序性死亡受体1阻断组中恶性上皮细胞、巨噬细胞、髓系细胞的比例显著降低,T细胞、B细胞的比例显著升高;免疫荧光染色验证显示,Linc00673敲除组肿瘤组织中CD8+、CD4+T细胞的浸润数量显著增加,M2型巨噬细胞标志物CD163、CD206的表达显著降低,与单细胞测序结果一致。产品关联:实验所用关键产品:10x Genomics的Chromium Next GEM Single Cell 3ʹ Reagent Kits v3,Illumina的NovaSeq 6000测序平台,免疫荧光检测所用一抗、二抗试剂盒品牌货号文献未明确提及,领域常规使用抗CD8、CD4、CD163、CD206特异性一抗及荧光标记二抗。
3.4 T细胞亚群的功能调控机制解析
本环节核心目标为明确Linc00673敲除对CD8+、CD4+T细胞亚群组成、转录功能的调控作用。方法细节:从单细胞测序数据中提取CD8+T细胞和CD4+T细胞的表达矩阵进行重新聚类,根据亚群特异性marker基因注释细胞亚群;比较不同实验组的亚群比例差异,通过差异基因分析、基因本体富集分析解析亚群的功能变化。结果解读:T细胞亚群分析结果如图4所示,
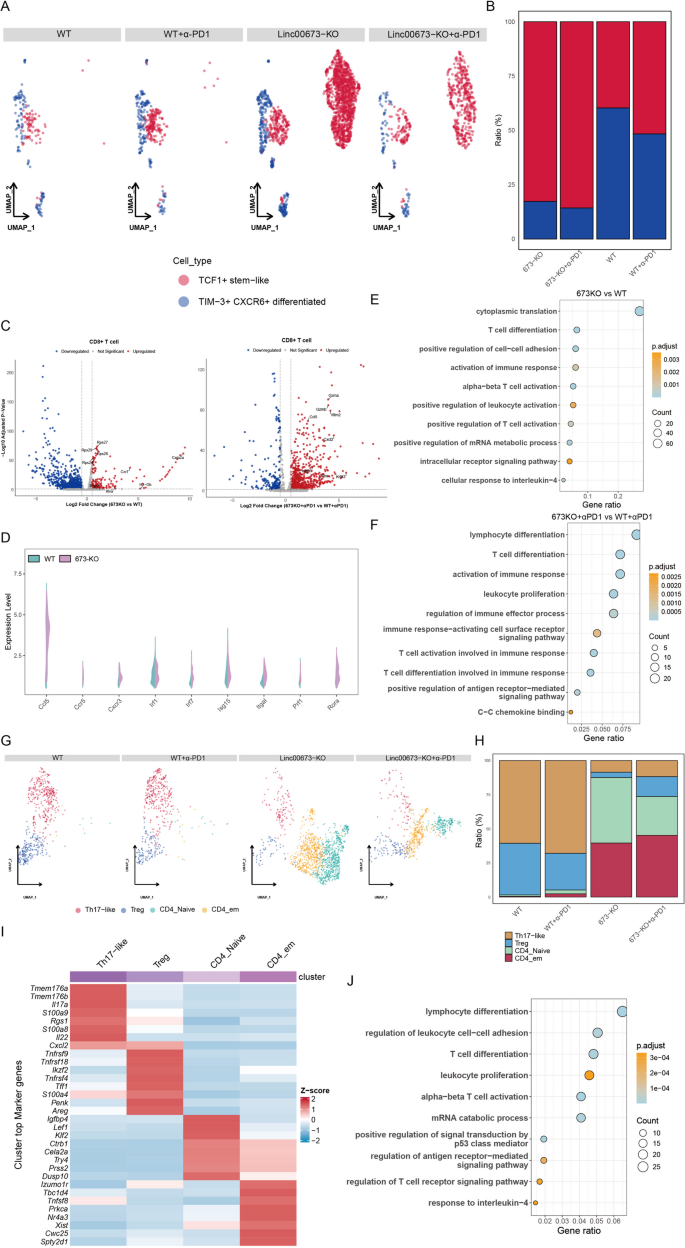
CD8+T细胞可分为两个功能亚群:TCF1+干细胞样CD8+T细胞、TIM-3+CXCR6+分化型CD8+T细胞;野生型组中分化型T细胞占比更高,而Linc00673敲除组中干细胞样T细胞的占比显著升高,联合程序性死亡受体1阻断后可促进干细胞样T细胞向效应细胞分化;差异基因分析显示,与野生型组相比,Linc00673敲除组的CD8+T细胞中翻译相关基因、T细胞激活相关基因(Rps24、Il6ra、Ccr7等)显著上调,联合程序性死亡受体1阻断后细胞毒性相关基因(Gzma、Gzmb、Il2ra等)进一步上调;小提琴图显示敲除组CD8+T细胞中Ccl5、Cxcr3、Irf1、Prf1等效应功能相关基因的表达显著升高;基因本体富集分析显示,敲除组CD8+T细胞富集于细胞质翻译、T细胞分化、αβT细胞激活等通路,联合程序性死亡受体1阻断后富集于免疫反应激活、白细胞增殖、免疫效应过程调控等通路。CD4+T细胞可分为初始T细胞、效应记忆T细胞、调节性T细胞、Th17样细胞4个亚群,Linc00673敲除组中免疫抑制性调节性T细胞的比例显著降低,效应记忆T细胞、Th17样细胞的比例显著升高;基因本体富集分析显示敲除组CD4+T细胞富集于淋巴细胞分化、T细胞激活、白细胞增殖等通路。产品关联:文献未提及该环节具体实验产品,领域常规使用T细胞亚群特异性marker抗体、单细胞测序数据分析相关R包。
3.5 髓系细胞与B细胞的调控机制解析
本环节核心目标为明确Linc00673敲除对髓系细胞、B细胞亚群组成与功能的调控作用。方法细节:从单细胞测序数据中提取巨噬细胞、树突状细胞、中性粒细胞、B细胞的表达矩阵分别进行重新聚类,根据亚群特异性marker基因注释细胞亚群,比较不同实验组的亚群比例差异,通过差异基因分析、基因本体富集分析解析亚群的功能变化。结果解读:髓系细胞与B细胞分析结果如图5所示,
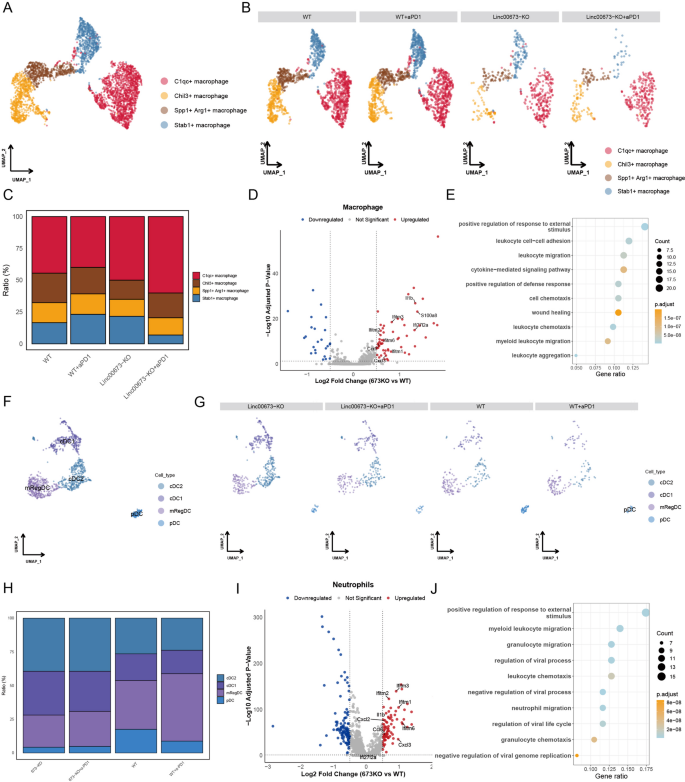
B细胞的总数量在Linc00673敲除组显著升高(野生型组206个,敲除组3420个,敲除+程序性死亡受体1组5566个),其中绝大多数为激活型B细胞,差异基因富集于RNA剪接、核糖体生物发生、翻译调控等与B细胞激活、抗体产生相关的通路。巨噬细胞可分为4个亚群:C1qc+促炎型巨噬细胞、Stab1+免疫抑制型巨噬细胞、Spp1+Arg1+免疫抑制型巨噬细胞、Chil3+巨噬细胞;与野生型组相比,Linc00673敲除组中免疫抑制型的Spp1+Arg1+、Stab1+巨噬细胞比例显著降低,C1qc+促炎型巨噬细胞比例显著升高;差异基因分析显示敲除组巨噬细胞中Il1b、Ifitm3、Cxcl3等促炎基因显著上调,基因本体富集于免疫反应正调控、白细胞迁移、细胞趋化等通路。树突状细胞可分为4个亚群:经典1型树突状细胞(cDC1)、经典2型树突状细胞(cDC2)、浆细胞样树突状细胞(pDC)、调节性树突状细胞(mRegDC);敲除组中负责抗原交叉呈递的经典1型树突状细胞、经典2型树突状细胞比例显著升高,免疫抑制性调节性树突状细胞比例显著降低。中性粒细胞的差异基因分析显示,敲除组中性粒细胞中干扰素刺激基因(Ifitm1、Ifitm2、Ifitm3)、趋化相关基因(Cxcl2、Cxcl3)显著上调,基因本体富集于粒细胞迁移、炎症反应正调控等通路。产品关联:文献未提及该环节具体实验产品,领域常规使用髓系细胞、B细胞亚群特异性marker抗体。
3.6 肿瘤细胞表型重塑与细胞间互作分析
本环节核心目标为明确Linc00673敲除对肿瘤细胞生物学特征、免疫细胞-肿瘤细胞间互作的调控作用。方法细节:从单细胞测序数据中提取上皮细胞的表达矩阵进行重新聚类,通过inferCNV R包分析拷贝数变异(CNV),结合上皮细胞marker基因确认恶性细胞亚群;比较不同实验组的恶性细胞亚群比例差异,通过基因本体富集分析解析亚群的功能特征;采用CellPhoneDB软件分析免疫细胞与恶性细胞之间的配体-受体互作变化。结果解读:肿瘤细胞与细胞间互作分析结果如图6所示,
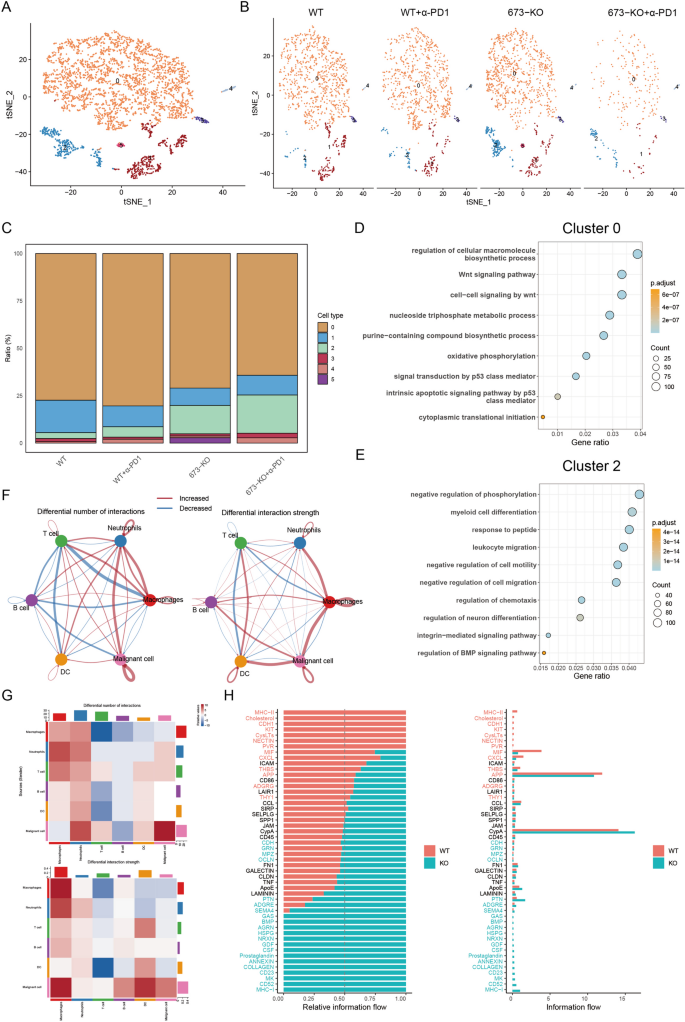
恶性上皮细胞共分为6个亚群,其中Cluster 0富集于Wnt信号通路、氧化磷酸化、核苷生物合成等促癌通路,其在Linc00673敲除组中的比例显著降低;Cluster 2富集于磷酸化负调控、髓系细胞分化、白细胞迁移等通路,其在敲除组中的比例显著升高。细胞间互作分析显示,与野生型组相比,Linc00673敲除组中T细胞与恶性细胞的互作数量和强度均显著升高,MHC-I介导的信号通路互作显著增强,而免疫抑制性巨噬细胞与恶性细胞的互作显著降低。产品关联:文献未提及该环节具体实验产品,领域常规使用拷贝数变异分析工具、细胞间互作分析相关R包。
3.7 体外功能验证与临床相关性分析
本环节核心目标为体外验证LINC00673对CD8+T细胞细胞毒性的调控作用,及LINC00673表达与免疫检查点抑制剂治疗响应的临床相关性。方法细节:采用CRISPR/Cas9技术构建LINC00673稳定敲除的MC38结肠癌细胞系,通过CCK8实验、Transwell迁移实验、划痕实验检测LINC00673敲除对肿瘤细胞增殖、迁移能力的影响;构建MC38皮下荷瘤模型(雌性C57BL/6小鼠,每组n=6),监测肿瘤生长,实验终点采用流式细胞术检测肿瘤浸润免疫细胞的表型;构建表达OVA抗原的MC38细胞系,与OT-I转基因小鼠来源的CD8+T细胞共培养,检测CD8+T细胞的激活标志物、效应分子表达及肿瘤细胞杀伤效率;通过实时荧光定量PCR、流式细胞术检测LINC00673敲除对肿瘤细胞MHC-I抗原呈递通路的影响;分析癌症基因组图谱结直肠癌数据集、接受免疫检查点抑制剂治疗的公共患者队列中LINC00673表达与免疫激活特征、治疗响应、预后的相关性。结果解读:体外功能实验与临床相关性分析结果如图7、8所示,
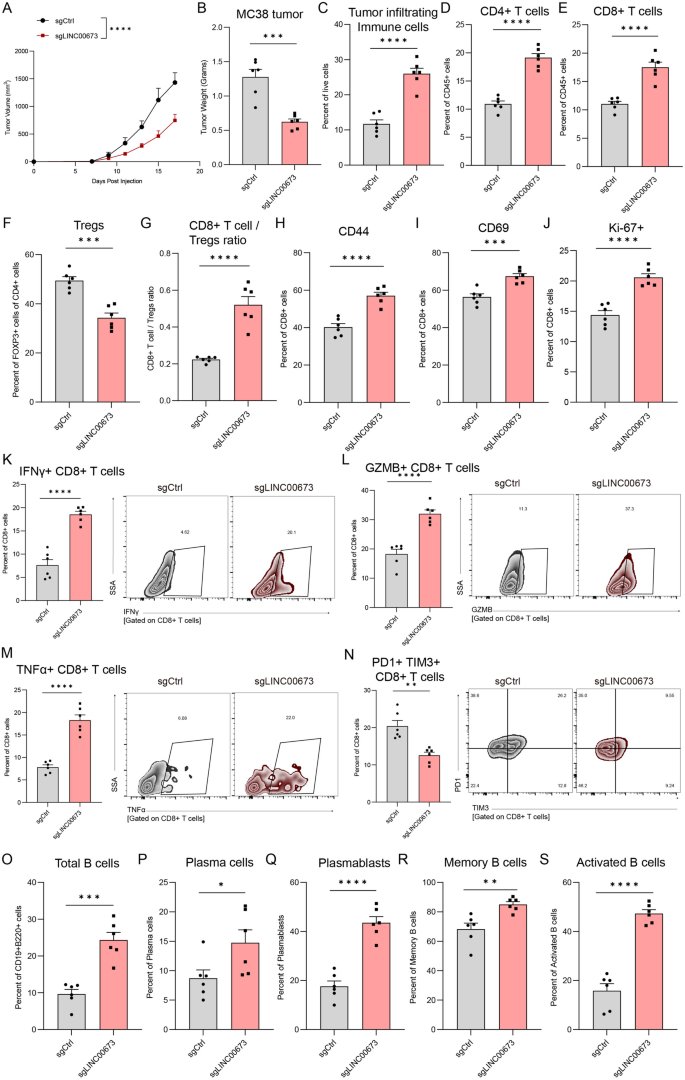
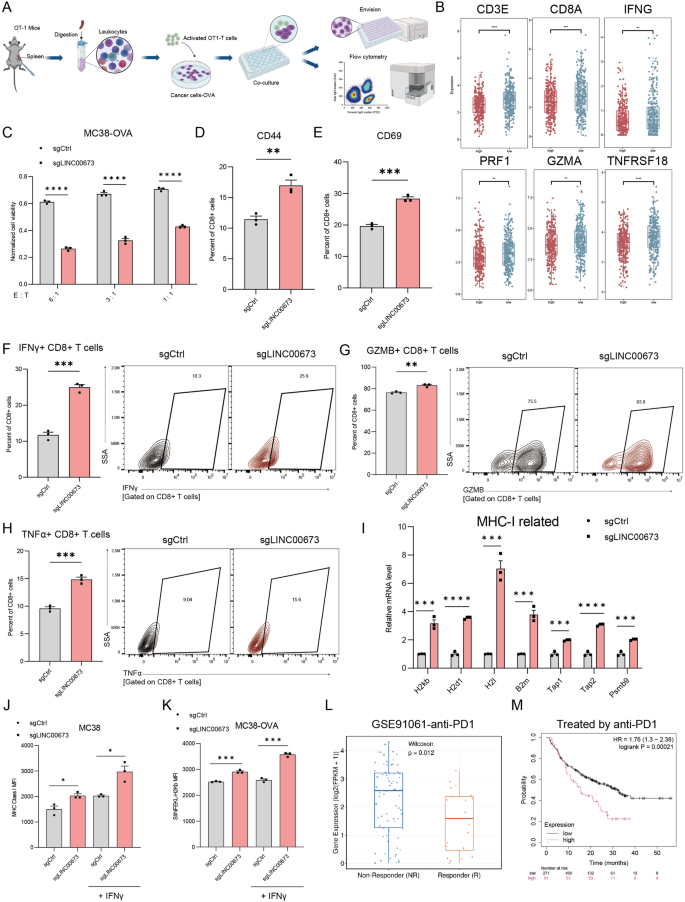
LINC00673敲除不影响MC38细胞的体外增殖,但可诱导G1期细胞周期阻滞、细胞凋亡增加,细胞迁移、侵袭能力显著降低。皮下荷瘤模型结果显示,LINC00673敲除组的肿瘤生长速率显著低于对照组,第21天的肿瘤体积较对照组减少65%(n=6,P<0.001);流式细胞术显示敲除组肿瘤中CD8+T细胞的浸润比例、激活标志物(CD44、CD69)表达、增殖标志物Ki67表达、效应分子(干扰素-γ、颗粒酶B、肿瘤坏死因子-α(TNF-α))表达均显著升高,PD-1+TIM-3+耗竭型CD8+T细胞比例显著降低;同时B细胞总数量、激活型B细胞、浆细胞、记忆B细胞的比例均显著升高。体外共培养实验显示,在不同效应靶比(E:T)下,LINC00673敲除组的肿瘤细胞杀伤率均显著高于对照组,E:T=10:1时杀伤率升高42%(n=3,P<0.01);CD8+T细胞的CD44、CD69表达升高1.7-1.9倍(n=3,P<0.01),干扰素-γ、颗粒酶B、肿瘤坏死因子-α表达分别升高2.1倍、2.3倍、1.8倍(n=3,P<0.001)。机制验证显示,LINC00673敲除的MC38细胞中MHC-I通路相关基因(H2-D1、H2-Kb、B2m、Tap1、Tap2等)的mRNA表达显著上调1.5-3.2倍(n=3,P<0.05-0.001),细胞表面MHC-I分子、抗原肽-MHC-I复合物的平均荧光强度显著升高。临床队列分析显示,接受免疫检查点抑制剂治疗的患者中,LINC00673低表达组的治疗响应率显著高于高表达组,总生存期显著更长(风险比HR=1.76,log-rank P=0.00021)。产品关联:实验所用关键产品:STEMCELL公司的EasySep小鼠CD8+T细胞分离试剂盒,BioLegend的流式细胞术相关抗体(CD45、CD3ε、CD4、CD8a、干扰素-γ、颗粒酶B等,货号文献未明确提及)。
4. Biomarker 研究及发现成果
本研究涉及的核心Biomarker为长链非编码RNA LINC00673,属于肿瘤细胞表达的功能性分子Biomarker,其筛选与验证遵循“生物信息学数据库初筛→临床组织样本验证→动物模型功能验证→体外细胞实验机制验证→公共临床治疗队列验证”的完整逻辑链条,具备作为结直肠癌预后评估、免疫检查点抑制剂治疗响应预测Biomarker及免疫治疗靶点的潜力。
LINC00673的研究来源包括癌症基因组图谱结直肠癌转录组数据集、复旦大学附属肿瘤医院的20对结直肠癌新鲜组织样本、106例结直肠癌组织微阵列样本、公共数据库中接受程序性死亡受体1阻断治疗的结直肠癌患者队列;验证方法涵盖实时荧光定量PCR检测RNA表达、免疫印迹检测蛋白表达、免疫组化检测组织水平表达、流式细胞术检测免疫细胞表型、单细胞RNA测序分析转录组特征;目前文献未明确提供其作为诊断或预测Biomarker的ROC曲线数据,基于临床样本表达差异推测其区分结直肠癌与癌旁组织的准确性较高,在预测免疫检查点抑制剂治疗响应方面,低表达患者的响应率较高表达患者升高2.8倍(基于公共队列数据)。
核心成果主要包括三个方面:第一,预后价值:LINC00673高表达的结直肠癌患者总生存期显著更差,在接受免疫检查点抑制剂治疗的患者中,高表达者的死亡风险较低表达者升高1.76倍(HR=1.76,95%CI未明确提供,P=0.00021);第二,功能关联:LINC00673通过抑制肿瘤细胞MHC-I抗原呈递通路,减少CD8+T细胞的浸润与激活,同时促进免疫抑制性髓系细胞(免疫抑制型巨噬细胞、调节性树突状细胞)的富集,塑造免疫抑制肿瘤微环境,介导免疫检查点抑制剂耐药;第三,创新性:首次证实LINC00673是结直肠癌的免疫抑制调控分子,可同时作为结直肠癌预后评估Biomarker、免疫检查点抑制剂治疗响应预测Biomarker,以及潜在的免疫治疗增敏靶点。统计学结果显示,临床结直肠癌组织中LINC00673的表达较癌旁组织升高2.7倍(n=20,P<0.001),敲除LINC00673联合程序性死亡受体1阻断可使小鼠肿瘤负荷降低79%(n=6,P<0.0001),差异均具有统计学显著性。
推测:LINC00673可作为结直肠癌免疫治疗的伴随诊断Biomarker,同时开发靶向LINC00673的抑制剂联合程序性死亡受体1抑制剂,有望成为微卫星稳定型结直肠癌的新型治疗策略,需进一步开展临床前药物研发及临床研究验证其安全性与有效性。
