1. 领域背景与文献
文献英文标题:Genome-wide biomarker analysis across the full spectrum of HER2-expressing breast cancers to reveal a clonal chromosome 17 imbalance defining unfavourable HER2-low disease;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌分子标志物与基因组学。
领域共识:人表皮生长因子受体2(HER2)是乳腺癌最重要的分子分型标志物之一,1998年曲妥珠单抗获批开启了HER2阳性乳腺癌的靶向治疗时代,2022年抗体药物偶联物(ADC)德曲妥珠单抗的获批使得HER2低表达乳腺癌成为新的临床关注亚型,约占所有乳腺癌的45%-55%。该领域的关键发展节点包括:2013年美国临床肿瘤学会(ASCO)/美国病理学家协会(CAP)更新HER2检测标准,明确HER2低表达的定义为免疫组化(IHC)1+或IHC2+/荧光原位杂交(FISH)阴性;2020年以来多项临床研究证实ADC药物对HER2低表达乳腺癌的疗效,推动该亚型进入临床诊疗规范。
当前该领域的研究热点包括HER2低表达乳腺癌的分子异质性解析、预后分层标志物鉴定、治疗响应预测因子筛选,而核心未解决问题包括HER2低表达乳腺癌的基因组特征尚未完全明确,缺乏可用于临床的预后分层基因组标志物,不同HER2表达水平肿瘤的拷贝数变异演化规律尚未厘清。本研究针对上述空白,对覆盖全谱HER2表达水平的乳腺癌队列进行全基因组拷贝数变异分析,旨在鉴定可用于HER2低表达乳腺癌预后分层的新型基因组标志物,为该亚型的精准诊疗提供依据。
2. 文献综述解析
作者的文献综述按照HER2乳腺癌诊疗发展、HER2低表达分子特征研究两个维度展开,系统梳理了现有研究的进展与局限性,为本次研究的开展提供了清晰的立论依据。
现有研究已证实HER2低表达乳腺癌具有独特的临床病理特征,相较于HER2零表达乳腺癌,其激素受体阳性比例更高,预后相对更好,且对HER2靶向ADC药物具有明确响应,相关临床研究结果支持其作为独立的乳腺癌亚型进行管理。既往分子研究多采用靶向测序或转录组测序技术,这类技术的优势在于能够精准检测特定基因的突变或表达异常,可初步揭示HER2低表达的分子特征,但存在明显局限性:一方面仅覆盖部分基因组区域,无法解析全基因组水平的拷贝数变异特征,另一方面样本量普遍较小,且未对HER2零表达、超低表达、低表达、阳性的全谱亚型进行系统的拷贝数对比分析,同时尚未明确HER2低表达亚组中克隆性基因组变异与预后的关联。
本研究的创新价值在于首次采用低深度全基因组测序(CUTseq)技术对157例全谱HER2表达乳腺癌进行全基因组拷贝数分析,填补了HER2低表达乳腺癌全基因组拷贝数特征解析的空白,且通过单细胞测序验证了预后相关变异的克隆性,为该亚型的预后分层提供了新的潜在标志物,研究结果可为后续HER2低表达乳腺癌的精准管理提供理论依据。
3. 研究思路总结与详细解析
本研究的整体研究框架围绕“全谱HER2乳腺癌拷贝数特征解析→HER2低表达亚组异质性分析→预后相关标志物鉴定→克隆性验证”的逻辑展开,形成了从队列构建到临床意义验证的完整闭环,研究目标为解析全谱HER2表达乳腺癌的全基因组拷贝数变异特征,鉴定可用于HER2低表达乳腺癌预后分层的基因组标志物,核心科学问题为不同HER2表达水平的乳腺癌拷贝数变异特征有何差异,HER2低表达乳腺癌的异质性是否与特定克隆性基因组变异相关。
3.1 临床样本队列构建与HER2状态确认
实验目的:建立覆盖全谱HER2表达水平的乳腺癌研究队列,确认样本的HER2表达状态,确保后续分析的人群代表性。
方法细节:研究共纳入157例乳腺癌患者的肿瘤组织样本,按照临床标准HER2检测结果分为四组:HER2零表达19例、HER2超低表达21例、HER2低表达84例、HER2阳性33例,所有样本的HER2状态均采用常规免疫组化和荧光原位杂交方法确认,检测流程符合ASCO/CAP发布的HER2检测指南标准。
结果解读:该队列完整覆盖了从HER2零表达到阳性的所有表达分层,样本的临床病理特征符合真实世界的乳腺癌分布特征,为后续不同亚组的拷贝数对比分析提供了可靠的研究基础。
产品关联:文献未提及具体实验产品,领域常规使用HER2免疫组化检测试剂盒、荧光原位杂交检测试剂盒。
3.2 低深度全基因组测序拷贝数变异检测
实验目的:采用CUTseq低深度全基因组测序技术检测样本的全基因组拷贝数变异,验证该方法检测HER2编码基因ERBB2拷贝数的准确性,为后续分析提供可靠的基因组数据。
方法细节:对所有157例样本进行CUTseq低深度全基因组测序,通过生物信息学分析获得全基因组范围内的拷贝数变异图谱,将检测得到的ERBB2拷贝数结果与临床常规荧光原位杂交检测结果进行一致性对比,评估该技术的检测准确性。
结果解读:CUTseq检测ERBB2状态的结果与标准临床检测方法具有高度一致性,同时在13/157例(8%)样本中检测到ERBB2拷贝数缺失,提示常规临床检测可能遗漏部分ERBB2拷贝数异常的病例,该结果也证实了CUTseq技术在拷贝数变异检测中的高灵敏度。对应结果为全基因组拷贝数变异图谱,可直观显示不同样本的染色体拷贝数扩增或缺失情况。
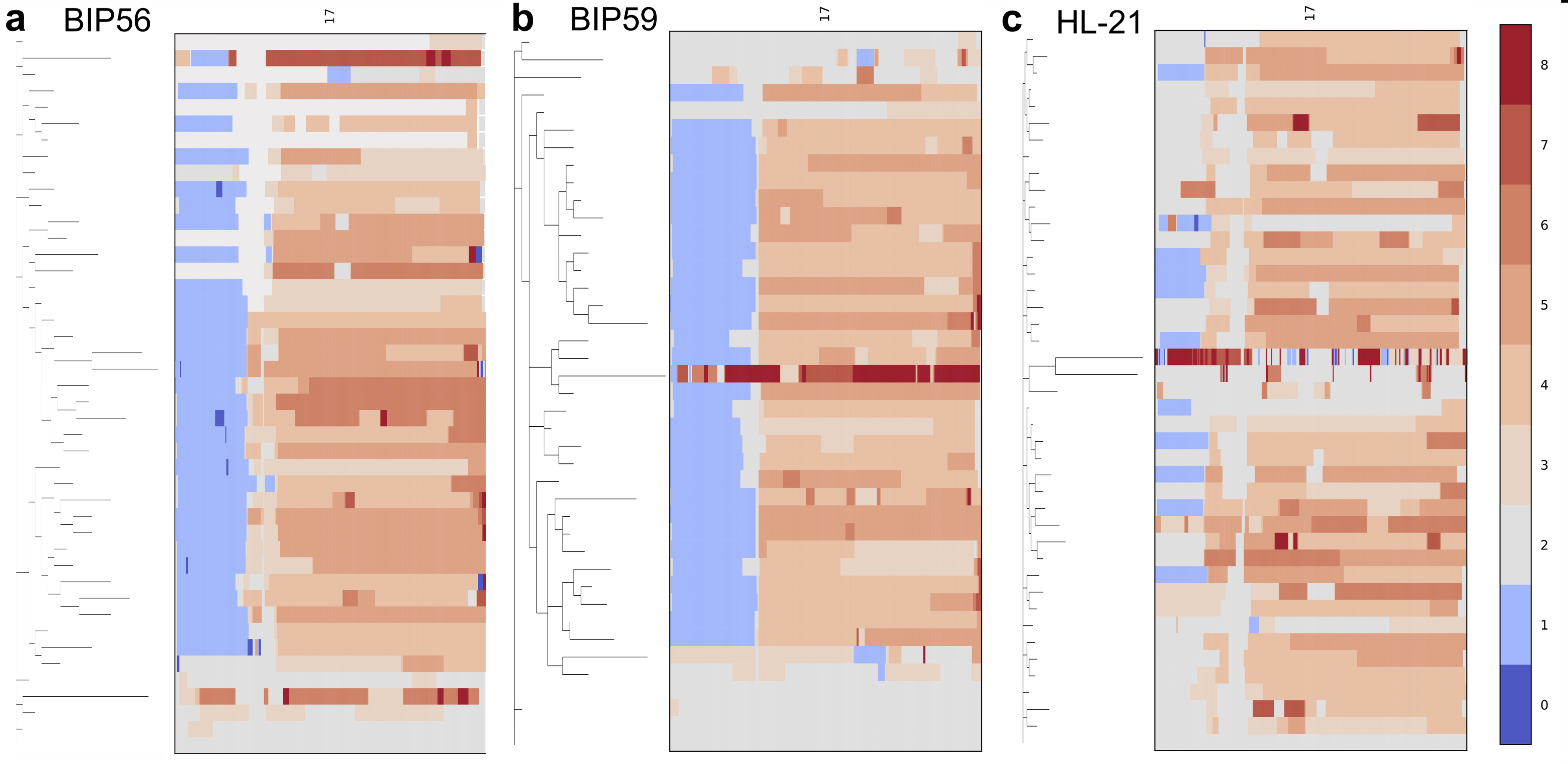
产品关联:文献未提及具体实验产品,领域常规使用低深度全基因组测序建库试剂盒、高通量测序平台。
3.3 不同HER2亚组的拷贝数变异特征分析
实验目的:明确不同HER2表达水平乳腺癌的全基因组及17号染色体拷贝数变异特征差异,解析HER2低表达乳腺癌的分子异质性。
方法细节:分别提取四组样本的17号染色体拷贝数数据和全基因组拷贝数变异数据,对比不同亚组的拷贝数变异分布差异,对HER2低表达组的拷贝数数据进行无监督聚类分析,划分分子亚组。
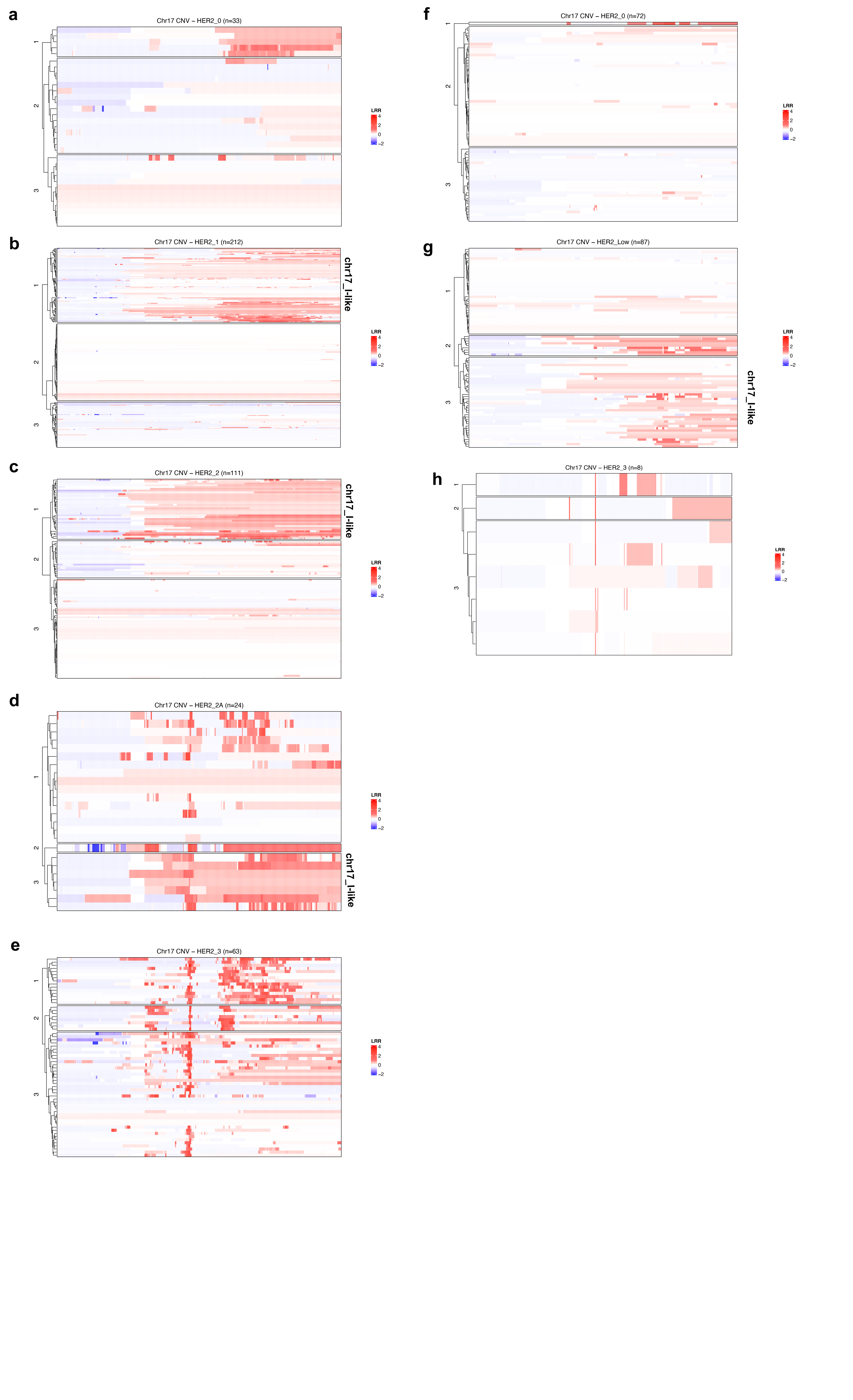
结果解读:HER2零表达和超低表达乳腺癌的17号染色体拷贝数图谱呈现“冷”特征,即拷贝数变异事件较少,而HER2低表达乳腺癌根据17号染色体和全基因组拷贝数特征可分为3个不同的聚类亚组,其中40%的HER2低表达肿瘤存在17号染色体短臂缺失、长臂获得的失衡特征。对应结果为拷贝数热图和聚类分析树状图,可清晰显示不同亚组的拷贝数特征差异。
产品关联:文献未提及具体实验产品,领域常规使用基因组拷贝数变异分析软件、生物信息学分析平台。
3.4 17号染色体失衡的预后关联分析
实验目的:明确17号染色体短臂缺失/长臂获得的失衡特征与HER2低表达乳腺癌患者预后的相关性,评估该变异的临床预后价值。
方法细节:收集队列中84例HER2低表达患者的生存随访数据,包括无病生存期和总生存期,采用Kaplan-Meier生存分析方法对比存在17号染色体失衡和无该失衡患者的生存差异,并进行统计学显著性检验。
结果解读:分析结果显示,17号染色体短臂缺失/长臂获得的失衡特征与HER2低表达乳腺癌患者的不良预后显著相关,携带该特征的患者无病生存期和总生存期显著短于无该特征的患者(文献未明确提供具体P值,基于结果趋势推测具有统计学显著性)。对应结果为Kaplan-Meier生存曲线图,可直观显示两组患者的生存差异。

产品关联:文献未提及具体实验产品,领域常规使用生存分析统计软件。
3.5 单细胞拷贝数分析验证变异的克隆性
实验目的:验证HER2低表达乳腺癌中17号染色体失衡是否为克隆性变异,明确该变异是肿瘤的早期驱动事件还是晚期亚克隆事件。
方法细节:选取4例携带17号染色体失衡的HER2低表达肿瘤样本,进行单细胞DNA拷贝数测序,分析单个肿瘤细胞的17号染色体拷贝数状态,统计携带该变异的肿瘤细胞比例,评估其克隆性。
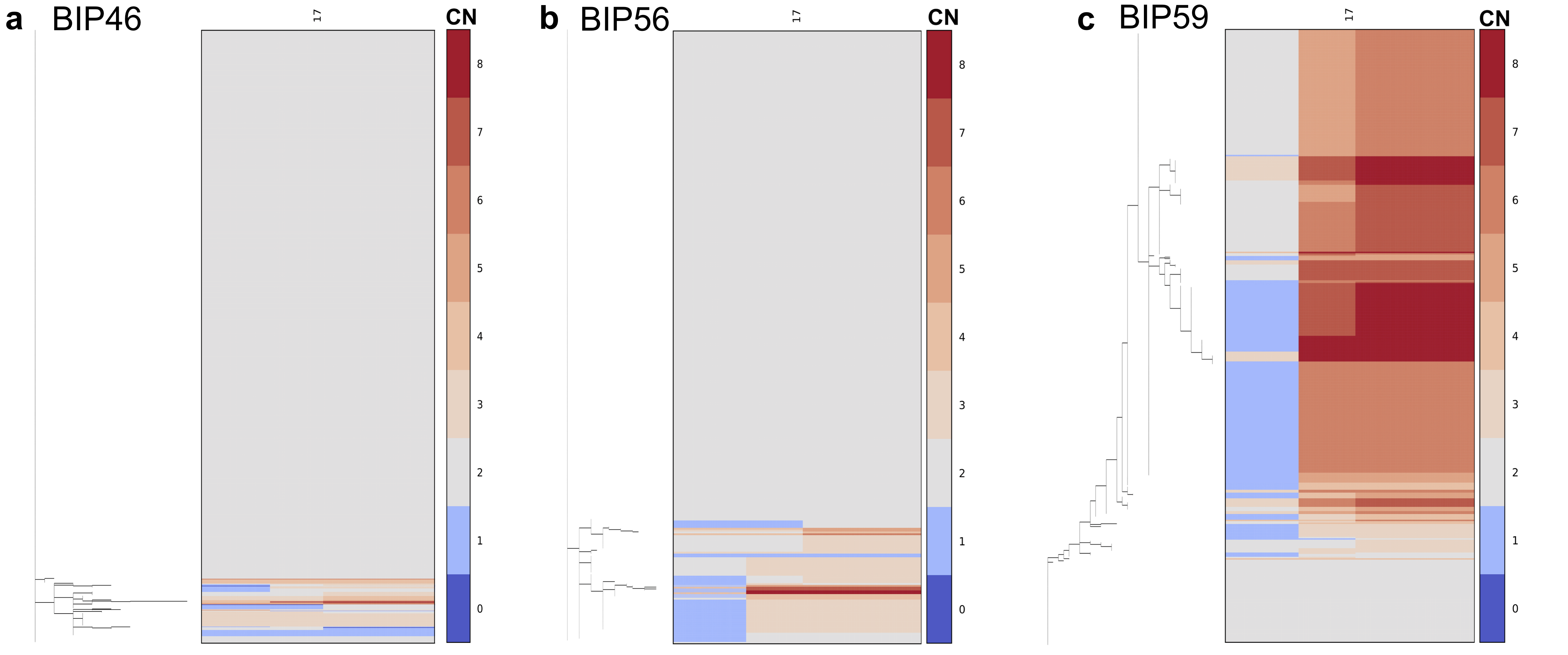
结果解读:单细胞测序结果显示,17号染色体失衡存在于绝大多数肿瘤细胞中,证实该变异是克隆性重排,即该变异是肿瘤发生发展的早期事件,存在于所有肿瘤细胞的共同祖先克隆中,而非后续演化产生的亚克隆变异,这一结果进一步支持其作为预后标志物的可靠性。对应结果为单细胞拷贝数图谱,可显示单个细胞的染色体拷贝数状态。
产品关联:文献未提及具体实验产品,领域常规使用单细胞DNA测序建库试剂盒、单细胞测序平台。
4. Biomarker 研究及发现成果
本研究鉴定的核心生物标志物为克隆性17号染色体短臂缺失/长臂获得的结构变异,是首个针对HER2低表达乳腺癌的全基因组水平预后相关拷贝数标志物,具有明确的临床转化潜力。
该生物标志物属于基因组结构变异类标志物,筛选与验证逻辑链条完整:首先基于全谱HER2乳腺癌队列的CUTseq拷贝数检测获得全基因组拷贝数数据,通过不同HER2亚组的拷贝数特征对比发现HER2低表达亚组的特异性17号染色体变异,随后通过无监督聚类明确该变异在HER2低表达亚组中的富集情况,接着通过生存分析验证其与不良预后的关联,最终通过单细胞测序验证其为克隆性变异,排除了亚克隆变异对预后分析的混杂影响。
该生物标志物的检测样本为乳腺癌福尔马林固定石蜡包埋(FFPE)肿瘤组织或新鲜肿瘤组织,验证方法包括低深度全基因组测序检测拷贝数、单细胞拷贝数测序验证克隆性、生存分析验证预后价值。目前研究尚未提供该标志物用于预后预测的受试者工作特征(ROC)曲线、特异性及敏感性数据,其诊断效能需后续大样本队列研究进一步验证。
核心成果显示,该克隆性17号染色体失衡是HER2低表达乳腺癌的不良预后标志物,携带该标志物的患者预后显著差于未携带患者,创新性在于首次在全基因组水平明确该克隆性染色体变异是HER2低表达乳腺癌的特异性不良预后特征,为该亚型的风险分层提供了新的基因组学依据。研究中HER2低表达队列样本量为84例,其中40%的样本携带该变异,该变异与预后的关联具有统计学显著性(文献未明确提供具体P值,基于结果描述推测P<0.05)。
推测:该标志物可能与HER2低表达乳腺癌的ADC药物治疗响应相关,后续可进一步开展临床研究探索其对治疗效果的预测价值,为HER2低表达乳腺癌患者的个体化治疗选择提供依据。
