1. 领域背景与文献
文献英文标题:Transposable element–mediated evolutionary expansion of Sox2- and Brn2-binding regulatory modules for mammalian neural-cell differentiation;发表期刊:Genome Biology;影响因子:17.9(2024版期刊引证报告);研究领域:进化基因组学、神经发育基因调控。
领域共识:转座元件(TE)占哺乳动物基因组的30%~50%,曾被认为是无功能的“自私DNA”,近年来大量研究证实其可通过被驯化为顺式调控元件(增强子、启动子等)参与基因表达调控,是物种特异性基因调控网络重编程的重要来源。神经发生是哺乳动物尤其是灵长类进化中关键的性状创新过程,Sox2是维持胚胎干细胞(ESC)多能性与神经前体细胞(NPC)干性的核心转录因子,Brn2是调控灵长类端脑发育的关键神经元转录因子,二者共同构成了神经分化过程中的核心调控网络。当前领域未解决的核心问题包括:转座元件在神经分化过程中转录因子结合谱的动态变化规律尚不明确,转座元件介导的神经调控网络进化扩张的分子机制仍缺乏系统解析,灵长类特异性神经发育调控的序列基础仍有待挖掘。本研究针对上述空白,系统解析人胚胎干细胞向神经前体细胞分化过程中,转座元件介导的Sox2、Brn2结合位点的进化起源与功能动态,为理解哺乳动物神经调控网络的进化机制提供新的理论依据。
2. 文献综述解析
作者对领域现有研究按研究方向分为三类进行梳理,分别为转座元件的调控功能研究、神经发生的转录调控网络研究、转座元件介导的转录因子结合位点扩张研究,系统梳理了各方向的研究进展与局限性,突出本研究的创新价值。
第一类转座元件调控功能研究中,作者总结了转座元件被驯化为顺式调控元件参与胎盘发育、先天免疫调控、乳腺发育等多种生物学过程的证据,明确了转座元件作为调控元件的普遍性与功能多样性,该类研究的优势在于覆盖了多物种、多组织的功能验证,但局限性在于多聚焦于单一细胞类型的静态分析,缺乏细胞分化过程中的功能动态追踪。第二类神经发生转录调控研究中,作者明确了Sox2、Brn2在神经分化中的核心作用,证实二者通过结合远端增强子调控神经发生相关基因的表达,该类研究的优势在于解析了核心调控网络的组成与功能,但局限性在于分析多聚焦于非重复基因组区域,系统忽略了占基因组近半数的转座元件区域的转录因子结合位点。第三类转座元件介导的结合位点扩张研究中,作者梳理了转座元件通过在基因组中扩散转录因子结合基序,实现调控网络重编程的分子机制,该类研究的优势在于揭示了进化上调控网络创新的重要路径,但局限性在于缺乏神经分化相关的案例解析,且未明确分化过程中转座元件的功能动态变化。本研究的创新价值在于首次将转座元件的进化分析与神经分化过程中的转录因子结合动态、功能验证结合,系统揭示了转座元件对哺乳动物尤其是灵长类神经调控网络进化的贡献。
3. 研究思路总结与详细解析
本研究的核心目标是阐明转座元件介导的Sox2、Brn2结合调控模块在哺乳动物神经细胞分化中的进化模式与调控功能,核心科学问题为转座元件如何参与神经分化转录调控网络的进化与动态调控,技术路线遵循“公共数据集重分析→结合位点鉴定→进化起源解析→基序验证→表观功能注释→靶基因功能分析”的闭环逻辑,所有分析均基于公开可及的高通量测序数据集完成。
3.1 Sox2与Brn2结合转座元件的全基因组鉴定
实验目的为系统鉴定人胚胎干细胞、神经前体细胞中Sox2,以及神经前体细胞中Brn2的结合位点中转座元件来源的比例与类型。方法细节为采用公共的染色质免疫沉淀测序(ChIP-seq)数据集,将测序读段比对到人类参考基因组hg38,采用MAPQ>35的严格过滤标准排除多重比对的读段以保证结合位点的准确性,使用MACS3软件进行峰 calling,将每个峰的信号最高点(summit)与RepeatMasker数据库注释的转座元件区域进行重叠分析。结果解读显示,胚胎干细胞中共鉴定到21756个Sox2结合位点,其中27.4%(n=5956)位于转座元件内;神经前体细胞中鉴定到85006个Sox2结合位点,其中20.2%(n=17132)位于转座元件内;神经前体细胞中鉴定到4461个Brn2结合位点,其中35.6%(n=1586)位于转座元件内。胚胎干细胞与神经前体细胞中转座元件来源的Sox2结合位点仅1821个重叠,提示分化过程中转座元件上的转录因子结合位点发生了显著重塑。该部分结果对应文献图1:
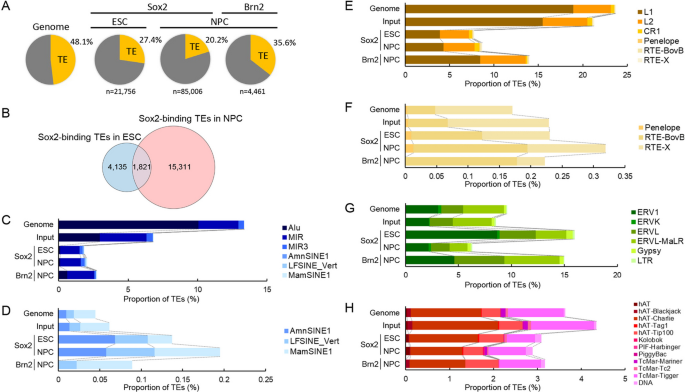
实验所用关键产品:文献未提及具体实验产品,领域常规使用高通量测序比对工具Bowtie2、峰 calling 工具MACS3、转座元件注释数据库RepeatMasker与Dfam。
3.2 转座元件结合位点的进化起源分析
实验目的为明确Sox2、Brn2结合的转座元件的进化插入时间与扩张模式。方法细节为通过计算每个转座元件家族与共识序列的Kimura 2-参数(K2P)分歧度评估其相对进化年龄,同时通过liftOver工具将人类的结合位点序列比对到60种脊椎动物的基因组中,推断转座元件插入的进化节点。结果解读显示,Sox2结合的转座元件呈现双波扩张模式:胚胎干细胞中结合的转座元件有23.6%来源于简鼻亚目(灵长类)共同祖先,57.9%的神经前体细胞中Sox2结合的转座元件来源于真兽类共同祖先;Brn2结合的转座元件也呈现类似的双波扩张模式,21.5%来源于简鼻亚目共同祖先,46.3%来源于真兽类共同祖先。转座元件来源的结合位点比非转座元件来源的结合位点进化起源更晚,93%以上的转座元件结合位点在真兽类共同祖先及之后插入,提示转座元件参与了真兽类诞生后神经调控网络的扩张。该部分结果对应文献图2:
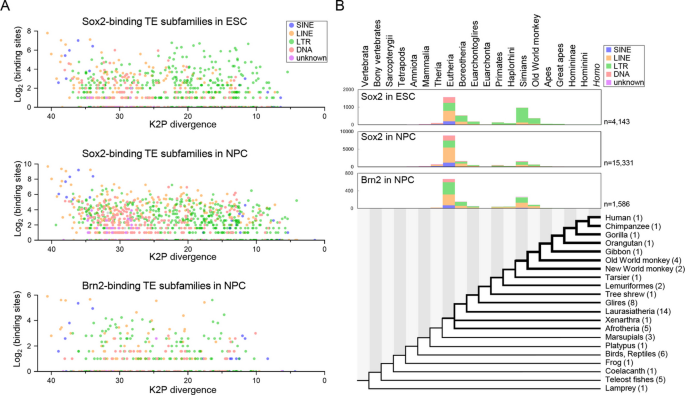
实验所用关键产品:文献未提及具体实验产品,领域常规使用基因组比较分析工具liftOver、多序列比对工具MAFFT、物种分歧时间数据库TimeTree。
3.3 转座元件家族的结合富集与基序验证
实验目的为筛选显著富集Sox2或Brn2结合的转座元件家族,并验证其是否携带保守的转录因子结合基序。方法细节为采用二项分布检验评估每个转座元件家族中结合位点的富集程度,对显著富集的转座元件家族分析结合位点在其共识序列上的位置分布,采用FIMO工具验证转座元件共识序列中是否存在匹配的转录因子结合基序。结果解读显示,共筛选到32个转座元件家族在胚胎干细胞中显著富集Sox2结合,24个转座元件家族在神经前体细胞中显著富集Sox2或Brn2结合,其中属于内源性逆转录病毒(ERV)ERV1家族的MER51A显著富集Sox2结合,同属ERV1家族的MER49显著富集Brn2结合。MER51A的共识序列587-599位存在保守的Sox2结合核心基序5"-CTTTGT-3",MER49的共识序列693-709位存在保守的Brn2结合基序,两个家族均为灵长类特异性内源性逆转录病毒,提示其在灵长类进化过程中扩散了对应的转录因子结合位点。该部分结果对应文献图3与图4:


实验所用关键产品:文献未提及具体实验产品,领域常规使用基序分析工具FIMO、转录因子结合基序数据库HOCOMOCO。
3.4 转座元件结合位点的表观功能注释
实验目的为评估Sox2、Brn2结合的转座元件的顺式调控元件活性及分化过程中的功能动态变化。方法细节为采用ChromHMM工具基于公共的组蛋白修饰数据集(H3K4me1、H3K4me3、H3K27ac、H3K27me3、H3K36me3、H3K9me3)对基因组进行染色质状态注释,分析结合位点所在区域的染色质状态,以及胚胎干细胞向神经前体细胞分化过程中的状态变化。结果解读显示,约67.2%(n=4002)的胚胎干细胞中Sox2结合的转座元件、46.7%(n=8003)的神经前体细胞中Sox2结合的转座元件、52.3%(n=831)的Brn2结合的转座元件位于顺式调控元件区域(启动子或增强子),且显著富集H3K4me1、H3K27ac等活性增强子修饰(P<0.0001,二项式检验)。胚胎干细胞特异性结合的Sox2转座元件中,42.8%在分化为神经前体细胞后从活性调控状态转变为沉默或异染色质状态;而神经前体细胞特异性结合的Sox2转座元件中,48.3%在胚胎干细胞中处于非活性状态,分化后获得调控活性,提示转座元件的功能随分化过程中Sox2的结合动态发生转换。该部分结果对应文献图5与图6:
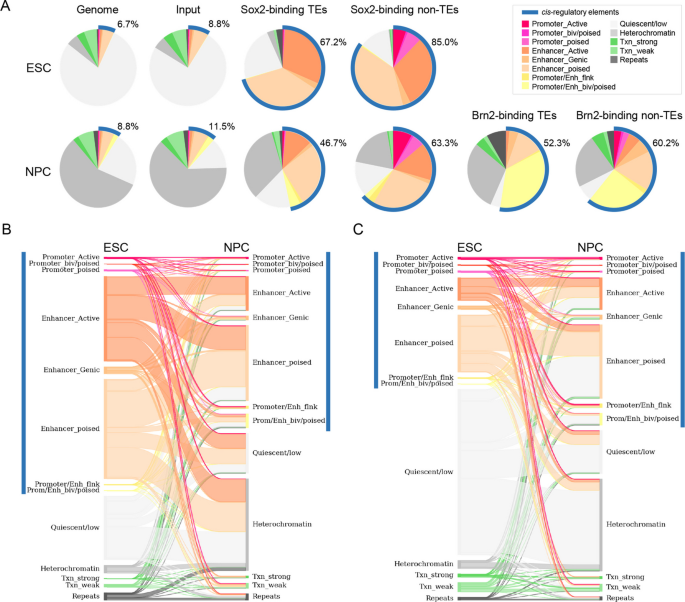

实验所用关键产品:文献未提及具体实验产品,领域常规使用染色质状态分析工具ChromHMM、测序信号可视化工具deepTools。
3.5 转座元件结合位点的靶基因调控效应分析
实验目的为明确Sox2结合的转座元件对邻近基因表达的调控作用及功能关联。方法细节为将转座元件结合位点关联到距离最近的基因转录起始位点,采用公共的胚胎干细胞与神经前体细胞转录组数据分析基因表达变化,采用GREAT工具进行基因功能富集分析。结果解读显示,神经前体细胞特异性Sox2结合转座元件的邻近基因在神经前体细胞中显著上调,上调基因数量是下调基因的1.6倍(3685 vs 2324),强差异表达(变化倍数>8倍)的上调基因是下调的2.1倍(643 vs 300)。功能富集分析显示这些上调基因的敲除表型显著关联神经系统、海马、体感皮层发育异常,提示这些转座元件参与调控神经发生相关基因的表达。该部分结果对应文献图7:
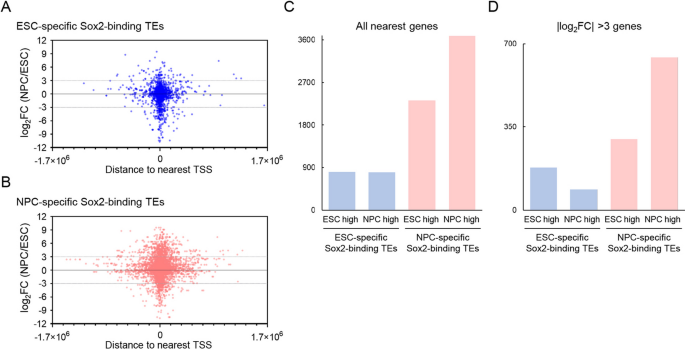
实验所用关键产品:文献未提及具体实验产品,领域常规使用基因富集分析工具GREAT、转录组差异表达分析工具DESeq2。
4. Biomarker 研究及发现成果
本研究鉴定到的生物标志物为转座元件来源的Sox2/Brn2结合顺式调控元件,属于调控类生物标志物,可用于指示神经分化的阶段特异性调控状态,同时为灵长类神经发育的进化机制研究提供候选靶点。
该类生物标志物的筛选与验证逻辑为:通过染色质免疫沉淀测序筛选神经分化不同阶段的Sox2、Brn2结合位点→转座元件注释区分转座元件来源的结合位点→进化保守性分析明确其起源节点→表观组分析验证其顺式调控活性→邻近基因表达分析验证其调控效应。生物标志物的来源为人类基因组中的转座元件插入序列,验证方法包括染色质免疫沉淀测序结合验证、组蛋白修饰分析、染色质状态注释、结合基序保守性分析。其中灵长类特异性的MER51A家族在人类基因组中有1180个拷贝,其中30个存在Sox2结合,40%的结合拷贝位于活性顺式调控区域;同属灵长类特异性的MER49家族在人类基因组中有1444个拷贝,其中50个存在Brn2结合,20%的结合拷贝位于活性顺式调控区域。
核心成果显示,该类转座元件来源的调控元件具有神经分化阶段特异性的调控活性,神经前体细胞特异性结合的Sox2转座元件的邻近基因显著富集神经发生相关功能,其中灵长类特异性的转座元件来源调控元件共包含3261个Sox2结合位点、579个Brn2结合位点,可能是灵长类神经发育调控网络特异性的重要分子基础。这些调控元件的功能转换与Sox2的结合动态显著相关,胚胎干细胞中结合的转座元件在分化后多失去调控活性,而神经前体细胞中结合的转座元件多在分化后获得活性,统计学上转座元件结合位点位于顺式调控区域的比例显著高于随机背景(P<0.0001,二项式检验)。推测:灵长类特异性转座元件扩增带来的Brn2结合位点增加,可能是Brn2在灵长类端脑发育中功能不可或缺的分子基础,后续可通过CRISPR-Cas9基因编辑敲除对应转座元件,验证其对靶基因表达与神经分化过程的调控功能。