
1. 领域背景与文献
文献英文标题:ER tethering and active transport govern condensate diffusion during hyperosmotic stress;发表期刊:Genome Biology;影响因子:未公开;研究领域:细胞生物物理学(生物分子相分离方向)。
领域共识:生物分子相分离是细胞内无膜细胞器形成的核心机制,自2009年首次被系统论证以来,已被证实参与基因表达调控、应激响应、信号转导等多种关键生命过程,2018年领域内解析了RNA结合蛋白相分离的分子语法,为后续凝集体的功能与调控研究奠定了基础。高渗胁迫是肾脏等器官的细胞常经历的生理刺激,2020年研究首次发现高渗胁迫会诱导细胞快速形成高渗相分离(HOPS)凝集体,但其在压缩细胞内的动态调控机制尚未明确。当前领域内普遍存在“高渗压缩导致胞质拥挤固化,分子扩散受限来自物理屏障”的假说,但缺乏直接实验证据,本研究针对这一核心空白展开探究,旨在明确应激状态下细胞内凝集体的时空调控机制,为完善细胞内物质运输的理论模型提供实验依据。

2. 文献综述解析
作者在综述部分按照“相分离的生理功能→高渗胁迫下的细胞响应→凝集体动力学调控”的逻辑框架梳理现有研究,系统对比了不同条件下凝集体的动态特征差异。现有研究已证实,生物分子凝集体可通过快速响应环境变化调控细胞生理过程,高渗诱导的高渗相分离凝集体具有可逆性,参与细胞的渗透压稳态维持;单粒子追踪(SPT)技术的发展已实现活细胞内纳米级颗粒的动态定量,其时间分辨率可达毫秒级,能够精准区分自由扩散、亚扩散、超扩散等不同运动模式,近年开发的高通量相分离检测技术也为凝集体的表型分析提供了更多工具。

但现有研究存在明显局限性:一方面,对凝集体动力学的研究多集中于生理渗透压条件,高渗压缩状态下的研究仅关注凝集体的形成机制,对其扩散调控的分子机制缺乏系统解析;另一方面,“高渗下胞质扩散受限来自物理拥挤”的假说未被直接验证,无法解释凝集体的异质性运动特征。本研究的创新价值在于首次系统解析了高渗下高渗相分离凝集体的双模式扩散调控机制,明确内质网锚定是亚扩散的核心原因,微管依赖的主动运输介导超扩散事件,同时推翻了高渗下胞质静态固化的传统观点,证实扩散受限来自特异性分子互作而非物理屏障,为细胞应激响应的物理调控机制提供了新的认知。
3. 研究思路总结与详细解析
本研究的核心目标是解析高渗胁迫下高渗相分离凝集体的扩散动力学特征及其调控机制,核心科学问题为高渗压缩细胞中凝集体的异质性扩散模式由哪些细胞结构与分子过程调控,整体技术路线遵循“表型表征→机制验证→假说修正”的闭环逻辑:首先通过活细胞单粒子追踪定量高渗相分离凝集体的扩散模式,其次通过细胞器标记与药物干预分别验证亚扩散与超扩散的调控机制,最后通过纳米探针示踪明确胞质的物理可及性,修正现有高渗下胞质扩散的调控模型。
3.1 高渗相分离凝集体扩散模式的定量表征
实验目的:明确高渗胁迫下模型凝集体的扩散模式异质性特征。方法细节:以mRNA脱帽酶1A(DCP1A)作为高渗相分离凝集体的标记蛋白,通过基因编码荧光蛋白标记目的分子,采用活细胞高帧率荧光单粒子追踪技术,跨时间尺度采集凝集体的运动轨迹,通过扩散系数统计与运动模式分类算法分析轨迹特征。结果解读:轨迹定量分析显示,高渗相分离凝集体主要表现为亚扩散模式,仅小部分凝集体存在爆发性的超扩散运动,两类模式的占比存在显著差异(文献未明确具体占比与统计学数据,基于结果描述)。产品关联:文献未提及具体实验产品,领域常规使用高灵敏度活细胞荧光成像系统、基因编辑相关试剂及单粒子追踪分析软件。
3.2 内质网锚定调控凝集体亚扩散的验证
实验目的:解析高渗相分离凝集体亚扩散的分子调控机制。方法细节:采用内质网(ER)特异性标记分子KDEL连接红色荧光蛋白(RFP)标记细胞内质网结构,通过双荧光共定位分析凝集体与内质网的空间关联,同时使用毒胡萝卜素处理细胞诱导内质网结构重塑,对比处理前后凝集体的运动参数变化。内质网作为细胞内面积最大的膜结构,其管状网络的动态特征此前已被广泛研究,代表性结果如下:
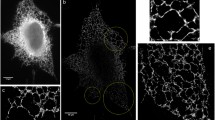
结果解读:双荧光成像显示高渗相分离凝集体与内质网存在显著共定位,提示二者存在直接相互作用;补充视频1直观展示了凝集体锚定在内质网表面的受限运动特征,毒胡萝卜素诱导内质网重塑后,凝集体的运动范围进一步缩小,亚扩散特征更为显著(补充视频2),证实内质网锚定是凝集体亚扩散的核心原因。产品关联:文献未提及具体实验产品,领域常规使用内质网荧光标记试剂、毒胡萝卜素等内质网应激诱导剂及双荧光共定位分析软件。
3.3 微管依赖主动运输调控凝集体超扩散的验证
实验目的:明确高渗相分离凝集体超扩散的细胞骨架调控机制。方法细节:分别采用微管解聚药物诺考达唑、肌动蛋白微丝解聚药物latrunculin A处理细胞,对比药物处理前后凝集体超扩散事件的发生频率与运动参数变化,结合高帧率单粒子追踪定量分析不同细胞骨架的调控作用。结果解读:微管解聚处理后,高渗相分离凝集体的超扩散事件完全消失,而肌动蛋白微丝解聚对超扩散的发生无显著影响,证实凝集体的超扩散是微管依赖的主动运输过程(文献未明确具体统计学数据,基于结果描述)。产品关联:文献未提及具体实验产品,领域常规使用细胞骨架干预药物、高帧率活细胞成像系统。
3.4 高渗压缩下胞质空间可及性分析
实验目的:验证高渗下凝集体扩散受限是否来自胞质物理拥挤形成的屏障。方法细节:使用基因编码多聚纳米颗粒(GEMs)作为被动扩散探针,该类探针无特异性细胞内相互作用,仅反映胞质的物理扩散环境,通过追踪GEMs的运动轨迹重构高渗压缩细胞内的空间可及性,对比生理渗透压与高渗条件下的扩散参数差异。结果解读:GEMs的轨迹分析显示,即使在高渗压缩导致细胞体积显著缩小的情况下,胞质仍保持良好的扩散可及性,无物理围堵导致的扩散受限区域,说明高渗相分离凝集体的扩散受限并非来自物理拥挤,而是与内质网的特异性相互作用导致。本部分结果直接推翻了“高渗下胞质静态固化”的传统假说,更新了对应激状态下胞质物理环境的认知。产品关联:文献未提及具体实验产品,领域常规使用基因编码纳米颗粒探针、高分辨率活细胞成像系统及轨迹重构分析软件。
4. Biomarker研究及发现成果
本研究为基础细胞生物物理机制研究,聚焦于高渗胁迫下生物分子凝集体的扩散调控规律解析,未开展疾病相关生物标志物的筛选、验证及临床相关性分析,无相关Biomarker数据产出。研究成果的核心价值在于完善了细胞应激响应过程中凝集体的时空调控模型,为后续肾脏渗透压相关疾病的机制研究提供了新的理论方向。推测:高渗相分离凝集体的异常调控后续可作为肾脏损伤的候选生物标志物开展进一步验证研究。